基于HPLC 指纹图谱和多成分含量测定结合化学计量学的暖宫七味丸质量评价研究
籍学伟,陈备尧,白 妍,韩 峰
内蒙古自治区药品检验研究院 内蒙古自治区中蒙药标准研究重点实验室,内蒙古 呼和浩特 010020
暖宫七味丸(Nuangong Qiwei Pills,NQP)又名苏格木勒-7 味丸,是蒙古族治疗妇科疾病经典名方,处方出自《观者之喜》[1]。本品由白豆蔻(豆蔻)、天冬、手掌参、沉香、肉豆蔻、黄精、丁香七味药材组成复方制剂[2],具有调经止血、温暖子宫、驱寒止痛的功效,主要用于治疗气滞腰痛、月经不调等症[3-6]。NQP 现收载于《卫生部药品标准》蒙药分册中,现行质量标准仅收载了性状和检查项,尚无有效控制本品质量的定量方法。目前文献报道对NQP 的药理活性及作用机制研究居多,在质量控制方面研究文献报道较少,且大都停留在对利用单一化学成分进行含量测定水平[7-9]。
中成药的化学成分复杂,单一指标评价模式难以全面反映制剂的整体质量,利用指纹图谱技术结合多成分含量测定并利用化学计量学,如聚类分析、主成分分析(principal component analysis,PCA)及正交偏最小二乘-判别分析(orthogonal partial least squares- discriminant analysis,OPLS-DA)等分析方法,对复杂的数据进行整合,可以更加直观地反映不同企业和批次间药品质量差异,近几年已在成方制剂研究分析中广泛应用[10-13]。本实验通过利用高效液相色谱法建立NQP 指纹图谱,对沉香四醇、丁香酚、肉豆蔻木脂素、去氢二异丁香酚含量进行同时检测,利用化学计量学分析方法对14 批NQP 测定结果进行分析,为本品整体质量控制提供方法依据和研究数据支持。
1 仪器与材料
1.1 仪器
岛津LC-20A 型高效液相色谱仪,配SPD-20A型二极管阵列检测器,日本岛津公司;KQ-500DE 型超声波清洗器,昆山市超声仪器有限公司;PL-203型千分之一电子天平(感量1.0 mg)、XP-205 型万分之一电子天平(感量0.1 mg),梅特勒-托利多仪器有限公司;ME 5 型百万分之一电子天平,感量0.001 mg,赛多利斯仪器有限公司。
1.2 材料
对照品沉香四醇(批号111980-201904,质量分数98.6%)、丁香酚(批号110725-201917,质量分数99.1%)、去氢二异丁香酚(批号111838-201804,质量分数98.6%)、桉油精(批号110788-202108,质量分数99.4%)、肉豆蔻醚(批号190180-201701,供鉴别用)、天麻素(批号110807-202010,质量分数95.5%)、腺苷(批号110879-202204,质量分数99.4%)、对羟基苯甲醇(批号111970-201702,质量分数99.4%),对照药材丁香(批号121039-201906)、沉香(批号121222-202104)、肉豆蔻(批号120926-202109)、豆蔻(批号121341-201705)、天冬(批号121139-201906)均购于中国食品药品检定研究院;对照品dactylorhin A(批号DSTDD023301,质量分数98%)、肉豆蔻木脂素(批号MUST-19102316,质量分数99.4%),均购于成都曼斯特生物科技有限公司。甲醇为色谱纯,水为超纯水。
豆蔻、手掌参均为内蒙古蒙药股份有限公司提供,经内蒙古自治区药品检验研究院林燕主任药师鉴定,豆蔻为姜科豆蔻属植物白豆蔻Amomum kravanhPierre ex Gagnep.的干燥成熟果实,手掌参为兰科手参属植物手参Gymnadeniaconopsea(L.)R.Br.的干燥块茎。
NQP 来源与编号分别为内蒙古蒙药股份有限公司,批号2202015、2207024、2208015、2210010、2210011、2210022,编号S1~S6;内蒙古大唐药业股份有限公司,批号 22449001、22449002、22664002、22664003,编号S7~S10;内蒙古库伦蒙药有限公司,批号200132,编号S11;乌兰浩特中蒙制药有限公司,批号210535、210728、221012,编号S12~S14。
2 方法与结果
2.1 溶液的制备
2.1.1 对照品溶液的制备 取沉香四醇、丁香酚、肉豆蔻木脂素、去氢二异丁香酚对照品适量,精密称定,加甲醇制成含沉香四醇206.50 µg/mL、丁香酚2 011.75 µg/mL、肉豆蔻木脂素52.05 µg/mL、去氢二异丁香酚49.50 µg/mL 的混合对照品储备液,精密量取对照品储备液5.0 mL,置25 mL 量瓶中,加甲醇稀释至刻度,摇匀,即得对照品溶液。
2.1.2 供试品溶液的制备 取NQP 粉末(过三号筛)约2.5 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,称定质量,超声处理(功率500 W、频率40 kHz)30 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,取续滤液,用0.45 μm 滤头滤过,作为供试品溶液。
2.1.3 单味药材供试品溶液的制备 按处方比例折算,分别取处方中7 味对照药材粉末,分别按“2.1.2”项下供试品溶液制备方法处理,即得。
2.1.4 阴性供试品溶液的制备 按NQP 的制备工艺分别制备缺沉香、缺肉豆蔻、缺丁香、豆蔻、肉豆蔻的阴性样品,按“2.1.2”项下供试品溶液制备方法处理,即得。
2.2 色谱条件
采用Grace Alltima HP C18(250 mm×4.6 mm,5 μm)色谱柱;体积流量1.0 mL/min;柱温30 ℃;进样量10 μL;检测波长220 nm;流动相为甲醇-水,梯度洗脱:0~10.00 min,25%~38%甲醇;10.00~12.00 min,38%~47%甲醇;12.00~22.00 min,47%甲醇;22.00~70.00 min,47%~70%甲醇;70.00~85.00 min,70%~92%甲醇。
2.3 指纹图谱研究
2.3.1 精密度试验 取NQP(S1),按“2.1.2”项下方法制备供试品溶液,再按“2.2”项下色谱条件连续进样测定6 次,以8 号峰(丁香酚)为参照峰,测得各共有峰相对保留时间的RSD 为0.13%~0.17%,相对峰面积的RSD 为0.06%~0.19%,结果表明方法精密度良好。
2.3.2 稳定性试验 取同1 份NQP(S1)的供试品溶液,分别于制备后的2、4、8、12、16、24 h,按照“2.2”项下色谱条件进样分析,以8 号峰(丁香酚)为参照峰,测得各共有峰的相对保留时间的RSD 为0.29%~0.70%,相对峰面积的RSD 为0.12%~0.79%,结果表明,供试品溶液在室温放置24 h 稳定性良好。
2.3.3 重复性试验 取NQP(S1),按“2.1.2”项下方法平行制备6 份供试品溶液,再按“2.2”项下色谱条件分别进样分析,以8 号峰(丁香酚)为参照峰,测得各共有峰相对保留时间的RSD 为0.20%~0.53%,相对峰面积的RSD 为0.63%~2.52%,结果表明该方法重复性良好。
2.3.4 对照指纹图谱的建立及相似度评价 取14批NQP 样品,按“2.1.2”项下方法制备供试品溶液,再按“2.2”项下色谱条件分别进样分析,将相关色谱数据导入《中药色谱指纹图谱相似度评价系统(2012 年版)》进行处理,得到NQP HPLC 指纹图谱叠加图(图1)。以编号为S1 样品图谱为参考图谱,时间窗宽度设定为0.4 min,采用中位数法,进行了全谱峰匹配,生成NQP HPLC 对照指纹图谱(R)。共标示出21 个共有峰,其中8 号峰(丁香酚)稳定性好,色谱响应高,保留时间适中,故选择该色谱峰为参照峰(S),计算得14 批NQP(S1~S14)指纹图谱相似度分别为0.991、0.990、0.994、0.997、0.995、0.996、0.992、0.993、0.994、0.995、0.987、0.989、0.988、0.990,均大于0.98,表明14 批NQP样品批次间相似度较好。
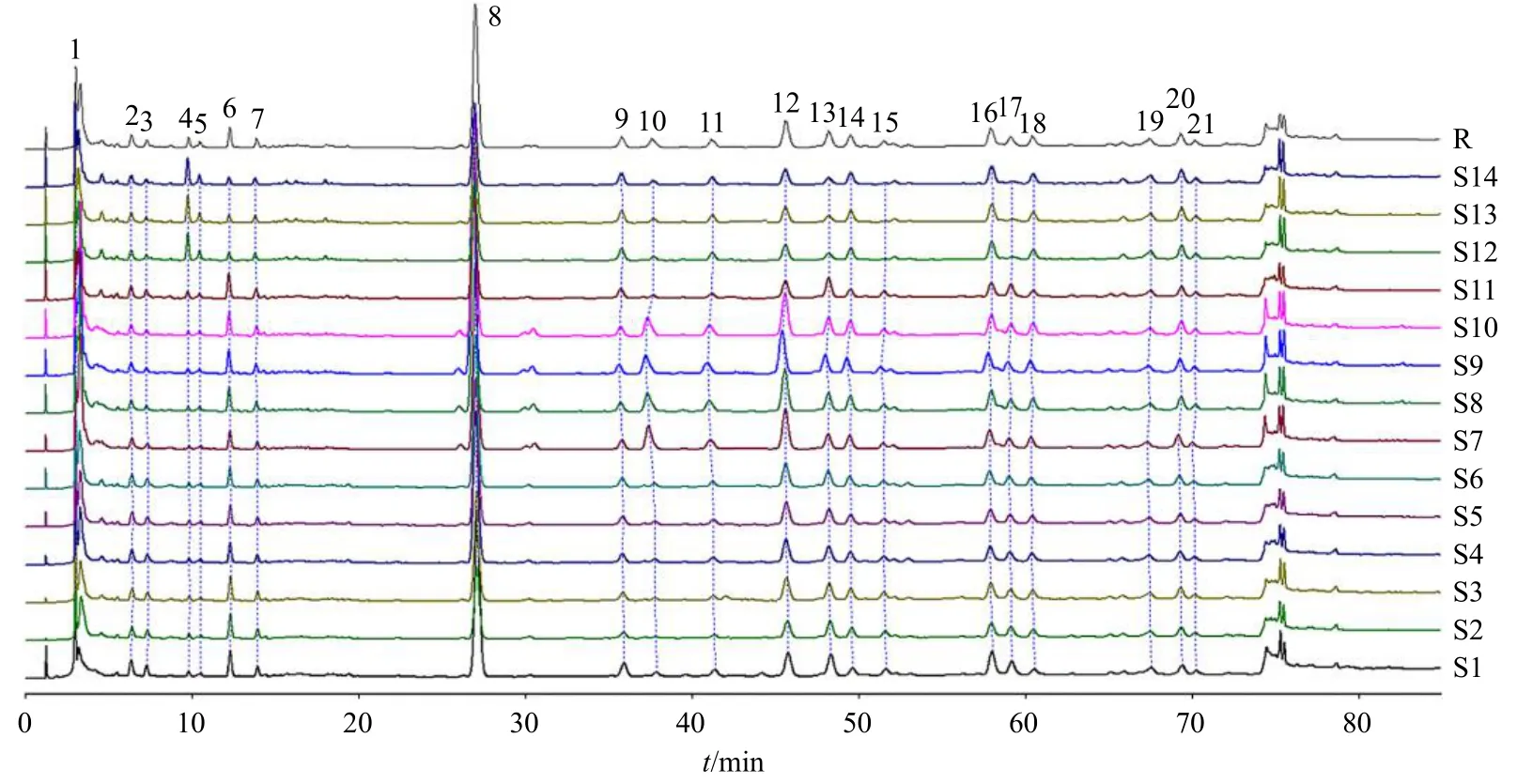
图1 14 批NQP (S1~S14) 和对照指纹图谱 (R)Fig.1 HPLC fingerprint of 14 batches of NQP (S1—S14) and reference (R)
2.3.5 色谱峰药材归属及指认 精密吸取“2.1”项下混合对照品溶液、供试品溶液、单味药材供试品溶液,再按“2.2”项色谱条件分别进样分析,记录色谱图,与指纹图谱共有峰进行对比。结果21 个共有峰有19 个色谱峰分属沉香、丁香、肉豆蔻、豆蔻4 味药材,其余2 个色谱峰未成功归属(表1)。对照品指认4 个色谱峰(图2),分别为沉香四醇(6号峰)、丁香酚(8 号峰)、肉豆蔻木脂素(14 号峰)、去氢二异丁香酚(20 号峰)。
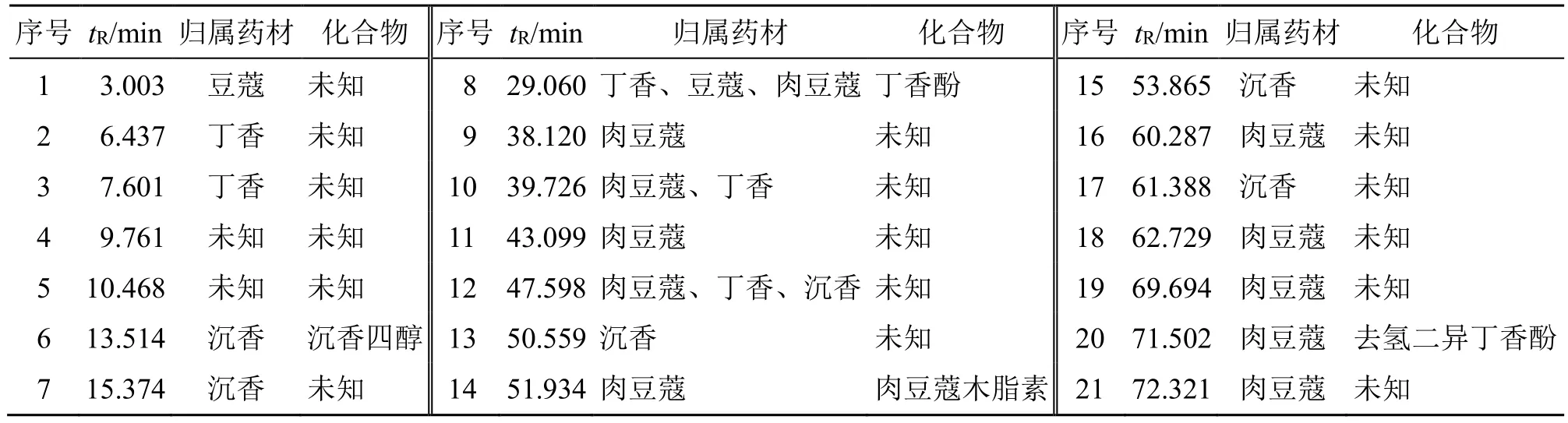
表1 指纹图谱共有峰药材归属Table 1 Fingerprints of common peaks of medicinal materials attributed
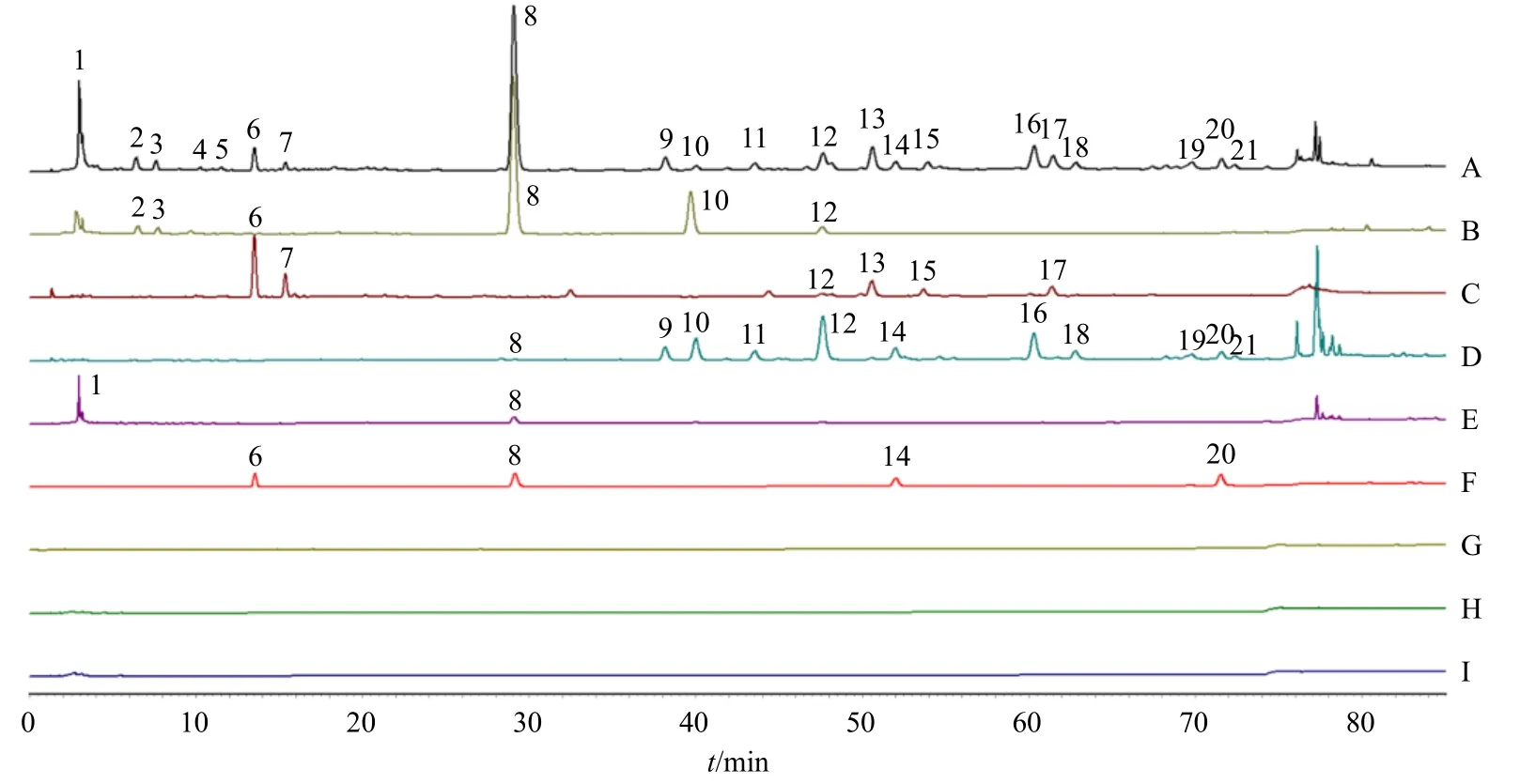
图2 指纹图谱色谱峰归属图Fig.2 Chromatographic peak attribution of fingerprints
2.4 多指标成分含量测定
2.4.1 专属性考察 分别精密吸取“2.1”项下混合对照品溶液、供试品溶液及阴性供试品溶液各10 μL,按“2.2”项下色谱条件进样分析并记录色谱图(图3)。可见供试品呈现与对照品保留时间相同的色谱峰,阴性对照在相应位置无色谱峰。
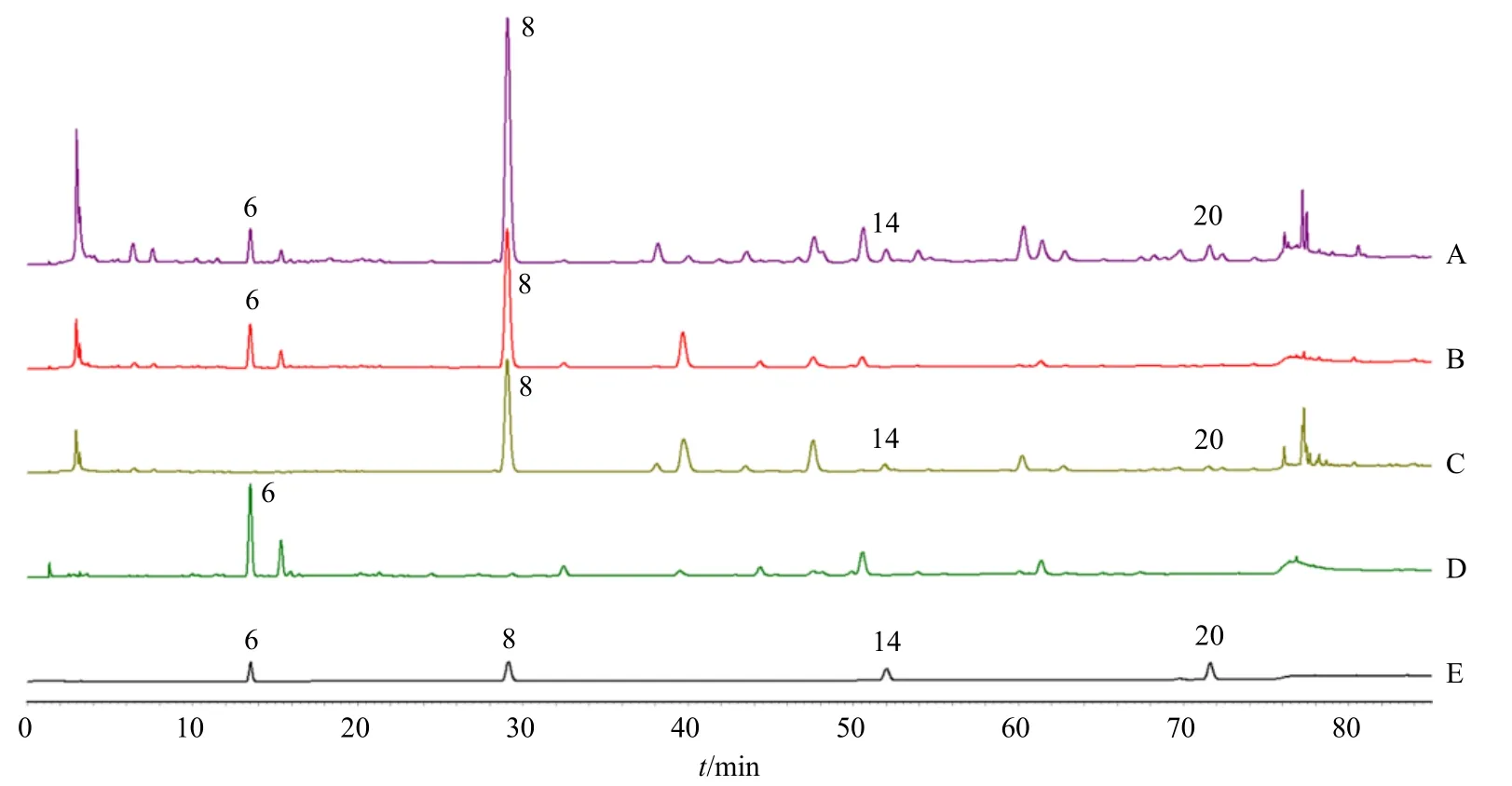
图3 含量测定专属性HPLC 色谱图Fig.3 Specific HPLC chromatogram for content determination
2.4.2 线性关系考察 分别精密量取“2.1.1”项下混合对照品储备溶液1.0、2.0、3.0、5.0、10.0、15.0 mL,分别置于25 mL 量瓶中,加甲醇定容至刻度,摇匀。按“2.2”项下色谱条件测定峰面积,以峰面积为纵坐标(Y),对照品质量浓度为横坐标(X),进行回归分析,绘制各组分的标准曲线,计算回归方程和相关系数,结果分别为沉香四醇Y=31 350.5X+3 597.89,r=0.999 2,线性范围8.26~123.90 μg/mL;丁香酚Y=24 258.8X+35 126.2,r=0.999 5,线性范围80.47~1 207.05 μg/mL;肉豆蔻木脂素Y=35 095.5X+1 984.49,r=0.999 0,线性范围2.08~31.23 μg/mL;去氢二异丁香酚Y=67 465.5X+3 187.37,r=0.999 4,线性范围1.98~29.70 μg/mL;结果表明,各成分在各自质量浓度范围内,相关系数均≥0.999 0,线性关系良好。
2.4.3 精密度试验 精密吸取“2.1.1”项下对照品溶液10 μL,按“2.2”项下色谱条件连续进样6 次,记录峰面积,结果显示,沉香四醇、丁香酚、肉豆蔻木脂素、去氢二异丁香酚峰面积的RSD 分别为0.13%、0.24%、0.16%、0.19%,结果表明仪器的精密度良好。
2.4.4 稳定性试验 取同一NQP 供试品溶液(S1),分别于制备后室温下放置2、4、8、12、16、24 h,按“2.2”项下色谱条件进样测定,记录峰面积,结果显示,沉香四醇、丁香酚、肉豆蔻木脂素、去氢二异丁香酚峰面积的RSD 分别为0.97%、1.51%、0.68%、1.32%,结果表明供试品溶液在室温下放置24 h 稳定。
2.4.5 重复性试验 取同一批NQP 样品(S1),按“2.1.2”项下方法制备供试品溶液,共6 份,按“2.2”项下色谱条件分别进样测定,记录色谱图,计算样品中沉香四醇、丁香酚、肉豆蔻木脂素、去氢二异丁香酚质量分数的平均值分别为0.394、4.005、0.103、0.099 mg/g,RSD 分别为1.40%、0.60%、1.03%、1.98%,结果表明该方法重复性良好。
2.4.6 加样回收率试验 取同一批NQP 样品(S1)细粉1.25 g,置具塞锥形瓶中,共9 份,分为3 组,分别加混合对照品溶液5、10、15 mL(沉香四醇、丁香酚、肉豆蔻木脂素、去氢二异丁香酚峰的质量浓度分别为48.91、504.72、12.92、13.07 μg/mL),再分别加甲醇20、15、10 mL,按“2.1.2”项下方法制备加样回收率溶液,再按“2.2”项下色谱条件进样测定,记录色谱图,计算各成分的加样回收率,结果沉香四醇、丁香酚、肉豆蔻木脂素、去氢二异丁香酚峰的平均加样回收率分别为99.2%、101.4%、101.0%、96.4%,RSD 分别为0.94%、0.98%、1.28%、0.33%。
2.4.7 样品测定 取14 批NQP 样品(S1~S14),各约2.5 g,精密称定,按“2.1.2”项下方法平行制备2 份供试品溶液,再按“2.2”项下色谱条件进样测定,记录峰面积,按外标法计算上述4 种成分的含量,测定结果见表2。
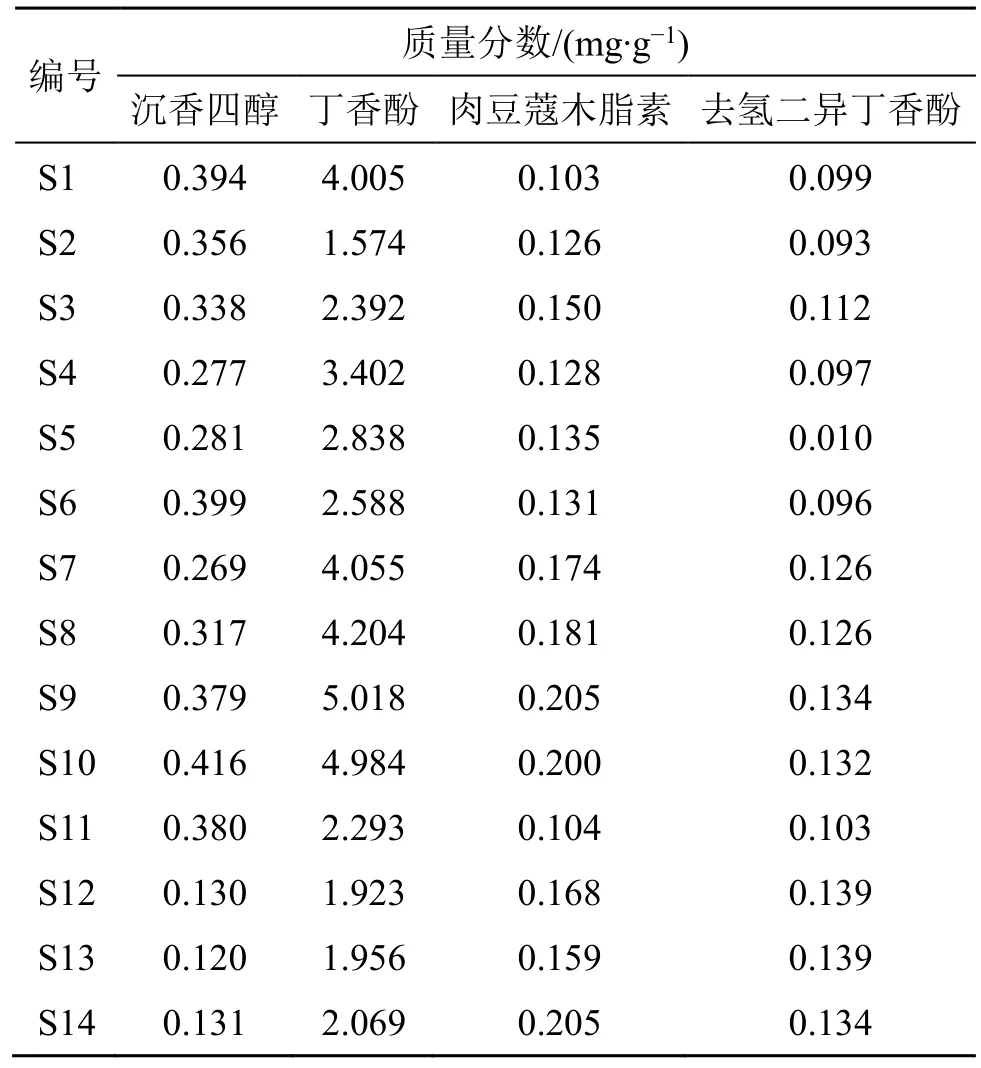
表2 不同批次4 种指标性成分含量测定结果 (n = 2)Table 2 Determination results of four index components in different batches (n = 2)
2.5 化学计量学分析
2.5.1 聚类分析 用SPSS 20.0 软件,以14 批NQP的4 个指标成分含量测定结果为变量,以平方欧式(Euclidean)距离为区间,采用Word 连结法对14 批次NQP 进行聚类分析,结果如图4 所示,可以看出当平方欧氏距离为15 时,14 批NQP 样品可聚为3类,内蒙古蒙药股份有限公司的6 批NQP 样品(S1~S6)和内蒙古库伦蒙药有限公司的1 批NQP样品(S11)聚为一类;内蒙古大唐药业股份有限公司的4 批NQP 样品(S7~S10)聚为一类;乌兰浩特中蒙制药有限公司的3 批NQP 样品(S12~S14)聚为一类。
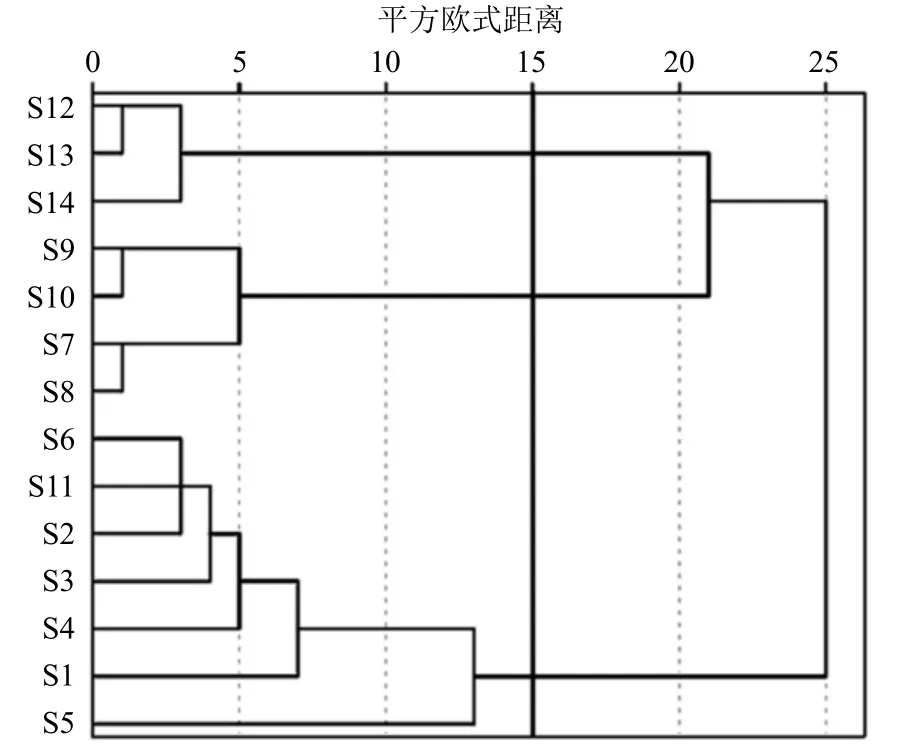
图4 14 批NQP 样品系统聚类分析Fig.4 Systematic cluster analysis of 14 batches of NQP samples
2.5.2 PCA PCA 是以降维为核心思想,是在尽可能保持原有数据信息前提下的一种数据分析方法。采用SIMICA 14.1 软件,以14 批NQP 样品中4 个指标成分含量测定结果为变量进行PCA,结果见图5。有2 个主成分的累积贡献率为98.7%,超过85%。按照PCA 结果可将14 批NQP 划分为3 类:S1~S6、S11 为第I 类,S7~S10 为第II 类,S12~S14为第III 类。PCA 结果与聚类分析结果一致。
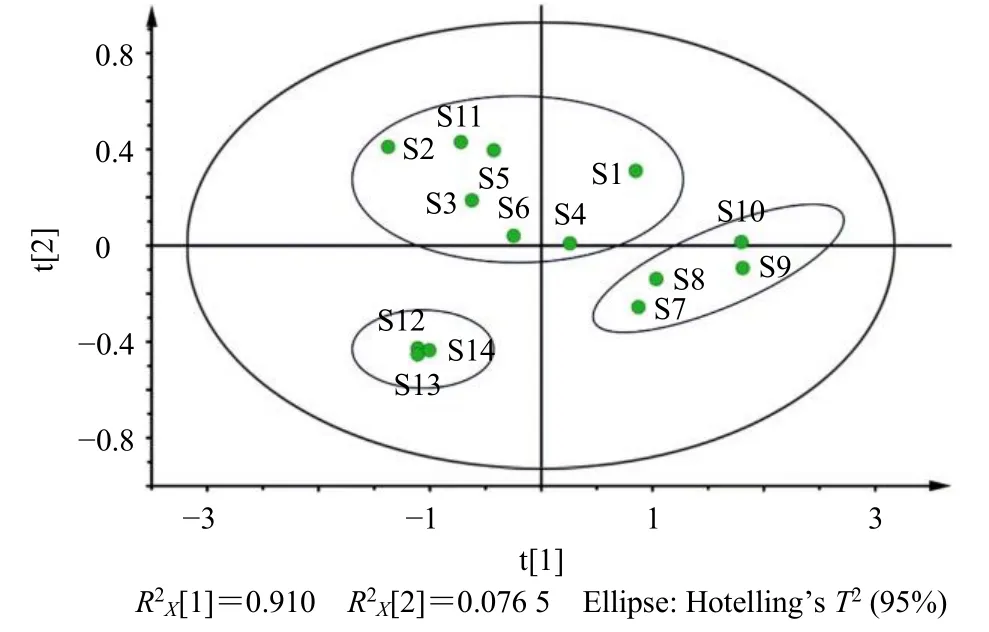
图5 14 批NQP 样品PCA 得分图Fig.5 PCA score chart of 14 batches of NQP samples
为进一步分析4 组分对于PCA 模型的贡献能力,研究其载荷散点图可以发现,丁香酚对第1 主成分的贡献最大,沉香四醇对第2 主成分的贡献度最大,结果见图6。
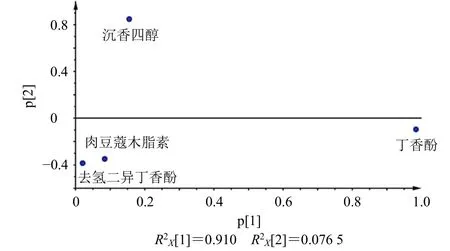
图6 14 批NQP 样品PCA 散点图Fig.6 PCA scatter plot of 14 batches of NQP samples
2.5.3 OPLS-DA 为了进一步比较4 家企业14 批NQP 样品化学成分的差异和寻找各批次含量之间的差异性标志化合物,将14 批次NQP 样品21 个共有峰峰面积为变量进行了OPLS-DA 建模分析。OPLS-DA 模型中,RX2为0.696,Q2为0.597,均大于0.5,说明所建立的模型稳定可靠。由OPLS-DA得分图,结果见图7。14 批NQP 样品明显分为3类,与前述2 种分析方法结果一致。通过变量重要性投影值(variable importance for the projection,VIP)筛选出化学成分差异的主要标志性成分,结果见图8,横坐标为指纹峰号。以VIP 值大于1 作为标准筛选,贡献依次由大到小的VIP 变量为指纹峰10、4、17、15、18、6、14、13、20、12、5、8、21。通过对照品指认出4 个成分,分别为峰6 沉香四醇,峰8 丁香酚,峰14 肉豆蔻木脂素,峰20 去氢二异丁香酚。对差异性的贡献顺序为沉香四醇>肉豆蔻木脂素>去氢二异丁香酚>丁香酚,但4 者均为重要差异性标志化合物,因此可作为指标定量的化合物。
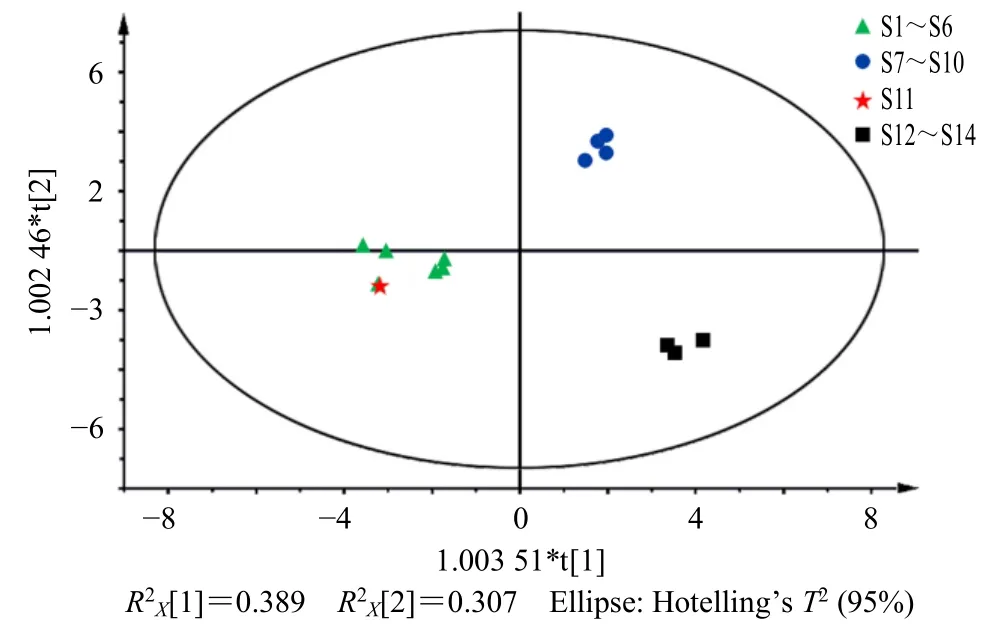
图7 14 批NQP 样品21 个指纹峰的OPLS-DA 得分图Fig.7 OPLS-DA score chart of 14 batches of NQP samples with 21 fingerprint peaks
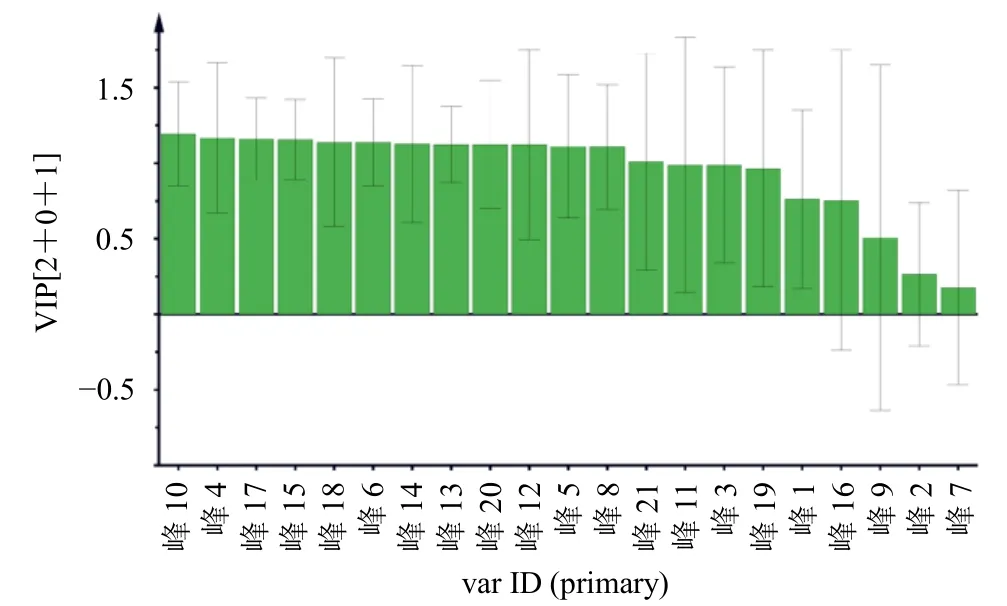
图8 14 批NQP 样品21 个指纹峰的VIP 值分析图Fig.8 VIP value analysis of 21 fingerprint peaks in 14 batches of NQP samples
3 讨论
3.1 处方中部分药材未纳入指纹图谱研究原因分析
通过查阅文献发现,处方中天冬主含甾体皂苷类化学成分[14],目前,这类成分主要采用高效液相色谱-蒸发光散射检测器(HPLC-ELSD)或高效液相色谱-电雾式检测器(HPLC-CAD)建立含量测定方法[15-16]。
黄精多糖是黄精的主要化学成分[17],目前多以硫酸-蒽酮为显色剂,通过紫外分光光度法测定多糖含量[18-19],虽有文献报道采用高效液相色谱-紫外检测器(HPLC-DAD)对黄精中黄酮类化合物进行含量测定[20],但通过实验证明,本品中含量较低,色谱峰较小,无法纳入指纹图谱研究。相对处方中其他药味,针对手掌参的研究资料较少,有研究证明手掌参中含多糖、卞酯糖苷及天麻素等化学成分[21],本实验前期以卞酯糖苷类化学成分dactylorhin A 及天麻素为对照品进行实验[22],发现NQP 中2 种成分含量较低,色谱峰过小,本研究也尝试参照文献方法[23]以腺苷、对羟基苯甲醇为对照品进行试验,结果上述3 种成分最大吸收波长为270 nm,在此波长处,指纹图谱色谱峰数量明显变少,且部分色谱峰无法有效分离,故未将其纳入指纹图谱研究。
3.2 色谱峰归属及对照品指认
液相色谱指纹图谱共出现21 个共有峰,以相应的对照药材制备供试品溶液依法测定,通过保留时间对色谱峰进行归属。结果2、3 号色谱峰为丁香专属,化学成分未知,8 号色谱峰为丁香、肉豆蔻、豆蔻共有,以丁香为主,经对照品指认,该色谱峰化学成分为丁香酚。6、7、13、15、17 号色谱峰为沉香专属,12 号峰为沉香、肉豆蔻共有,《中国药典》2020 年版一部“沉香”项下收载了特征图谱鉴别项,规定有6 个特征峰[24],本指纹图谱研究只获得沉香四醇对照品,经对照品定位6 号色谱峰为沉香四醇。本指纹图谱研究归属肉豆蔻药材色谱峰较多,分别为9、14、16、18~21 号色谱峰,经过对文献资料的梳理,肉豆蔻主含挥发油、木脂素类化学成分[25-26],本研究以肉豆蔻木脂素、去氢二异丁香酚、肉豆蔻醚为对照品进行色谱峰指认,结果14 号色谱峰为肉豆蔻木脂素、20 号色谱峰为去氢二异丁香酚,未成功定位肉豆蔻醚色谱峰,分析原因可能是该成分在原药材中含量较低,加之为挥发性成分,在制剂过程中有损失导致。豆蔻主含挥发油,其中以桉油精为主,含量占比超70%[27],本指纹图谱1 号色谱峰为豆蔻药材专属,参照文献方法以桉油精为对照进行色谱峰定位[28],结果桉油精在该色谱条件下,未出现色谱峰,分析原因,可能因为样品用甲醇提取,桉油精不易溶于甲醇,提取效率不高导致。21个共有峰中19 个色谱峰进行归属,但4、5 号色谱峰不属于上述7 味药材,怀疑可能是在制剂过程中新生成的化学成分。
3.3 指标性成分的选择
本研究通过对指纹图谱共有峰进行OPLS-DA及对含量测定结果聚类分析、PCA 后发现对照品指认的4 种成分可以作为表征本品质量差异性的化合物。结合含量测定方法学研究,4 种成分在同一色谱条件下,色谱峰与相邻色谱峰分离度均大于1.5,通过二极管阵列器检测,未发现不纯物,理论塔板数均大于8 000。故选择此4 种成分作为指标性成分。查阅文献发现肉豆蔻、豆蔻中也含有丁香酚[29-30],试验过程中也进一步验证这一结果,虽然以丁香酚作为丁香指标性化学成分在专属性方面存在缺陷,但考虑到肉豆蔻、豆蔻中丁香酚含量较低,一定程度上也可反映丁香药材的质量。在法标基础上,本研究建立了肉豆蔻专属性化学成分肉豆蔻木脂素的含量测定方法,为肉豆蔻质量控制提供新的依据。
3.4 色谱条件的优化
本研究在条件摸索过程中,利用二极管阵列检测器(DAD)在波长200~370 nm 进行全扫描,以10 nm 为增量导出色谱图进行比对,结果在220 nm波长处,色谱峰数量较多,分离度较好,且能兼顾指标性成分的含量测定,所以指纹图谱的检测波长为220 nm。
流动相体系考察方面,先后考察了乙腈-水、乙腈-水(含0.1%磷酸)、甲醇-水等流动相体系,从混合对照品和样品中被测成分的分离情况、基线的稳定性以及分析时间因素等综合考量,最终选择以甲醇-水为流动相按“2.2”项下方法进行梯度洗脱较为合适。对供试品提取方法进行考察,兼顾提取溶剂选择及提取效率2 方面因素,最终确定提取以甲醇为提取溶剂,超声提取(500 W、40 kHz)30 min 为提取方法。
3.5 指纹图谱相似度及含量测定化学计量学分析结果
本研究采用HPLC 法建立了14 批NQP 样品的指纹图谱,确定了21 个共有峰,指认4 个化学成分。指纹图谱相似度结果表明,不同厂家及批号的样品指纹图谱相似度良好。说明企业按处方要求对丁香、肉豆蔻、豆蔻、沉香进行投料。化学计量学分析结果将NQP 样品按不同生产企业分为3 类,说明不同企业间从生产工艺到原药材质量均存在明显差别。含量测定结果表明,乌兰浩特中蒙制药有限公司沉香四醇含量明显低于其他3 家生产企业,说明该公司沉香原药材质量较差,后期需要关注。
本次研究成功建立了NQP 样品HPLC 指纹图谱及沉香四醇、丁香酚、去氢二异丁香酚、肉豆蔻木脂素的含量测定方法。该方法操作简便,结果稳定,重现性好,可用于NQP 质量控制。生产企业可参照该方法严格生产过程控制,从而保证药品质量稳定,疗效可靠。
利益冲突所有作者均声明不存在利益冲突