基于客观赋权法结合正交优选玉女煎提取工艺
骆艺珠,李 婷,刘 云,张 彤,丁 越
上海中医药大学,上海 201203
经典名方玉女煎,首次记载于明代张景岳的《景岳全书·新方八阵》[1],其由君药石膏,臣药熟地黄,佐药知母、麦冬,使药牛膝5 味药组成。在《中国药典》2020 年版[2]中地黄苷D、知母皂苷BII、芒果苷、β-蜕皮甾酮分别为熟地黄、知母、牛膝的指标成分。其中芒果苷作为主要的有效物质在质量传递过程中,会因为煎煮时间等原因含量产生变化[3]。石膏以及麦冬成分的含量测定由于在标准汤剂中的转移率太小,基本检测不到或者检测条件有限等原因目前并未加入经典名方质量传递的研究中,在后期的研究中将继续开发玉女煎标准汤剂中其他成分的检测方法。
玉女煎具有清胃滋阴的功效主治水亏火盛,六脉浮洪滑大,少阴不足,阳明有余,烦热干渴,头痛牙疼[4-7],失血[8]。在治疗中应用玉女煎加减治疗,可降低血糖[4,6,9-11]、糖化血红蛋白水平,可提升糖尿病临床治疗效果[12]。目前,玉女煎作为经典名方,已被收录于第一批国家中医药管理局所公布的《古代经典名方目录》,可作为3.1 类经典名方新药进行开发。
在经典名方中药复方制剂的开发中要以遵古为基本原则,如何利用现代制剂工艺重现经典名方古法制备工艺,制备出与古方制备的标准煎液质量一致性的现代制剂是经典名方研究的重点。保证现代制剂工艺与传统“古法”工艺两者的产品质量一致性是经典名方研究成功的关键。为了解决该问题,以玉女煎中β-蜕皮甾酮、地黄苷D、芒果苷、知母皂苷BII 转移率和浸膏得率为评价指标,开展其水提工艺的单因素和正交试验考察,这也是目前大部分经典名方现代制剂工艺的主要研究思路[13-15]。
但是分析时发现,在其正交试验数据处理过程中,如果直接采用传统权重法计算综合评分,优选的工艺可能超出标准煎液指标成分的限度范围,不符合中药经典名方现代制剂工艺的研究要求。究其原因,主要是传统的正交试验计算方法以指标成分的转移率或浸膏得率的数值大小进行筛选,并未以与传统“古法”工艺样品的产品质量一致性为目标。
因此,首先采用古法制备玉女煎标准煎液,建立15 批玉女煎标准煎液制备过程中关键参数的范围。以正交试验结合客观赋权法确定各种评价指标在正交试验中的权重系数,进行综合评分。并基于重现古法制备的标准煎液指标工艺为目标,采用公式最终评分(Y)=1/|综合评分-15 批标准煎液平均值综合评分|对各正交试验的综合评分进行数据处理。与传统权重法直接计算获得的提取工艺相比,采用新算法筛选的提取工艺制备的玉女煎提取液中各项指标参数均在玉女煎标准煎液质量控制关键参数范围内,为经典名方玉女煎的现代制剂研究提供技术支持。
1 仪器与材料
1.1 仪器
Agilent-1260 Infinity II 高效液相色谱仪,美国安捷伦公司;Welchrom C18色谱柱,上海月旭科技有限公司;RE-52AA 旋转蒸发器,上海亚荣生化仪器厂;DLSB-5/20 低温冷却液循环泵,郑州长城科工贸有限公司;Centrifuge 5424R 离心机,德国艾本德公司;XS105DU 电子天平,美国梅特勒-托利多公司;ML203T 电子天平,美国梅特勒-托利多公司;SB-5200DTD 超声波清洗机,宁波新芝生物科技股份有限公司;BSA124S 分析天平,赛多利斯科学仪器有限公司;HWS-24 电热恒温水浴锅,上海一恒科学仪器有限公司;XMTD-8222 电热恒温鼓风干燥箱,上海精宏实验设备有限公司;30BII 液体加热器多功能煲,潮州市潮安区康雅顺电器有限公司;SHB-III 循环水式多用真空泵,郑州长城科工贸有限公司;DZF-6096 型真空干燥箱,上海一恒科学仪器有限公司;PTHW2000ML 电热套,郑州科泰实验设备有限公司;600Y 高速多功能粉碎机,永康市铂欧五金制品有限公司;Milli-QAdvantageA10 超纯水系统,美国密理博公司;DW-86L626 医用低温保存箱,青岛海尔生物医疗股份有限公司。
1.2 对照品与试剂
对照品β-蜕皮甾酮(批号111638-201706,质量分数≥98%)、芒果苷(批号111607-201704,质量分数≥95%)、知母皂苷BII(批号111839-202107,质量分数≥98%)均购于中国食品药品检定研究院;对照品地黄苷D,批号040005-202005,质量分数≥98%,上海鸿永生物科技有限公司;甲醇、磷酸,分析纯,均为国药集团化学试剂有限公司;甲醇、乙腈,色谱纯,均为赛默飞世尔科技中国有限公司。
1.3 药材
玉女煎处方中5 味原料药材均收集不少于3 个产地,总批次不少于15 批,优选出品质优良且稳定的符合中药材生产质量管理规范(GAP)要求的药材。经过药材-饮片炮制质量研究,并制定了相对应的质量标准,符合质量标准的纳入15 批饮片并进行排列组合制备15 批标准煎液,具体分组见表1。

表1 玉女煎标准煎液对应饮片批次Table 1 Yunv Decoction standard decoction corresponds to batches of decoction pieces
生石膏(批号201217,产地湖北省孝感市应城市)、熟地黄(批号210218,产地河南省焦作市武涉县)、知母(批号210526,产地河北省安国市)、麦冬(批号210205,产地四川省绵阳市三台县)、牛膝(批号210103,产地河南省焦作市武涉县)为提取工艺研究及标准煎液中地黄苷D含量测定方法所用药材。上述药材均由上海中医药大学中药学院张红梅副教授鉴定,结果石膏均为硫酸盐类矿物硬石膏族石膏,主要成分为含水硫酸钙(CaSO4·2H2O)。生地黄均为玄参科地黄属植物地黄Rehmannia glutinosaLibosch.的新鲜或干燥块根。知母均为百合科知母属植物知母AnemarrhenaasphodeloidesBge.的根茎。麦冬均为百合科麦冬属植物麦冬Ophiopogonjaponicus(L.f) Ker-Gawl.的干燥块根。牛膝均为苋科牛膝属植物牛膝Achyranthes bidentataBl.的干燥根。并按照《中国药典》2020 年版各药材项下检测方法进行检测,均符合药典标准。
2 方法与结果
2.1 玉女煎标准煎液的制备
收集玉女煎处方中的生石膏、熟地黄、知母、麦冬、牛膝各15 批(表1),将以上饮片导入Excel,设定随机编码后进行排列组合,生成15 组随机组合得到的玉女煎标准煎液组合。在国家中医药管理局公布的《古代经典名方目录(第一批)》收录的《景岳全书》中玉女煎的处方为“生石膏三五钱,熟地三五钱或一两,麦冬二钱,知母、牛膝各一钱半,水一盅半,煎七分,温服或冷服”。根据《古代经典名方关键信息表》中剂量为范围值的一般取中间值,又根据明清时期,盅为日常饮水用的小容积茶具,也是药液的约略计量单位,1 盅体积约为200 mL,1 盅半即300 mL。本课题组前期确定玉女煎标准煎液的制备方法为称取生石膏15.0 g、熟地黄15.0 g、麦冬7.5 g、知母5.6 g、牛膝5.6 g 放到煎煮锅中,加入300 mL 的水,浸泡30 min,武火20 min 煮沸,文火20 min 微沸,煮至140 mL,滤过,即得[16-17]。
2.2 玉女煎标准煎液中地黄苷D 含量测定方法的建立
玉女煎汤剂中β-蜕皮甾酮、芒果苷、知母皂苷BII 的含量测定方法已确定[18],本研究建立了玉女煎标准煎液中地黄苷D 的含量检测方法。
2.2.1 色谱条件 色谱柱为Welchrom Ultimate XBC18柱(250 mm×4.6 mm,5 μm);流动相为乙腈-0.1%磷酸水溶液,梯度洗脱:0~15.00 min,3%~8%乙腈;15.00~15.01 min,8%~20%乙腈;15.01~30.00 min,20%~28%乙腈;30.00~35.00 min,28%~3%乙腈;体积流量为1.0 mL/min;检测波长为203 nm;柱温为30 ℃;进样量为10 µL。在此条件下地黄苷D 与其他组分能实现完全分离(R≥1.5),理论板数按地黄苷D 峰计算不低于5 000。
2.2.2 对照品溶液的制备 取地黄苷D 对照品适量,精密称定,加25%甲醇溶解并定容至相应刻度,70.000 μg/mL 的地黄苷D 对照品溶液。
2.2.3 供试品溶液的制备 精密移取玉女煎标准煎液1 mL 于2 mL 量瓶中,加50%甲醇定容,摇匀,过0.45 μm 微孔滤膜,取续滤液,即得供试品溶液。
2.2.4 阴性样品溶液的制备 按经方组成称取除熟地黄以外的饮片,按“2.2.3”项下方法制备,即得阴性样品溶液。
2.2.5 方法学考察 按照中药含量分析要求,对本方法进行专属性、线性关系、加样回收率、精密度、重复性、稳定性等方法学考察实验。
(1)专属性考察:分别精密吸取地黄苷D 对照品溶液、玉女煎标准煎液供试品溶液与阴性样品溶液10 μL,按“2.2.1”项下色谱条件分别进样分析,记录色谱图。结果检测过程中无干扰供试品溶液成分,表明本实验专属性良好,结果见图1。

图1 地黄苷D 对照品 (a)、玉女煎标准煎液样品 (b) 和阴性样品 (c) 的HPLC 图Fig.1 HPLC of rehmannioside D reference substance (a),Yunv standard decoction sample (b) and negative sample (c)
(2)线性关系的考察:精密移取适量对照品溶液,用25%甲醇进行稀释后分别得到质量浓度为4.257、8.514、42.570、106.400、170.300、1 064.000 μg/mL 的对照品溶液。将上述6 种质量浓度对照品溶液各10 μL 进样,以地黄苷D 的质量浓度为横坐标(X),峰面积为纵坐标(Y),得到标准曲线Y=5.294 3X-7.877 9,r=0.999 9,结果表明地黄苷D在质量浓度4.257~1 064.000 μg/mL 线性关系良好。
(3)精密度考察:分别取低、中、高质量浓度(4.257、42.570、1 064.000 µg/mL)地黄苷D 对照品溶液各10 μL 进样,按“2.2.1”项下色谱条件进行地黄苷D 含量测定,重复进样6 次,实验结果表明,RSD 分别为0.25%、0.06%、0.24%,说明该含量方法的精密度良好。
(4)稳定性考察:按“2.2.3”项下方法制备供试品溶液,取同一供试品溶液,分别于室温下放置0、2、4、6、8、12、24 h,按“2.2.1”项下色谱条件进行玉女煎标准煎液中地黄苷D 含量测定,结果其峰面积的RSD 为2.90%,表明供试品溶液在24 h内稳定性良好。
(5)重复性考察:按“2.2.3”项下制样方法,平行制备6 份供试品溶液,按“2.2.1”项下色谱条件进行玉女煎标准煎液中地黄苷D 含量的测定,实验结果表明,6 次含量测定结果分别为755.7、719.9、758.9、767.1、763.7、749.1 μg/g,平均质量分数为752.4 μg/g,RSD 为2.30%,结果表明该含量测定方法重复性良好。
(6)加样回收率考察:分别取0.5 mL 已知测定指标成分含量的玉女煎标准煎液9 份,加入相当于样品中指标成分含量50%、100%、150%的对照品,按“2.2.3”项下方法制备供试品溶液,平行处理3份,按“2.2.1”项下色谱条件进行样品中地黄苷D含量测定,结果表明,该方法测定复方中地黄苷D的平均加样回收率为102.1%,RSD 为2.85%,结果表明该实验准确性良好。
2.3 玉女煎标准煎液中指标成分量值传递规律及关键参数确定
采用本课题组前期建立的玉女煎标准煎液中β-蜕皮甾酮、芒果苷和知母皂苷BII 含量测定方法[17],并在此基础上,建立了玉女煎标准煎液中地黄苷D的含量测定方法。将上述方法用于分析15 批玉女煎标准煎液指标成分的转移率。参考《中国药典》2020 年版,测定玉女煎标准煎液的浸膏得率。按照《按古代经典名方目录管理的中药复方制剂药学研究技术指导原则(试行)》,制定了标准煎液中β-蜕皮甾酮、芒果苷、知母皂苷BII、地黄苷D 的转移率以及浸膏得率的范围。采用HPLC 法对15 批玉女煎标准煎液供试品进行HPLC 分析,测定结果见表2。

表2 玉女煎中4 个指标成分在饮片-标准煎液的转移率及浸膏得率Table 2 Transfer rate and extract yield of four index components of Yunv Decoction in decoction slices and standard decoction
转移率=测得的标准煎液中有效成分的质量分数/所用饮片中有效成分的质量分数
由表2 结果可知,地黄苷D 从熟地黄饮片到标准煎液的转移率均值为60.73%,15 批标准煎液(S1~S15)中地黄苷D 的转移率为46.70%~74.27%,在均值的70%~130%(42.51%~78.95%)。芒果苷从知母饮片到标准煎液的转移率均值为56.86%,15 批标准煎液(S1~S15)中芒果苷的转移率为42.60%~72.56%,在均值的70%~130%(39.82%~73.95%)。知母皂苷BII 从知母饮片到标准煎液的转移率均值为33.85%,15 批标准煎液(S1~S15)中知母皂苷BII 的转移率为27.75%~40.15%,在均值的70%~130%(23.70%~44.01%)。β-蜕皮甾酮从牛膝饮片到标准煎液的转移率均值为63.58%,15 批标准煎液(S1~S15)中β-蜕皮甾酮的转移率为52.16%~74.63%,在均值的70%~130%(44.51%~82.67%)。浸膏得率均值为29.21%,15 批标准煎液(S1~S15)的浸膏为27.03%~31.44%,在均值的90%~110%(26.29%~32.13%)。
故初步确定标准煎液中地黄苷D 的转移率为42.51%~78.95%,芒果苷的转移率为39.82%~73.95%,知母皂苷BII 转移率为23.70%~44.01%,β-蜕皮甾酮转移率为44.51%~82.67%,浸膏得率为26.29%~32.13%,作为现代制剂提取工艺筛选实验的标准。
2.4 玉女煎提取工艺的优选
2.4.1 单因素考察提取次数和提取时间
(1)提取次数:按处方的2 倍量,称取石膏30.00 g,熟地黄30.00 g,知母11.19 g,麦冬14.92 g,牛膝11.19 g,加9 倍量的水加入到圆底烧瓶中,浸泡30 min,加热回流40 min,用100 目尼龙纱布滤过。按上述方法,分别提取1、2、3 次,合并煎液。平行处理3 份,考察不同提取次数对玉女煎标准煎液中主要化学成分提取率和浸膏得率的影响。结果显示,提取次数对玉女煎标准煎液中β-蜕皮甾酮、芒果苷、知母皂苷BII、地黄苷D 转移率和浸膏得率影响较大,结果见表3。其中提取3 次,各项指标均超出标准煎液的范围;提取2 次,除了地黄苷D 的转移率外,其他4 个指标都超出标准煎液的范围。提取1 次,除了浸膏得率超出标准煎液的范围,其他4 个指标均在范围内,可能与其提取时间过长有关,需要进一步优化其提取时间。故选择提取次数为1 次。
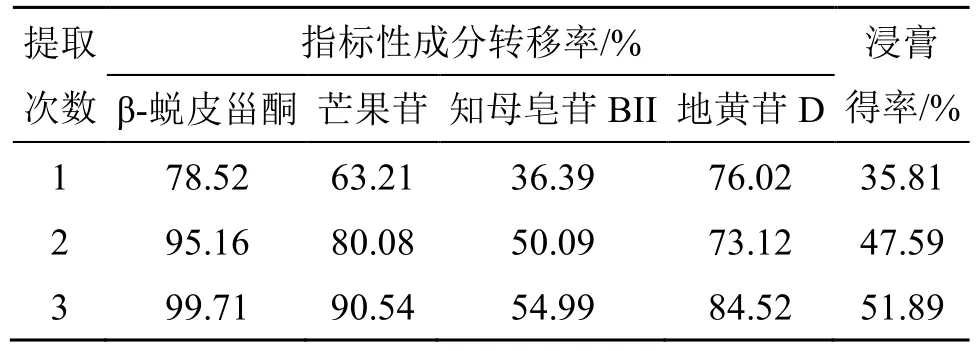
表3 提取次数对玉女煎中指标成分转移率的影响 (n = 3)Table 3 Effects of extraction times on transfer rate of index components in Yunv Decoction (n = 3)
(2)提取时间:按处方的2 倍量,称取石膏30.00 g,熟地黄30.00 g,知母11.19 g,麦冬14.92 g,牛膝11.19 g,加9 倍量的水加入到圆底烧瓶中,浸泡30 min,分别加热回流30、60、90 min,平行处理3 份。考察不同提取时间对玉女煎标准煎液中主要化学成分提取率和浸膏得率的影响。结果显示,提取时间对玉女煎标准煎液中各项指标均有较大影响,结果见表4。提取60 min 和90 min 的玉女煎标准煎液中,芒果苷的转移率、浸膏得率或地黄苷D转移率超出标准煎液的范围。而提取30 min 的玉女煎标准煎液中,β-蜕皮甾酮、芒果苷、知母皂苷BⅡ、地黄苷D 转移率均在15 批水煎液转移率的70%~130%范围内,浸膏得率最接近15 批标准煎液转移率的90%~110%,故初步确定玉女煎水煎提取时间为30 min。
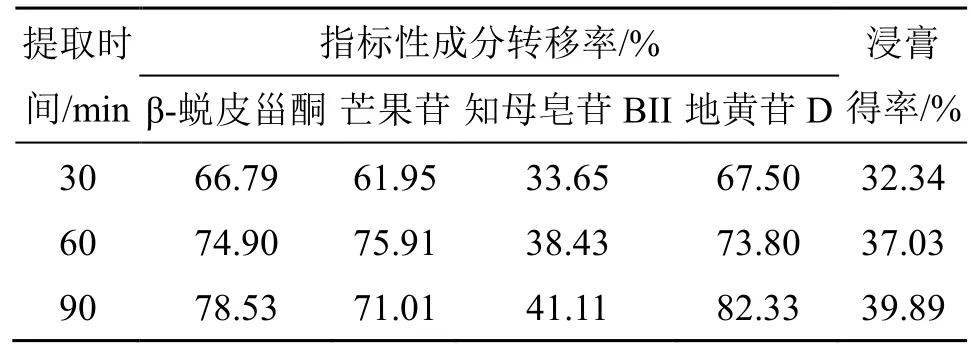
表4 提取时间对玉女煎中指标成分转移率的影响 (n = 3)Table 4 Effects of extraction time on transfer rate of index components in Yunv Decoction (n = 3)
2.4.2 正交试验考察玉女煎的提取工艺 在单因素实验结果基础上,进一步采用正交试验优选玉女煎的提取纯化工艺,以加水量(A)、浸泡时间(B)和提取时间(C)3 个因素为考察对象,以提取物中的β-蜕皮甾酮、芒果苷、地黄苷D 和知母皂苷BII的转移率,浸膏得率为指标,分别采用传统权重法和客观赋权法设计的新算法,筛选与标准煎液平均评分接近的现代制剂工艺。
(1)正交试验设计:在单因素实验结果基础上,选择提取时间为20、30、40 min,加水量为8、10、12 倍量,浸泡时间为0、15、30 min 进行正交试验设计,结果见表5。
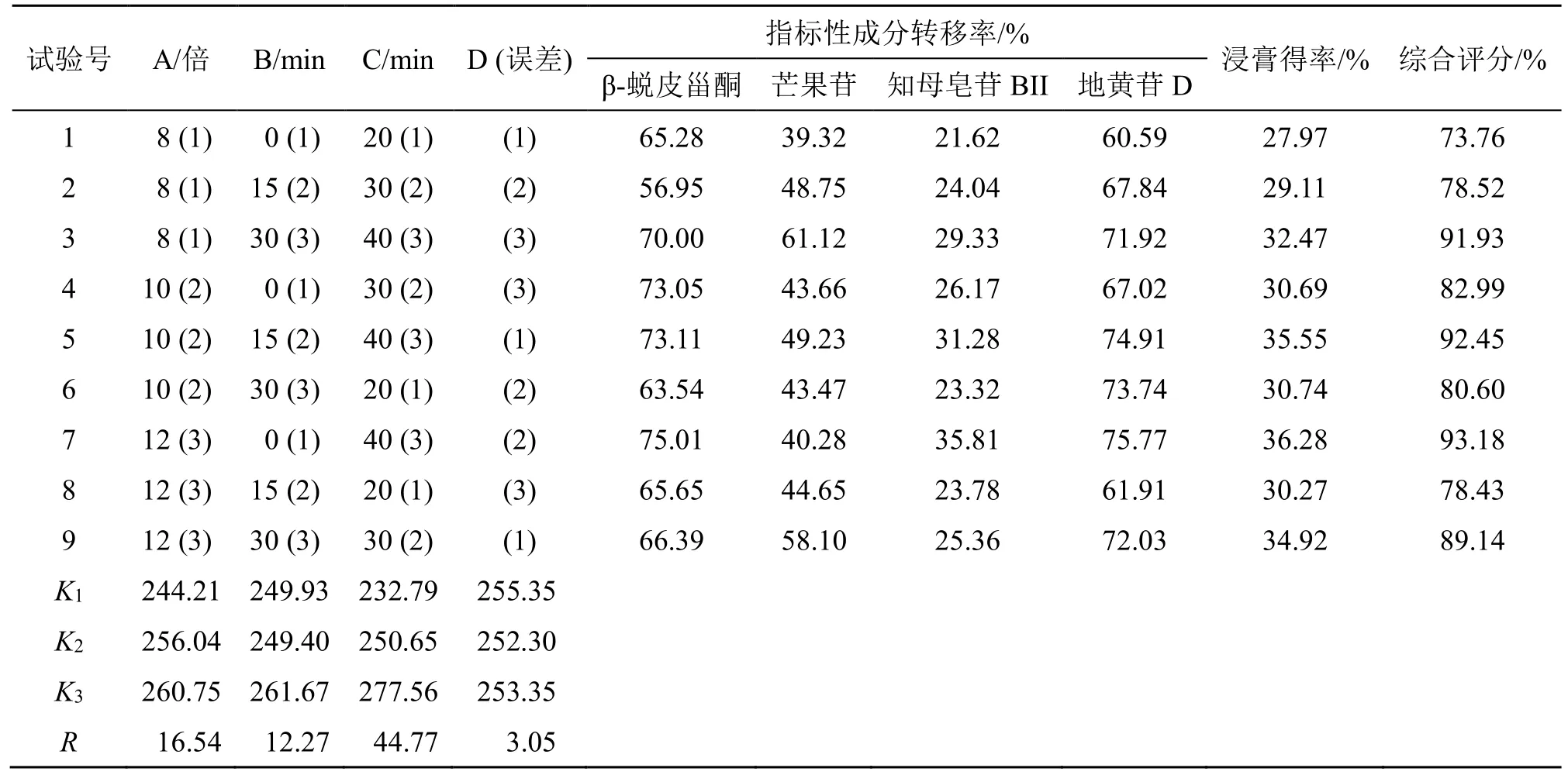
表5 玉女煎现代制剂提取工艺传统L9(34)正交试验设计与结果Table 5 Traditional orthogonal experiment of Yunv Decoction for modern preparation technology
(2)正交提取试验传统数据处理方法:以提取物中的β-蜕皮甾酮、芒果苷、地黄苷D、知母皂苷BII 和浸膏得率为指标进行综合评分[18-19],正交试验结果见表5。
综合评分=∑(各个成分转移率/各个成分最高转移率×0.2)
正交试验方直观分析结果表明各因素对综合评分影响大小依次为提取时间(C)>加水量(A)>浸泡时间(B)。方差分析结果表明,加水量、提取时间对综合评分的影响有统计学意义(P<0.05)。结合直观分析中K值大小选择,最佳提取工艺为A3B3C3,即加入12 倍水,浸泡30 min,提取40 min,结果见表6。
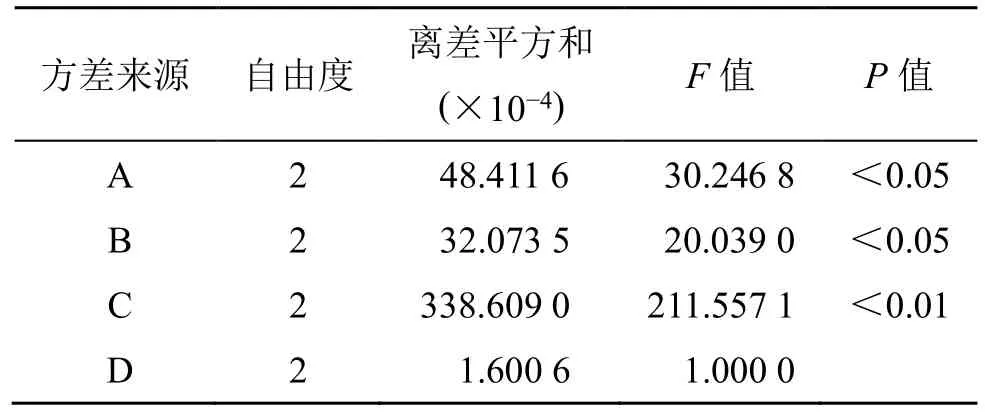
表6 方差分析结果Table 6 Results of analysis of variance
(3)验证试验:3 批玉女煎提取工艺验证实验结果显示β-蜕皮甾酮、地黄苷D、知母皂苷BⅡ的转移率和浸膏得率平均值分别为76.11%、52.87%、81.62%、32.62%、36.14%,RSD 为4.55%、1.99%、6.05%、1.44%、1.50%,见表7。与玉女煎标准煎液相比,上述指标浸膏得率超出15 批标准煎液的关键参数范围,不符合经典名方现代制剂工艺要求,需要探索新方法进行玉女煎提取工艺优化。
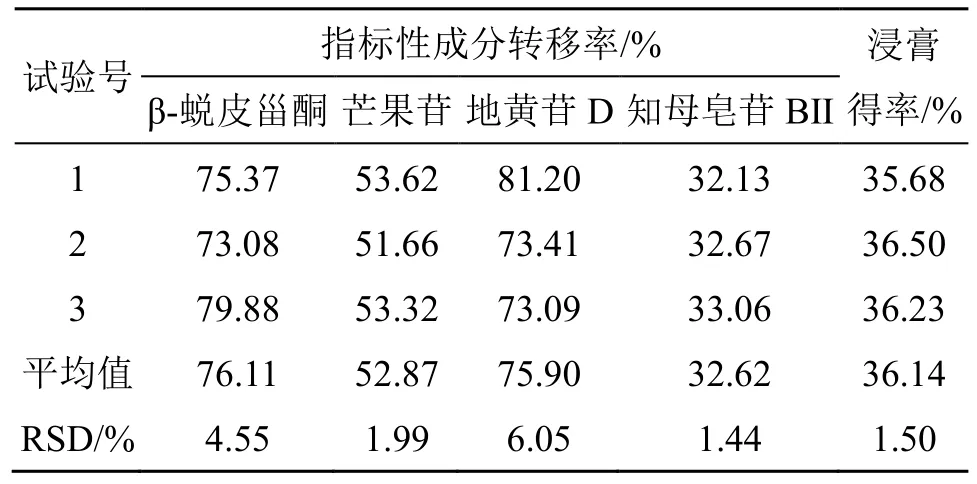
表7 玉女煎工艺验证试验结果Table 7 Results of Yunv Decoction technology validation test
2.4.3 正交提取试验新方法数据处理 《按古代经典名方目录管理的中药复方制剂药学研究技术指导原则(试行)》文件要求。文章将以按古籍记载内容制备的标准煎液中β-蜕皮甾酮、芒果苷、知母皂苷BII、地黄苷D 转移率和浸膏得率的范围为标准。由于玉女煎现代制剂正交试验研究过程中,存在多指标权重问题。
同时,优选的现代制剂工艺应在标准煎液各项指标范围内,为避免实验者主观想法影响实验结果,因此未采用层次分析法,而是单独采用客观赋权法先获得正交试验中β-蜕皮甾酮、芒果苷、知母皂苷BII、地黄苷D 转移率和浸膏得率的权重系数,并以15 批标准煎液平均值综合评分为基准值,设计公式最终评分(Y)=1/|综合评分-15 批标准煎液平均值综合评分|对正交试验的综合评分进行预处理,此数值越大说明在该指标下的现代工艺参数制得的样品与标准煎液相似度越高,并作为正交试验最终评分,由此得到最佳的提取工艺。流程图如图2 所示。并将该算法优选的提取工艺与传统权重法优选的提取工艺进行比较,论证本算法的合理性。

图2 方法流程图Fig.2 Flow chart of method
(1)客观赋权法确定权重:客观赋权法是一种能客观反映实际样本数据的权重计算方法,该法以某特征类间的对比强度和特征间的冲突性为基础,通过标准偏差的形式体现对比强度,以指标间的相关性体现指标间的冲突性,能够客观地反映指标间的相互作用。本研究拟采用客观赋权法确定各指标间的权重,将表中的数据按以下公式进行线性插值处理。进行数据标准化之后,根据SPSS PRO(https://www.spsspro.com/)网址中客观赋权法处理得到指标变异性、指标冲突性、信息量与权重等参数,其中β-蜕皮甾酮、芒果苷、地黄苷D、知母皂苷BII,浸膏得率的客观权重系数分别为16.56%、40.17%、12.49%、19.82%、10.95%,结果见表8。

表8 CRITIC 法相关计算数据Table 8 Critic-related computational data
指标成分值=实测值/最大值
(2)玉女煎提取工艺数据处理的优化:根据客观赋权法获得各项指标的权重系数,并按照公式(1~6)计算各正交试验综合评分值(F)。
以15 批标准煎液平均值综合评分为基准值,设计公式:1/|综合评分-15 批标准煎液平均值综合评分为82.81%|,按照公式(7),对正交试验的综合评分进行预处理,获得各正交试验的最终评分(Y),并将其用于正交试验数据处理,筛选玉女煎提取的最佳工艺。
2.4.4 正交试验优化玉女煎提取工艺
(1)正交提取试验传统数据处理方法:正交试验设计与结果见表9。直观分析结果(表10)表明,各考察因素对综合评分影响大小依次为提取时间(C)>浸泡时间(B)>加水量(A)。由直观分析中K值大小选择,最佳提取工艺为A2B1C2,即加入10 倍水,提取30 min。但是方差分析结果(表11)显示,加水量、浸泡时间对正交各实验的综合评分无显著性影响,在实验过程中,发现玉女煎提取时间仅为30 min,提取前用水进行浸泡15 min,有利于药材提取的稳定性,故此次选择的最佳工艺为A2B2C2。
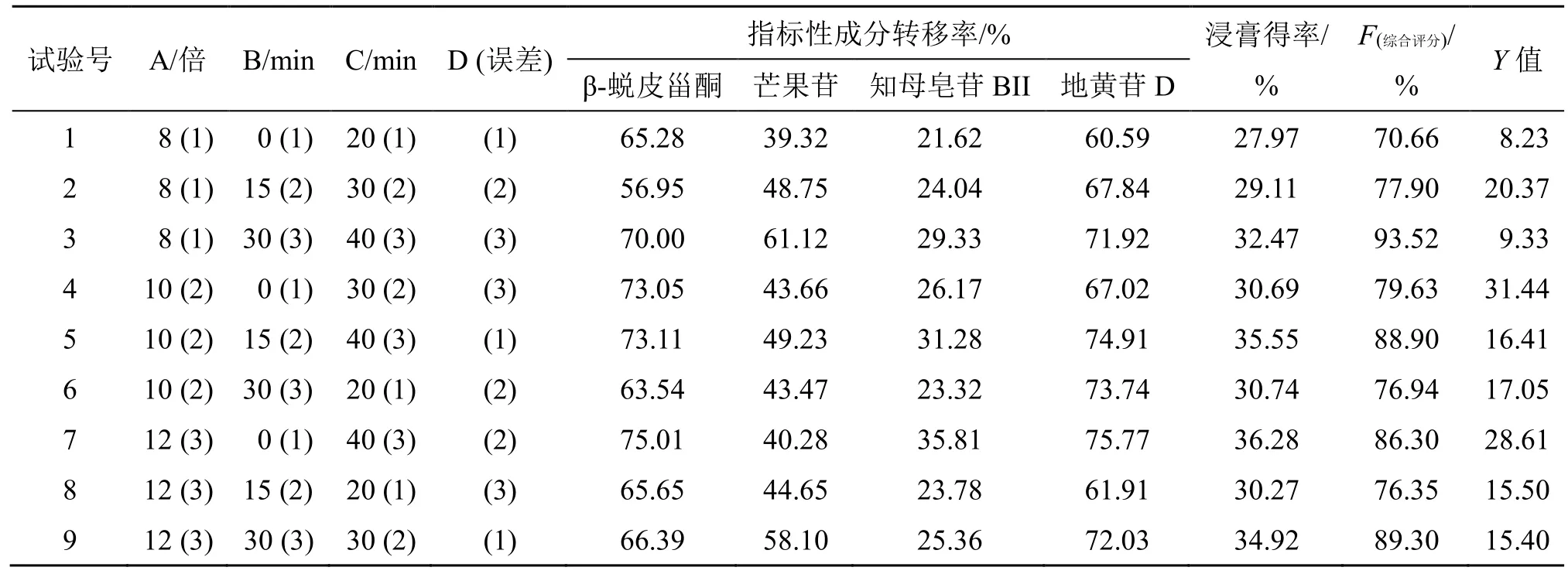
表9 玉女煎现代制剂提取工艺正交试验设计与结果Table 9 Design and results of orthogonal experiment of Yunv Decoction for modern preparation technology
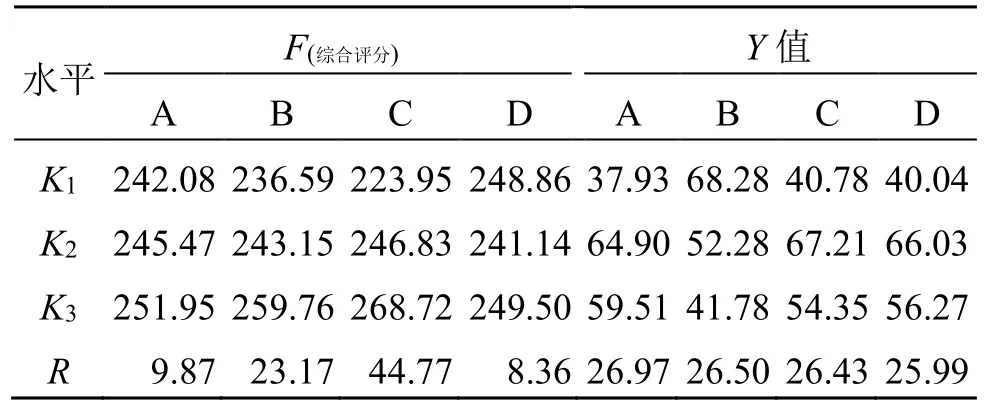
表10 直观分析结果Table 10 Results of analysis of variance

表11 方差分析结果Table 11 Results of analysis of variance
(2)优化正交验证试验:验证实验结果表明,3 批玉女煎提取工艺验证其β-蜕皮甾酮、芒果苷、地黄苷D、知母皂苷BⅡ的转移率和浸膏得率平均值为66.54%、45.86%、64.30%、29.14%和32.11%,RSD 为4.08%、6.09%、3.15%、8.55%和0.04%。与玉女煎标准煎液相比,上述指标均未超出标准煎液范围,证明了通过客观赋权法优化的正交计算方式更为合理,结果见表12。

表12 玉女煎工艺验证试验结果Table 12 Results of Yunv Decoction technology validation test
3 讨论
经典名方玉女煎的煎煮方法按照古籍记载,药材炮制完,以水为提取溶剂,最终根据失水量来确定提取时间,而现代工艺大多是以饮片投料,提取方式大多是“封闭性”的回流提取方式,这就造成了古方煎煮工艺与工业生产的实际工艺严重不符[20-21]。目前有很多文献还基于正交试验传统数据处理,得出的结果会偏向于成分转移率和浸膏得率越大越好的结果,从而容易超出指标的限度范围。因此以标准煎液的质量标准为基准整体评价提取工艺包括浸泡时间、提取时间、提取次数、加水量等因素,确定与传统工艺基本一致的现代提取工艺参数显得尤为重要。
目前,采用正交试验优选中药复方的提取纯化工艺,是较为常用的研究方法。但是在正交试验结果数据处理过程中,通常优选的工艺以某些成分的转移率或浸膏得率的最高条件为优,并不是以重现经典名方的标准煎液为目标。在本实验中,采用传统的正交试验算法,优选的提取工艺所制备的提取液中各指标均超出标准煎液的范围。因此,本实验以加水量、浸泡时间和提取时间3 个因素为考察对象,以提取物中的β-蜕皮甾酮、芒果苷、地黄苷D、知母皂苷BII 的转移率和浸膏得率为指标用客观赋权法进行权重分析,计算综合评分,筛选与标准煎液平均评分接近的提取工艺水平。为避免传统计算方法造成的转移率或浸膏得率最大为最优结果的缺点,以15 批标准煎液平均值综合评分为基准值,设计公式最终评分(Y)=1/|综合评分-15 批标准煎液平均值综合评分|对正交试验的综合评分进行预处理,此数值越大说明在该指标下的现代工艺参数制得的样品与标准煎液相似度越高,并作为正交试验最终评分,从而得出经典名方提取工艺正交试验新的评价方法。通过验证实验比较,新算法筛选的工艺制备出的提取物中各指标均在玉女煎标准煎液的范围内,可以较好地重现玉女煎标准煎液的条件,为经典名方的开发提供了新的思路和方法。
利益冲突所有作者均声明不存在利益冲突