KCl活化核桃壳热解制备的生物炭对亚甲基蓝的吸附性能
刘 翠,徐世艾,张 庆,殷国俊
(烟台大学化学化工学院,山东 烟台 264005)
目前,从工业废水中脱除染料的方法主要有吸附法[1-2]、生物降解法[3]、氧化法[4]和膜分离法[5]等,其中吸附法在实际操作中被大量使用和研究,被认为是最有效的方法之一。制约吸附法性能好坏的关键因素是吸附剂的选择,常见的吸附剂包括炭材料、沸石分子筛和蒙脱土等[3]。相比于其他吸附材料,炭材料具备环境友好、制备成本低、再生容易等特点,已成为处理染料废水的主要吸附材料[1]。
炭材料种类繁多,包括煤质炭、生物炭、复合炭材料等。生物炭是生物质热解后剩余的固体产物,该材料具有发达的孔隙结构、丰富的表面化学性质,在能源、化工、环保等领域应用广泛[6]。为了提高生物炭的性能,通常会对生物炭进行物理或化学活化,物理活化是指在热解过程中通入CO2和水蒸气来改变生物炭的物化性质[6];化学活化是指将生物质与化学试剂(HF、H3PO4、KOH、KCl、NaOH等)混合后进行热解[7-8]。与物理活化法相比,化学活化法具有操作简单、制备时间短等优点,但是化学活化制备的生物炭会残留大量的化学试剂,它们如何影响生物炭对染料的吸附性能,目前文献中尚无该方面的报道。
基于上述讨论,本研究利用KCl与核桃壳混合热解制备生物炭,测量KCl活化生物炭对亚甲基蓝吸附性能,与直接热解的生物炭进行对比,并采用SEM、XRD、FTIR和N2吸脱附对样品进行表征,来分析活化前后生物炭对亚甲基蓝吸附性能差异产生的原因。该研究对于指导生物炭的制备,实现对染料废水的高效处理具有理论指导和实用价值。
1 实验部分
1.1 生物炭的制备
将核桃壳磨碎至 20~40目,在 120 ℃ 下干燥2 h,即得到核桃壳颗粒。取10 g核桃壳颗粒置于管式电炉中,在N2气氛下以10 ℃/min的加热速率升至800 ℃,停留15 min后冷却至室温,即得到核桃壳炭(Walnut-shell biochar,标记为Wb)[6]。
采用浸渍法在核桃壳颗粒中添加质量分数为1%的KCl,按照上述步骤进行热解实验,即得到KCl活化的核桃壳炭(标记为K-Wb)[9]。
为了分析KCl对亚甲基蓝吸附性能的影响,对核桃壳炭进行处理。采用浸渍法在Wb上负载质量分数为1%的KCl,标记为Wb-K。对K-Wb和Wb-K进行水洗,按照每克样品和150 mL去离子水混合,搅拌1h后抽滤,重复操作5次,来降低它们所含KCl的浓度,水洗后的核桃壳炭分别标记为K-Wb(d)和Wb-K(d)。
1.2 吸附实验
将0.05 g不同处理的核桃壳炭与100 mL亚甲基蓝溶液混合,分别放入25、35、45 ℃恒温振荡器(150 r/min)中进行吸附实验。采用紫外可见分光光度计(UV-1780,岛津仪器有限公司)在664.5 nm波长下测定溶液中的亚甲基蓝的吸光度。配置2、4、6、8、10 mg/L的亚甲基蓝溶液,测定其吸光度,质量浓度(C)与吸光度(x)的关系是C=12.13x+0.036。平衡吸附量(qe,mg/g)由式(1)计算:

(1)
式中:C0和Ce分别为亚甲基蓝初始质量浓度和吸附平衡质量浓度(mg·L-1);V为溶液体积(L);m为核桃壳炭的质量(g)。
1.3 表征分析
利用扫描电子显微镜(SEM,JSM-7900F)分析核桃壳炭的表观形貌;采用X射线衍射仪(XRD,Rigaku SmartLab Ⅲ,Japan)对核桃壳炭进行晶体结构测试,用Cu Kα X射线(0.154 nm)作为激发源,扫描速度为10°/min,扫描范围为10~80°;利用红外光谱(FT-IR,Shimadzu IRAffinity-1S)测定核桃壳炭的表面官能团,与KBr按质量比1∶200混合研磨,称取0.1 g压片,扫描范围为4000~400 cm-1;采用气体吸附仪(Quantachrome,USA)测定核桃壳炭的孔径分布,以N2作为吸附质,分压P/P0的范围为10-3~1,吸附温度为77 K。
2 结果与讨论
2.1 核桃壳炭对亚甲基蓝的吸附性能
首先,对比Wb和K-Wb在25 ℃下对亚甲基蓝染料的吸附性能,结果如图1。从图1可以看出,KCl活化制备的核桃壳炭K-Wb对亚甲基蓝染料的吸附较大,这说明KCl活化有助于提高生物炭对亚甲基蓝染料的脱除能力。吸附量的增大可能与KCl的添加或者核桃壳炭物化性质的改变有关,为此又测量了Wb-K、K-Wb(d)和Wb-K(d)对亚甲基蓝的吸附性能。经过不同处理的五种核桃壳炭对亚甲基蓝的吸附性能不同,从大到小依次为:K-Wb(d)> K-Wb> Wb> Wb-K(d)> Wb-K。Wb-K的吸附性能最低,KCl是水溶性的,经水洗后Wb-K(d)的吸附量增大,但是仍低于Wb的吸附量。此外,K-Wb经水洗后吸附量也增大了,这说明KCl的存在不利于亚甲基蓝的吸附。上述结果表明,KCl活化核桃壳炭对亚甲基蓝吸附量的增大可能与核桃壳炭物化性质的改变有关。
2.2 吸附剂的表面形貌
为了分析KCl对核桃壳炭物化性质的影响,利用SEM对其表观形貌进行表征,如图2。Wb含有大量的孔道结构,KCl改性后的K-Wb表面除了大量孔道外,还出现了大量的固体颗粒附着在孔道附近。由于KCl的负载,Wb-K的孔道减少了,其表面也出现了固体小颗粒,这些固体小颗粒应该是KCl,这说明KCl可能堵塞Wb的孔道。经水洗之后,K-Wb(d)表面固体颗粒含量减少,而且孔道数量也显著增多,这说明KCl改性可以增加生物炭孔道数量;Wb-K(d)表观形貌的变化与K-Wb(d)的一样,进一步证明KCl可以堵塞生物炭的孔道。值得注意的是,水洗可以有效脱除生物炭中所含的KCl。
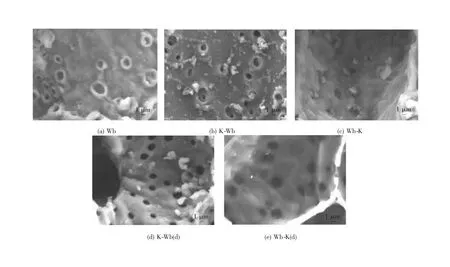
图2 核桃壳炭的SEM图
2.3 吸附剂的晶体结构
利用XRD对核桃壳炭的晶体结果进行分析,如图3。可以看出,本研究所制备的生物炭在2θ=23°和43°附近出现两个弥散的宽峰,没有形成石墨碳的(002)和(100)晶面[9]。对于K-Wb和Wb-K,除了生物炭的衍射峰外,还出现其他物质的衍射峰。通过对比标准谱图库,发现这些衍射峰是KCl晶体产生的。XRD表征结果说明KCl改性后的生物炭中会残留KCl,负载法也可以增加生物炭的KCl含量。经水洗之后,K-Wb(d)和Wb-K(d)的KCl特征衍射峰消失,说明水洗可以脱除生物炭所含的部分KCl,这与SEM的结果一致。

图3 核桃壳炭的XRD图
2.4 表面官能团分析

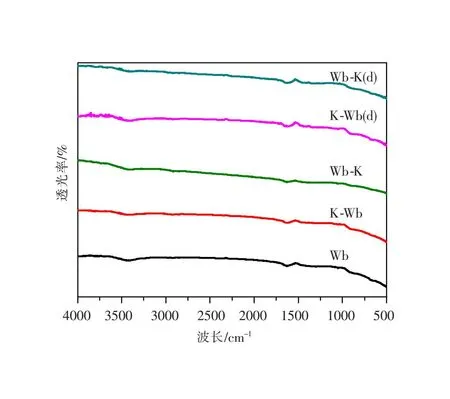
图4 样品的红外光谱图
2.5 孔结构分析
上述结果表明,KCl改性可以促进核桃壳炭孔道的形成,为了进一步考察KCl活化对核桃壳炭孔结构的影响,对Wb和K-Wb进行N2吸脱附测试,结果如图5。所有样品的吸附等温线属于第Ⅲ类吸附等温线,说明本研究所制备生物炭属于中孔炭[9]。利用BJH方法计算获得孔结构分布情况,如图6。所有样品的孔径主要分布在3 nm以下,K-Wb的孔道数量比Wb的多,这与前面的表征结果一致,KCl改性法可以促进核桃壳炭3 nm以下孔结构的形成。Wb-K的孔含量最低,说明KCl可以堵塞部分孔道。然而,水洗处理之后,K-Wb(d)和Wb-K(d)的孔含量均高于K-Wb和Wb-K的,说明部分KCl可以被水洗脱除,重新暴露出来的孔道成为亚甲基蓝的吸附位点。

图5 N2吸脱附等温线

图6 BJH方法分析孔结构
2.6 吸附机理
为了分析亚甲基蓝在K-Wb上的吸附机理,对该吸附过程进行详细的研究。图7是K-Wb在不同温度下对亚甲基蓝的吸附等温线,随着平衡浓度的增大,吸附量增大;随着吸附温度的升高,吸附量增大。利用Langmuir方程(2)和Freundlich方程(3)对吸附等温线进行拟合[1],如图8。
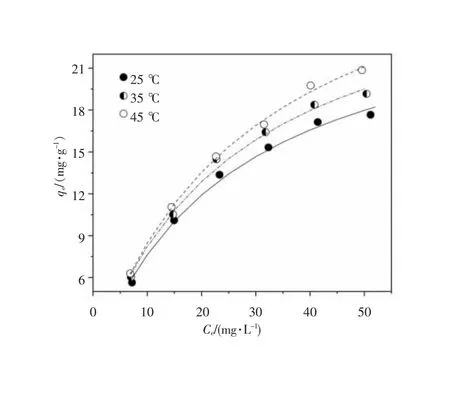
图7 不同温度下生物炭对亚甲基蓝染料的吸附

图8 吸附等温线拟合

(2)
式中:qm是最大吸附量;KL是等温线系数。
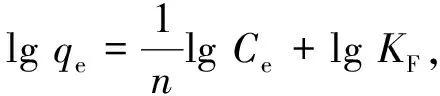
(3)
式中:KF、n为与吸附剂、吸附质和吸附温度有关的常数。
表1列出了Langmuir和Freundlich方程的拟合参数。显然,Langmuir方程对实验数据的拟合度较好(R2>0.99),不同温度下拟合的最大吸附量与实验结果相符合,这表明亚甲基蓝在K-Wb上的吸附是单层吸附过程[1-2]。
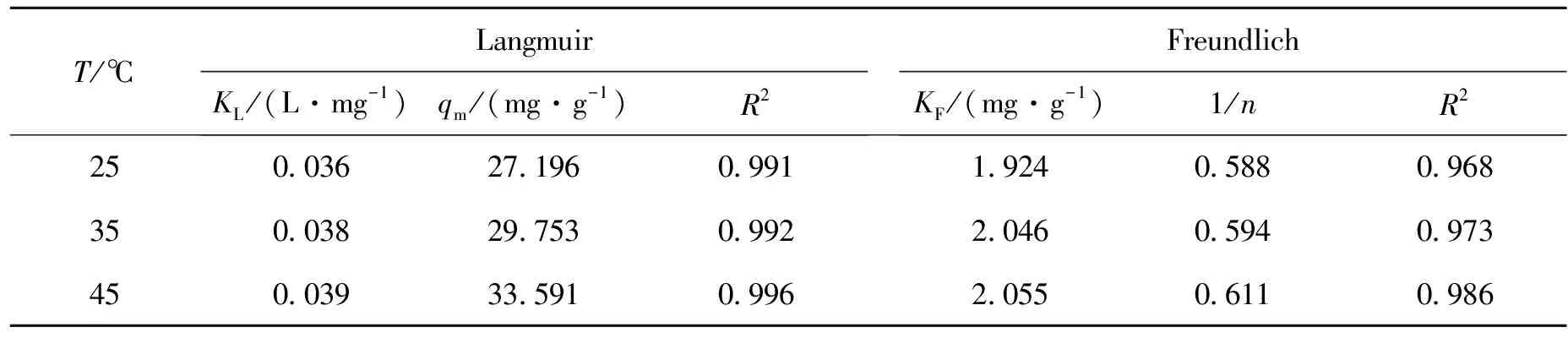
表1 Langmuir和Freundlich方程的拟合参数
为了进一步确定亚甲基蓝的吸附机理,计算了自由能(ΔG0)、焓(ΔH0)和熵(ΔS0)。这些参数的计算公式为[1]

(4)
ΔG0=-RTlnKL,
(5)
式中:R是理想气体常数;KL是Langmuir方程等温线常数(L·mg-1);T是温度(℃)。
如表2,ΔG0<0,说明K-Wb对亚甲基蓝的吸附过程是自发进行的,不需要外界能量的参与;0 <ΔH0<42 kJ·mol-1,说明吸附过程是物理吸附,且吸附过程吸热;ΔS0>0,表明吸附过程是随机且无序地进行[10]。

表2 热力学参数
3 结 论
相比于直接热解获得的核桃壳炭,KCl活化法制备的核桃壳炭对亚甲基蓝的吸附量更大。KCl的添加会增加核桃壳炭的孔道数量,尤其是小于3 nm的中孔,而对表面官能团的形成没有影响。核桃壳炭上的KCl会堵塞部分孔道,经水洗后部分KCl被脱除,可以使被堵塞的孔道暴露出来。经过设计实验和对样品物化性质的表征分析,发现KCl对亚甲基蓝的吸附不起作用,孔道数量的多少是影响生物炭对亚甲基蓝吸附量大小的关键因素。利用Langmuir和Freundlich方程对吸附等温线进行拟合,结果表明Langmuir方程的拟合度较高。热力学计算分析证明亚甲基蓝在KCl活化法制备的核桃壳炭上的吸附为自发的物理吸附过程。

