钙通道阻滞剂1,4-二氢吡啶类药物的绿色合成
谢建武, 刘俊男, 谢玄升
(陕西科技大学 生物与医药学院, 陕西 西安 710021)
0 引言
心脏及心脑血管疾病是发达国家人群的第一死因,也是中国人死亡的首位原因.因而,心血管系统的创新药物研究已成为世界各国医学及药学领域的科学家们关注的热点.全世界正在研究开发的3 000多种新药中几乎有 1/4~1/3 的品种与心血管系统有关.心血管系统药物种类繁多.它不仅需要对冠心病、脑卒中或脑栓塞等疾病本身进行药物治疗,而且与这些疾病有关的症状如高血压、心律不齐、心力衰竭、心绞痛等以及形成这类疾病的病因,如高血脂、动脉粥样硬化等因素也需要用药物防治,可见在本类药物中除治疗性药物外预防性药物也占有重要的份额.

钙通道阻滞剂作为治疗心血管系统药物的使用是重大发现,不但在疾病治疗上具有重大价值,而且推动了离子通道作为一个新的药物靶点,进行深入的基础及应用研究,具有划时代的意义.
1882年,化学家Arthur Hantzsch首次合成了1,4- 二氢吡啶( 1,4-DHP)[1].随后,1,4- 二氢吡啶类钙通道阻滞剂作为一类新结构类型药物[2],硝苯地平(nifedipine)于1975年上市,是该类中第一个上市的药物,此后几十年,已成功地研制了许多1,4- 二氢吡啶类药物.此外,该类化合物具有其他很好的生理活性,在生物、医药等方面有广泛应用.如抗肿瘤[3]、消炎[4]、镇痛[5]、抗血小板凝聚[6]、抗糖尿病活性[7,8],也作为帕金森疾病的抗脑萎缩剂[6]和肿瘤治疗的化疗剂[9,10].目前,有十几个重要的1,4-二氢吡啶类钙通道阻滞剂,如非洛地平、氨氯地平、尼莫地平,作为药物在全球内生产和使用[11],如图1所示.
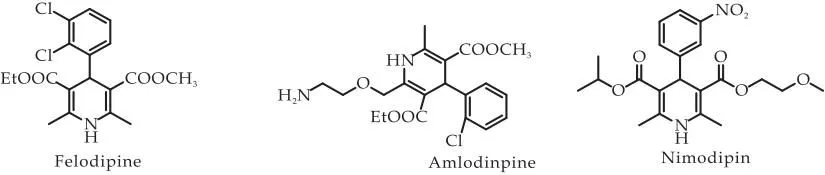
图1 具有表性的1,4- 二氢吡啶类钙通道阻滞剂
由于1,4- 二氢吡啶类钙通道阻滞剂的重要性,国内外对该类钙通道阻滞剂的合成十分活跃.目前,合成该类化合物的策略和方法有微波法[12]、超声波法[13]、离子液体法[14]、相转移催化剂法[15]、布朗斯酸法[16]、无溶剂法[17]、路易斯酸法[18]等.然而,大多数方法存在许多不足,如反应时间长、产率低、后处理繁琐、大量使用有机溶剂、催化剂无法回收利用、大批量生产工业化比较困难等.最近,国内化学家蔡小华等[19]、刘竹兰等[20]课题组在合成1,4-二氢吡啶类钙通道阻滞剂也取得了较好的结果.但是,发展一种简单、高效的1,4-二氢吡啶类钙通道阻滞剂合成方法仍然是十分必要的.本文提供一种以Amberlyst 15离子交换树脂作为催化剂,无溶剂下高效的合成1,4-二氢吡啶类钙通道阻滞剂的方法.该方法还有三个显著的特点:(1)催化剂可以回收利用;(2)反应可以放大,对收率影响不大;(3)该反应后处理简单,有望实现工业化生产.
1 实验部分
1.1 试剂与仪器
WRS-1B 数字熔点仪(温度计未经校正); Bruker Avance 400型或600型核磁共振波谱仪(DMSO-d6或CDCl3为溶剂,TMS为基准物质);有机反应用薄层硅胶板(TLC)跟踪监测.德国Bruker高分辨质谱仪(BioTOFⅢQ).
1.2 合成1,4- 二氢吡啶类钙通道阻滞剂的一般步骤
在25 mL的烧瓶里,加入芳香醛(10 mmol)、乙酰乙酸乙酯(2.6 g,20 mmol)和醋酸铵(1.0 g,13 mmol),以及100 mg的Amberlyst 15,搅拌下加热到90 ℃反应1 h,待反应完成后,趁热滤弃催化剂,并用少量乙醇洗涤.将滤液密封好,冷冻,即析出大量晶体,过滤,乙醇洗涤,干燥即得到纯的产物.滤液可以进一步浓缩,继续析出晶体,或者母液浓缩后柱层析(石油醚∶乙酸乙酯=4∶1),将所得的产物合并,可以得到较好的收率.
对于反应过程如果产生的产物是固体的,则过滤,并用少量乙醇洗涤;随后过滤的固体溶于二氯甲烷,过滤,回收催化剂.滤液通过减压旋转蒸发仪回收溶剂,同时得到目标产物.
1.3 催化剂回收利用
在25 mL的烧瓶里,加入苯甲醛(50 mmol)、乙酰乙酸乙酯(100 mmol)和醋酸铵(65 mmol),搅拌下加热到90 ℃反应1 h,待反应完成后,趁热过滤,少量乙醇洗涤催化剂,直接用于下一次反应.
1.4 放大反应
在250 mL的烧瓶里,加入苯甲醛(300 mmol)、乙酰乙酸乙酯(600 mmol)和醋酸铵(390 mmol),搅拌下加热到90 ℃反应1 h,待反应完成后,趁热过滤,滤液冷却后,置于冰箱冷冻,析出晶体,过滤,得到目标产物.
2 结果与讨论
经过文献调研,发现利用酸,如硫酸[21]、负载硫酸[21]、负载高氯酸[22]作为催化剂,可以催化合成1,4-二氢吡啶类钙通道阻滞剂的合成.然而,他们所利用的催化剂存在不能回收利用或者催化剂合成困难,成本高,不利工业化生产.Amberlyst 15离子交换树脂是一种固体酸催化剂,广泛应用于酯化、 烷基化、酰化、醚化、缩合、水合等化学合成的反应,它不溶于溶剂,反应后可以通过简单的过滤回收利用.本文直接购买商业化的Amberlyst 15 离子交换树脂作为催化剂,考察了他们在不同温度及不同介质的反应情况(如方程式(1)和表1所示).如表1所示,在Amberlyst 15 离子交换树脂(200 mg)催化下,苯甲醛(10 mmol)、乙酰乙酸乙酯(20 mmol)、醋酸铵(13 mmol)的摩尔比为1∶2∶1.3进行条件筛选.以水为溶剂在70 ℃反应1个小时,收率仅为52%(如表1,entry 1所示),而在无溶剂下反应收率达到72%(如表1,entry 2所示).本研究也尝试在相同条件下,将反应置于水热反应釜中进行反应,但是收率明显低于在常压搅拌下的反应(如表1,entries 3~4所示),原因可能是在水热反应釜无法搅拌,反应物无法进行充分接触反应.通过温度筛选,反应在90 ℃及无溶剂条件下,1 h后,苯甲醛完全消失,收率可以达到92%(如表1,entry 5所示).接着,降低催化剂的用量,本文发现,1 h后,苯甲醛同样消失,分离收率没有多大的变化(如表1,entry 6所示).

表1 反应条件的优化
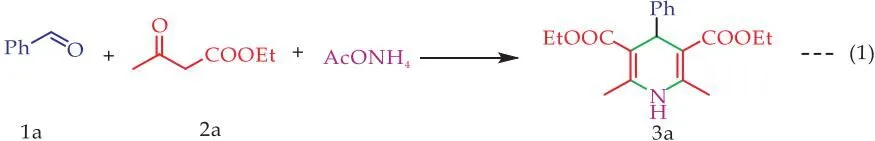
在优化的条件(无溶剂,Amberlyst 15 离子交换树脂为催化剂,90 ℃下反应)下,考察了芳香醛上取代基电子效应对该反应的影响(如图2所示).从图2可以看出:(1)反应的适用范围比较广.所有的反应在60 min内都可以反应完全,收率为72%~95%;(2)带有供电子基团(CH3,-OCH3)的反应进行了60 min后,收率只有72%(3b,3c).反之,带有拉电子基团的芳香醛,在该反应体系可以获得较为满意的结果,收率最高可以达到93%(3c-3i);(3)对于带有杂环的醛,如2-呋喃甲醛及2-噻吩甲醛,在该反应条件下,15 min内就产生大量固体,反应完全,分离收率分别为88%和90%(3j-3k);(4)芳环上位阻效应不明显,如芳环上取代基是氯时,分别在邻位(3f)、间位(3e)和对位(3d),收率都非常高(88%~93%).
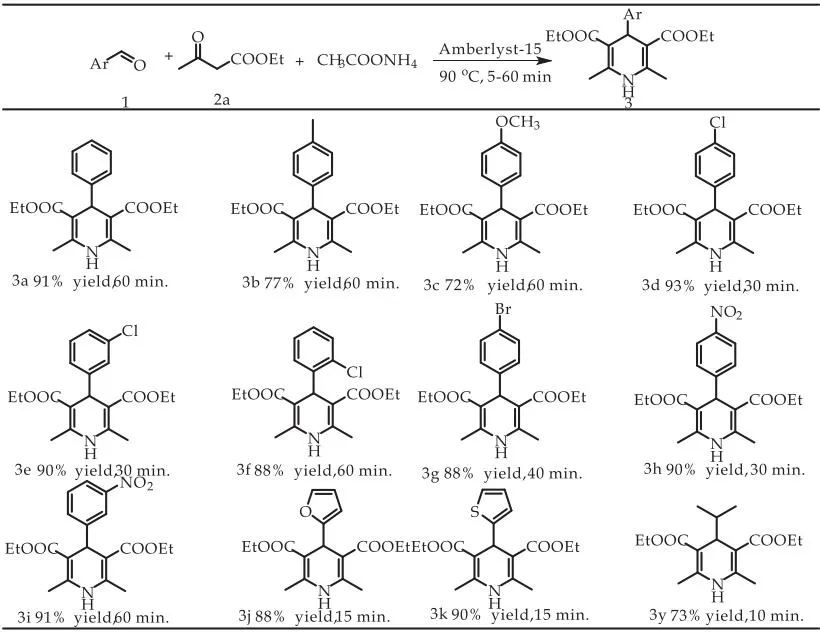
图2 基于芳香甲醛和β-酮酸酯的底物的扩展
在获得了一系列含有两个酯基的1,4-二氢吡啶类钙通道阻滞剂后,本研究转向合成含有其他官能团,如含有酮羰基的新型的1,4-二氢吡啶类钙通道阻滞剂,例如,以1,3-二酮代替乙酰乙酸乙酯,则可以合成含有二酮基的1,4-二氢吡啶类钙通道阻滞剂,如图3所示.

图3 基于1,3-二酮的底物扩展
首先,以1,3-戊二酮为反应底物,反应得以顺利进行,有趣的是,主要产物并不是1,4-二氢吡啶类钙通道阻滞剂,而是直接被氧化得到了吡啶衍生物,收率非常高(3l-3n,90%~95%).但是,以环状的1,3-环己二酮为底物时,则可以顺利获得1,4-二氢吡啶类钙通道阻滞剂,收率也很高,但是芳香甲醛上芳环上有拉电子基团要比有供电子基团的活性高,在相同时间收率也比较高,产物一般可以直接通过乙醇洗涤、二氯甲烷洗涤,可以得到纯度为95%左右的产物(3o-3s).当芳香醛为水杨醛时,反应也能顺利进行,但是收率偏低(3t-3w).
由于Amberlyst 15离子交换树脂不溶于反应体系,本文对它的回收利用进行了研究(如方程式(2)和表2所示).将反应在优化条件下进行反应,当反应完毕后,趁热过滤,少量乙醇洗涤,回收得到催化剂,不需要进一步处理,直接进行下一次反应,经过10次使用后,该催化剂还保留着高的催化活性,转化率可以达到100%,收率变化不大,始终介于86%~91%之间.

表2 催化剂的回收利用

最后,本文对反应放大进行了研究.如方程式(3)所示,将反应放大30倍,可以一次获得约83克目标产物,收率为84%.

基于以上结果,本文对反应机理进行了推测,如图4所示.在酸性的条件下,苯甲醛质子化得到活化,乙酰乙酸乙酯I进攻活化的苯甲醛,接着失去一分子水得到Knoevenagel产物III,随后质子化得到中间体IV.乙酰乙酸乙酯与醋酸铵发生反应得到烯胺V,烯胺进攻中间体IV得到中间体VI,最后失去一分子水得到目标产物3.
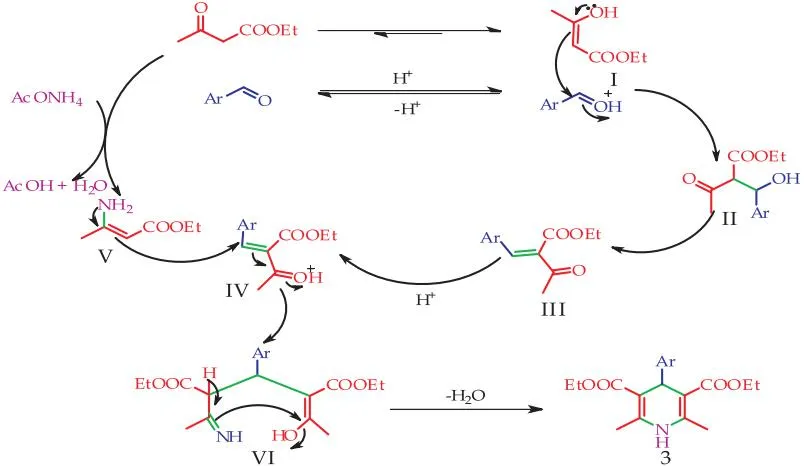
图4 可能的反应机理
3 产物的表征数据
3,5-Pyridinedicarboxylic acid,1,4-dihydro-2,6-dimethyl-4-phenyl-,3,5-diethyl ester (3a) Yellow solid M.p.155-157 ℃.1H NMR (600 MHz,CDCl3) δ 7.32 - 7.25 (m,2H),7.20 (t,J=7.6 Hz,2H),7.14 - 7.10 (m,1H),5.58 (s,1H),4.99 (s,1H),4.13 - 4.04 (m,4H),2.33 (s,6H),1.22 (t,J=7.1 Hz,6H).13C NMR (150 MHz,CDCl3) δ 167.7,147.8,143.9,128.0,127.8,126.1,104.1,59.7,39.6,19.6,14.3; 高分辨质谱m/z:计算值 C19H24NO4(M+H)+330.170 0,测量值 330.169 1.
3,5-Pyridinedicarboxylic acid,1,4-dihydro-2,6-dimethyl-4-(4-methylphenyl)-,3,5-diethyl ester(3b) Yellow solid M.p.129-130 ℃.1H NMR (600 MHz,CDCl3) δ 7.19 (d,J=8.0 Hz,2H),7.04(d,J=7.9 Hz,2H),5.75 (s,1H),4.97 (s,1H),4.15 - 4.07 (m,4H),2.34 (s,6H),2.30 (s,3H),1.26 (t,J=7.1 Hz,6H).13C NMR (151 MHz,CDCl3) δ 167.72 (s),144.89 (s),143.83 (s),135.54 (s),128.59 (s),127.85 (s),104.25 (s),59.75 (s),39.10 (s),21.09 (s),19.62 (s),14.28 (s); 高分辨质谱m/z:计算值 C20H26NO4(M+H)+344.185 6,测量值 344.185 1.
3,5-Pyridinedicarboxylic acid,1,4-dihydro-4-(4-methoxyphenyl)-2,6-dimethyl-,3,5-diethyl ester (3c) Yellow solid M.p.156-158 ℃.1H NMR (600 MHz,CDCl3) δ7.23 - 7.17 (m,2H),6.77 - 6.72 (m,2H),5.58 (bs,1H),4.93 (s,1H),4.14 - 4.03 (m,4H),3.75 (s,3H),2.32 (s,6H),1.23 (t,J=7.1 Hz,6H).13C NMR (150 MHz,CDCl3) δ 167.7,157.9,143.5,140.3,129.0,113.2,104.4,59.7,55.1,38.7,19.6,14.3 高分辨质谱m/z:计算值 C20H26NO5(M+H)+360.180 5,测量值 360.180 1.
3,5-Pyridinedicarboxylic acid,4-(4-chlorophenyl)-1,4-dihydro-2,6-dimethyl-,3,5-diethyl ester (3d) Yellow solid M.p.197-199 ℃.1H NMR (600 MHz,CDCl3) δ7.24 (d,J=8.5 Hz,2H),7.19 (d,J=8.5 Hz,2H),5.65 (bs,1H),4.98(s,1H),4.18 - 4.01 (m,4H),2.35 (s,6H),1.24 (t,J=7.1 Hz,6H);13C NMR (150 MHz,CDCl3) δ 167.4,146.3,143.9,131.7,129.4,127.9,103.9,59.8,39.3,19.6,14.3; 高分辨质谱m/z:计算值 C19H23ClNO4(M+H)+364.131 0,测量值 364.129 1.
3,5-Pyridinedicarboxylic acid,4-(3-chlorophenyl)-1,4-dihydro-2,6-dimethyl-,3,5-diethyl ester (3e) Yellow solid M.p.142-144 ℃.1H NMR (600 MHz,CDCl3) δ7.26 (t,J=1.7 Hz,1H),7.20 (dt,J=7.5,1.4 Hz,1H),7.16 (t,J=7.6 Hz,1H),7.14 - 7.10 (m,1H),5.64 (bs,1H),4.99 (s,1H),4.21 - 4.03 (m,4H),2.37 (s,6H),1.25 (t,J=7.1 Hz,6H);13C NMR (150 MHz,CDCl3) δ 167.3,149.7,144.1,133.6,129.0,128.2,126.3,126.2,103.7,59.8,39.7,19.6,14.2; 高分辨质谱m/z:计算值 C19H23ClNO4(M+H)+364.131 0,测量值 364.130 4.
3,5-Pyridinedicarboxylic acid,4-(2-chlorophenyl)-1,4-dihydro-2,6-dimethyl-,3,5-diethyl ester (3f) Yellow solid M.p.120-121 ℃.1H NMR (600 MHz,CDCl3) δ 7.40 (dd,J=7.8,1.6 Hz,1H),7.25 (dd,J=7.9,1.1 Hz,1H),7.14 (td,J=7.6,1.1 Hz,1H),7.06 (td,J=7.8,1.6 Hz,1H),5.79 (s,1H),5.42 (s,1H),4.14 - 4.06 (m,4H),2.32 (s,6H),1.22 (t,J=7.1 Hz,6H).13C NMR (151 MHz,CDCl3) δ 167.70 (s),145.63 (s),143.93 (s),132.47 (s),131.62 (s),129.29 (s),127.32 (s),126.70 (s),103.86 (s),59.79 (s),37.53 (s),19.56 (s),14.31 (s); 高分辨质谱m/z:计算值 C19H24NO4(M+H)+364.131 0,测量值364.130 9.
3,5-Pyridinedicarboxylic acid,4-(4-bromophenyl)-1,4-dihydro-2,6-dimethyl-,3,5-diethyl ester (3g) Yellow solid M.p.165-166 ℃.1H NMR (600 MHz,CDCl3) δ7.32 (d,J=8.3 Hz,2H),7.16 (d,J=8.3 Hz,2H),5.60 (bs,1H),4.94(s,1H),4.14 - 4.04 (m,4H),2.33 (s,6H),1.22 (t,J=7.1 Hz,6H);13C NMR (150 MHz,CDCl3) δ 167.4,146.8,143.9,130.9,129.8,119.9,103.9,59.8,39.3,19.6,14.3; 高分辨质谱m/z:计算值 C19H23BrNO4(M+H)+408.080 5,测量值 408.076 8.
3,5-Pyridinedicarboxylic acid,1,4-dihydro-2,6-dimethyl-4-(4-nitrophenyl)-,3,5-diethyl ester (3h) Yellow solid M.p.113-114 ℃.1H NMR (600 MHz,CDCl3) δ1H NMR (600 MHz,CDCl3) δ 8.11 (d,J=8.7 Hz,2H),7.47 (d,J=8.7 Hz,2H),5.73 (bs,1H),5.12 (s,1H),4.16 - 4.06 (m,4H),2.38 (s,6H),1.24 (t,J=7.1 Hz,6H);13C NMR (150 MHz,CDCl3) δ 167.0,155.1,146.4,144.5,128.9,123.3,103.3,60.0,40.1,19.7,14.3; 高分辨质谱m/z:计算值 C19H23N2O6(M+H)+375.155 1,测量值 375.154 3.
3,5-Pyridinedicarboxylic acid,1,4-dihydro-2,6-dimethyl-4-(3-nitrophenyl)-,3,5-diethyl ester (3i) Yellow solid M.p.163-164 ℃.1H NMR (600 MHz,CDCl3) δ 8.14 (s,1H),8.04 - 8.00 (m,1H),7.66 (d,J=7.6 Hz,1H),7.39 (t,J=7.9 Hz,1H),5.98 (s,1H),5.11 (s,1H),4.18 - 4.02 (m,4H),2.38 (s,6H),1.24 (t,J=7.1 Hz,6H).13C NMR (151 MHz,CDCl3) δ 167.16 (s),149.95 (s),148.14 (s),144.81 (s),134.55 (s),128.61 (s),123.13 (s),121.34 (s),103.30 (s),60.02 (s),39.97 (s),19.61 (s),14.24 (s); 高分辨质谱m/z:计算值 C19H24NO4(M+H)+375.155 1,测量值375.154 9.
3,5-Pyridinedicarboxylic acid,4-[4-(2-furanyl)phenyl]-1,4-dihydro-2,6-dimethyl-,3,5-diethyl ester (3j) Yellow solid M.p.162-163 ℃.1H NMR (600 MHz,CDCl3) δ7.25-7.23 (dd,J=1.7,0.8 Hz,1H),6.24 (dd,J=3.1,1.8 Hz,1H),5.97 (d,J=3.1 Hz,1H),5.72 (bs,1H),5.22 (s,1H),4.29 - 4.09 (m,4H),2.36 (s,6H),1.29 (t,J=7.1 Hz,6H);13C NMR (150 MHz,CDCl3) δ 167.4,158.6,144.9,140.9,110.0,104.4,100.8,59.8,33.4,19.6,14.3; 高分辨质谱m/z:计算值 C17H22NO5(M+H)+320.149 2,测量值 320.149 0.
3,5-Pyridinedicarboxylic acid,1,4-dihydro-2,6-dimethyl-4-[4-(2-thienyl)phenyl]-,3,5-diethyl ester (3k) Yellow solid M.p.184-185 ℃.1H NMR (600 MHz,CDCl3) δ7.07 (d,J=5.0 Hz,1H),6.89 - 6.84 (m,1H),6.83 - 6.81 (m,1H),6.07 (bs,1H),5.37 (s,1H),4.27 - 4.11 (m,4H),2.35 (s,6H),1.29 (t,J=7.1 Hz,6H);13C NMR (150 MHz,CDCl3) δ 167.4,151.6,144.6,126.3,123.2,123.1,103.6,103.5,59.9,34.4,19.4,14.3; 高分辨质谱m/z:计算值C17H22NO4S (M+H)+336.126 4,测量值 336.126 7.
2,6-Dimethyl-4-iso-propyl-1,4-dihydropyridine-3,5-dicarboxylic acid diester (3y) White solid M.p.89-91 ℃.1H NMR (600 MHz,CDCl3) d 4.33-4.11 (m,4H),3.95 (d,J=5.6 Hz,1H),2.33(s,6H),1.71-1.65 (m,1H),1.31 (t,J=7.1 Hz,6H),0.86 (d,J=6.8 Hz,6H).13C NMR (150 MHz,CDCl3) d 168.3,145.2,102.1,60.3,39.1.8,35.9,19.7,18.9,14.8.高分辨质谱m/z:计算值 C16H25NO4(M+H)+296.185 6,测量值 296.186 1.
(3,5-Diacetyl-2,6-dimethyl-4-phenylpyridine (3l) Yellow solid M.p.183-184 ℃.1H NMR (600 MHz,CDCl3) δ 7.58 - 7.55 (m,2H),7.48-7.46 (m,3H),2.59 (s,3H),2.57 (s,3H),2.23 (s,3H),2.00 (s,3H).13C NMR (151 MHz,CDCl3) δ 206.1,205.9,154.6,152.5,139.5,139.1,136.3,134.6,129.5,128.9,32.3,32.2,22.7,21.4,16.2; 高分辨质谱m/z:计算值 C17H18NO2(M+H)+268.133 2,测量值 268.132 7.
3,5-Diacetyl-2,6-dimethyl-4-(4-methylphenyl)pyridine (3m) Yellow solid M.p.156-157 ℃.1H NMR (600 MHz,CDCl3) δ 7.46 (d,J=8.1 Hz,2H),7.27 (d,J=7.9 Hz,2H),2.58 (s,3H),2.55 (s,3H),2.42 (s,3H),2.21 (s,3H),2.01 (s,3H).13C NMR (151 MHz,CDCl3) δ 206.1,205.9,154.6,152.5 139.5,139.1,136.3,134.6,129.5,128.9,32.3,32.2,22.7,21.4,16.2; 高分辨质谱m/z:计算值 C18H20NO2(M+H)+282.148 9,测量值 282.147 3.
3,5-Diacetyl-4-(4-chlorophenyl)-2,6-dimethylpyridine (3n) Yellow solid M.p.173-174 ℃.1H NMR (600 MHz,CDCl3) δ 7.54 - 7.50 (m,2H),7.45 (d,J=8.4 Hz,2H),2.58 (s,3H),2.56 (s,3H),2.22 (s,3H),2.05 (s,3H).13C NMR (151 MHz,CDCl3) δ 205.8,205.5,153.1,152.7,139.3,137.6,136.8,135.7,130.9,130.4,129.4,129.1,32.3,22.7,16.2; 高分辨质谱m/z:计算值 C17H17ClNO2(M+H)+302.094 2,测量值302.093 6.
9-Phenylacridine-1,8-dione (3o) Yellow solid M.p.276-277 ℃,1H NMR (600 MHz,DMSO-d6) δ9.45 (s,1H),7.21 - 7.13 (m,4H),7.08-7.00 (m,1H),4.92 (s,1H),2.56 - 2.50 (m,4H),2.22-2.19 (m,4H),1.94 - 1.90 (m,2H),1.81 - 1.77 (m,2H);13C NMR (150 MHz,DMSO-d6) δ194.9,151.4,147.4,127.8,127.6,125.5,112.5,36.8,32.2,26.4,20.9; 高分辨质谱m/z:计算值 C19H20NO2(M+H)+294.148 9,测量值294.149 3.
3,4,6,7,9,10-Hexahydro-9-(4-methylphenyl)-1,8(2H,5H)-acridinedione (3p) Yellow solid M.p.>300 ℃.1H NMR (600 MHz,DMSO-d6) δ 9.43 (s,1H),7.03 (d,J=8.0 Hz,2H),6.95 (d,J=7.9 Hz,2H),4.86 (s,1H),2.51 (s,5H),2.24 - 2.16 (m,7H),1.91 (dt,J=13.0,4.9 Hz,2H),1.83 - 1.72 (m,2H).13C NMR (151 MHz,DMSO-d6) δ 195.2,151.6,145.0,134.8,128.8,127.9,113.1,37.3,32.1,26.8,21.3,21.0; 高分辨质谱m/z:计算值 C20H22NO2(M+H)+308.164 5,测量值 308.164 7.
9-(4′-Methoxyphenyl)acridine-1,8-dione (3q) Yellow solid M.p.>300 ℃.1H NMR (600 MHz,DMSO-d6) δ 9.43 (s,1H),7.05 (d,J=8.5 Hz,2H),6.72 (d,J=8.5 Hz,2H),4.85 (s,1H),3.67 (s,3H),2.50 (d,J=13.7 Hz,5H),2.25 - 2.14 (m,4H),1.95 - 1.87 (m,2H),1.83 - 1.72 (m,2H).13C NMR (151 MHz,DMSO-d6) δ 195.3,157.6,151.5,140.2,128.9,113.6,113.2,55.3,37.3,31.6,26.8,21.3; 高分辨质谱m/z:计算值 C20H22NO3(M+H)+324.159 4,测量值 324.159 1.
3,4,6,7,9,10-Hexahydro-9-(4-chlorophenyl)-1,8(2H,5H)-acridinedione (3r) Yellow solid M.p.296-297 ℃.1H NMR (600 MHz,DMSO-d6) δ 9.52 (s,1H),7.22 (d,J=8.4 Hz,2H),7.16 (d,J=8.5 Hz,2H),4.88 (s,1H),2.51 (d,J=1.5 Hz,6H),2.25 - 2.16 (m,4H),1.91 (dt,J=13.1,4.8 Hz,2H),1.79 (dt,J=18.3,7.9 Hz,2H).13C NMR (151 MHz,DMSO-d6) δ 195.3,152.0,146.7,130.5,129.9,128.2,112.5,37.2,32.4,26.8,21.2;高分辨质谱m/z:计算值 C19H19ClNO2(M+H)+328.109 9,测量值328.110 7.
9-(4-Bromophenyl)-3,4,6,7,9,10-hexahydro-1,8(2H,5H)-acridinedione (3s) Yellow solid M.p.>300 ℃.1H NMR (600 MHz,DMSO-d6) δ 9.52 (s,1H),7.35 (d,J=8.3 Hz,2H),7.11 (d,J=8.3 Hz,2H),4.87 (s,1H),2.51 (d,J=7.8 Hz,4H),2.25 - 2.16 (m,4H),1.95-1.86 (m,2H),1.84 - 1.72 (m,2H).13C NMR (151 MHz,DMSO-d6) δ 195.3,152.0,147.2,131.1,130.3,119.0,112.5,37.2,32.5,26.8,21.2; 高分辨质谱m/z:计算值 C19H19BrNO2(M+H)+372.059 4,测量值372.059 7.
3,4,6,7,9,10-Hexahydro-9-(2-hydroxyphenyl)-1,8(2H,5H)-acridinedione (3t) Yellow solid M.p.>300 ℃.1H NMR (600 MHz,DMSO-d6) δ 9.86 (s,1H),9.72 (s,1H),6.96 (t,J=7.5 Hz,1H),6.83 (d,J=7.0 Hz,1H),6.69 (dd,J=11.7,7.7 Hz,2H),4.88 (s,1H),2.70 - 2.53 (m,4H),2.35 - 2.21 (m,4H),1.98 - 1.89 (m,2H),1.82 (dt,J=23.5,9.1 Hz,2H).13C NMR (151 MHz,DMSO-d6) δ 197.2,153.7,134.43(s),128.4,127.6,120.4,117.6,112.8,36.8,26.9,26.7,21.0,14.6; 高分辨质谱m/z:计算值 C19H20NO3(M+H)+310.143 8,测量值 310.143 1.
9-(5-chloro-2-hydroxyphenyl)-3,4,6,7,9,10-hexahydroacridine-1,8(2H,5H)-dione (3u) Yellow solid M.p.>300 ℃.1H NMR (600 MHz,DMSO-d6) δ 9.92 (s,1H),9.89 (s,1H),7.00 (dd,J=8.5,2.7 Hz,1H),6.76 (d,J=2.6 Hz,1H),6.71 (d,J=8.6 Hz,1H),4.85 (s,1H),2.62(dd,J=13.4,8.7 Hz,2H),2.59 - 2.52 (m,2H),2.34 - 2.24 (m,4H),1.95 (dt,J=13.1,4.9 Hz,2H),1.87 - 1.75 (m,2H).13C NMR (151 MHz,DMSO) δ 197.1,153.9,153.1,136.4,128.1,127.5,123.7,119.4,112.1,100.0,36.8,27.6,26.8,21.1; 高分辨质谱m/z:计算值 C19H19ClNO3(M+H)+ 344.104 8,测量值 344.105 1.
9-(5-Bromo-2-hydroxyphenyl)-3,4,6,7,9,10-hexahydro-1,8(2H,5H)-acridinedione (3v) Yellow solid M.p.>300 ℃.1H NMR (600 MHz,DMSO-d6) δ 9.94 (s,1H),9.89 (s,1H),7.12 (dd,J=8.5,2.2 Hz,1H),6.88 (d,J=2.2 Hz,1H),6.66 (d,J=8.5 Hz,1H),4.84 (s,1H),2.62(dd,J=13.0,8.7 Hz,2H),2.57 (dd,J=9.9,4.7 Hz,2H),2.29 (d,J=13.5 Hz,4H),1.99-1.89 (m,2H),1.87 - 1.74 (m,2H).13C NMR (151 MHz,DMSO-d6) δ 211.7,197.0,153.9,153.6,136.8,131.1,130.4,119.9,112.1,111.5,36.8,27.7,26.9,21.1,14.6; 高分辨质谱m/z:计算值 C19H19BrNO3(M+H)+388.054 3,测量值 388.053 5.
9-(2-hydroxy-5-methylphenyl)-3,4,6,7,9,10-hexahydroacridine-1,8(2H,5H)-dione (3w) Yellow solid M.p.>300 ℃.1H NMR (600 MHz,DMSO-d6) δ 9.82 (s,1H),9.53 (s,1H),6.76 (dd,J=8.1,1.9 Hz,1H),6.58 (d,J=8.1 Hz,2H),4.85 (s,1H),2.66 - 2.59 (m,2H),2.59-2.53 (m,2H),2.34-2.23 (m,4H),2.11 (s,3H),1.95(dt,J=13.1,4.8 Hz,2H),1.87-1.77 (m,2H).13C NMR (151 MHz,DMSO-d6) δ 197.2,153.6,151.5,134.2,128.7,128.1,117.5,112.8,36.9,26.9,26.7,21.0; 高分辨质谱m/z:计算值 C20H22NO3(M+H)+324.159 4,测量值 324.159 7.
4 结论
在无溶剂及非均相条件下,Amberlyst 15 离子交换树脂为催化剂,以芳香醛、1,3-二羰基化合物、醋酸铵于90 ℃缩合,高收率地得到一系列的药物1,4-二氢吡啶类钙通道阻滞剂.该方法具有无需溶剂,原料便宜易得、反应产率高、反应时间短以及后处理简单等优点.由于Amberlyst 15 离子交换树脂在反应体系不溶,可以很好的回收利用,回收利用可以达到10次,且产率没有明显变化.此外,反应可以放大,可以一次性合成80 g以上的产物,收率为84%.该方法收率高、成本低、易操作、适合工业化大生产,为国内心脑血管疾病类药物提供了一种很好的工业化路线.

