VDPAP 方案对急性淋巴细胞白血病患儿凝血功能及血常规指标的影响
李敖龙,王铁锋,张琪
周口市中心医院1儿科,2新生儿重症监护室,河南周口 466000
急性淋巴细胞白血病(acute lymphoblastic leukemia,ALL)是一种由T 系或B 系淋巴祖细胞引起的异质性疾病,具体表现为器官组织浸润、出血、感染、发热、贫血、中性粒细胞减少、血小板减少等,病情严重者甚至会引起死亡[1-2]。调查研究显示,ALL 在3~7 岁儿童中发病率较高,约占儿童急性白血病的80%[3]。既往临床采用泼尼松+左旋门冬酰胺酶+长春新碱+柔红霉素(ADLP)方案治疗ALL,该方案以左旋门冬酰胺酶为主,虽然可控制疾病进展,但容易引发肝功能损伤、凝血功能异常、脂肪酶升高、淀粉酶升高、过敏反应等,安全性较差,且整体治疗效果欠佳,不能满足临床需求[4]。培门冬酶是近年来临床出现的一种新型门冬酰胺酶制剂,在化学偶联修饰作用下,保持了原有门冬酰胺酶的活性,同时降低了免疫原性,患儿在泼尼松+培门冬酶+长春新碱+柔红霉素(VDPAP)方案治疗后一般不会出现过敏反应[5-6]。基于此,本研究探讨VDPAP 方案对ALL 患儿凝血功能及血常规指标的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取2020 年5 月至2022 年5 月在周口市中心医院住院的ALL 患儿。纳入标准:①符合《儿童急性淋巴细胞白血病诊疗建议(第四次修订)》[7]中ALL 的诊断标准;②年龄3~10 岁;③初次接受化疗;④听说、阅读能力正常;⑤临床资料完整。排除标准:①治疗前肾、肝功能异常;②合并脓毒症等疾病;③近1 个月接受过化疗等对症治疗;④合并其他恶性肿瘤;⑤过敏体质;⑥合并先天性、遗传性疾病;⑦合并严重代谢性疾病。依据纳入和排除标准,本研究共纳入98 例ALL 患儿,依据治疗方法的不同分为对照组和观察组,每组49 例,对照组患儿给予ADLP 方案化疗,观察组患儿给予VDPAP 方案化疗。观察组中,男26 例,女23 例;年龄3~10 岁,平均(6.52±1.34)岁;危险度分层:高危7例,中危23 例,低危19 例;病程3~8 周,平均(5.16±0.64)周;FAB 分型:L1 型24 例,L2 型25 例。对照组中,男28 例,女21 例;年龄4~9 岁,平均(6.54±1.28)岁;危险度分层:高危9 例,中危21 例,低危19例;病程4~8 周,平均(5.18±0.61)周;FAB 分型:L1型22 例,L2 型27 例。两组患儿性别、年龄、危险度分层、病程、FAB 分型比较,差异均无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会批准通过,所有患儿家属均知情同意。
1.2 治疗方法
对照组患儿接受ADLP 方案化疗:泼尼松片40 mg 口服,每天1 次,连续服药7 天;柔红霉素25 mg/m2静脉滴注,每周1 次,共治疗4 次;长春新碱1.5 mg/m2静脉滴注,每周1 次,共治疗4 次;左旋门冬酰胺酶5000 U/m2肌内注射,隔日1 次,高危者注射8 次,低危者注射6 次。7 天为1 个疗程,共治疗8 个疗程。
观察组患儿接受VDPAP 方案化疗:泼尼松、柔红霉素、长春新碱用药方案同对照组。对于体表面积>0.6 m2的患儿,给予培门冬酶2500 U/m2肌内注射,每隔2 周肌内注射1 次;对于体表面积≤0.6 m2的患儿,给予培门冬酶82.50 U/kg,每隔2 周肌内注射1 次。14 天为1 个疗程,共治疗4 个疗程。
1.3 观察指标及评价标准
①治疗后参考《小儿急性淋巴细胞白血病诊疗建议(第二次修改草案)》[8]评估两组患儿的临床疗效:完全缓解(complete response,CR),巨核细胞系、红细胞系正常,中性粒细胞、血小板等指标恢复正常,骨髓象原始粒细胞Ⅰ+Ⅱ型≤5%,感染、发热等症状消失;部分缓解(partial response,PR),巨核细胞系、红细胞系、中性粒细胞、血小板比治疗前好转,但未恢复正常,感染、发热等症状减轻,骨髓象原始粒细胞Ⅰ+Ⅱ型>5%但≤20%;未缓解(no response,NR),巨核细胞系、红细胞系、中性粒细胞、血小板无变化,感染、发热等症状无改善;总有效率=(CR+PR)例数/总例数×100%。②治疗前后,比较两组患儿的凝血功能指标,包括活化部分凝血活酶时间(activited partial thromboplastin time,APTT)、纤维蛋白原(fibrinogen,FIB)、凝血酶原时间(prothrombin time,PT)。③治疗前后,比较两组患儿的血常规指标,包括血小板计数、红细胞计数、血红蛋白(hemoglobin,Hb)。④治疗前后,比较两组患儿的血清炎症因子指标,包括超敏C 反应蛋白(high-sensitive C-reactive protein,hs-CRP)、白细胞介素-6(interleukin-6,IL-6)。⑤比较两组患儿的不良反应发生情况,包括末梢神经炎、肾脏损伤、肝脏损伤、过敏反应、骨髓抑制。⑥采用电话访视、上门访视的方式对两组患儿进行为期6 个月的随访,记录两组患儿的复发情况。
1.4 统计学方法
采用SPSS 26.0 软件对所有数据进行统计分析,正态分布的计量资料以均数±标准差(±s)表示,组间比较采用t检验;计数资料以例数和率(%)表示,组间比较采用χ2检验;以P<0.05 为差异有统计学意义。
2 结果
2.1 临床疗效的比较
观察组患儿的治疗总有效率为93.88%(46/49),与对照组患儿的89.80%(44/49)比较,差异无统计学意义(χ2=0.544,P>0.05)。(表1)

表1 两组患儿的临床疗效[n(%)]*
2.2 凝血功能指标的比较
治疗前,两组患儿血清FIB、APTT、PT 比较,差异均无统计学意义(P>0.05)。治疗后,两组患儿APTT、PT 均长于本组治疗前,FIB 水平均低于本组治疗前,观察组患儿APTT、PT 均长于对照组,FIB水平低于对照组,差异均有统计学意义(P<0.05)。(表2)
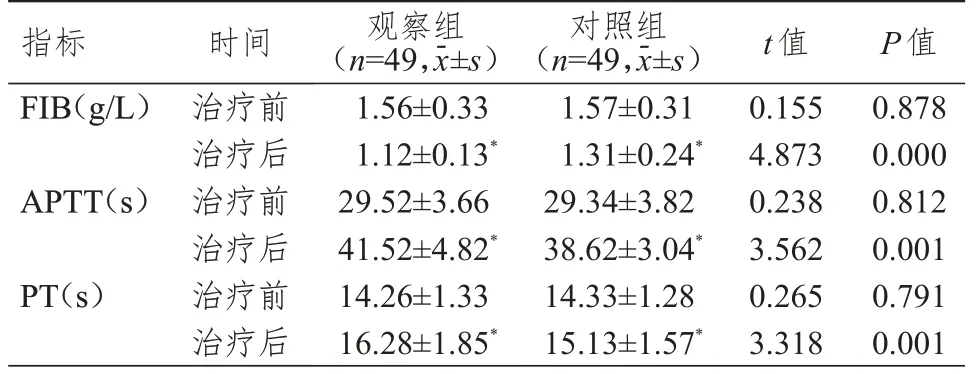
表2 治疗前后两组患儿凝血功能指标的比较
2.3 血常规指标的比较
治疗前,两组患儿血小板计数、红细胞计数、Hb 水平比较,差异均无统计学意义(P>0.05)。治疗后,两组患儿血小板计数、红细胞计数、Hb 水平均高于本组治疗前,观察组患儿血小板计数、红细胞计数、Hb 水平均高于对照组,差异均有统计学意义(P<0.05)。(表3)
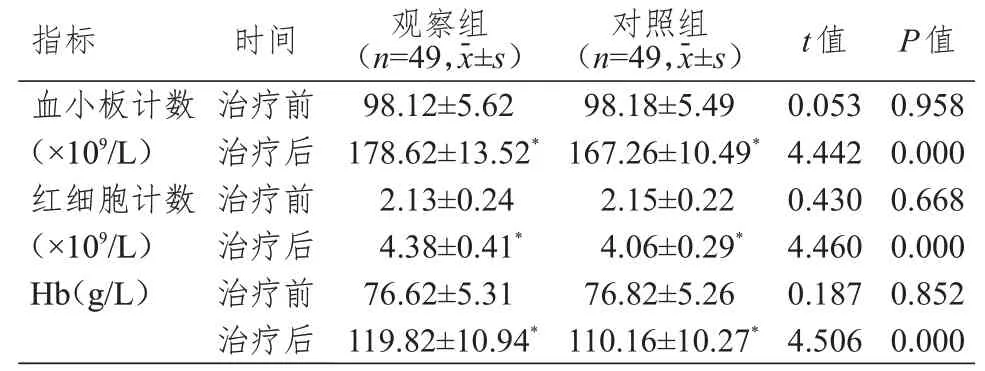
表3 治疗前后两组患儿血常规指标的比较
2.4 血清炎症因子指标的比较
治疗前,两组患儿血清hs-CRP、IL-6 水平比较,差异均无统计学意义(P>0.05)。治疗后,两组患儿血清hs-CRP、IL-6 水平均低于本组治疗前,观察组患儿血清hs-CRP、IL-6 水平均低于对照组,差异均有统计学意义(P<0.05)。(表4)
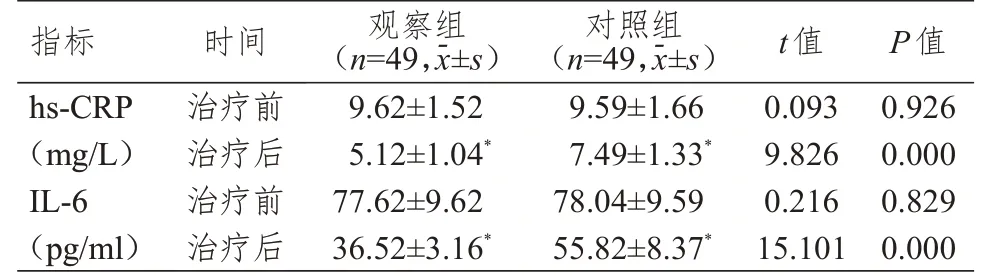
表4 治疗前后两组患儿血清炎症因子指标的比较
2.5 不良反应及复发情况的比较
两组患儿肾脏损伤、肝脏损伤、骨髓抑制发生率比较,差异均无统计学意义(P>0.05);观察组患儿的末梢神经炎、过敏反应发生率均低于对照组,差异均有统计学意义(P<0.05)(表5)。观察组患儿6 个月内复发率为2.04%(1/49),低于对照组患儿的20.41%(10/49),差异有统计学意义(χ2=6.554,P=0.010)。
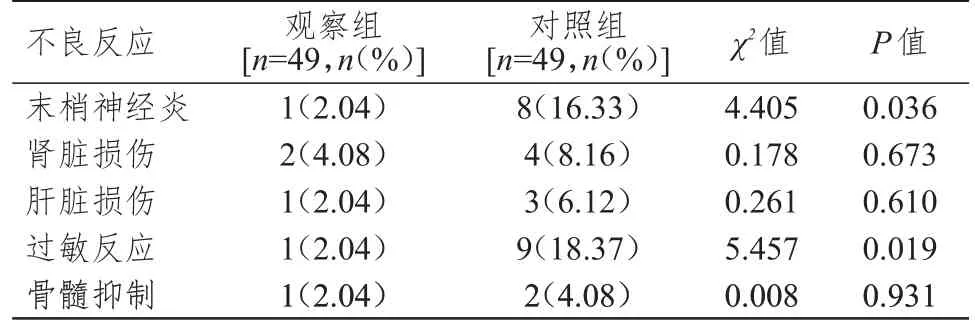
表5 两组患儿的不良反应发生情况的比较
3 讨论
ALL 是儿童常见的恶性肿瘤,是原始细胞异常增殖及聚集的结果,目前,临床普遍认为该病的发生与家族遗传、生物因素、环境污染、药物滥用、病毒感染等有关[9-10]。ALL 表现为免疫功能减退、感染、出血、贫血、全身骨痛等,具有治愈难度大、恶性程度高、易复发、病死率高等特点[11-12]。ALL的治疗难度较大,若不给予及时、有效的治疗,随着肿瘤细胞的快速增殖,机体正常造血功能会受到抑制,侵犯淋巴结、脾、肝等多种脏器,破坏神经系统,严重影响患儿的生活质量,威胁患儿的生命健康,给社会及家庭均带来了沉重负担[13-14]。
本研究结果显示,观察组患儿的治疗总有效率为93.88%,与对照组患儿的89.80%比较,差异无统计学意义(P>0.05),说明VDPAP 方案与ADLP 方案均可提高ALL 的临床疗效。这可能是因为左旋门冬酰胺酶的免疫原性较高,肌内注射后可对体内L-天冬酰胺产生刺激,将外源L-天冬酰胺供给的蛋白质阻断,从而杀灭并清除体内的白血病细胞,促进骨髓造血功能恢复,发挥治疗ALL 的目的[15-16]。1994 年美国食品药品管理局(FDA)批准培门冬酶用于治疗ALL,其在保持左旋门冬酰胺酶性能的同时,通过化学修饰及物理包埋,获得了更多的优势性能,如延长半衰期、降低肾脏清除率、提高生物利用度、降低免疫原性及提高水溶性等[17-18]。培门冬酶的注射次数较少,一定程度上减轻了患儿治疗期间所承受的痛苦,缩短了治疗疗程,具有一定优势。
本研究结果显示,治疗后,两组患儿APTT、PT均长于本组治疗前,FIB 水平均低于本组治疗前,观察组患儿APTT、PT 均长于对照组,FIB 水平低于对照组,差异均有统计学意义(P<0.05)。表明VDPAP、ADLP 方案均有引起凝血功能异常的风险。这可能是因为左旋门冬酰胺酶会降低肝细胞合成蛋白质的能力,导致蛋白质合成原料缺乏,降低多种凝血因子浓度,延长APTT、PT,最终出现凝血功能障碍。培门冬酶在抗肿瘤的同时会抑制肝脏细胞合成蛋白,也会引起原料缺乏,减少纤维蛋白溶酶、纤维蛋白原合成,出现凝血功能障碍。因此,左旋门冬酰胺酶与培门冬酶治疗期间,应加强凝血功能监测,从而及早发现异常,及早给予针对性血液制品输注,抵抗药物不良反应。本研究结果显示,治疗后,两组患儿血小板计数、红细胞计数、Hb 水平均高于本组治疗前,观察组患儿血小板计数、红细胞计数、Hb 水平均高于对照组,差异均有统计学意义(P<0.05)。表明培门冬酶可有效提高血小板计数,改善血常规指标。这可能是因为以培门冬酶为主的化疗方案可在彻底清除白血病细胞的同时,产生免疫抑制、抗过敏、抗炎作用,抑制细胞增殖以及感染细胞RNA、DNA 合成,避免由于免疫过度引发过敏反应,对机体具有一定的保护作用,可促进患儿受损的骨髓细胞功能恢复,从而改善血常规指标。培门冬酶在抑制ALL 细胞增殖的同时,不会损伤、影响正常免疫细胞的转导通路,是该药物改善血常规指标的原因之一。
ALL 患儿化疗期间,由于化疗药物损伤消化道上皮细胞,体内会产生不同程度炎症反应,导致水电解质紊乱、肠道菌群失衡、免疫功能减退,刺激机体释放大量的促炎因子,形成恶性循环[19-20]。因此,在ALL 治疗中及时调控、减轻炎症反应对改善患儿的预后有重要意义。本研究结果显示,治疗后,两组患儿血清hs-CRP、IL-6 水平均低于本组治疗前,观察组患儿血清hs-CRP、IL-6 水平均低于对照组,差异均有统计学意义(P<0.05),表明培门冬酶可有效抑制炎症因子释放。这可能是因为培门冬酶具有双向免疫调节、抗病毒、抗肿瘤作用,可有效抑制细胞增殖,增强患儿机体免疫力,抵抗化疗引起的炎症因子水平升高。本研究结果显示,观察组患儿的末梢神经炎、过敏反应发生率均低于对照组,6 个月复发率低于对照组,差异均有统计学意义(P<0.05),说明培门冬酶致敏反应较轻,且不易复发。这可能是因为左旋门冬酰胺酶由于具有外源性细菌蛋白质的性质,患儿在肌内注射后会迅速产生抗体,这也是引起过敏反应的原因之一。培门冬酶的不良反应主要是过敏反应、转氨酶升高、高胆红素血症,本研究观察组患儿出现1 例肝脏损伤、1 例过敏反应,其余不良反应的发生率较低,整体来讲,培门冬酶的安全性较高。培门冬酶不良反应较少的原因是经过化学修饰,降低了过敏反应及免疫原性的发生风险。培门冬酶可增强患儿机体免疫功能,提高患儿对疾病的抵抗力,促使肿瘤细胞凋亡,与左旋门冬酰胺酶相比,可有效降低ALL患儿复发率,提高远期生存率。
综上所述,VDPAP 方案与ADLP 方案均可提高ALL 患儿的总有效率,其中VDPAP 方案可有效降低ALL 患儿血清IL-6 等炎症因子水平,提高血小板计数,降低末梢神经炎等不良反应发生率及复发率,但可能会引起凝血功能异常,临床需重点关注。

