骨髓增生异常综合征患者异基因造血干细胞移植后继发慢性肥大细胞白血病现象分析
丁 静 刘伟玲 夏新新 蔺丽慧
(1.上海交通大学医学院附属第一人民医院检验科,上海 201600;2.上海交通大学医学院附属第一人民医院血液科,上海 201600)
骨髓增生异常综合征(myelodysplastic syndrome,MDS)是一组克隆性造血干细胞疾病,异基因造血干细胞移植是目前唯一可能治愈MDS的方法[1]。系统性肥大细胞增多症是克隆性、肿瘤性肥大细胞增殖性疾病,肥大细胞白血病在系统性肥大细胞增多症各亚型中侵袭性最强、预后最差,患者中位生存时间仅约为2个月[2]。本研究回顾分析1例异基因造血干细胞移植后继发肥大细胞白血病的MDS患者疾病进程,总结相关实验室检验结果与疾病发生发展的关系,以提高临床对该类疾病的认识。
1 材料和方法
1.1 研究对象
患者,女,60岁。2014年因白细胞、血红蛋白降低确诊高危型骨髓增生异常综合征伴原始细胞增多1型(myelodysplastic syndrome with excess blasts 1,MDS-EB-1)。2014年9月行全相合异基因造血干细胞移植,移植成功。该患者移植术后6年间反复发热;伴干咳、气喘,并夜间加重;头痛,盗汗,消瘦,乏力。2016年4月曾因“间断发热、咳嗽、咳痰”就诊,骨髓检查提示含嗜碱性颗粒的细胞增多(约占36%),外周血涂片示含嗜碱性颗粒的细胞约占10%,电子计算机断层扫描提示肺部感染,行抗感染治疗后稍好转,但症状仍有反复。有过敏性鼻炎史。2020年7月,患者胸闷气促加重、面色潮红,血常规示两系降低。于上海市第一人民医院血液科住院治疗。
住院期间骨髓病理检查示:有核细胞高度增生,原始细胞高度增生、形态一致,正常造血细胞增生高度受抑,网状纤维增生(MF Ⅱ级)。免疫组化:MPO(-)、CD20(-)、CD34(-)、CD2(-)、CD117(+)、BM2(+)、Ki-67(个别+)、CD42b(-)、CD7(-)、CD68(+)。正电子发射断层显像/X线计算机体层成像(positron emission tomography/computed tomography,PET/CT)提示全身多发骨病灶伴葡萄糖代谢轻度增高,肝脾肿大,倾向血液系统疾病。腹部B超提示肝脾大,门静脉高压,腹腔积液,提示肝硬化。行甲磺酸伊马替尼联合小剂量醋酸泼尼松片治疗。2021年7月电话随访获知预后良好。
1.2 实验室检验
采集患者乙二胺四乙酸抗凝血,采用深圳迈瑞公司Mindray6800流水线及配套试剂进行血细胞计数。
收集患者骨髓细胞,制片后采用珠海贝索生物技术有限公司Wright-Giemsa染液染片,采用日本OLYMPUS公司CX33显微镜观察。
抽取患者骨髓液,乙二胺四乙酸二钾抗凝。采用美国贝克曼库尔特公司Navios流式分析仪及配套试剂进行免疫表型分析,采用江苏康为世纪生物科技公司柱式抽提试剂盒提取总RNA,采用多重巢式聚合酶链反应(polymerase chain reaction,PCR)检测RUNX1-RUNX1T1、BCR-ABL1、CBFβ-MYH11、KMT2A-MLLT6、KMT2A-MLLT11、KMT2A-MLLT3,KMT2AMLLT10等56种急性白血病相关融合基因(上海源奇生物医药有限公司),以循环阈值(cycle threshold,Ct)<33为阳性。采用逆转录试剂盒(日本TaKaRa公司)合成cDNA;然后提取DNA,试剂盒购自江苏康为世纪生物科技公司;采用美国illumina公司illumina测序平台进行测序,平均靶基因覆盖率≥90%,平均测序深度≥1 000×;单核苷酸多态性(single nucleotide polymorphism,SNP)检测参照文献[3]。
抽取患者肝素抗凝骨髓液,采用短期培养法对骨髓细胞进行染色体分析,培养基购自上海乐辰生物科技公司。
收集患者相关临床表现和诊疗经过等相关资料。
2 结果
2.1 实验室检验结果和诊断
2.1.1 血常规
血红蛋白73 g/L,红细胞2.16×1012/L,白细胞2.45×109/L,中性粒细胞绝对值1.48×109/L,血小板193×109/L。
2.1.2 细胞形态学特征
骨髓有核细胞增生明显活跃。肥大细胞约占96.5%。细胞中等偏大,多数规则,约8%为梭形;核中等,圆形,居中或稍偏位,染色质偏成熟;胞质偏多,布满紫黑色粗大颗粒,可盖于核上。约21%胞体偏大,核畸形,呈哑铃样或双核,染色质偏细,可见少数细胞颗粒缺乏。细胞化学染色:过氧化物酶染色(-),特异性酯酶染色(+++),糖原染色(++),甲苯胺蓝染色(+++),非特异性酯酶染色(++)且不被氟化钠抑制。提示:肥大细胞增多症骨髓象,肥大细胞白血病待排。形态学结果见图1。

图1 形态学涂片和染色结果(×1 000)
2.1.3 细胞免疫学分型结果
共分析约4.9 个万细胞,其中异常细胞约占白细胞总数的88.35%,免疫表型为:CD45dimSSC高CD34-CD117+CD13+CD33+CD16+CD64partCD123dimCD2-CD25dimCD203c+FcεRI+,提示肥大细胞待排。见图2。
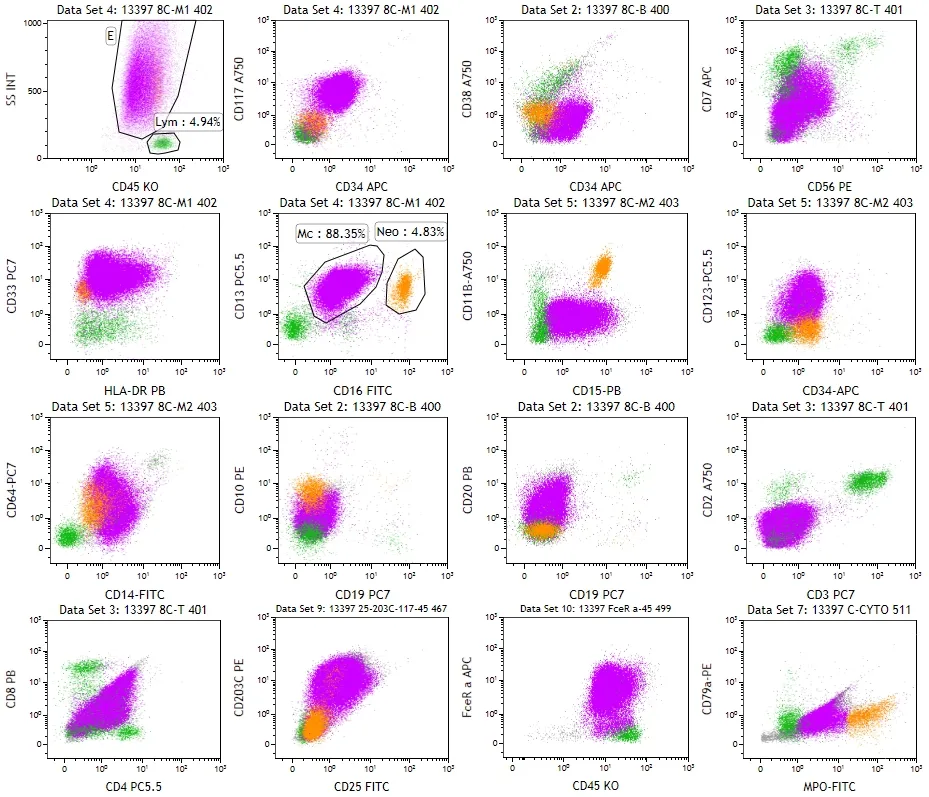
图2 细胞免疫学分型结果
2.1.4 基因检测结果
检出突变KITD816H48.57%,IDH2R140Q40.30%,DNMT3AW601X34.01%。融合基因未检出。移植后SNP和骨髓肥大细胞比例始终呈负相关(图3)。
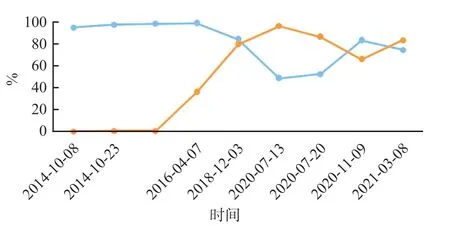
图3 SNP和骨髓肥大细胞的变化曲线
2.1.5 染色体
染色体核型分析结果示:46,XX[3]。
3 讨论
系统性肥大细胞增多症的确诊需要符合主要标准和1个次要标准,或符合至少3个次要标准[4-5]。依据文献[5],本例患者存在外周血两系减低、肝脾肿大伴肝功能异常等“C所见”表现,骨髓穿刺液形态学、流式细胞学和基因检测结果符合3项次要标准,同时,骨髓穿刺液涂片示肥大细胞≥20%,可诊断为系统性肥大细胞增多症中的肥大细胞白血病。
肥大细胞白血病预后极差,而回顾本例患者病史,2016年4月骨髓穿刺液中即出现肥大细胞,占骨髓有核细胞的36%,外周血肥大细胞占10%,已符合肥大细胞白血病诊断标准。直至2021年7月随访时状态良好,与既往研究中的中位生存时间[2]分歧较大。
有研究发现,少数肥大细胞白血病患者病程较为缓慢、稳定,有时甚至在早期没有“C所见”[6]。此类患者疾病可能会进展,但总体预后优于急性肥大细胞白血病患者,尤其是当没有“C所见”时,其形态学也以典型肥大细胞或非典型肥大细胞Ⅰ型为主。另外,急性肥大细胞白血病通常显示出高增殖率(Ki-67阳性肥大细胞>50%),而慢性肥大细胞白血病则显示出低增殖率(Ki-67阳性肥大细胞<10%)[6]。肥大细胞在Wright-Giemsa染色中可显示出4种形态:1)典型肥大细胞,圆形,颗粒丰富,圆形核居中;2)非典型肥大细胞Ⅰ型,具有细长的细胞表面呈纺锤形、胞质颗粒减少、核呈椭圆形且疏松中的2或3个特征;3)非典型肥大细胞Ⅱ型/前母细胞,具有双叶或多叶核;4)异染性原始细胞,原始细胞伴有少量异染颗粒[6]。SPERR等[7]认为Ⅰ型非典型肥大细胞中,梭形肥大细胞相对于规则形状肥大细胞更成熟,而高比例的Ⅱ型非典型肥大细胞与不良预后相关。本例患者的骨髓细胞形态多数为相对成熟的典型肥大细胞和Ⅰ型非典型肥大细胞,骨髓病理免疫组化Ki-67仅个别阳性,病程进展缓慢,符合慢性肥大细胞白血病的特征。
查阅国内外文献,仅见2例异基因造血干细胞移植术后发生肥大细胞白血病的病例[8-9],临床病程、形态学特征、治疗与预后见表1。

表1 本例患者与文献报道的2例患者基本情况
与文献报道的2例移植后发生肥大细胞白血病的患者对比后,我们发现本例患者与病例1在移植前均未发现肥大细胞,均接受了异基因造血干细胞移植,移植后肥大细胞形态均较为成熟,生存时间均超过5年,预后均符合文献[6]。不同于本例患者移植后继发肥大细胞白血病混合嵌合状态,病例1通过供者淋巴细胞输注有效实现了骨髓肥大细胞的清除。病例2在化疗复发后即被诊断为系统性肥大细胞增多症-急性髓系白血病,移植前骨髓中原始细胞占31.2%,肥大细胞占5.8%;半相合移植后骨髓中的肥大细胞增多,以异染性原始细胞和非典型肥大细胞Ⅱ型为主,肥大细胞脱颗粒后高水平的肝素引起临床显著出血,颅内出血是病例2死亡的主要原因。
值得注意的是,本例患者虽然在移植前无肥大细胞浸润证据,但其全部病程进展很可能涉及肥大细胞合并克隆性造血组织非肥大细胞系疾病(associated haematological neoplasm,AHN),这类血液系统恶性肿瘤多为髓系,如MDS、骨髓增生性肿瘤(myeloproliferative neoplasm,MPN)、MDS/MPN或急性髓系白血病,5%~40%的系统性肥大细胞增多症病例,AHN在其诊断的同时、之前或之后均可被发现。疾病初发时肥大细胞可能被造血系统肿瘤细胞的增殖掩盖,而在治疗引起的增生减低或造血恢复后变得明显[10]。目前,关于肥大细胞合并AHN的发病机制有2种理论,一种是突变的骨髓干细胞由于存在c-KIT突变而分化并增殖为肥大细胞,另一种是具有获得性C-KIT突变的骨髓祖细胞亚克隆转化导致共存的肥大细胞增多症[11]。CRAIG等[12]的研究中纳入64例具有C-KIT突变的患者,其中患MDS、MPN或MDS/MPN的患者约占1/3,形态学和免疫表型特征表明有91%的患者检出肥大细胞;队列中有30名肥大细胞合并AHN患者,其中近1/3在疾病初期未检出肥大细胞[12]。FRITSCHE-POLANZ等[13]发现,在101例急性髓系白血病患者中,有7例(6.9%)检出KIT D816V伴肥大细胞,最终诊断为肥大细胞合并急性髓系白血病。JAWHAR等[14]认为,肥大细胞合并AHN时,2种疾病可能互相掩盖,他们发现KITD816mut/CBFnegSMAML和KITD816mut/CBFnegAML2个数据库显著相似,提示很大比例的急性髓系白血病患者体内有潜在的肥大细胞,并可通过检测血清类胰蛋白酶、规范骨髓活检,提高肥大细胞的检出率。
已发表的关于肥大细胞-急性髓系白血病伴t(8;21)的研究显示了关于移植后肥大细胞来源的不同观点,有研究认为移植后肥大细胞可检出t(8;21),来源于受者[15-17],而CHEN等[18]在1例t(8;21)的MCL-AML患者移植后31 d,发现了供体来源肥大细胞,该患者移植前后均未发现C-KIT突变。本病例移植后SNP结果和骨髓肥大细胞的比例变化呈负相关,SNP检测异基因造血干细胞移植术后供者细胞嵌合率降低,提示供者来源细胞减少,受者来源细胞增多,间接提示肥大细胞可能来源于受者自身,有待于基因测序加以确认。
综上所述,本例罕见的MDS行异基因造血干细胞移植术后发生慢性肥大细胞白血病的病例,揭示了较成熟的肥大细胞形态与良好预后的相关性。人类肥大细胞主要分布于机体与外界环境相通的组织器官,如皮肤、呼吸道和消化道,这些部位经常可以接触到病原体、变应原,以及环境中的其他物质。因此,当血液肿瘤患者出现反复、不明原因的发热、潮红、骨质疏松症、过敏反应、呼吸道和胃肠道疾病或慢性腹部绞痛症状时,应高度怀疑肥大细胞增殖。建议具有KITD816V突变的急性髓系白血病、MDS、MPN或MDS/MPN的患者均应通过血清类胰蛋白酶检测、骨髓活检筛查肥大细胞。由于持续肥大细胞增多症会增加出血风险和其他不良影响,因此可能需要考虑积极的干预措施,如输注供体淋巴细胞。血液学检验工作者在日常工作中应提高对罕见疾病的敏感性,加强对疾病进展的认识,完善疾病的诊断,为临床工作提供帮助。

