Plackett-Burman法筛选电-Fenton降解水中盐酸四环素的主要因素
李 庆,董海山,郑 雪,徐 欣,梁月明
(西南交通大学地球科学与环境工程学院,四川 成都 610000)
四环素类抗生素(TCs)是一种常见的广谱抗生素,其在临床医学、水产及畜牧养殖业中均受到了广泛应用。有研究表明,在水生生态环境、土壤环境、大气和生物介质中均检出了四环素类抗生素[1-4],但其检出浓度较低往往易被人们所忽视,导致残留的四环素在环境中不断累积、传播。在水环境中,残留的四环素不仅会对水生生物直接产生毒性作用,影响其正常生长,还可能通过食物链富集对整个生态环境乃至人体健康构成威胁[5]。目前,国内外处理四环素类抗生素废水的主要方法有生物法和物化法。物化法包括臭氧氧化法、Fenton法、光催化法等[6]。其中,Fenton氧化法因其成本低、氧化效率高、操作简单而被广泛应用于抗生素废水处理[7],但传统的Fenton法在应用过程中仍存在耗时长、去除效率低等问题。因此本试验基于Fenton氧化技术引入电解,利用电-Fenton法降解水中盐酸四环素,探讨了降解过程中初始pH、H2O2投加量、电流强度、电解质浓度、极板间距对TC降解效率的影响,反应原理如下[8]。同时,探究了各因素影响电-Fenton法降解盐酸四环素的作用原理,为实际处理盐酸四环素废水提供参考。

(1)

(2)

(3)

(4)
1 实 验
1.1 实验材料
盐酸四环素,成都化夏化学试剂有限公司;无水硫酸钠、硫酸亚铁、双氧水(30%),成都金山化学试剂有限公司;浓硫酸、氢氧化钠,成都市科龙化工制品厂。
1.2 主要仪器设备
78HW-1恒温磁力搅拌水浴锅;电-Fenton反应器,自制;UV-2600紫外-可见分光光度计;直流稳定电源,深圳兆信。
1.3 实验方法
向500 mL反应体系中加入适量盐酸四环素溶液,使用无水硫酸钠作为电解质,用一定浓度的氢氧化钠和浓硫酸调节水样pH至指定范围,向水样中投加过氧化氢和适量硫酸亚铁。将水样置于78HW-1型恒温磁力搅拌器中反应,按设置的试验时间间隔取样。取样后使用0.45 μm的微孔滤膜过滤样品并于盐酸四环素最大吸收波长355 nm处进行测定,记录各样品吸光度T。绘制电-Fenton氧化体系TC去除率随各反应条件变化的关系曲线图,确定试验最佳条件。反应装置如图1所示。

图1 电-Fenton反应装置图
1.4 分析方法
配制浓度为20、40、60、80、100 μmol/L的TC溶液,使用0.45 μm的微孔滤膜将其过滤后于355 nm波长处测定吸光度。以盐酸四环素浓度为横坐标,吸光度作为纵坐标绘制标准曲线,得到线性回归方程:y=0.004 4x+0.002 8,R2=0.999 8。利用此线性回归方程可求得不同吸光度下的盐酸四环素浓度。
2 结果与讨论
2.1 单因素试验
2.1.1 电解质浓度的影响
Yan Fan等[9]在罗丹明B降解实验中,分别以硫酸钠、硝酸钠和碳酸钠作为反应电解质,得到RhB降解率分别为93.8%、62.8%、20.6%。因此,本试验选择硫酸钠为反应电解质。
如图2所示,TC去除率随着硫酸钠浓度的增加呈现先上升后下降的趋势。TC去除率在硫酸钠浓度为0.1 mol/L时达到极大值。分析原因可能是:当硫酸钠浓度未达到0.1 mol/L时,此时溶液中的离子数少、导电性低、·OH产生量少,从而导致TC降解率低;当硫酸钠浓度超过0.1 mol/L时,此时溶液中离子数过多、电流紊乱也会导致TC降解率减小。
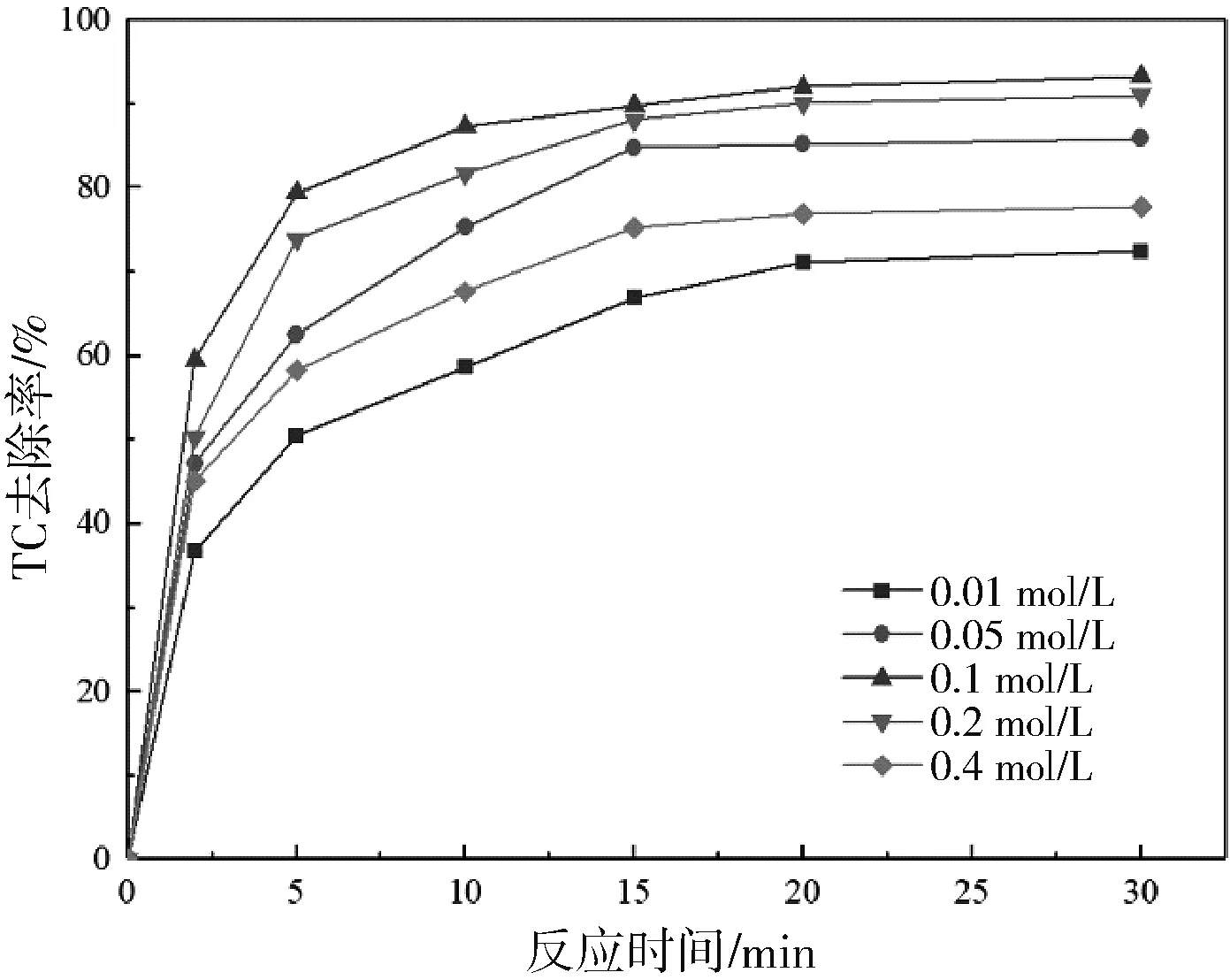
图2 不同电解质浓度对电-Fenton氧化体系降解TC的影响
2.1.2 初始pH的影响
如图3所示,随着溶液初始pH的不断增大,TC去除率先增大后减小。当pH=3.0时,电-Fenton氧化降解盐酸四环素的效果最为显著,TC去除率可达94.55%;当pH值继续增加时,TC去除率出现不断降低的趋势。当pH=6.0时,TC去除率降低到59.89%。这是由于pH过低会破坏Fe3+/Fe2+的转换平衡,阻碍Fe2+催化H2O2分解产生·OH的进程,从而导致TC去除率降低。而当pH过高时,Fe2+促进中间产物碳酸盐和碳酸氢盐与羟基自由基发生反应,消耗·OH;且在碱性条件下,溶液中的Fe3+更易生成Fe(OH)3沉淀或铁络合物,抑制催化剂的生成,使得TC去除率大幅降低。
2.1.3 电流强度的影响
如图4所示,TC去除率随着电流强度的增加呈现先增加后下降的趋势。这是由于增大电流会促进Fe3+被还原成为Fe2+,催化H2O2反应产生·OH,从而增大TC去除率。但当电流过大且在酸性条件时,开始发生副反应析氢、析氧反应,溶液中的二价、三价铁离子容易与阴极周围的氢氧根离子生成难降解的Fe(OH)2、Fe(OH)3,使Fe3+数量减少,还原生成的Fe2+数量也因此减少,阻碍Fe2+的利用,从而TC去除率减少。因此,确定了该体系下最佳电流强度为0.5 A。

图4 电流强度对电-Fenton体系降解TC的影响
2.1.4 温度的影响
如图5所示,TC去除率随温度增加先增大后减小,当温度为30 ℃时,电-Fenton氧化降解盐酸四环素的效果最为显著,分析原因可能为:当样品溶液温度持续升高,TC分子吸收外部热量克服彼此间分子间作用力,使得溶液中活化分子数增加,反应物与羟基自由基接触概率增大,从而TC降解率增加。后续随着温度的持续升高,反应速率明显降低,这可能是因为在反应过程中Fe2+易被氧化为Fe3+,这也会消耗一部分H2O2,同时温度越高,H2O2分解速率越快[10],导致H2O2生成·OH数量减少,从而反应速率降低。

图5 温度对电-Fenton体系降解TC的影响
2.1.5 H2O2投加量的影响
如图6所示,TC去除率随着H2O2投加量的增加先增加后降低。当H2O2投加量=10 mmol/L时,电-Fenton氧化降解TC的效果最为显著。当继续增加H2O2投加量至15 mmol/L时,去除率反而有所下降。分析原因可能是:在反应初始阶段,增大H2O2投加量有利于·OH产生,使更多的TC被羟基自由基降解,详见公式(2)和公式(5)。但当H2O2投加过量时,TC降解率反而有所降低。一方面,Fe2+被氧化生成Fe3+的过程会消耗反应体系内的H2O2,产生的羟基自由基也逐渐变少,TC降解速率减缓;再者如公式(6)所示,过量的H2O2会与样品中游离的羟基自由基继续反应,使溶液中的·OH数量减少,并且反应生成的·OOH降解TC能力远低于·OH,从而令TC降解速率降低[11-12]。

图6 H2O2投加量对电-Fenton体系降解TC的影响

(5)

(6)
2.1.6 H2O2/Fe2+摩尔比的影响
如图7所示,本文通过改变Fe2+投加量改变H2O2/Fe2+的摩尔比。TC去除率在H2O2/Fe2+的摩尔比=16:1时达到峰值。H2O2/Fe2+摩尔比降低为8:1时,去除率较峰值下降了33.52%。当H2O2/Fe2+的摩尔比超过16:1时,TC降解率开始下降。分析原因可能是:在一定范围内,羟基自由基的产生量随着Fe2+的投加量增大而增大,溶液中·OH数量越多则反应速率越快。但由于溶液中投加的双氧水含量未变化,过量的Fe2+会与样品中游离的羟基自由基继续反应,使溶液中的·OH淬灭,从而使得TC降解速率降低。

图7 H2O2/Fe2+摩尔比对电-Fenton体系降解TC的影响
2.1.7 极板间距的影响
如图8所示,TC去除率随着反应时间的延长而增加,当极板间距由4.5 cm缩短至2.5 cm时,TC去除率显著增加。当极板间距为2.5 cm时,电-Fenton对盐酸四环素的降解效果最为显著。继续缩小极板间距至1.5 cm时,TC降解率较峰值降低了2.62%。分析原因可能是:

图8 极板间距对电-Fenton体系降解TC的影响
在废水体积相同的情况下,极板间距越大,电解槽越宽,液体浸没的极板面积就越小。由于电流密度相等,极板面积越小,电流越低。单位时间内阳极溶出的Fe2+减少,羟基自由基减少,从而TC降解率降低。当极板间距增大时,电阻增大,两极间的电耗将显著增大。但若极板间距过小,则会导致极板间污染物堆积造成堵塞,从而阻碍TC降解[13]。
2.2 Plackett-Burman试验
通过上述单因素试验可知影响电-Fenton试验的因素众多,但并不是所有的影响因素对试验指标都有显著影响,因此通过引入Plackett-Burman试验确定影响电-Fenton氧化体系降解TC的显著单因素。
Plackett-Burman(PB)法是一种以不完全平衡块为原理的实验设计,它能够从众多的过程变量中快速、有效地筛选出有显著影响的单因素的方法[14]。本次试验以TC去除率为响应值对各单因素进行筛选。
根据实验数据,利用线性函数方程式式(7)对上述各单因素进行筛选[15]。
(7)
式中:Y——响应值,%
Xi——试验中的独立变量
β0——常数
βi——线性回归系数
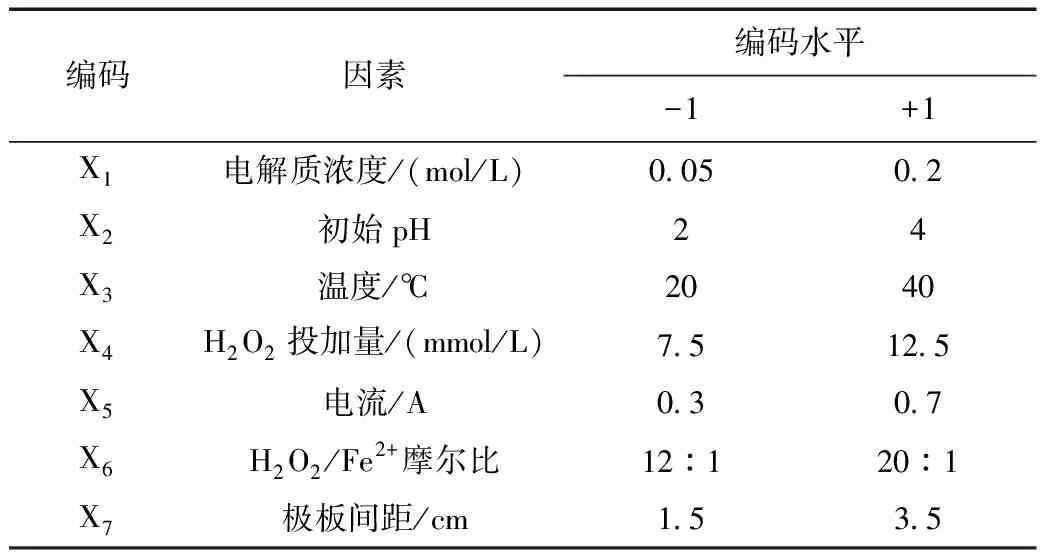
表1 Plackett-Burman试验各因素及其编码水平
采用Design Expert 8.0.6软件对表2进行分析,得到各影响因素的偏回归系数及其显著性,分析结果见表3。

表2 Plackett-Burman试验结果一览表

表3 偏回归系数及影响因子的显著性分析
由表3可得,模型的P值=0.001 7<0.01极显著,F值为38.34表明整个筛选试验的数据都在99.99%的置信区间内,数据真实模型可靠、误差小,可以建立回归方程拟合试验结果。通过逐步回归拟合分析,得出各单因素与TC去除率之间的多元一次回归方程,见式(8)。
Y=77.66-2.55X1+8.08X2-1.24X3+0.21X4+5.2X5+0.56X6-1.5X7
(8)

综上,由上述Plackett-Burman筛选试验可得初始pH、电流强度对电-Fenton法降解TC的影响极显著(P<0.01)、电解质浓度对电-Fenton法降解TC影响显著(P<0.05)。
3 结 论
(1)当盐酸四环素初始浓度为100 μmol/L时,各单因素试验的最佳条件为:溶液初始pH=3、温度为30 ℃、H2O2投加量为10 mmol/L、电流强度为0.5 A、H2O2/Fe2+摩尔比为16:1、电解质浓度为0.1 mol/L、极板间距为2.5 cm;
(2)在一定范围内,TC降解效率随着各影响因素的增加而增加。对于低浓度TC废水,通过Plackett-Burman试验筛选出对TC去除率有显著影响的三个单因素为溶液初始pH、电流强度和电解质浓度。其中,溶液初始pH对TC降解效果的影响极显著,当pH由2.0增加到6.0时,TC降解效率的波动可达到34.66%。

