复合保温干预对老年胃肠外科手术患者体温和苏醒质量的影响
杨西紫
(湖南省人民医院,湖南师范大学附属第一医院麻醉复苏室,湖南 长沙 410000)
胃肠疾病比较常见。严重的胃肠疾病,需采用手术治疗的方法。临床胃肠手术治疗中,受多种因素的影响,如手术患者年龄较高、麻醉剂使用状况不佳、手术室环境温度低等,患者术中可出现低体温,这会影响到手术治疗的效果,对患者的术后恢复以及苏醒造成不利影响[1]。术中低体温的出现,也直接增加了患者出现并发症的概率,对患者的生命安全造成极大威胁。对此,需为患者提供有效的保暖措施,改善以往保温处理的局限性。复合保温是一种新型的干预手段,可维持患者术中体位以及生理指标的稳定性,降低患者低体温以及其他并发症的发生风险,保障手术的安全性以及有效性[2]。本文对2022 年4 月至2023年4 月期间湖南省人民医院收治的100 例老年胃肠外科手术患者进行研究,旨在探讨复合保温干预对老年胃肠外科手术患者体温和苏醒质量的影响。现报告如下:
1 资料与方法
1.1 基线资料
选取2022 年4 月至2023 年4 月期间湖南省人民医院收治的100 例老年胃肠外科手术患者,随机分成研究组与参照组,各50 例。研究组中,女26 例、男24 例;年龄60 岁~81 岁,平均年龄(72.20±5.23)岁。参照组中,女27 例、男23 例;年龄61 岁~82 岁,平均年龄(72.41±5.19)岁。两组患者基线资料比较,差异无统计学意义(P>0.05)。纳入标准:符合胃肠手术治疗的相关标准;知情同意参与本次研究;可正常语言交流。排除标准:存在凝血功能障碍;一般资料不完整;中途退出研究;存在传染性疾病;对麻醉药物过敏。此次研究经医院伦理委员会批准。
1.2 方法
参照组给予常规保温干预,在手术过程中将手术室的温度调整到23 ~25℃之间,室内的湿度控制在43% 左右。在手术期间要使用毛毯覆盖患者暴露在外的皮肤,并做好常规消毒处理。此外,手术期间要观察患者是否有低体温表现,若患者寒战状况持续时间超过5 分钟,要加用毛毯。
研究组在常规护理基础上给予复合保温干预,方法是:(1)对手术室温度进行调节:在患者进入手术室后的前半个小时,要将手术室的温度调节到23 ~25℃,通常室内的湿度应当设定在55%。行皮肤消毒处理以及麻醉处理时,需将手术室温度调整到25 ~28℃,手术开始前需将室内的温度调整到22 ~24℃之间。(2)体表加温处理:手术前应当在床上铺设好无菌单,之后放置温度为38℃的循环水毯,最后铺好充气式保温毯。使用温度加热到40℃的消毒液完成对患者局部皮肤的消毒处理。手术过程中要根据室内的温度,对患者暴露在外的皮肤予以保暖处理,如上肢、下肢、肩部、头部等。另外,消毒处理患者的皮肤时,手术室最适宜的温度为26℃,尽可能快速完成消毒处理,缩短整体的消毒时间。(3)体温监测:手术过程中需要监测患者的体温,并观察患者的生命体征改变。应提前对患者的静脉输入液及冲洗液进行加温处理,或者是使用加温器持续加温液体,最适宜的温度是39 ~41℃。对于加温处理过后的输入液体,通常应当在两个小时以内完成应用。(4)复苏期的保温处理:手术完成以后患者要保持平卧位,并在患者肢体上覆盖棉被。运送患者的过程中,要观察患者的体征变化。患者处在苏醒期时,要监测其生命体征,如果有异常要立刻进行处理。
1.3 观察指标
对比两组患者不同时间点的体温,包括麻醉前、麻醉后、手术前、手术开始1 小时以及手术后。对比两组患者的苏醒质量,指标包括苏醒时间、拔管时间、麻醉苏醒室滞留时间。对比两组患者的并发症发生情况,包括低体温、切口感染、深静脉血栓、呼吸抑制等。
1.4 数据处理
选用SPSS 19.0 统计学软件处理分析数据,计量资料采用t检验,计数资料采用χ² 检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者不同时间点体温对比
麻醉前、麻醉后、手术前、手术开始1 小时、手术后,研究组的体温分别为(36.80±0.40)℃、(36.50±0.40)℃、(36.30±0.31)℃、(36.20±0.30)℃、(36.10±0.33)℃,参照组的体温分别为(36.90±0.30)℃、(36.30±0.30)℃、(35.97±0.40)℃、(35.60±0.40)℃、(35.31±0.40)℃。麻醉前两组患者体温比较无明显差异(P>0.05),麻醉后、手术前、手术开始1 小时、手术后研究组患者体温均高于参照组(P<0.05)。见表1。
表1 两组患者不同时间点体温比较(℃,±s)
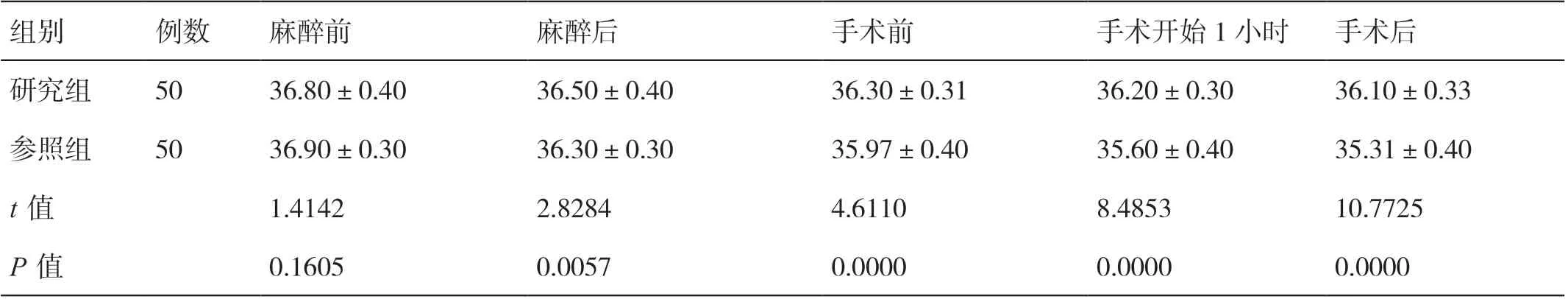
表1 两组患者不同时间点体温比较(℃,±s)
组别例数麻醉前麻醉后手术前手术开始1 小时手术后研究组5036.80±0.4036.50±0.4036.30±0.3136.20±0.3036.10±0.33参照组5036.90±0.3036.30±0.3035.97±0.4035.60±0.4035.31±0.40 t 值1.41422.82844.61108.485310.7725 P 值0.16050.00570.00000.00000.0000
2.2 两组患者苏醒质量对比
研究组的拔管时间、苏醒时间、麻醉苏醒室滞留时间分别为(15.60±4.25)min、(7.92±2.14)min、(22.50±3.68)min,参照组的拔管时间、苏醒时间、麻醉苏醒室滞留时间分别为(17.81±3.92)min、(9.66±2.87)min、(28.91±4.51)min。研究组苏醒时间、拔管时间、麻醉苏醒室滞留时间均短于参照组(P<0.05),见表2。
表2 两组患者苏醒质量比较(min,±s)
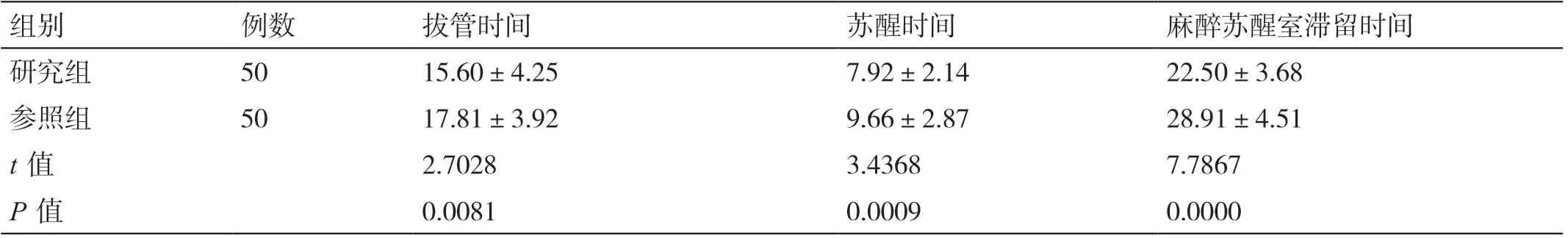
表2 两组患者苏醒质量比较(min,±s)
组别例数拔管时间苏醒时间麻醉苏醒室滞留时间研究组5015.60±4.257.92±2.1422.50±3.68参照组5017.81±3.929.66±2.8728.91±4.51 t 值2.70283.43687.7867 P 值0.00810.00090.0000
2.3 两组患者并发症对比
研究组出现1 例深静脉血栓,并发症发生率为2%;参照组出现3 例深静脉血栓、2 例低体温、2 例切口感染以及2 例呼吸抑制,并发症发生率为18%。研究组并发症发生率低于参照组(χ²=7.0400,P=0.0079 <0.05)。
3 讨论
在胃肠手术过程中,患者会因受到手术牵拉、麻醉、腹腔暴露等因素的刺激而出现胃肠神经性抑制,肠道的蠕动功能会受到影响,从而影响术后胃肠道功能的恢复[3]。特别是老年手术患者,他们本身的机体免疫力以及抵抗力较低,器官功能也出现了退行性改变,故术后恢复受到直接影响[4]。胃肠外科手术中患者低体温的风险如下:(1)会增加手术切口感染的风险。手术过程中人体温度较低,此时血管收缩能力降低,极易出现局部组织缺血缺氧,可对伤口愈合造成影响,增加感染发生的概率。(2)降低基础代谢。低体温会使药物的代谢速度变慢,影响到麻醉手术患者的苏醒时间,故术中对患者体温的监测十分重要。(3)增加了患者手术过程中出血的风险。患者体温过低,血小板功能会随之受到影响,导致凝血功能下降,极易出血。(4)低体温极易导致老年患者出现交感神经兴奋的表现,此时患者血压增高、心率过快,一些患者还容易演变成心衰或者是心律失常。
上述情形的出现,对手术患者的机体健康造成的影响极大,也影响到手术的安全性。对此,要做好患者的围术期保温处理,以免患者出现低体温[5]。若患者术中出现低体温,会对其手术治疗期间生命体征的平稳造成影响,出现并发症的风险增加,也会在一定程度上影响到患者的麻醉苏醒质量[6]。传统的围术期保温处理,会使用盖毛毯的方法,此种保温措施属于被动方法,仅仅是减少患者术中热量的丢失,无法为患者提供热量[7]。胃肠手术过程中麻醉药物的运用以及静脉输液可导致患者的体温直线降低,单一采用传统的保温处理方法,无法取得理想的保温效果[8]。手术过程中患者体温的降低幅度过大,可导致其出现心律失常、心动过速以及呼吸抑制等表现,对手术治疗的效果造成影响,也威胁到患者的生命安全[9]。因此,应探索一种全新的保温干预方法,避免手术时患者体温过度降低。复合保温干预在近几年的应用比较频繁,也取得了比较理想的运用效果[10]。复合保温干预会在围术期为患者提供有效的保温处理,使患者出现低体温的概率大幅度降低,稳定患者的生命体征[11]。
本研究的结果显示,麻醉前两组患者体温比较无明显差异(P>0.05),麻醉后、手术前、手术开始1 小时、手术后研究组患者体温均高于参照组(P<0.05)。研究组苏醒时间、拔管时间、麻醉苏醒室滞留时间均短于参照组(P<0.05)。研究组并发症发生率低于参照组(P<0.05)。通过本次研究的结果得知,研究组患者的苏醒时间短于参照组患者,且患者术中出现低体温以及呼吸抑制等并发症的概率较低,这表明复合保温干预可使患者麻醉苏醒的时间缩短,降低并发症的发生概率[12]。常规保温干预会通过调节手术室的温度、使用电热毯等方式,维持患者的术中体温[13]。但是,使用电热毯可能会导致患者背部的血管受到压迫,致使血液流动速度缓慢[14]。复合保温干预是采用多种手段,从多个角度、多个层面实施保温处理。研究表明,进行复合保温干预可提高患者的苏醒质量[15]。
综上所述,对老年胃肠外科手术患者进行复合保温干预可改善其围术期低体温的情况,提升其苏醒质量,减少术后并发症的发生,值得推广应用。

