Al含量对Cu-Ni系粉末冶金合金耐蚀性能的影响
常延丽,洪 实,张思瑶
(西安工程大学材料工程学院,陕西 西安 710048)
0 前 言
随着我国加快对海洋资源的开发利用,金属材料在海洋环境中面临的腐蚀是开发海洋资源必须考虑的问题。在众多金属材料中,铜及其合金由于其良好的耐蚀性能和综合力学性能,被广泛应用于航空航海、海洋新型能源、海工装备等众多领域[1-3]。海洋环境盐度和湿度较高,铜及其合金作为海洋工程领域的关键材料,在海洋环境下的耐蚀性能及安全可靠性是重点考虑因素。因此,研究提高铜及其合金的耐腐蚀性具有重要的理论意义和实用价值。
目前研究开发的耐蚀铜合金主要有:添加Cr、Mn的铝青铜,如0.2Mn的Cu-6Al合金;Cu-Ni系白铜合金,如Cu-2Ni-1Ti、Cu-5Ni-2.5Ti合金、B10(Cu-10Ni-1Fe-1Mn)、B15(Cu-15Ni-0.5Cr-0.5Mn-0.7Fe)、B30(Cu-30Ni-1Fe-1Mn)等;加入Si元素的Cu-Ni-Sn斯匹诺达尔合金[4]等。上述合金在各种介质中均具有较好的耐腐蚀性能,但因其制作成本高、加工性能较差,应用受到一定的限制。目前,应用较为广泛的是Cu-Ni系白铜合金,白铜合金具有一定的抗污损能力,能防止海洋微生物的黏附和污损侵蚀,在海洋工程领域具有非常广阔的应用前景[5]。
添加及优化合金元素含量是改善Cu-Ni合金耐蚀性的有效途径,其中主要以镍、铝、铁、锰、稀土等其中的一种或多种为主要添加元素。本工作在对比分析Cu-10Ni合金相关报道[4,5]基础上,设计了一系列不同Ni、Al含量的Cu-Ni系合金,制备得到新型Cu-Ni-Al合金,通过静态全浸腐蚀试验、电化学测试、扫描电镜观察合金的微观腐蚀形貌等手段,研究Al元素添加量和Cl-浓度对新型Cu-Ni-Al合金耐蚀性能的影响,探讨新型Cu-Ni-Al合金在人工海水中的耐蚀性能。
1 试 验
1.1 放电等离子烧结(SPS)制备Cu-Ni-Al合金
选用金属粉末性能如下:铜粉(≥99.99%,500 nm);镍粉(≥99.999%,链状);铝粉(≥95%,30 μm);铁粉(≥98%,500 nm);锰(99%,50 nm)。
将一定比例(质量分数)的金属粉末(Al 1%,3%,5%;Ni 9%,7%,5%;Fe 1%;Mn 1%;Cu 88%)放入F-P2000E行星式球磨机进行研磨,转速300 r/min,球料比为10∶1(φ5 mm钢球),球磨时间为8 h。将球磨后的金属粉末装入石墨模具内,采用SPS-20T-10型放电等离子烧结炉,利用上、下模冲和通电石墨电极将压制压力和特定冶金烧结电源施加于烧结粉末上,经过放电活化(时间25 min,功率20 kW,输入电源AC 380 V 50 Hz 三相,输出电流DC 0~1 500 A,输出电压DC 0~10 V)、热塑变形(温度为800 ℃,时间为15 min,压力为3 MPa)、随炉缓慢冷却3个阶段,将粉末制成致密的Cu-Ni-Al合金块状材料。
1.2 测试分析
1.2.1 静态全浸腐蚀试验
使用线切割将SPS烧结得到的不同系列的合金加工成φ7 mm×5 mm的试样,表面经180,400,800,1 000,1 200号水砂纸逐级打磨后抛光,然后放入超声波清洗仪中用酒精清洗干净,60 ℃下烘干。试验腐蚀介质为浓度为0.1,0.4,0.8 mol/L的NaCl溶液。将不同浓度NaCl溶液和试样放入烧杯,试样互不接触并且不与烧杯壁接触,如表1编号后,浸泡240 h后冲洗,再放入烘箱中80 ℃烘干取出样品,观测试样腐蚀情况。
1.2.2 相对密度、硬度、电导率
密度采用精度为0.001 g的AL-104电子天平进行测试计算。使用HVS-1000Z维氏硬度计进行硬度测试,压头为正四棱锥金刚石,加载负荷20 N,加载时间为5 s。使用DP-D60K数字金属电导率测量仪进行电导率测试。每种测试每个试样均测试4~5次,取平均值。
1.2.3 腐蚀产物形貌及成分
采用PR4XC金相显微镜观测Cu-Ni-Al合金腐蚀前的形貌。采用QUANTA-450-FEG场发射扫描电镜(FESEM)观测Cu-Ni-Al合金腐蚀后形貌,然后配合Oxford能谱仪(EDS)来进行腐蚀产物的成分分析。使用DX-2700BH型X射线衍射仪(XRD)对表面腐蚀产物进行分析,管压40 kV,管流200 μA,Cu靶,扫描速度2 (°)/min,扫描范围10°~90°。
1.2.4 电化学测试
使用CS350H型电化学工作站进行测试,通过测试试样的交流阻抗谱和极化曲线等电化学性能,研究合金的电化学性能与合金中Al元素含量以及腐蚀时Cl-浓度的关系。交流阻抗谱测试频率范围为1.0×(105~10-2) Hz。测试采用三电极体系,工作电极为待测样品,与对电极铂电极相对,测试时尽量保持样品与铂片相平行,参比电极为带鲁金毛细管饱和甘汞电极(SCE)。动电位极化曲线测试时,初始电位设置为-0.5 V,终止电位设置为0.2 V,扫描速度为2 mV/s,测试温度为24 ℃。
2 结果与讨论
2.1 基本性能
Cu-Ni-Al系列合金的相对密度、硬度及电导率指标如表2所示。由表2可以看出,与Cu-10Ni合金相比,Cu-Ni-Al合金的相对密度、硬度和电导率大致呈提高趋势。随着Al含量的增加,合金的硬度越来越高。这是因为少量的Al在Cu-Ni合金中可以析出一些沉淀强化相,起到沉淀硬化作用,大幅度提高合金的强度硬度,增强合金的力学性能。而Al元素的含量对电导率影响不大,但与未添加Al的Cu-10Ni相比,Al元素的添加可提高合金电导率,这是因为纯铝的电导率(3.52×107S/m)比纯镍的电导率(1.46×107S/m)高所致。
图1为Cu-Ni-Al合金的金相组织。由图可以看出合金表面孔洞较少,组织较为致密。这是由于SPS技术在真空条件下同时加压和烧结成型可以提高合金的密度,同时SPS加热速度快,避免了晶粒长大,有助于制备出致密度优良的合金。

图1 不同 Al含量Cu-Ni-Al合金形貌Fig. 1 Metallographic structure of Cu-Ni-Al alloys with different Al contents
结合表2 和图1 可知,SPS等离子热压烧结可制备出致密且硬度、导电率等综合性能优良的Cu-Ni-Al合金。
2.2 微观腐蚀形貌
2.2.1 不同Al含量
图2为Al含量3%样品在0.4 mol/L Cl-腐蚀液中(样品2-2)腐蚀240 h后表面形貌。由图可以看出样品在腐蚀液中腐蚀240 h后,表面可见明显的腐蚀产物(图2中白色物质),表面已经被腐蚀生成疏松、颗粒状的腐蚀产物,散乱分布在样品表面,由图2c,2d可以很明显看出,腐蚀产物的颗粒呈规则枝晶状,随着倍数的增大,枝晶状越明显。
图3为不同 Al含量Cu-Ni-Al合金试样在0.8 mol/L的Cl-腐蚀介质中静态浸泡240 h后表面SEM形貌。由图可以看出,随着Al元素含量的增加,表面腐蚀产物的数量减少。这是因为Al元素对Cu-Ni合金表面具有强化作用,可以在合金表面形成一层Al2O3钝化膜,降低表面活性,进而阻止了腐蚀的进一步发生,提高了合金的耐腐蚀性能[6-8]。
2.2.2 不同 Cl-浓度
图4为Al 含量为1%的Cu-Ni-Al合金在不同浓度Cl-介质中腐蚀240 h 后表面形貌SEM形貌。由图可以看出,在Al元素含量相同时,Cl-浓度越高,样品表面腐蚀产物越多,表面越粗糙,腐蚀越严重,原因是因为Cl-与金属表面的氧化亚铜发生反应形成了点蚀,促进了金属的破坏,这种反应在一定范围内与Cl-浓度呈正相关[9]。

图4 Al 含量为1%的Cu-Ni-Al合金在不同浓度腐蚀液中腐蚀240 h 后表面形貌 Fig. 4 Surface morphology of Cu-Ni-Al alloys with 1% Al after corrosion 240 h in different concentrations of corrosive liquid
2.3 腐蚀产物
图5为不同 Al含量Cu-Ni-Al合金在0.8 mol/L腐蚀液中浸泡腐蚀240 h后EDS谱。由图5可以看出,腐蚀产物中主要有O、Cl、Fe、Al、Ni、Cu元素,其中Cu元素主要来自样品本身以及腐蚀产物,O元素含量也比较高,主要来自腐蚀产物Cu、Al、Fe、Ni的氧化物。此外,Al元素含量为1%时,EDS未检测到Al元素,而Al元素含量为3%和5%时,EDS检测到了Al元素,且与Al元素为3%相比,Al元素为5%时EDS测试到的Al元素原子比例有所增加,这说明Al元素含量增加,表面腐蚀产物中的Al2O3增多。这与上述SEM分析结果一致。
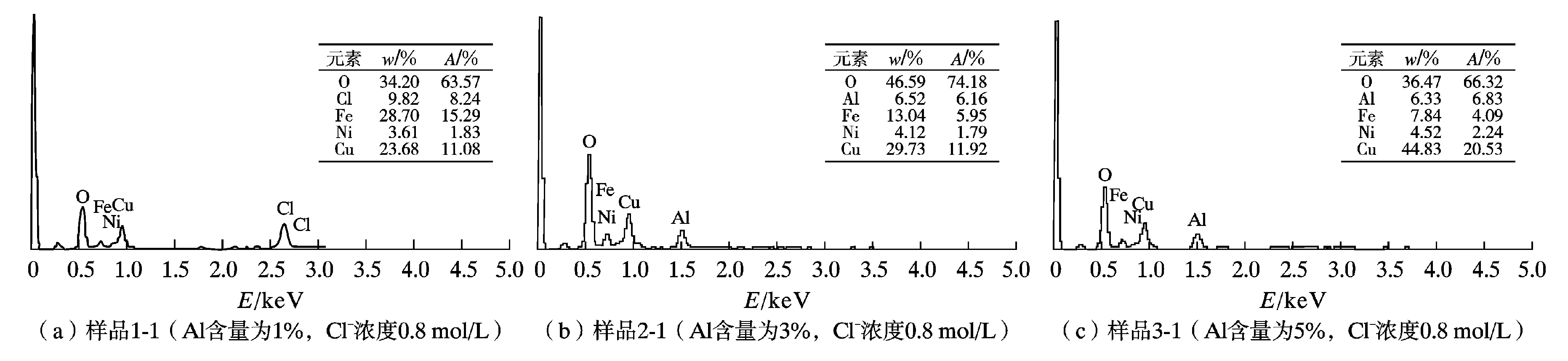
图5 不同 Al含量Cu-Ni-Al合金在0.8 mol/L介质中浸泡腐蚀后EDS谱Fig. 5 EDS analysis of Cu-Ni-Al alloys with different Al contents after soaking in 0.8 mol/L corrosion solution
图6为样品1-3、2-3和3-3静态浸泡240 h后的XRD谱。

图6 样品1-3、2-3和3-3腐蚀240 h后的XRD谱Fig. 6 XRD diffraction pattern of 1-3、2-3 and 3-3 after corrosion for 240 h
由图6可知,合金表面腐蚀产物有Cu2O和Cu2(OH)3Cl,结合EDS以及文献分析,合金材料的表面腐蚀产物膜为双层膜结构,外层表面疏松产物主要为Cu2(OH)3Cl膜层,内层为结构致密的Cu2O膜层。值得注意的是,样品1-3和2-3静态浸泡240 h后的XRD谱检测到了Cu2O和Cu2(OH)3Cl,但是样品2-3只检测到了Cu2(OH)3Cl而未检测到Cu2O。腐蚀的整个反应如下所示:合金材料中的Cu、Ni、Al在腐蚀介质中Cl-的作用下发生优先溶解并于合金材料表面有效生长堆积形成Al2O3、NiO和Cu2O产物膜[10],其反应过程如式(1)、(2)、(3)、(4)所示。Cu2O膜增厚后进一步与Cl-发生反应形成Cu2(OH)3Cl,其反应过程如式(5)所示。因此推测样品2-3只检测到了Cu2(OH)3Cl而未检测到Cu2O,可能是此样品测试区域内多数Cu2O与Cl-发生反应形成Cu2(OH)3Cl导致Cu2O含量较少,故未检测到。但因为检测到了Cu2(OH)3Cl,根据腐蚀过程可以推断出腐蚀产物是有Cu2O的。
(1)
Ni2++2OH-→NiO+H2O
(2)
(3)
(4)
(5)
2.4 电化学测试
2.4.1 交流阻抗谱
图7为不同含量Al元素合金在不同Cl-浓度腐蚀介质中腐蚀240 h后的阻抗谱。由图7可以看出,交流阻抗谱由高频区、中频区、低频区3部分组成,在低频区呈现出1个类似线性的趋势,中频区呈现出半圆形趋势,高频区呈现类似线性趋势。随着腐蚀液浓度的降低,高频阻抗弧越来越大,且阻抗弧的完整性越来越差。阻抗弧完整性越好表明表面的膜层更加完整。高频阻抗弧半圆直径越大,耐蚀性能越好。由图7a,7b,7c可看出,随着Cl-浓度的增加,半圆直径逐渐变小,表明材料耐蚀性能越来越差[4]。由此可见,腐蚀液浓度的升高促进合金腐蚀行为的发生。这与图4,Al 含量为1%的Cu-Ni-Al合金在不同浓度腐蚀液中腐蚀240 h 后表面形貌的分析结果一致。这是由于腐蚀介质中Cl-浓度增大,会抑制Cu-Ni-Al合金材料表面Cu2O腐蚀产物膜的形成,阻碍破坏合金表面致密腐蚀产物膜的生成,削弱Cu2O膜对内部合金材料的保护能力,降低合金材料的耐腐蚀性。

图7 不同含量Al元素合金在不同Cl-浓度腐蚀介质中腐蚀240 h后的阻抗谱Fig. 7 Impedance spectra of Al alloys with different content in different Cl- concentration corrosive media after corrosion for 240 h
由图7f可以看出,当Cl-浓度为 0.1 mol/L时,随着Al元素含量的增加,半圆直径越来越大,表明合金的耐蚀性能随Al含量的增加而提高。这与图3(不同 Al含量Cu-Ni-Al合金在0.8 mol/L的Cl-介质中静态浸泡240 h后表面形貌)和图5(不同 Al含量Cu-Ni-Al合金在0.8 mol/L介质中浸泡腐蚀后EDS谱)的分析结果是一致的。
然而,图7d和图7e随着Al含量的提高,高频阻抗弧半圆直径逐渐减小,表明此时随着Al元素含量的增加,合金的耐腐蚀性能反而是下降的,这是由于钝化膜处于一种动态平衡过程中,在腐蚀反应中钝化膜处于不断地生成又被腐蚀破坏然后再次钝化生成这样一种循环过程中[11],因此,Al含量5%的合金在Cl-浓度为 0.4 mol/L和0.8 mol/L中腐蚀240 h,由于钝化膜处于被破坏后重新生成的阶段,此时腐蚀加剧,阻抗谱中容抗弧半径有所减小。
2.4.2 极化曲线
图8为不同含量Al元素合金在不同Cl-浓度腐蚀介质中腐蚀240 h后的极化曲线。表3为由极化曲线拟合得到各样品的自腐蚀电位与腐蚀电流密度。结合图8和表3可以看出,在Al元素含量相同时,以含Al量为3%的3个样品(图8b)为例,随着腐蚀溶液浓度的降低,自腐蚀电位由-0.294 7 V上升到-0.219 6 V,腐蚀电流密度由6.816 3×10-5A/cm2下降到2.506 3×10-5A/cm2,自腐蚀电位逐渐增加,腐蚀电流密度逐渐减小,合金耐蚀性能逐步增强[12,13]。这说明,腐蚀液浓度的升高有利于腐蚀的进行。在腐蚀液浓度相同时,随着Al元素含量的增加,以0.8 mol/L Cl-腐蚀液中3个样品(图8d)为例, 自腐蚀电位由-0.261 4 V下降到-0.314 9 V,腐蚀电流密度由3.818 3×10-5A/cm2上升到9.513 7×10-5A/cm2,自腐蚀电位降低,电流密度反而增加,合金的耐蚀性能逐渐降低。这与阻抗谱分析一致,是由于钝化膜处于一种动态平衡过程中,在腐蚀反应中钝化膜处于不断地生成又被腐蚀破坏然后再次钝化生成这样一种循环过程。
此外值得注意的是,由表3拟合数据可知,样品1-3,2-3和3-3的自腐蚀电位相差很微小,这与图8f一致,图8f中的曲线水平部分几乎重叠,所以自腐蚀电位相差无几。同时,由表3也可以看出样品1-3,2-3和3-3的电流密度也相差不大。1-3到3-3有小幅度的增加,这与图8f是一致的,但与图7f所得结论不一致。这可能是因为这2种方法本身测试的重点不同,极化曲线是用强烈极化的动态电极行为外推平衡状态时,切线拟合时因人而异引入人为误差的可能性极大;而阻抗谱则是在电极处于稳定平衡状态的测试的,因此,EIS结果更能表征电极在静态平衡时的行为。结合图3腐蚀表面形貌SEM图和图5 EDS分析结果认为阻抗谱更能说明本试验中Cu-Ni-Al合金的耐腐蚀性,即随着Al元素含量的增加,半圆直径越来越大,表明合金的耐蚀性能随Al含量的增加而提高。
3 结 论
(1)SPS等离子热压烧结可制备出致密且硬度、电导率等综合性能优良的Cu-Ni-Al合金,且与Cu-10Ni合金相比,Cu-Ni-Al合金的致密度、硬度和电导率均有提高。
(2)Cu-Ni-Al合金在NaCl腐蚀介质中长时间浸泡,合金表面逐渐形成含有Cu2O的腐蚀保护膜,同时Cu2O保护膜外层会与腐蚀介质中的Cl-发生进一步反应,形成一层Cu2(OH)3Cl产物膜,进而于合金表面形成Cu2O和Cu2(OH)3Cl双层膜结构。
(3)Al含量相同时,随着腐蚀液中Cl-浓度的增加,阻抗谱半圆直径逐渐变小,合金腐蚀逐渐加剧,表明在一定范围内Cl-浓度的提升会促进Cu-Ni-Al合金的腐蚀。

