羟考酮通过TLR4/p38MAPK通路抑制小胶质细胞的活化缓解大鼠骨癌痛①
方 军 董庆永 刘志东 陶 宏(滕州市中心人民医院麻醉科,滕州 277599)
骨癌痛是指部分癌症发生骨转移造成的疼痛反应,发病时引发患者剧烈疼痛,且疼痛效果往往持续很长时间,对患者的身体健康和生活造成极大困扰[1]。由于其发病原因多种多样,难以对症下药,目前仅通过缓解疼痛类药物减缓疾病发作,但副作用极大,故开发具有针对性的治疗药物一直是研究的热点[2-3]。已知有多种信号通路参与调控骨癌疼痛反应,其中发挥重要作用的是Toll 样受体4(Toll-like receptor 4,TLR4)及其下游p38 丝裂原活化蛋白激酶(p38 mitogen-activated protein kinase,p38MAPK),TLR4 在中枢神经系统小胶质细胞中特异性高表达[4]。小胶质细胞作为神经系统中的巨噬细胞,在神经反应初期即被激活引发疼痛反应。在神经病理性疼痛中,TLR4 是关键受体,调控疼痛反应[5]。TLR4高表达可参与激活p38MAPK,两者共同作用激活小胶质细胞,加速神经疼痛传递,加重病情[6]。
羟考酮作为一种生物碱的半合成蒂巴因衍生物,可缓解神经传递,因此已被应用于神经麻醉[7]。临床试验证实其可参与缓解神经病理性疼痛,且具有给药途径广泛、成本低廉的优点[8]。但其作用机制尚未明确,推测其可通过调控TLR4 阻碍神经传递,缓解骨癌疼痛反应,但还需进一步实验加以说明。本研究通过构建骨癌痛大鼠模型,探究羟考酮是否通过TLR4/p38MAPK 通路调控骨癌引起的神经疼痛。
1 材料与方法
1.1 材料
1.1.1 实验动物 SD 雄性健康大鼠72 只,体质量(230±20)g,许可证号:SCXK(豫)2020-0004,购于河南环宇康禾生物科技有限公司。
1.1.2 主要试剂及仪器 羟考酮(国药准字:J20171086)购于国药集团工业有限公司;Walker256乳腺癌细胞液(货号:AC340389)购于美国ATCC 公司;盐酸曲马多缓释片(国药准字:H20100175)购于康德乐大药房;TNF-α ELISA检测试剂盒(货号:XGS64726)购于上海西格生物科技有限公司;IL-1β ELISA 检测试剂盒(货号:AZ0646)购于北京普利莱基因技术有限公司;TLR4 激活剂Kdo2-Lipid A ammonium(货号:HY-N8277)购于MCE 公司;TLR4抗体(货号:ab13556)、p38MAPK 抗体(货号:ab170099)、p-p38MAPK 抗体(货号:ab284564)购于Abcam 公司;热测痛仪(Bioserve,北京友诚嘉业生物科技有限公司);纤维丝刺激针(上海玉研科学仪器有限公司);荧光定量PCR 仪(7500,ABI公司);凝胶成像系统(H-120,上海生工)。
1.2 方法
1.2.1 动物模型的构建 将72只大鼠随机分为假手术组、骨癌痛组、阳性药物组、羟考酮高浓度组、羟考酮低浓度组、羟考酮+TLR4 激活组,每组12只。麻醉各组大鼠,固定于操作台上,各组大鼠左后肢消毒处理,手术刀切开表面组织,剥离筋膜暴露胫骨,假手术组立即缝合伤口并消毒处理。除假手术组外,其余大鼠于骨髓腔内注射Walker256 乳腺癌细胞液10 µl,骨蜡封合针孔后缝合伤口,消毒处理。5 d后,除假手术组外,其余各组大鼠切开枕部皮肤,进行鞘内置管,采用无菌注射器刺破寰枕膜,观察到脑脊液流出后置入PE-10导管,固定后缝合皮肤,消毒处理,假手术组不做处理。各组术后肌内注射少量青霉素防止感染。术后阳性药物组大鼠腹腔注射曲马多10 mg/kg,羟考酮高浓度组大鼠腹腔注射羟考酮25 µg/kg,羟考酮低浓度组大鼠腹腔注射羟考酮5 µg/kg,羟考酮+TLR4 激活组大鼠腹腔注射羟考酮25 µg/kg和TLR4激活剂Kdo2-Lipid A ammonium 10 mg/kg,假手术组、骨癌痛组大鼠注射等剂量生理盐水,1 次/d,连续注射10 d。该研究得到滕州市中心人民医院动物伦理委员会批准,符合动物实验3R原则。
1.2.2 动物行为学检测
1.2.2.1 后足热缩足反射潜伏期(thermal withdrawal latency,TWL)检测 依据文献[9]方法,分别于术前1 h、术后3 d、5 d、7 d、10 d进行TWL检测,将各组大鼠分别置于玻璃箱中,设定测痛仪器指数,使辐射热控制为定值(基础值15 s 左右),照射持续时间18 s,待玻璃箱中大鼠逐渐适应环境后,将辐射热光源对准大鼠足部中心位置,若大鼠出现缩足反应则关闭辐射热光源,记录该反应出现的时间。如无反应则继续照射直至18 s。相同实验重复测量3次。每次测量间隔3 min以上。
1.2.2.2 机械缩足反射阈值(mechanical withdraw threshold,MWT)检测 每次TWL 检测后,将各组大鼠置于底部由铁丝网构成的透明玻璃箱中,采用特制的纤维丝构造的刺激针,待大鼠充分适应环境后,透过下层铁丝网,将纤维丝以垂直方式刺激大鼠后肢足底中心位置,先是缓慢接触,而后逐渐用力。直至大鼠回缩,记录大鼠回缩时的最小刺激力度,取平均值,连续测量5次,每次测量间隔1 min。
1.2.3 大鼠脊髓神经炎症相关因子检测 末次注射24 h 后,处死各组大鼠,手术刀切开背部皮肤,充分暴露背部组织,取脊神经中的脊髓(L4-L6 脊髓段),部分置于4%多聚甲醛中固定备用。剩余部分液氮处理研磨至粉,取部分冻存备用,剩余粉末制成匀浆,充分振荡后离心获取上层清液,按照ELISA试剂盒说明书方法检测脊髓中TNF-α、IL-1β水平。
1.2.4 免疫荧光染色法检测OX-42 蛋白水平 部分脊髓固定24 h 后,脱水包埋处理,冷冻切片机切片(厚度20 µm),H2O2室温孵育后,山羊血清封闭,滴加OX-42 抗体(1∶200),4 ℃孵育过夜。滴加荧光二抗(1∶1 000),常温孵育50 min,置于荧光显微镜下观察,软件计算荧光积分光密度(integrated optical density,IOD)。
1.2.5 脊髓TLR4、p38MAPK、p-p38MAPK、OX-42蛋白检测 取出冻存备用的脊髓粉末,加入蛋白裂解液1 ml,充分裂解细胞后提取蛋白与上样缓冲液混合振荡,加热变性后加入凝胶孔道中,电泳后转膜,5%脱脂牛奶封闭2 h,加入一抗(GAPDH、TLR4、p38MAPK、p-p38MAPK、OX-42,1∶2 000),4 ℃孵育过夜。TBST 反复清洗3 次,2 min/次。加入二抗(1∶1 000),常温孵育45 min,TBST 反复清洗3 次,2 min/次。混合发光液后倒于膜上,充分浸泡30 s,吸去多余液体,置于光密度扫描系统下检测各组条带灰度。
1.3 统计学方法 各组数据均通过表示,通过SPSS22.0 软件进行分析,组间差异采用单因素方差分析(One-way ANOVA)比较,两两比较采用SNK-q检验,P<0.05为差异有统计学意义。
2 结果
2.1 羟考酮对骨癌痛大鼠TWL、MWT 的影响 术前1 h 检测,各组间TWL、MWT 值差异无统计学意义(P>0.05)。术后3 d、5 d、7 d、10 d,与假手术组相比,骨癌痛组TWL、MWT 值显著降低(P<0.05);与骨癌痛组相比,阳性药物组、羟考酮高浓度组、羟考酮低浓度组TWL、MWT 值显著升高(P<0.05);与羟考酮高浓度组相比,羟考酮低浓度组、羟考酮+TLR4 激活组TWL、MWT 值显著降低(P<0.05);阳性药物组与羟考酮高浓度组相比,TWL、MWT 值差异无统计学意义(P>0.05),见表1、表2。
表1 各组大鼠TWL比较(,n=12,s)Tab.1 Comparison of TWL of rats in each group(,n=12,s)

表1 各组大鼠TWL比较(,n=12,s)Tab.1 Comparison of TWL of rats in each group(,n=12,s)
Note:Compared with sham operation group,1)P<0.05;compared with bone cancer pain group,2)P<0.05;compared with oxycodone high dose group,3)P<0.05.
表2 各组大鼠MWT比较(,n=12,g)Tab.2 Comparison of MWT of rats in each group(,n=12,g)
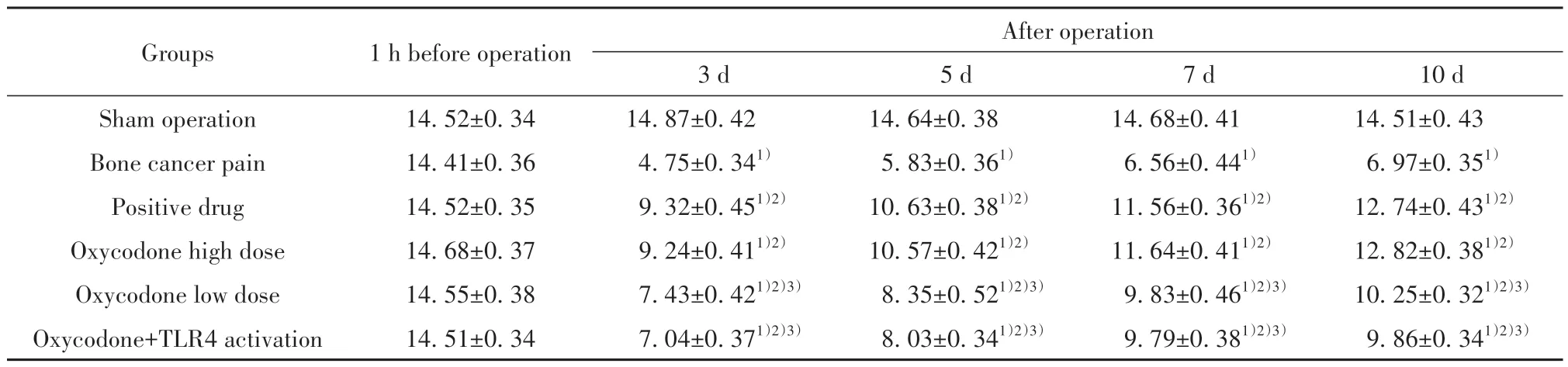
表2 各组大鼠MWT比较(,n=12,g)Tab.2 Comparison of MWT of rats in each group(,n=12,g)
Note:Compared with sham operation group,1)P<0.05;compared with bone cancer pain group,2)P<0.05;compared with oxycodone high dose group,3)P<0.05.
2.2 羟考酮对骨癌痛大鼠神经炎症的影响 与假手术组相比,骨癌痛组大鼠脊髓TNF-α、IL-1β 含量显著升高(P<0.05);与骨癌痛组相比,阳性药物组、羟考酮高浓度组、羟考酮低浓度组大鼠脊髓TNF-α、IL-1β 含量显著降低(P<0.05);与羟考酮高浓度组相比,羟考酮低浓度组、羟考酮+TLR4 激活组大鼠脊髓TNF-α、IL-1β 含量显著升高(P<0.05),阳性药物组与羟考酮高浓度组相比,脊髓各炎症因子含量差异无统计学意义(P>0.05),见图1。

图1 各组大鼠脊髓TNF-α、IL-1β含量比较Fig.1 Comparison of TNF-α and IL-1β contents in spinal cord of rats in each group
2.3 羟考酮对骨癌痛大鼠脊髓小胶质细胞活化的影响 与假手术组相比,骨癌痛组大鼠脊髓OX-42 IOD 水平显著升高(P<0.05);与骨癌痛组相比,阳性药物组、羟考酮高浓度组、羟考酮低浓度组大鼠脊髓OX-42 IOD 水平显著降低(P<0.05);与羟考酮高浓度组相比,羟考酮低浓度组、羟考酮+TLR4 激活组大鼠脊髓OX-42 IOD 水平显著升高(P<0.05),阳性药物组与羟考酮高浓度组相比,脊髓OX-42 IOD水平差异无统计学意义(P>0.05),见图2、表3。

图2 各组大鼠脊髓OX-42蛋白表达(×200)Fig.2 Expression of OX-42 protein in spinal cord of rats in each group(×200)
表3 各组大鼠脊髓OX-42蛋白表达比较(,n=12)Tab.3 Comparison of OX-42 protein expression in spinal cord of rats in each group(,n=12)

表3 各组大鼠脊髓OX-42蛋白表达比较(,n=12)Tab.3 Comparison of OX-42 protein expression in spinal cord of rats in each group(,n=12)
Note:Compared with sham operation group,1)P<0.05;compared with bone cancer pain group,2)P<0.05;compared with oxycodone high dose group,3)P<0.05.
2.4 羟考酮对骨癌痛大鼠脊髓TLR4、p38MAPK、pp38MAPK 蛋白表达的影响 与假手术组相比,骨癌痛组大鼠脊髓TLR4 蛋白表达量、p-p38MAPK/p38MAPK 显著升高(P<0.05);与骨癌痛组相比,阳性药物组、羟考酮高浓度组、羟考酮低浓度组大鼠脊髓TLR4 蛋白表达量、p-p38MAPK/p38MAPK 显著降低(P<0.05);与羟考酮高浓度组相比,羟考酮低浓度组、羟考酮+TLR4 激活组大鼠脊髓TLR4 蛋白表达量、p-p38MAPK/p38MAPK 显著升高(P<0.05);阳性药物组与羟考酮高浓度组相比,脊髓TLR4 蛋白表达量、p-p38MAPK/p38MAPK 差异无统计学意义(P>0.05),见图3。

图3 各组大鼠脊髓TLR4、p38MAPK、p-p38MAPK 蛋白表达比较Fig.3 Comparison of TLR4,p38MAPK and p-p38MAPK protein expressions in spinal cord of rats in each group
3 讨论
骨癌是一种骨恶性肿瘤,发病速度较快且发病原因多种多样,因此难以防范和有效治疗[10]。随着肿瘤的生长,往往会引发炎症和强烈的疼痛反应,严重时会形成局部肿块并引发功能障碍[11]。因此检测炎症相关因子含量变化和疼痛反应是检测骨癌损伤程度的重要指标。本研究通过构建骨癌痛大鼠模型,发现术后3 d、5 d、7 d、10 d,与假手术组相比,骨癌痛组TWL、MWT 值显著降低,且大鼠脊髓TNF-α、IL-1β 含量显著升高,表明骨癌痛大鼠疼痛明显,存在炎症反应,验证模型构建成功,具有明显骨癌疼痛症状。
羟考酮具有缓解神经传递作用,因此被应用于神经麻醉。近年来被证实对于癌症癌痛具有治疗效果,羟考酮可以和吗啡混合使用共同缓解肝功能受损患者癌症癌痛[12-13]。羟考酮也可应用于多种术后治疗,缓解骨骼治疗后引发的疼痛反应[14]。因而推测羟考酮对于骨癌疼痛同样具有治疗效果。本实验选用与羟考酮具有类似功效,且被应用于临床治疗骨癌的盐酸曲马多缓释片作为阳性对照,用于评估羟考酮的作用[15],发现阳性药物和不同浓度羟考酮处理后TWL、MWT 值显著升高,且大鼠脊髓TNF-α、IL-1β 含量显著降低,表明羟考酮可缓解炎症反应,消除疼痛,缓解骨癌病情,但其具体作用机制有待探索。近年的研究指出,神经胶质细胞在神经疼痛中发挥重要作用,小胶质细胞作为神经胶质细胞中的重要组成部分,在神经反应早期激活,其表面抗原OX-42 特异性高表达[16-17]。本研究发现,骨癌痛大鼠中OX-42 水平显著升高,与JIN 等[18]描述一致。阳性药物和不同浓度羟考酮处理后,OX-42 水平显著降低,表明羟考酮通过抑制OX-42 表达,减轻小胶质细胞活化,从而发挥作用。
有研究指出,TLR4在小胶质细胞活化过程中高表达,参与调控神经疼痛[19]。TLR4介导的免疫反应可促进胫骨癌痛的疼痛表达,加剧炎症反应[20]。TLR4高表达可激活下游p38MAPK 蛋白诱导产生持续性阵痛[21]。因而推测羟考酮可能通过调控TLR4/p38MAPK 通路产生作用。本研究发现,骨癌痛组大鼠脊髓TLR4蛋白表达量和p38MAPK磷酸化程度显著升高,阳性药物和不同浓度羟考酮处理后TLR4蛋白表达量和p38MAPK磷酸化程度显著降低,证实了羟考酮很可能通过调控TLR4/p38MAPK 通路参与影响骨癌痛。本实验在羟考酮作用的同时激活TLR4,发现激活TLR4 后,大鼠脊髓TLR4 蛋白表达量和p38MAPK 磷酸化程度显著升高,同时TWL、MWT值显著降低,脊髓TNF-α、IL-1β含量、OX-42水平显著升高,进一步证实相关推测。
综上所述,羟考酮通过调控TLR4/p38MAPK 通路,促进相关蛋白表达和激活,减轻炎症反应,抑制小胶质细胞活化,从而阻碍神经传递,缓解骨癌疼痛。羟考酮是否还通过其他通路间接参与调控骨癌疼痛,有待进一步实验加以说明。

