基于MOF@TiN-Ag/银溶胶复合基底的茶碱表面增强拉曼检测
张晓琳,张 帆,刘艳坤,王志武,李 波,吴振刚,魏颖娜*,魏恒勇,李景武*
(1.华北理工大学 药学院 河北 唐山 063210;2.华北理工大学 材料科学与工程学院 河北 唐山 063210;3.唐山市人民医院 肿瘤研究所 河北 唐山 063001;4.华北科技学院 河北省危险化学品安全与控制技术重点实验室 河北 廊坊 065201)
茶碱(Theophylline,THO)是茶叶中一种重要的嘌呤类生物碱,其化学结构与咖啡因高度相似。茶碱可舒缓支气管平滑肌,强心利尿、缓解支气管痉挛,主要用于治疗支气管哮喘和慢性阻塞性肺疾病等[1]。与此同时茶碱又是违禁药物咖啡因的主要代谢产物,因此茶碱成为运动赛场最常被检出的违禁药物之一[2-3]。而中药中非法添加茶碱的不良现象,增大了药品安全隐患[4]。因此对食品药品中非法添加的茶碱进行检测尤为重要[5-6]。
目前茶碱的检测方法主要有气相色谱、液相色谱、液相色谱-质谱、毛细管电泳、免疫分析和生物传感等技术[7-8],但这些方法操作均较为繁琐、分析时间长且需要复杂的样品前处理过程。表面增强拉曼光谱(SERS)在药物分析领域的应用广泛,其检测灵敏度高,可达单分子检测水平,且适合多元检测,具有无损、用量少等优势,《中国药典》2015年版和2020年版将拉曼光谱法作为理化分析通则方法收载。SERS技术已在药物研发、检测和使用方面得到应用,涉及体内药物检测、痕量药物检测和中药分析等领域[9]。然而,获得高灵敏的SERS基底仍是实现药物表面增强拉曼光谱检测的关键技术之一。
氮化钛(TiN)由于自身优异的热稳定性、化学稳定性以及良好的生物相容性等特性成为表面增强拉曼光谱的候选材料,其与贵金属如金、银复合后表现出优异的SERS性能。TiN 的等离子体近场增强激发了其作为SERS基底的应用[10],纳米TiN 对吸附在其上的罗丹明R6G 的拉曼信号增强因子高达104[11]。刘燕梅等[12]通过制备贵金属/氮化钛复合薄膜对烟酸进行SERS检测,测得其检出限为10-5mol/L。Guler等[13]指出金纳米粒子具有强大的光学性能,与氮化钛结合可实现较好的SERS 效应。Ban 等[14]制备出TiN 与Ag 的纳米球复合基底,通过等离子体共振协同作用提升SERS 性能,实现了对罗丹明R6G 分子的高灵敏和高稳定性检测。裴媛等[15]将银溶胶自组装在Au/TiN 复合薄膜上,并对恩诺沙星进行了检测。
使用贵金属银作为SERS 基底虽能达到相对较好的增强效果,但银易氧化,会导致存放期间的SERS 能力降低。为了实现稳定性好的表面增强拉曼光谱检测,通常利用金属有机框架(Metal-organic framework,MOF)的热稳定性及化学惰性防止银的氧化变质并起到防护作用。Zhai等[16]制备了具有较高稳定性和检测灵敏度的MOF-Au@Ag 复合SERS基底;Kim 等[17]深入研究了MOF对Ag纳米线SERS特性的保护作用,发现复合MOF材料后即使在多种环境条件下储存,Ag纳米线仍能保持优异的SERS性能。此外,研究发现MOF具有孔隙多、表面积大和吸附能力强的特点,其高效吸附和富集能力有助于提升SERS基底的检测灵敏度。
本文利用电化学阳极氧化结合氨气还原氮化法制备出TiN 纳米管阵列,通过电化学沉积法制备TiN-Ag 复合基底,并在该复合基底表面生长出MOF 保护层,得到MOF@TiN-Ag 复合基底,再复配银溶胶,实现了对茶碱的SERS检测。
1 实验部分
1.1 仪器与试剂
D/MAX 2500PC 型X 射线衍射仪(XRD,日本理学株式会社); S-4800 型场发射扫描电子显微镜(SEM,日本日立公司); JEM2800型透射电子显微镜(TEM,日本日立公司); Lambda 750S紫外-可见分光光度计(UV-Vis,美国Perkinelmer公司);DXR型拉曼光谱仪(美国热电公司)。
丙酮、异丙醇、N,N-二甲基甲酰胺、硝酸银、柠檬酸三钠、硝酸钴、2-甲基咪唑均为分析纯,购自上海阿拉丁试剂网;无水乙醇为分析纯,购自天津市兴复精细化工研究所;茶碱购自国药集团化学试剂有限公司;高纯氨气(99.99%)和高纯氮气(99.99%)购自唐山市路北区万嘉气体公司。
1.2 实验方法
本实验制备流程图如图1所示。
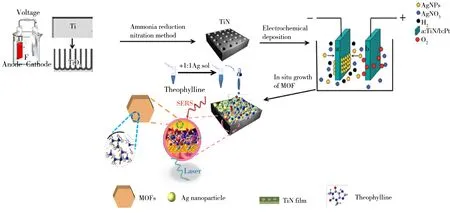
图1 MOF@TiN-Ag/银溶胶复合基底制备及其对茶碱SERS检测的实验流程图Fig.1 Experimental flow chart of preparation of MOF@TiN-Ag/Ag sol composite substrate and SERS detection of theophylline
首先采用阳极氧化法和氨气还原氮化法获得TiN 纳米管阵列结构,再利用电化学沉积技术在其表面沉积Ag 纳米材料,在此基础上,通过原位生长方式在TiN-Ag 表面形成MOF 保护层,得到MOF@TiN-Ag 复合SERS 基底。将茶碱配制成0.5 mol/L 的溶液,分别滴加在银溶胶、MOF/银溶胶、TiN/银溶胶、MOF@TiN-Ag 以及MOF@TiN-Ag/银溶胶基底上进行SERS 测试,后稀释成一定浓度,测试SERS性能最强的MOF@TiN-Ag/银溶胶复合基底对茶碱的检出限。
1.2.1 二氧化钛纳米管阵列的制备参照文献[18],将10 mm×20 mm 的钛片依次放入丙酮、异丙醇和去离子水中超声清洗10 min,接着置于体积比为1∶4∶5的HCl-HNO3-H2O的混合酸溶液中去除钛片表面的氧化物,再用去离子水超声清洗10 min,最后用乙醇溶液超声清洗3 min,在空气中自然晾干备用。以预处理后的钛片为阳极,铂片为阴极,电解液采用乙二醇-水-氟化铵体系(97 mL乙二醇、3 mL去离子水和0.446 g 氟化铵),两极相距2 cm。直流稳压电源设为60 V,氧化时间40 min,氧化温度为室温。氧化结束后将钛片取出,用去离子水超声5 min,以去除表面生成的杂质氧化物,80 ℃烘干后将其在空气中预烧,以3 ℃/min的速率升至600 ℃,保温2 h,得到TiO2纳米管阵列。
1.2.2 还原氮化法制备氮化钛纳米管阵列将TiO2纳米管阵列置于管式炉中进行氨气还原氮化。先以5 ℃/min的速率升温,并以80 mL/min 的速率向管式炉中通入N2至温度为300 ℃,再以400 mL/min 的速率通入NH3至500 ℃,随后将NH3流速调至800 mL/min 至温度升至600 ℃,接着以1 ℃/min 升温至800 ℃,保温0.5 h,即制得TiN纳米管阵列。
1.2.3 电化学沉积制备TiN-Ag 复合基底称取0.033 8 g硝酸银于烧杯中,加入40 mL去离子水使其完全溶解,再加入0.022 72 g柠檬酸三钠,得到沉积液。以TiN纳米管阵列基底为工作电极,铂片为对电极(两电极相距2 cm),采用恒电位模式沉积,电压为2 V。沉积时间5 min 时取出,在空气中自然晾干,即可制得TiN-Ag复合基底。
1.2.4 MOF@TiN-Ag 复合基底制备首先将2 mmol 硝酸钴(0.582 g)溶于10 mL 甲醇制备出溶液A;再将16 mmol 2-甲基咪唑(1.313 6 g) 溶于10 mL 甲醇得到溶液B。将B 溶液迅速加入A 溶液中,剧烈搅拌,制得MOF 溶液,将上述TiN-Ag 复合基底浸入其中,反应0.5 h,用甲醇清洗3 次制得MOF@TiNAg复合基底。为进行对比,将TiN-Ag复合基底换成石英基片,重复上述操作得到MOF@石英基片。
1.2.5 MOF@TiN-Ag/银溶胶复合基底制备将药物与银溶胶以1∶1 体积混合后滴加在MOF@TiNAg 复合基底表面,即可制得MOF@TiN-Ag/银溶胶复合基底。其中,柠檬酸还原制备银溶胶的过程[12]如下:称取硝酸银0.018 g 溶于100 mL 去离子水中,水浴加热至沸腾,逐滴滴加2 mL 质量浓度为0.1 g/mL的柠檬酸三钠溶液,100 ℃反应1 h,8 000 r/min离心10 min,去除上清液,即得纳米银溶胶。
1.3 SERS信号检测
将茶碱溶于甲醇中配成0.5、0.1、5×10-2、1×10-2、5×10-3、1×10-3、5×10-4、1×10-4、5×10-5、1×10-5mol/L的茶碱溶液。对茶碱进行检测时,激发波长为780 nm,激发功率为10 mW,采集时间为10 s,物镜为10×。
2 结果与讨论
2.1 银溶胶制备及表征
采用透射电子显微镜对柠檬酸钠还原合成的银溶胶粒子形貌进行观察,如图2A所示,所合成的银溶胶纳米粒子呈类球形,其衍射环明显,表明银溶胶中含有金属银纳米晶体。如图2B、C 所示,银溶胶纳米粒子的晶格条纹间距为0.235 nm,对应单质银晶体的(111)晶面。银溶胶粒子的粒径分布见图2D,可见其粒径主要集中在20~60 nm 之间。此外,银溶胶的UV-Vis 图谱在419 nm 波长附近出现了银纳米粒子的等离子体吸收峰,如图2E所示。
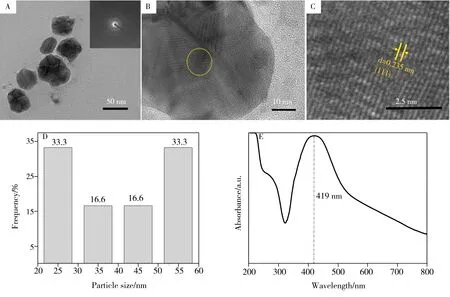
图2 银溶胶的TEM透射电子显微镜图(A~C)、粒径分布图(D)和UV-Vis图谱(E)Fig.2 TEM images(A-C),particle size distribution(D) and UV-visible spectroscopy(E) of silver sol
2.2 复合基底组成与结构表征分析
图3 为不同基底的X 射线衍射图。可见,石英基片上滴加银溶胶样品的XRD 图谱(图3a)在38.2°处出现单质银(111)晶面的特征衍射峰,证明石英基底表面存在银纳米粒子。对石英基片表面原位生长MOF 再滴加银溶胶的基底进行XRD 分析,发现其在38.2°和64.6°处有单质银的特征衍射峰,且衍射峰较强,并在12.32°、16.80°和17.90°处分别出现钴基MOF(100)、(101)和(002)晶面的衍射峰,说明银纳米粒子和钴基MOF 同时存在于石英基片上(图3b)。图3c 为TiN 基底上滴加银溶胶样品的XRD 图谱,可知在2θ为36.9°、42.9°和62.5°处分别出现了NaCl 型面心立方结构TiN 晶体(111)、(200)和(220)晶面的特征衍射峰,2θ为38.2°处对应单质银的(111)晶面,此外,还有少量金属钛的特征衍射峰。在MOF@TiN-Ag 复合基底的XRD 图谱(图3d)中,除了TiN 晶体(111)、(200)和(220)晶面和单质银(111)晶面的特征衍射峰以外,在2θ为12.32°、16.80°和17.90°处出现了对应于钴基MOF(100)、(101)和(002)晶面的特征衍射峰,说明样品中存在TiN 晶体、单质银和钴基MOF 3 种物相,表明银纳米粒子和钴基MOF同时存在于TiN纳米管阵列上。由图3e可知,在MOF@TiN-Ag复合基底上滴加银溶胶后,该样品的XRD 图谱中存在TiN 晶体、单质银和钴基MOF的特征衍射峰,且银单质的衍射峰强度相对较高,说明该复合基底中存在TiN 晶体、单质银和钴基MOF 3 种物相,且基底上金属银的相对含量较多。
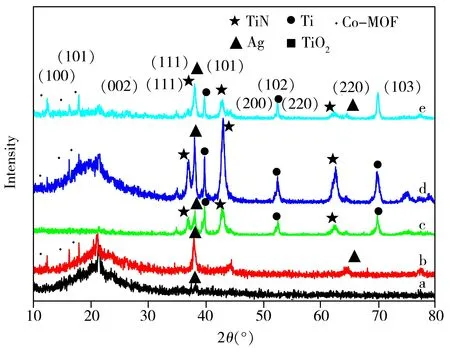
图3 不同基底的XRD图谱Fig.3 XRD spectra of different substrates
图4A为银溶胶滴加在石英基片上的扫描电镜图,可以清晰地观察到银纳米粒子呈球状聚集,粒径约为500 nm,部分粒子产生团簇现象,分布不均匀。在石英基片上生长MOF后再滴加银溶胶,石英基片表面的MOF粒子形态规整、排列紧密且表面吸附了较多的银纳米粒子(图4B)。在TiN 纳米阵列基底表面滴加银溶胶后,可以观察到大量较为规整的TiN 纳米管阵列,同时有银纳米粒子分布在其表面(图4C)。图4D 为MOF@TiN-Ag 基底的扫描电镜图,其中TiN 纳米管阵列排列整齐,单质银呈树枝状分布在TiN 纳米管阵列表面,MOF 粒子呈团簇状分散在复合基底表面。在MOF@TiN-Ag 复合基底上滴加银溶胶后,团聚的MOF 粒子表面吸附了大量的银纳米粒子,银纳米粒子沿其表面轮廓分布,并覆盖在TiN纳米管阵列表面(图4E)。对该样品进行能谱扫描,结果如图4F所示,复合基底表面分布有Ti、N、Ag、Co、C、O元素,其中Co元素来源于MOF中的钴,TiN中含有Ti、N,MOF中的咪唑环也含有一部分N、C、O元素。以上进一步印证了XRD 的检测结果,证明复合基底中存在TiN、单质银和MOF纳米粒子。

图4 银溶胶(A),MOF@银溶胶基底(B),TiN/银溶胶基底(C),MOF@TiN-Ag基底(D)和 MOF@TiN-Ag/银溶胶基底(E)的SEM图以及 MOF@TiN-Ag/银溶胶基底的能谱图(EDS)(F)Fig.4 SEM images of Ag sol(A),MOF@ Ag sol substrate(B),TiN/Ag sol substrate(C),MOF@TiN-Ag substrate(D),MOF@TiN-Ag/Ag sol substrate(E) and EDS spectrum of MOF@TiN-Ag/Ag sol substrate(F)
2.3 理论计算
利用Gaussian 软件,并通过密度泛函理论(DFT)优化计算茶碱的理论拉曼图谱。图5A 为高斯软件优化后的茶碱分子结构图,图5B为茶碱理论计算拉曼图谱,通过查阅文献和DFT计算得到的茶碱拉曼具体峰归属见表1。茶碱在497、562、681、799、977 cm-1处的理论拉曼位移来自茶碱嘧啶和咪唑环的伸缩振动;1 164 cm-1处为C—N 的伸缩振动、CH3和CH 的弯曲振动,1 262 cm-1处为C—N 的对称伸缩振动和C=C 的伸缩振动,1 363 cm-1处对应CH3的弯曲振动,1 600 cm-1处为C=C 和C—N 的拉伸振动,1 645 cm-1处为C=O 的拉伸振动[19-21]。其中,文献中的部分拉曼位移与DFT 理论计算结果有一定差别,例如,445、518、940、1 076、1 309、1 439、1 526 cm-1等。图5C 为茶碱粉体的拉曼图谱,由图可知,茶碱粉体自身的拉曼响应较弱,仅在799、1 028、1 590 cm-1处出现特征拉曼峰。

表1 茶碱主要谱带的理论拉曼位移和振动归属Table 1 Theoretical Raman shifts and vibrational assignments of theophylline major bands
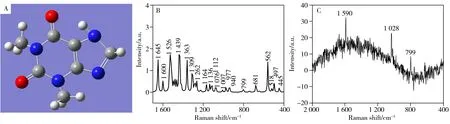
图5 DFT优化的茶碱结构(A)、茶碱的DFT计算拉曼图谱(B)及茶碱粉体的拉曼图谱(C)Fig.5 DFT optimized theophylline structure(A),DFT calculated Raman spectrum of theophylline(B) and Raman spectrum of theophylline powder(C)
2.4 复合基底对茶碱的SERS检测
由于茶碱本身的拉曼响应较差,故将茶碱配制成0.5 mol/L,与银溶胶以1∶1体积混合后分别滴加在石英基片、生长了MOF 的石英基片、TiN 基底、MOF@TiN-Ag 复合基底上进行拉曼检测,为进行对比,将未与银溶胶混合的茶碱单独滴加在MOF@TiN-Ag复合基底上进行SERS检测。茶碱在上述5种基底上的SERS图谱见图6A,拉曼信号强度的柱状图如图6B所示。
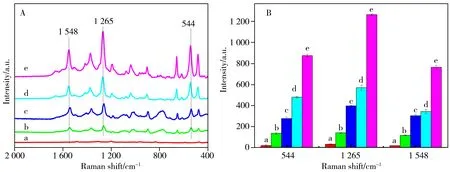
图6 茶碱溶液在不同基底上的SERS图谱(A)及其拉曼检测强度柱状图(B)Fig.6 SERS spectra of theophylline solution on different substrates(A) and their Raman detection intensity(B)
由图可知,相比较于仅滴加银溶胶的石英基片,在基片上生长MOF后再滴加银溶胶可提高茶碱的拉曼响应,这是因为,MOF较强的吸附能力可将银纳米粒子聚集在石英基片表面,形成更多SERS“热点”,因此在基底表面生长MOF 有助于银溶胶的捕获和分散。TiN/银溶胶复合基底对茶碱溶液的SERS响应程度明显高于银溶胶,这得益于TiN 与金属银结合后的电磁场耦合增加了“热点”的数量,同时两者间的电荷转移效应也使得基底的拉曼检测性能增强[22]。而MOF@TiN-Ag 复合基底对茶碱具有更强的SERS 性能。在此基础上,采用银溶胶与茶碱(体积比1∶1)复合滴加的方式,将银溶胶与茶碱的混合物滴加在MOF@TiN-Ag 复合基底表面,发现相比于前4 种基底,MOF@TiN-Ag/银溶胶基底对茶碱具有最强的表面增强拉曼响应,位于544、1 265、1 548 cm-1处特征峰的响应最高,且无明显荧光背底干扰。推测其原因可能是MOF 的多孔结构吸附能力强,可将银粒子较为均匀地吸附聚集在TiN-Ag 基底表面,吸附的银粒子与TiN-Ag基底之间更容易发生协同耦合效应,增加“热点”数量,从而使基底的SERS性能提升[23-24]。因此,相比于文献[19-20]采用100 mV 甚至更高功率的激光器,本文使用10 mV 的激光器,将药物溶液与银溶胶以1∶1体积比混合滴加在MOF@TiN-Ag复合基底上,利用复合基底的协同耦合效应,即可获得较为优异的SERS性能。
将茶碱配成0.5、0.1、5×10-2、1×10-2、5×10-3、1×10-3、5×10-4、1×10-4、5×10-5、1×10-5mol/L 的溶液,分别与银溶胶按1∶1体积比混合后滴加在MOF@TiN-Ag复合基底上进行拉曼测试。结果显示,随着茶碱溶液浓度的降低,基底上茶碱的信号强度逐渐降低。当茶碱浓度为1×10-5mol/L时,拉曼信号峰仍尖锐、清晰可见(图7A),此时544 cm-1处峰的拉曼强度为432 cps,表明以MOF@TiN-Ag/银溶胶为基底,茶碱的检出限可达1×10-5mol/L。不同浓度的茶碱溶液在544 cm-1处的拉曼信号强度如图7B 所示。以茶碱的浓度对数(X)与不同浓度下其在544 cm-1处的拉曼峰强度对数(Y)进行线性回归,得到线性方程Y=3.114+0.098X,r2=0.956 4。以544 cm-1处的SERS 强度对MOF@TiN-Ag/银溶胶复合基底进行增强因子(EF)计算,计算公式[25]为EF =(ISERS/cSERS)/(Iref/cref)。其中,ISERS和cSERS分别表示茶碱溶液吸附在MOF@TiN-Ag/银溶胶复合基底上的SERS信号强度和浓度,Iref和cref分别表示茶碱溶液非SERS检测的拉曼散射强度与浓度。当cSERS为1×10-5mol/L,cref为0.5 mol/L 时,MOF@TiN-Ag/银溶胶复合基底的EF 为1.08×106。
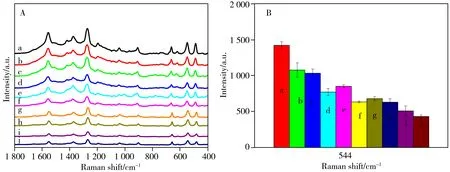
图7 不同浓度茶碱吸附在MOF@TiN-Ag/银溶胶基底上的SERS图(A)与不同浓度茶碱在544 cm-1处的拉曼强度(B)Fig.7 SERS spectra of different concentrations of theophylline adsorbed on MOF@TiN-Ag/Ag sol substrate(A) and Raman strength of different concentrations of theophylline at 544 cm-1(B)
2.5 MOF@TiN-Ag/银溶胶复合基底检测茶碱的SERS效应机理
由Gaussian 软件计算得到茶碱的最高占据分子轨道(HOMO)能级为-6.28 eV,最低未占分子轨道(LUMO)能级为-1.19 eV。文献显示[26],TiN 的禁带宽度为2.73 eV,其VB 能量值为-7.17 eV,ECB为-4.44 eV。功函数为真空能级与费米能级之差[27],TiN 的功函数为4.67 eV,Ag 纳米粒子的功函数为4.10 eV,TiN 与Ag 复合后的功函数为4.54 eV[28]。如图8 所示,TiN 与Ag 之间容易进行电荷转移至二者的轨道能级差相同。在TiN-Ag 界面产生的电荷累积,使得茶碱与该复合基底之间存在电荷转移机制,在780 nm 波长(1.63 eV)激光激发下,茶碱分子HOMO 轨道中的电子会向LUMO 轨道方向移动,产生的共振可有效增大体系极化率,使茶碱的拉曼信号增强,这也解释了单独使用银溶胶对茶碱进行SERS检测结果不理想的原因。
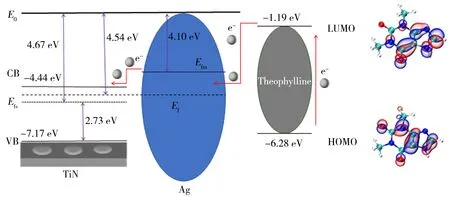
图8 TiN-Ag/银溶胶基底与茶碱的能级结构示意图Fig.8 Schematic diagram of energy level structure of TiN-Ag/Ag sol and theophylline
基底电磁场的增强因子大致与局域电场增强的四次方成正比,电磁强度是探测区域内热点获得的拉曼信号的总量,即取决于“热点”的数量和局域电磁场的强度[29-33]。为了更好地理解MOF@TiN-Ag/银溶胶对茶碱分子SERS的影响,利用时域有限分差法(FDTD)对基底进行电场强度模拟,探究TiN-Ag与TiN-Ag/银溶胶两种复合基底的电场分布情况,如图9 所示。可以看出,与单纯的TiN-Ag 复合基底局域电场相比,TiN-Ag/银溶胶基底局域电场强度相对较强,这是由于在MOF 的富集作用下,引入的银溶胶被富集形成聚集的Ag纳米粒子,其纳米间隙具有较强的局域电场;同时,银溶胶与TiN 基底也可形成耦合效应,使得TiN-Ag/银溶胶复合基底 “热点”的数量和大小均增多,局域表面等离子体共振引起的电场增强,从而赋予该基底更好的SERS 性能,这揭示了相比于其他4 类SERS 基底,采用MOF@TiN-Ag/银溶胶复合基底可以获得药物茶碱分子较强拉曼响应的物理机制[34]。
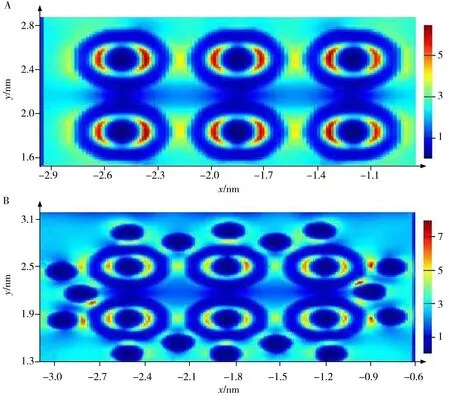
图9 不同基底的2D-FDTD模拟图Fig.9 2D-FDTD simulation of different substrates
2.6 实际样品测定
在空白的中成药枇杷露中添加茶碱,将0.5 mL 枇杷露与0.5 mL 银胶溶液混合均匀后,滴加至MOF@TiN-Ag 复合基底上进行SERS 检测。如图10 所示,在位移为752 cm-1及1 151 cm-1处出现了归属于枇杷露的特征峰。将20、40、80 mg/mL 的茶碱添加到枇杷露中,滴加至MOF@TiN-Ag/银溶胶复合基底上,茶碱在544 cm-1处的特征峰可以被清楚指认,表明利用表面增强拉曼光谱技术可以对药物的掺伪进行快速检测。
3 结 论
本文采用电化学阳极氧化法结合氨气还原氮化法制备出TiN 纳米管阵列,随后通过电化学沉积法制备出性能优异的TiN-Ag 复合基底,进一步在其表面生长MOF 纳米粒子并滴加银溶胶制得MOF@Ag-TiN/银溶胶复合基底。该复合基底中,TiN、Ag 和MOF 3 种物相共存,单质银呈树枝状均匀分布在TiN 纳米管阵列表面,且MOF纳米粒子也形成分子层覆盖在TiN-Ag 复合基底表面,同时MOF 的强吸附能力将银胶粒子聚集在TiN-Ag 基底表面形成更多“热点”,而TiN-银-茶碱之间的电荷转移,增强了基底的SERS 性能。利用MOF@TiN-Ag/银溶胶复合基底对茶碱进行拉曼检测,检出限为1×10-5mol/L。该方法在一定程度上拓宽了SERS技术在药物检测领域的应用。

