盐酸阿霉素/辛伐他汀双载药纳米粒的制备及质量评价
叶晓莉 王丛瑶 何佳 庄建建 朱学敏 王彬辉 林能明
肿瘤心脏病学主要研究抗肿瘤药物的心脏毒性、合并的心血管疾病与肿瘤共有的危险因素及心脏肿瘤等[1-2]。临床上使用药物治疗肿瘤经常导致心脏损伤[3]。在增强药物抗肿瘤作用的同时减轻心脏毒性成为目前肿瘤心脏病学临床亟需解决的关键问题。盐酸阿霉素(adriamycin,ADM)属蒽环类抗肿瘤药物,是治疗乳腺癌的一线抗肿瘤药物[4]。然而,ADM 稳定性差,血浆半衰期极短,长期服用会导致剂量依赖性的心脏毒性,临床应用受限[5-7]。他汀类药物具有内在抗氧化特性和抗细胞凋亡作用,可抑制肿瘤细胞增殖[8-9],降低心脏猝死发生率,可作为蒽环类药物的心脏毒性保护剂[10]。辛伐他汀(simvastatin,SIM)已应用于乳腺癌的临床治疗[11],与ADM 联用可增强抗乳腺癌作用,改善肿瘤药物靶向性,减轻全身毒性反应。纳米粒(nanoparticles,NPs)是指由天然或合成高分子材料制成的粒径为10~1 000 nm 的固态胶体微粒[12]。NPs包载可提高药物在体内的稳定性,延长药物驻留时间,具有靶向释药、增强疗效、提高生物利用度等优点[13-15]。本研究以聚乙二醇-聚乳酸(polyethyleneglycol polylacticacid,PEG-PLA)为载体构建靶向递药系统ADM/SIM 双载药纳米粒(adriamycin/simvastatin coloaded nanoparticles,ADM/SIM-NPs),探索治疗乳腺癌的新方法,以期为研制治疗恶性肿瘤的双载药纳米粒制剂提供理论和实验依据。
1 材料和方法
1.1 主要试剂 ADM 原料药、ADM 对照品购于上海阿拉丁生化科技股份有限公司,批号分别为K2013176、H2119032,纯度均≥98%;SIM 原料药、SIM对照品购于上海阿拉丁生化科技股份有限公司,批号分别为K2017172、K2017172,纯度均≥97%;PEG2000-PLA 购于山东济南岱罡生物工程有限公司,批号:2021050911;聚乙烯醇(PVA)购于江西阿尔法高科药业有限公司,批号:20160301。
1.2 方法
1.2.1 ADM 和SIM 色谱条件 ADM 色谱柱为Diamonsil C18(250.0 mm×4.6 mm,5 μm);流动相为乙腈∶0.2%磷酸水溶液=28∶72;柱温30 ℃;流速为1.0 mL/min;检测波长为254 nm;进样量为20 μL。SIM色谱柱为Diamonsil C18(250.0 mm×4.6 mm,5 μm);流动相为乙腈∶0.2%磷酸水溶液=80∶20;柱温30 ℃;流速为1.0 mL/min;检测波长为238 nm;进样量为20 μL。
1.2.2 ADM/SIM-NPs 的制备及工艺优化 取适量ADM 溶于双蒸水作为内水相;取一定量PEG2000-PLA和SIM 溶于甲醇溶剂作为有机相,调整ADM 和SIM 的质量比为2∶1。混合内水相与有机相,冰浴超声得到初乳;另取PVA 水溶液作为外水相;并与初乳混合,冰浴超声得到复乳;继续搅拌,室温减压蒸发掉有机溶剂和部分水,即得到ADM/SIM-NPs。不加药物即为空白NPs。选择总药物与PEG2000-PLA 质量比(A)、内水相与有机相体积比(B)、有机相与外水相体积比(C)、外水相PVA 质量浓度(D)为考察因素,通过L9(34)正交试验优化处方测定包封率和载药量。包封率和载药量各占50%的系数积分,综合评分=总药物包封率×50%+总药物载药量×50%。综合评分越高,说明制备工艺越佳。
1.2.3 色谱方法建立 分别精密移取ADM 和SIM 标准品贮备液,制备系列标准溶液,浓度分别为0.780、1.560、3.125、6.250、12.500、25.000、50.000、100.000 mg/L,线性回归后绘制标准曲线。分别配制低(6.250 mg/L)、中(12.500 mg/L)、高(25.000 mg/L)3 个浓度的ADM 或SIM 标准品溶液,按1.2.1 项条件测定日内、日间精密度。制备10.000、12.500、15.000 mg/L 的ADM 或SIM纳米粒溶液,测定回收率。分别取适量ADM 和SIM标准品贮备液,重复6 次,高效液相色谱测定药物浓度。分别取ADM 或SIM 同一样品溶液,于0、2、4、6、8、12 h 进样,测定溶液稳定性。分别取ADM 和SIM 标准品溶液、空白NPs 混悬液和ADM/SIM-NPs 进样分析,得到色谱图。
1.3 观测指标
1.3.1 ADM/SIM-NPs 形态学 取ADM/SIM-NPs 混悬液滴于铜网,采用磷钨酸负染法制备,透射电镜观察。
1.3.2 ADM/SIM-NPs 粒径 取ADM/SIM-NPs 混悬液用少量纯水稀释后,釆用马尔文激光粒度测定仪测定并采集粒径分布。
1.3.3 药物的包封率与载药量 ADM 的包封率和载药量通过超滤离心法测定。采用截留相对分子质量为30 kDa 超滤离心管,移取1.0 mL ADM/SIM-NPs 置上端,5 000 r/min 离心20 min,收集滤液,加入甲醇定容,0.22 μm 微孔滤膜过滤,取续滤液,采用高效液相测定ADM 质量(W游离)。另取1.0 mL ADM/SIM-NPs 加甲醇超声定容破乳,高效液相测定ADM 总质量(W总)。包封率(%)=(1-W游离/W总)×100%;载药量(%)=(W总-W游离)/Wt。其中W游离为ADM/SIM-NPs 中未被包封的ADM 质量;W总为ADM/SIM-NPs 中ADM 质量;Wt为ADM/SIM-NPs 的总质量。
SIM 的包封率和载药量通过低速离心法测定。移取1.0 mL ADM/SIM-NPs 加入1.5 mL 离心管,8 000 r/min 离心5 min,取上清液加甲醇定容,0.22 μm微孔滤膜过滤,取续滤液,釆用高效液相测定SIM 质量(W包封);另取1.0 mL ADM/SIM-NPs,加甲醇定容破乳,高效液相测定SIM 总质量(W总)。包封率(%)=(W包封/W总)×100%;载药量(%)=W包封/Wt。其中W包封为ADM/SIM-NPs 中包封的SIM 质量;W总为ADM/SIMNPs 中SIM 的质量;Wt为ADM/SIM-NPs 的总质量。
1.4 体外释放度测定 以含有2%吐温-80 的PBS(pH=7.4)为释放介质,移取ADM 溶液、SIM 溶液、ADM/SIM-NPs 各3 份,1 mL/份,分别转移到经预处理的透析袋内,确保透析袋全部浸没在介质中。开启恒温振荡仪,(37.0±0.5)℃,100 r/min 分别于0.5、1.0、2.0、4.0、6.0、8.0、12.0、24.0 h 取样,补加等量同温释放介质,经0.45 μm 微孔滤膜过滤,取续滤液测定ADM 和SIM 质量,计算累积释放百分率。
1.5 统计学处理 设计L9(34)正交试验。精密度、回收率、重复性和稳定性检测的相对偏差<5%,认为符合方法学要求。分别用零级、一级动力学模型、Higuchi 模型、Rigter-Peppas 模型对ADM/SIM-NPs 体外释药行为进行拟合。
2 结果
2.1 ADM 和SIM 方法学观测
2.1.1 ADM 和SIM 的专属性 高效液相色谱图结果显示ADM 和SIM 药物峰峰形良好,色谱峰专一,ADM和SIM 的保留时间分别为5.47 和8.94 min,见图1-2。

图1 ADM 高效液相色谱图(A:ADM 对照品溶液;B:空白NPs;C:ADM/SIM-NPs 混悬液)
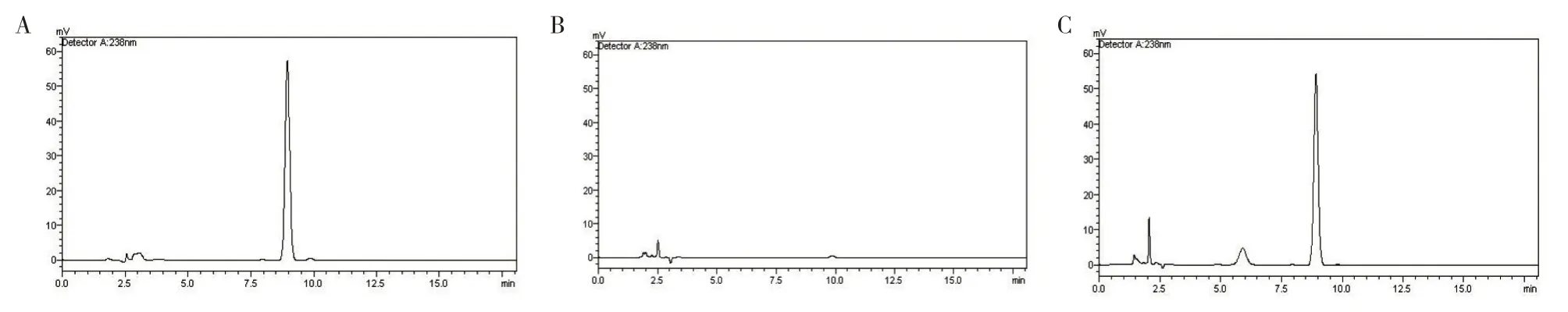
图2 SIM 高效液相色谱图(A:SIM 对照品溶液;B:空白NPs;C:ADM/SIM-NPs 混悬液)
2.1.2 ADM 和SIM 的标准曲线 ADM 标准曲线方程:y=55 763x+16 103,R2=0.999 9(n=3),表明ADM 在0.78~100.00 mg/L 与峰面积线性关系良好。SIM 标准曲线方程:y=68 759x+33 931,R2=0.999 7(n=3),表明SIM 在0.78~100.00 mg/L 与峰面积线性关系良好。
2.1.3 ADM 和SIM 的精密度和回收率 精密度试验结果见表1,回收率试验结果见表2,相对偏差均<5%,符合方法学要求。

表1 ADM和SIM的精密度检测(n=6)

表2 ADM和SIM的回收率检测(n=6)
2.1.4 ADM 和SIM 的重复性和稳定性 ADM 和SIM的重复性检测相对偏差分别为0.56%和0.40%(n=6),均<5%,符合方法学要求。稳定性检测的相对偏差分别为1.07%和1.15%,均<5%,符合方法学要求,表明样品在12 h 内稳定。
2.2 ADM/SIM-NPs 制备的优化工艺 选择药物与PEG2000-PLA 质量比(A)、内水相与有机相体积比(B)、有机相与外水相体积比(C)、外水相PVA 质量浓度(D)为考察因素,每个因素各取3 个水平,进行正交设计。A 因素选择1∶10、1∶15 和1∶20 3 个水平;B 因素选择1∶2、1∶5 和1∶10 3 个水平;C 因素选择1∶2、1∶5 和1∶10 3 个水平;D 因素选择1%、2%和3% 3 个水平。综合加权评分法对正交结果进行综合分析,结果显示,各因素对包封率和载药量的影响程度依次为:药物与PEG2000-PLA 质量比(A)>外水相PVA 质量浓度(D)>内水相与有机相体积比(B)>有机相与外水相体积比(C)。即药物与PEG2000-PLA 质量比是影响ADM/SIM-NPs 包封率的第一因素(P<0.05),内水相与有机相比例、有机相与外水相体积比、外水相PVA 浓度影响较小(P>0.05)。经过运算可得出每个因素各水平之和的平均值K1、K2、K3,综合各因素K值和直观比较,最佳处方为A3B3C1D2,见表3。
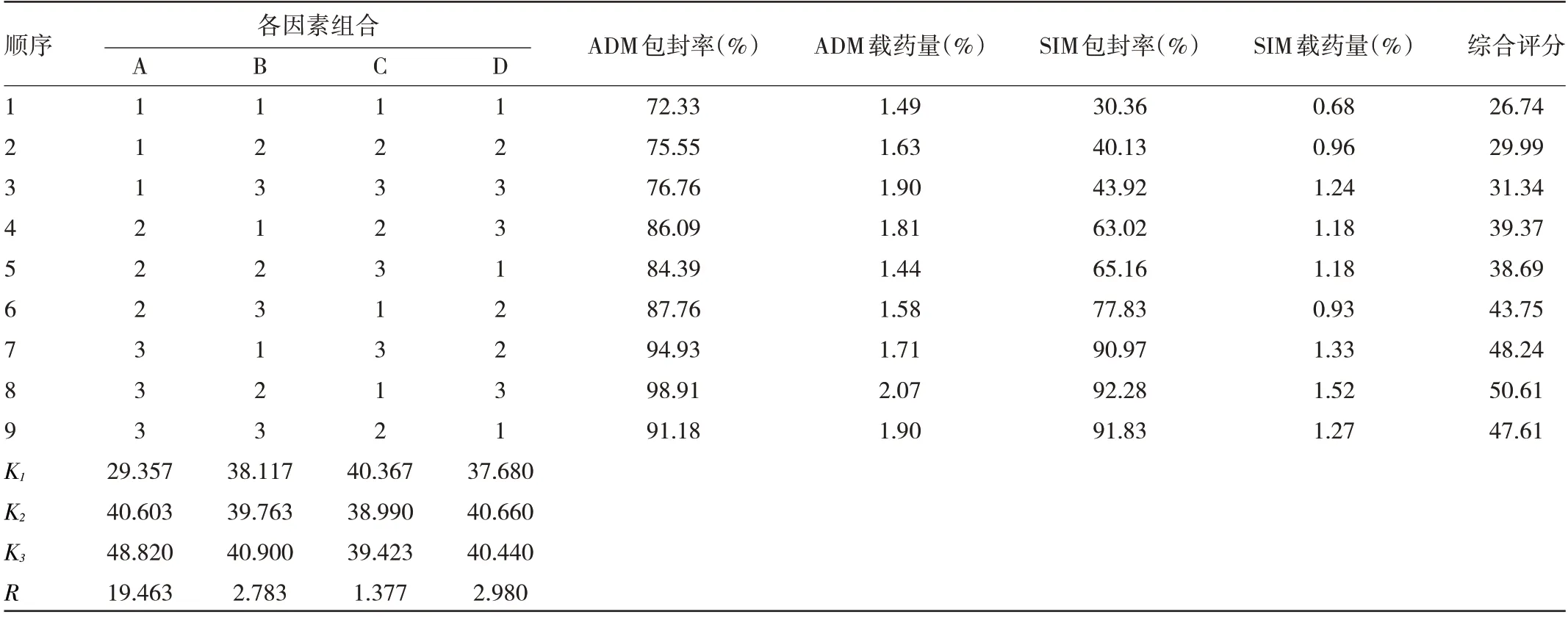
表3 正交试验设计和结果
2.3 最佳工艺验证 按最佳工艺制备ADM/SIM-NPs,粒径和Zeta 电位分别为(84.46±3.62)nm、(-3.13±0.11)mV;ADM 包封率和载药量分别为(95.57±0.82)%、(2.03±0.14)%,SIM 包封率和载药量分别为(90.81±0.02)%、(1.32±0.01)%。制成的ADM/SIMNPs 呈圆球形,粒径大小分布均匀,无团聚,工艺效果较好。
2.4 游离ADM、游离SIM 和ADM/SIM-NPs 体外释放检测 体外释放实验表明游离ADM 和SIM 溶液在2%吐温-80 的PBS 中释放较快,4 h 累积释放百分率分别达60%和80%,12 h 基本透出完全。ADM/SIM-NPs 释药较为缓慢,24 h ADM 和SIM 累积释放百分率约为50%和40%。ADM/SIM-NPs 的释药过程可分为2 个阶段:0~4 h 时快速释药,5~24 h 时释药渐平稳,见图3。以Q为释放量,t为时间,分别用零级、一级动力学模型、Higuchi 模型、Rigter-Peppas 模型对ADM/SIM-NPs体外释药行为进行拟合。结果发现,ADM 从ADM/SIM-NPs 中释出拟合的零级动力学模型方程为Q=0.016 6t+0.179 3,R2=0.904 7;一级动力学模型方程为ln(1-Q)=-0.026 0t-0.185 8,R2=0.955 9;Higuchi 模型方程为Q=0.097 7t+0.069 3,R2=0.991 6;Rigter-Peppas 模型方程为lnQ=0.379 6t-1.827 3,R2=0.994 5。SIM 从ADM/SIM-NPs释出的零级动力学模型方程为Q=0.009 1t+0.198 8,R2=0.785 9;一级动力学模型方程为ln(1-Q)=-0.012 7t-0.220 9,R2=0.820 6;Higuchi 模型方程为Q=0.097 7t+0.069 3,R2=0.940 2;Rigter-Peppas 模型方程为lnQ=0.252 7t-1.720 1,R2=0.984 5。Rigter-Peppas方程R2值最接近1,拟合度较高;故ADM/SIM-NPs 释放特性符合该方程。

图3 游离ADM、游离SIM 和ADM/SIM-NPs 的体外释放曲线(n=3)
3 讨论
乳腺癌发病率约占全球女性癌症的30%[16],严重威胁人类健康。ADM 是临床治疗乳腺癌的一线用药,但由于具有心脏毒性而被限制使用[17-19]。ADM 心脏毒性是多种因素共同作用的结果,原因是ADM 在体内可产生大量活性氧自由基,引发脂质过氧化,造成心肌细胞损伤[20]。目前临床应用较广泛的抗阿霉素心脏毒性药物有右丙亚胺、左卡尼汀等,但右丙亚胺会加重抗肿瘤药物对患者骨髓的抑制作用,左卡尼汀对阿霉素所致的心脏损伤仅有预防而无治疗作用。因此,如何在降低ADM 毒性反应的同时不影响甚至增强ADM的治疗效果成为研究热点。胆固醇是导致乳腺癌发病的重要风险因子,他汀类药物可通过阻断胆固醇合成起到抑制肿瘤细胞生长的作用[21-22]。SIM 在调节血脂的同时还具有抗炎、抗氧化、抑制心肌肥厚、抗心肌纤维化和细胞凋亡等多重作用[23],对蒽环类药物具有心脏保护作用。一项回顾性临床队列研究发现,化疗前和化疗同时不间断他汀类药物治疗能显著降低乳腺癌患者心力衰竭风险[24]。本研究制备的ADM/SIM-NPs 在降低ADM 毒副反应的同时增强ADM 的治疗效果,达到药物在靶器官浓集、缓释及增效减毒等目的。
本实验通过复乳溶液挥发法成功制备双载药纳米粒,方法简单,制得的双载药纳米粒粒径小且分布均匀、包封率较高。一方面可以发挥SIM 心脏保护作用,减少ADM 在化疗期间造成的心脏损伤,减轻药物毒副反应。另一方面ADM 和SIM 被动靶向递送于肿瘤组织,增强了ADM 在增殖肿瘤细胞中的摄取量,提高了药物的生物利用率。由于ADM/SIM-NPs 粒径仅(84.46±3.62)nm(<200 nm),可经肿瘤高通透滞留效应被动靶向于肿瘤所在部位,有效提高了药物在病灶处的浓度。以PEG-PLA 作为载体的NPs 具有血液长循环特性,可有效保护药物免受网状内皮系统的吞噬,从而减少给药次数和药量[25]。本研究发现在固定有机相的前提下,增加内水相可使药物在扩散到外水相的过程中油层变薄,更有利于药物扩散。因此,过大的内水相可导致药物有更多机会扩散出内乳剂,减少药物的包封率。
透析袋扩散法考察ADM/SIM-NPs 的释放特性发现,其释放特性符合Ritger-Peppas 方程且具有缓释的效果。由于SIM 属于脂溶性药物,难溶于水,在释放介质为pH 7.4 的PBS 中的累积释放百分率<20%,故选择含2%吐温-80 的PBS(pH=7.4)为溶出介质以增加溶解度。体外释放实验表明游离ADM 和SIM 溶液在该介质中释放较为平稳,处于缓慢释放状态,24 h累积释药量分别约为50%和40%,可能是由于药物主要通过载体表面膜的孔隙扩散及载体骨架的溶蚀。NPs 突释现象不明显,后期释放具有缓释特征,且ADM 释放速度和累积释放百分率均高于SIM,分析原因可能是ADM 的水溶性比SIM 好,在亲水性释放介质中更容易扩散,而SIM 由于疏水性较强,不易向外水相扩散。
综上所述,本研究采用复乳溶液挥发法成功制备了ADM/SIM-NPs,确定了最优制备处方工艺,制备的双载药纳米粒粒径分布均一、稳定性好、具有缓释效果。

