马钱子碱聚乳酸-羟基乙酸共聚物纳米粒表征及体内药动学评价
管庆霞,林泽榆,夏昭睿,张 雪,张国帅,李秀妍,杨志欣*
(1.黑龙江中医药大学,哈尔滨 150040;2.黑龙江省中医药科学院,哈尔滨 150040)
现代医学对马钱子碱(brucine,B)进行了大量研究,发现其具有通络止痛、散结消肿等作用,能够用于人体免疫系统调节以及肿瘤等疾病的治疗中[1-3],并且其对于人体的神经系统、骨骼系统等都有一定的药理作用[4]。秦建民等[5-7]通过体外培养肝癌细胞实验发现,马钱子碱可明显控制肝癌SMMC-7721 细胞和人HepG2 肝癌细胞的繁殖,阻止癌细胞的活动和入侵,这说明B对肝癌细胞的凋亡有一定的作用。朱建伟等[8]在对马钱子碱进行研究后发现,该物质还具有较强的止痛的作用。但是由于马钱子碱具有毒性大、水溶性差、生物利用度低等缺点临床应用受到了限制,故亟需一种能够降低药物不良反应,提高生物利用度的递药系统来使其更好的应用于临床[9]。而纳米制剂作为如今中药制剂领域一个重要的研究方向,具有提高生物利用度、降低毒性、实现靶向给药等优点,能够改善马钱子临床用药困难的缺点[10]。近年来也出现了将马钱子碱制成脂质体并成功改善其临床用药困难的相关研究[11-12]。
聚乳酸-羟基乙酸共聚物(PLGA)是乳酸与羟基乙酸通过聚合作用而获得的一种高分子的化合物,具有相容性、可降解性等诸多特点,现已被广泛地应用于生物医学材料领域、制药领域和现代化工业领域[13-17]。目前美国已经把该物质划分为可以在人体内注射的生物材料之一,因此该物质能够用于人体疾病的治疗。近年来其在纳米制剂载体方面也具有良好的表现[18]。
课题组前期成功采用沉淀法制备了马钱子碱聚乳酸-羟基乙酸共聚物纳米粒(B-PLGA),并对其制备工艺、表征及体外释药进行了研究[19]。成功制备了形态良好可控,且具有一定缓释效果的纳米粒。本实验采用HPLC 法建立马钱子碱含量测定方法,并通过尾静脉注射后各时间点眼眶取血测定其含量得到药动学参数,为其进一步研究提供参考。
1 材料
1.1 实验动物 清洁级的SD 大鼠12 只(200±20 g,6 ~7 周),雌雄各半,黑龙江中医药大学实验动物中心提供。
1.2 药物与试剂 马钱子碱对照品(批号:110706-200505),质量分数98%,中国食品药品检定研究院;肝素钠注射液(江苏万邦生化医药有限公司);泊洛沙姆188(F68),德国BASF 公司;甲醇,色谱纯,北京DIKMA 公司。
1.3 主要仪器 Waters e2695 高效液相色谱仪系统,美国Waters 公司;FA1204B 分析电子天平,济南鑫贝西生物技术有限公司;KQ-250DE 型数控超声波清洗机,昆山市超声仪器有限公司;BYN200-2 氮气吹干仪,上海秉越电子仪器有限公司;TGL-10B 离心机,上海安亭科学仪器厂;WH-2 微型涡旋混合器,上海沪西分析仪器厂有限公司。
2 方法
2.1 B-PLGA 纳米粒的制备 称取25 mg 的PLGA 共聚物,将其放入到10 mL 的丙酮中,超声使其溶解,作为有机相。称取1.2 mg 药物加入有机相中,再次超声使其充分溶解。配制20 mL 以0.05%的F68 为稳定剂的水溶液,将其作为水相。将有机相加入到水相中并将其放在转速为1 000 rpm 的磁力搅拌30 min。将溶液放入旋转蒸发仪中除去有机溶剂,即得B-PLGA 纳米粒溶液。
2.2 B-PLGA 纳米粒微观形态 取一定量的B-PLGA纳米粒溶液,经0.45 μm 滤膜过滤后滴入覆有支持膜的铜网上,待其自然干燥后,滴加2%的磷钨酸溶液,染色2 ~3 min,置于透射电子显微镜下观察并拍照。
2.3 粒径与Zeta 电位的测定 取出0.1 mL B-PLGA 纳米粒溶液,用蒸馏水稀释50 倍,取适量放入激光粒度分析仪中测定粒径、Zeta 电位。
2.4 包封率与载药量的测定 采用低温超速离心发测定其包封率载药量。取出2 mL 的B-PLGA 纳米粒混悬液,并将其放置在离心机中,15 000 r/min 转速下离心30 min,将沉淀的纳米粒收集,再用蒸馏水超声使其分散,继续离心,重复3 次,制成B-PLGA 混悬液。从准备好的B-PLGA 混悬液精确量取需要计量的溶液,将其加入到色谱甲醇中,在40 KHz、200 W 的环境下超声20 min,使纳米粒破乳将包载的药物充分释放,将处理后的溶液用孔径为0.22 μm 的过滤膜过滤后得到B-PLGA 纳米粒供试品溶液,用同样的方法制取PLGA 空白纳米粒溶液。采用高效液相色谱法在甲醇:水-乙酸-三乙胺(230:2.4:0.3)= 30:70、Dikma C18(250 mm×4.6 mm,5 μm)色谱柱、256 nm检测波长、1 mL/min 流速、进样量10 μL、柱温30 ℃条件下进样。计算其包封率和载药量。
2.5 马钱子碱含量测定方法建立
2.5.1 马钱子碱对照品溶液制备 首先称取2.64 mg 的马钱子对照品,将其加入到25 mL 的容量瓶中,向其中加入甲醇定容,此时溶液的浓度为105.6 μg/mL,用甲醇依次稀释至52.80、26.40、13.20、6.60、3.30、0.66 μg/mL,备用。
2.5.2 色谱条件 流动相为甲醇:水-乙酸-三乙胺(230:2.4:0.3)= 30:70,色谱柱为Dikma C18(250 mm×4.6 mm,5 μm),检测波长为265 nm,流速为(1 mL/min),进样量为20 μL,柱温为25 ℃。
2.5.3 血浆样品的处理方法 取大鼠血浆250 μL,加入内标(20 μg/mL 士的宁甲醇溶液)20 μL,加入100 μL的NaOH 溶液(1 mol/L),涡旋1 min,超声20 min,放入2 mL 萃取剂(二氯甲烷 : 甲醇=9 : 1),涡旋5 min,超声溶解20 min,离心5 min(转速5 000 r/min),收集下层液,上层血浆继续加2 mL 萃取剂,重复上述操作,合并两次下层液,置于37 ℃水浴氮气吹干,用200 μL色谱甲醇复溶,涡旋2 min,12 000 rpm 离心10 min,取上清液在“2.5.2”项色谱条件下进样测定。
2.5.4 专属性试验 取空白血浆、含B 对照品血浆和内标物士的宁对照品的血浆、尾静脉注射药品后的血浆样品,按“2.5.3”项下进行处理。
2.5.5 线性关系的考察 精密量取“2.5.1”项下各浓度B 对照品溶液,氮气吹干有机溶剂,加入等量空白大鼠血浆得到52.80、26.40、13.20、6.60、3.30、0.66 μg/mL 一系列浓度供试品溶液,按照“2.5.3”项血浆样品处理方法对其进行处理,在“2.5.2”项条件下进样检测。记录其色谱图与峰面积。
2.5.6 最低定量限 将B 对照品溶液用甲醇进行不断稀释,并在“2.5.2”项条件下进样分析,测定其最低定量限。
2.5.7 精密度与回收率 分别取52.80、13.20、0.66 μg/mL的B 对照品溶液(分别为高、中、低浓度组)200 μL,氮气吹干使有机溶剂挥发完全,将其加入到等量的空白血浆中稀释,依次按照“2.5.3”处理,并按“2.5.2”的方法在1 d 内和3 d 内连续进样分析,计算其精密度与回收率。
2.5.8 稳定性试验 分别量取52.80、13.20、0.66 μg/mL的等量B 对照品溶液,每个浓度设置三个平行样,氮气吹干使溶剂挥发完全后加入等量的大鼠空白血浆,室温25℃放置, 4、8、12 h 后取样,分别将取出的血浆按照“2.5.3”项下进行处理,在“2.5.2”项条件下进样分析,计算得出其RSD 值。
2.6 体内药动学研究 本实验中共有雌性和雄性大鼠各6 只,将这些大鼠随机分成2 组,分别是B 溶液组(将马钱子碱溶于含有10%乙醇的生理盐水溶液中即得)和B-PLGA 纳米粒组。在给药前12 h 禁食不禁水,采用尾静脉注射的方式进行给药,给药剂量为10 mg/kg。于10、30、60、90、120、150、180、210、240、300、420 min 眼眶静脉丛取血,取血量约为0.5 mL;置于肝素化离心管中。5 000 r/min离心15 min后取出其上清液,按照“2.5.3”项下进行处理,在“2.5.2”项条件下进样分析后对其血液中的药物浓度进行计算。
2.7 统计学方法 通过DAS 2.0 软件进行数据分析,采用SPSS 22.0 软件进行t检验。以P<0.05 表示差异具有统计学意义。
3 结果
3.1 B-PLGA 纳米粒表征结果
3.1.1 微观形态 透射电镜结果,如图1。B-PLGA 纳米粒呈类球型,粒径为100 nm 左右,粒子清晰可见。

图1 B-PLGA 纳米粒透射电镜图
3.1.2 粒径与Zeta 电位测定结果 粒径与Zeta 电位测定结果,如图2。平均粒径为 (99.80±1.11) nm,PDI 为 0.112±0.045,Zeta 电位为 (-27.6±0.32) mV。

图2 马钱子碱PLGA 纳米粒的粒径与Zeta 电位图
3.1.3 包封率与载药量测定结果 按上述方法测定3批B-PLGA,得到其平均包封率为 (67.35±1.24)%,载药量为 (2.83±0.06)%。
3.2 体内药动学方法学考察结果
3.2.1 专属性实验结果 专属性实验分析结果,如图3。由图可知血浆样品处理的过程中未引入干扰物质,血浆的内源性物质按此方法测定无干扰,说明该方法专属性良好。
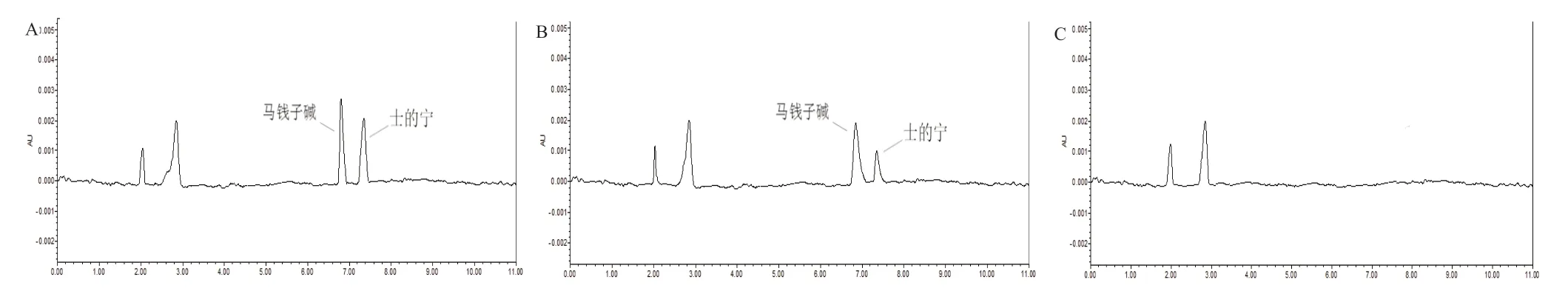
图3 高效液相色谱图
3.2.2 线性关系的考察结果 将横坐标(X)和纵坐标(Y)分别设置为B 质量浓度和对照品与内标物峰面积的比值,利用加权最小二乘法对其进行计算,标准曲线方程为:Y= 0.038X+0.084,R2= 0.998。结果表明浓度在0.66 ~52.80 μg/mL 范围内,二者呈良好的线性关系,可用于后续实验。
3.2.3 最低定量限结果 结果显示最低定量限(S/N =10)为0.660 μg/mL,符合后续实验的测定要求。
3.2.4 精密度与回收率结果 精密度及回收率实验结果表明马钱子碱不同浓度的精密度与回收率均良好,符合生物样品的测定要求,能够进行后续实验。见表1。静脉注射B 与B-PLGA 纳米粒后的药-时曲线均符合权重因子为1/C2的二室模型,其药动学参数,见表4。
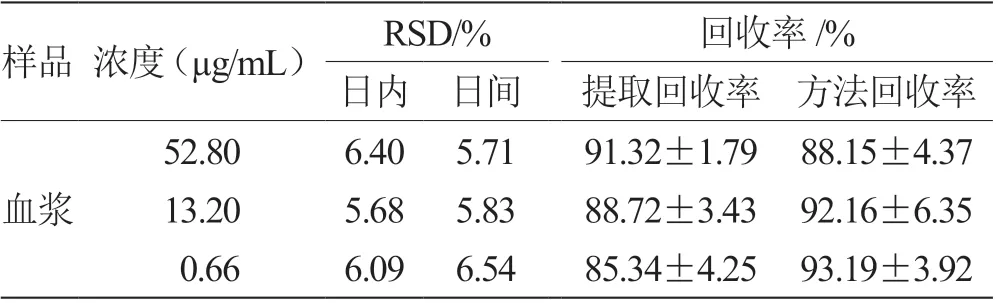
表1 精密度和回收率实验结果(n = 3)

表2 B 溶液组各时间点的血药浓度

表3 B-PLGA 组各时间点的血药浓度
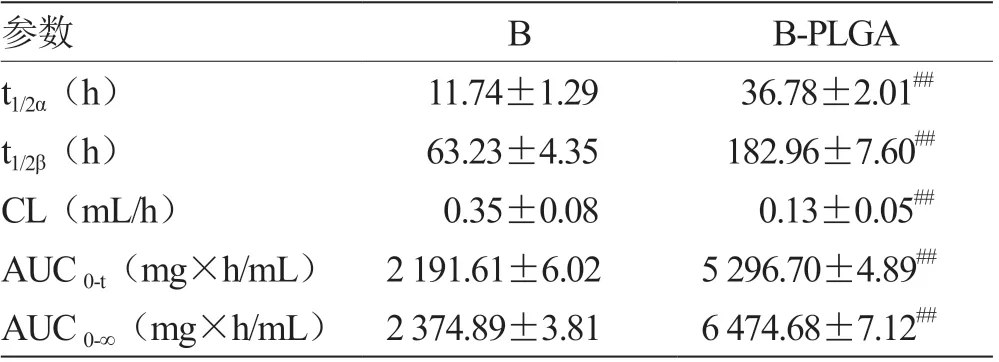
表4 马钱子碱和B-PLGA 纳米粒大鼠药动学参数(n = 6)
3.2.5 稳定性实验结果 稳定性实验结果表明RSD 值均小于5%,说明溶液12 h 内稳定性良好,可用于进行后续实验。
3.3 药动学研究结果
3.3.1 药时曲线 根据不同时间中取出的血液计算其药物浓度,计算得出B 溶液组、B-PLGA 纳米粒在各时间点的血药浓度结果,见表2 和表3。以时间为横坐标,药物浓度为纵坐标绘制出的血药浓度-时间曲线,结果如图4。

图4 马钱子碱和B-PLGA 纳米粒在大鼠体内药时曲线(n = 6)
3.3.2 药动学参数 通过DAS 2.0 软件对上文中的曲线进行拟合,通过F 检验和AIC 的值可以判定大鼠尾
从表中能看出,B-PLGA 纳米粒组与B 溶液组相比较,其AUC 值、Tl/2a值和T1/2β值均明显的增大,而CL 值显著下降。B-PLGA 纳米粒组的tl/2a值、t1/2β值分别是B 溶液组的3.13、2.89 倍,AUC 值是B 溶液组的2.42倍,CL值是B生理盐水组的0.37倍。综上可以发现,将B 制备成B-PLGA 纳米粒后,大大地改变了其原本的药物代谢动力学参数,延长药物在机体的生物半衰期及滞留时间,使其可以发挥长效的治疗作用。
4 讨论
为建立合理的大鼠血浆中马钱子碱含量的HPLC法,本研究通过预实验考察不同的色谱条件对含量测定的影响,当选择流动相为甲醇-含乙酸和三乙胺的混合水溶液(每230 mL 水中含乙酸 2.4 mL、三乙胺0.3 mL)(30 : 70,V/V)、检测波长为265 nm、流速为 1 mL/min、柱温为 25 ℃时,马钱子碱色谱峰的峰形明显区分度高,并且血浆中内源性物质不影响马钱子碱含量测定,故选择上述色谱条件进行HPLC 法建立。
体内药动学研究结果表明,B 溶液组与B-PLGA组的药动学参数相比,具有显著性差异,B 制备成纳米粒后,清除率降低,药物在体内的滞留时间明显延长,原因可能是游离的马钱子碱作为小分子药物,主要通过扩散作用释放到介质中,发挥作用较快;而B-PLGA 纳米粒主要通过胞吞进入细胞后由内核结构的解聚释放药物,发挥作用比游离的药物要慢,同时载体有效的保护了药物,避免被酶类分解,因此药物在机体的生物半衰期及滞留时间有所延长并提高了马钱子碱生物利用度,提高其缓释作用。同时有研究表明,纳米级药物可在伊派尔结中大量聚集,通过淋巴结中的M 细胞进入血液循环,从而改变了药物吸收途径及药动学[20],为B-PLGA 纳米粒的后续研究奠定了实验基础。
5 小结
综上所述,本文成功制备了表征良好的B-PLGA纳米粒,并通过体内药动学实验推测实验室制备的B-PLGA 纳米粒能够明显改变B 代谢动力学参数,降低清除率,延长B 在大鼠体内的滞留时间,发挥长效作用,提高了B 的生物利用度,为对其进一步研究提供了依据。

