二甲双胍治疗慢性阻塞性肺疾病合并2型糖尿病的研究进展*
朱宝强,陶雪,刘雨蒙,龙恩武,叶云
(1.西南医科大学药学院,泸州 646000;2.四川省医学科学院·四川省人民医院,电子科技大学附属医院药学部,个体化药物治疗四川省重点实验室,成都 610072;3.西南医科大学附属医院药学部,泸州 646000)
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)与2型糖尿病(type 2 diabetes mellitus,T2DM)是人群中常见的两种重大慢性疾病[1],均会对生命健康造成严重威胁。COPD是一种以气流受限和呼吸困难为特征的肺部疾病;T2DM是一种以血糖代谢异常为特征的疾病。一项针对我国COPD患病率的流行病学调查研究显示,我国COPD患病率8.6%,≥40岁人群患病率13.7%[2],而我国60~69岁人群糖尿病患病率28.8%,≥70岁人群患病率31.8%[3]。慢性共病常见于老年患者,由于其复杂性及相互影响,可提高不良结局发生风险,并增加治疗难度,提高医疗成本[4]。近几年的研究发现,作为经典降糖药的二甲双胍,表现出治疗COPD的多种药效机制,可能对T2DM合并COPD患者产生双重治疗作用,具有潜在治疗效益。笔者在本文对T2DM与COPD相关性、二甲双胍治疗COPD及T2DM并发症的相关基础研究和临床研究现状进行归纳介绍,以期为COPD合并T2DM的治疗提供研究参考。
1 T2DM与COPD相关性
许多研究证明,COPD与T2DM之间存在着紧密相互联系,但二者之间的关联还未明确。部分研究发现T2DM患者出现COPD的概率高于非T2DM人群[5],同样,COPD患者较非COPD患者具有更高的T2DM患病率[6],两种疾病互为患病风险和不良预后因素[7-8]。RAYNER等[9]的队列研究认为,T2DM可能为COPD保护因素,结果显示T2DM患者较正常人表现出更低的COPD患病率,但可能由于该研究中T2DM患者具有更好的自我管理(主动吸烟率更低等),本身会降低COPD的风险;也有研究[10]认为,超重可能降低COPD患者死亡率。当前,多数研究者认为二者间存在不良关联。
针对COPD对T2DM的影响,主要观点认为,COPD患者体内全身炎症因子高度表达、氧化应激活跃及免疫失调导致了代谢综合征,加之因呼吸困难引起活动量减少、不平衡饮食等不良的自我管理方式最终造成了T2DM。ZULKIFLI等[11]对无糖尿病史的COPD患者进行血糖监测后发现大量新诊断血糖异常现象。COPD患者主要采用糖皮质激素(glucocorticoids,GC)口服或吸入疗法,而长期使用GC会导致体内血糖异常升高[12],因此也被认为是COPD患者发生T2DM的诱因。
T2DM对COPD的影响可能与其肺部损伤有关,包括COPD在内的多种肺部疾病与T2DM存在紧密关联。高血糖可能引起患者肺功能及身体机能下降[13],DE SANTI等[14]对普通人群和T2DM患者的呼吸系统健康状况进行调查,发现与普通人群相比,多数患者存在限制平地行走速度的呼吸困难、咳嗽、多痰等症状。T2DM患者体内炎症、氧化应激及肺部微血管病变,可能对肺功能造成影响,此外,高血糖可引起气道表面葡萄糖浓度的增加,为细菌提供高糖营养环境,提高COPD患者肺部细菌感染的可能性[15]。
2 二甲双胍治疗COPD的基础研究
COPD患病与环境因素密不可分,粉尘、污染气体、香烟烟雾、病原菌都与COPD的发病存在相关性,而吸烟被认为是COPD最为关键的致病因素,香烟烟雾提取物(cigarette smoke extract,CSE)可刺激炎症因子释放,诱发氧化应激,加速肺部细胞凋亡,危害巨大。近年来,随着对二甲双胍不断地研究和深入了解,其降糖以外的抗衰老、抗肿瘤、抗抑郁等多种治病潜力被广泛挖掘出来。目前,许多基础研究发现了二甲双胍针对COPD在多个方面可能存在的药效机制。
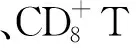
2.2抗氧化应激及改善细胞凋亡 COPD是一种加速肺部衰老的疾病。衰老机制较为复杂,包括细胞内部端粒长度缩短[22]、自噬损伤[23]、线粒体功能障碍、DNA损伤、内质网应激以及Nrf2、SIRT1等抗衰老因子的减少和磷酸肌醇3-激酶、NF-κB、雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)等促衰老分子的增加等表现,主要是由于CSE诱导氧化应激产生的内源性、外源性活性氧(reactive oxygen species,ROS)造成上述代谢过程紊乱和损伤。目前已发现多种二甲双胍可能在肺部发挥抗氧化、抗衰老功能的潜在机制。研究发现[24],二甲双胍可通过激活AMPK抑制mTOR活性,增强支气管上皮细胞自噬作用,认为可能是激活的AMPK通过抑制mTORC1亚型,减弱了mTORC1对自噬启动蛋白UNC-51样激酶1(UNC-51-like kinase 1,ULK1)的磷酸化抑制作用,或直接作用于ULK1来激活自噬。SAITO等[25]认为,二甲双胍也可通过增加含DEP结构域的mTOR相互作用蛋白(DEP domain-containing mTOR interactingprotein,DEPTOR)表达来强化核纤层蛋白B1(lamin B1)对mTOR的调控,防止COPD发病过程中mTOR的异常激活。香烟烟雾包含多种呼吸链抑制剂,可引起电子泄露,产生ROS,还可诱导线粒体自噬损伤,引起线粒体DNA和ROS流入基质甚至血浆[26]。CHENG等[27]观察到二甲双胍通过激活AMPK增强锰超氧化物歧化酶(manganese superoxide dismutase,MnSOD)和SIRT3蛋白表达。MnSOD是主要存在于线粒体中的重要的抗氧化酶,SIRT3是一种调节线粒体功能的线粒体去乙酰化酶,已有研究报道SIRT3对MnSOD的调节作用[28],表明二者在线粒体中可能存在抗氧化通路。此外,有研究认为,二甲双胍也可作用于复合体Ⅰ抑制呼吸链异常性反向传递减少ROS的生成[29]。除上述机制外,许多研究还报道了二甲双胍在其他方面的抗氧化、抗衰老机制,如激活SIRT1和Nrf2两种抗氧化因子,实现醌氧化还原酶、血红素加氧酶等多种抗氧化酶的表达[30-31],改善氧化物/抗氧化物的严重失衡;可降低DNA加合物(DNA与致癌物质形成的复合物)水平和8-oxo-dGuo(一种常见的DNA氧化损伤产物),使受烟雾诱导部分出现低表达的micro RNA正常化[32];可作用于AMPK减少CSE诱导的支气管上皮细胞p16、p21和p66shc等衰老基因的mRNA表达,并使起到抗衰老作用的klotho基因表达增加[27];通过减弱胞内未折叠蛋白反应降低内质网应激水平,并提升端粒酶逆转录酶的表达[33]。当前,在肺部细胞进行的相关基础研究仍然较少,有关减轻DNA损伤、减少内质网应激以及改善端粒长度的具体机制尚不明确,仍需进一步研究来探索其机制。
2.3抗感染作用 COPD急性加重(acute exacerbation of chronic obstructive pulmonary disease,AECOPD)患者常表现为咳嗽、咳脓痰和呼吸困难,是COPD进一步恶化的症状。目前的研究认为,细菌感染是COPD加重的主要致病因素[34-35]。正常情况下,气道上皮表面液体(airway surface liquid,ASL)中葡萄糖浓度约为0.4 mmol·L-1,可有效抑制细菌增殖,主要通过气道上皮细胞的紧密连接(由紧密连接蛋白的丰度决定)及膜上促进性葡萄糖转运体对葡萄糖的转运以达到动态平衡。T2DM、COPD的炎症表达、香烟烟雾会促进细胞旁通路通透性增加,造成上述动态平衡被破坏,诱发呼吸道细菌增殖[36]。PATKEE等[37]和GARNETT等[38]进行的多项体外研究发现,铜绿假单胞菌、金黄色葡萄球菌可通过降低跨上皮电阻(transepithelial electrical resistance,TEER)、诱导紧密连接蛋白表达降低而增加ASL浓度,可能与细胞间紧密蛋白连接处claudin-1和occludin两种蛋白表达减少相关。而二甲双胍可增加TEER、促进claudin-1和occludin表达抵消这种不良作用。目前的研究证据显示,二甲双胍对金黄色葡萄球菌的抑制可能通过激活AMPK,促进细胞外相关激酶表达,进一步上调TEER,促进occludin的磷酸化和组装发挥作用[39]。
2.4改善GC拮抗 GC是治疗COPD的常用药物。研究表明,GC可通过将组蛋白去乙酰化酶(histone deacetylase 2,HDAC2)募集到基因表达位点以降低组蛋白乙酰化程度,抑制炎症基因的表达,而CSE诱导及COPD中活跃的氧化应激,所产生的毒性代谢产物4-羟基壬烯醛(4-hydroxynonenal,4-HNE)可与HDAC2以共价键结合,从而降低GC的抗炎作用,此外,香烟还可抑制支气管上皮细胞中多药耐药蛋白1(multidrug resistance protein 1,MRP1)表达,减少4-HNE外排,引起GC拮抗。TAO等[40]发现,二甲双胍可通过激活Nrf2/HO-1信号通路上调MRP1表达,进而调节HDAC2蛋白表达来改善GC抵抗,对目前存在的GC耐药的缓解具有一定的积极作用。
3 二甲双胍治疗COPD合并T2DM的临床研究
二甲双胍在基础实验研究中表现出潜在的抗炎、抗氧化应激、抗感染益处,但其临床意义主要依赖于临床试验的有效性和安全性结果。对国内外已进行的多项临床研究(主要为观察性研究,包含病例对照研究及队列研究)汇总分析显示,二甲双胍对于共病患者症状的缓解及死亡风险的降低具有重要临床意义。
3.1有效性研究 国外多项观察性研究以COPD合并T2DM的患者队列为主要研究对象,按照是否暴露于二甲双胍展开长期随访或进行回顾性病例分析,研究指标包括肺功能指标、AECOPD风险、再住院风险、死亡风险等,详细数据见表1。COPDGene队列研究[33]与COSYCONET队列研究[41]以肺功能作为结局指标,结果显示,服用二甲双胍与未服用二甲双胍的参与者相比,传递系数(transfer coefficient,KCO)和肺一氧化碳转移因子(transfer factor for carbon monoxide of lung,TLCO)的平均年下降幅度显著降低(-0.2%vs-2.3%,-0.8%vs-2.8%,P<0.05),肺气肿百分比低于非暴露组[-0.92%,95%CI=(-1.7%,-0.14%),P=0.02],肺密度差异较明显[2.2 g·L-1,-2.7,-5.0,95%CI=(0.43,4.0 g·L-1),P=0.01]。关于死亡率指标,HO等[42]的研究结果显示,在Kaplan-Meier生存曲线中,使用二甲双胍的患者生存率显着提高,在HITCHINGS[43]的研究中也观察到相同的结果[中位生存期分别为5.2和1.9年,HR=0.57,95%CI=(0.35,0.94)],且二甲双胍组患者死亡HR为0.46[95%CI=(0.23,0.92),P=0.028],这与YEN等[44]的研究结论相一致(稳定期队列中,二甲双胍组aHR为0.84,P<0.000 1;AECOPD队列中,二甲双胍组aHR为0.89,P=0.002)。此外,其余研究表明,T2DM患者使用二甲双胍可降低COPD发生率(匹配队列总体HR为0.643)[45],其COPD特异性急诊就诊次数和住院率也有所下降(7.11%vs9.61%,P<0.000 1;61.63%vs71.27%,P<0.000 1)[46],这与徐斌[47]、周秋华等[48]报道的住院率结果一致。
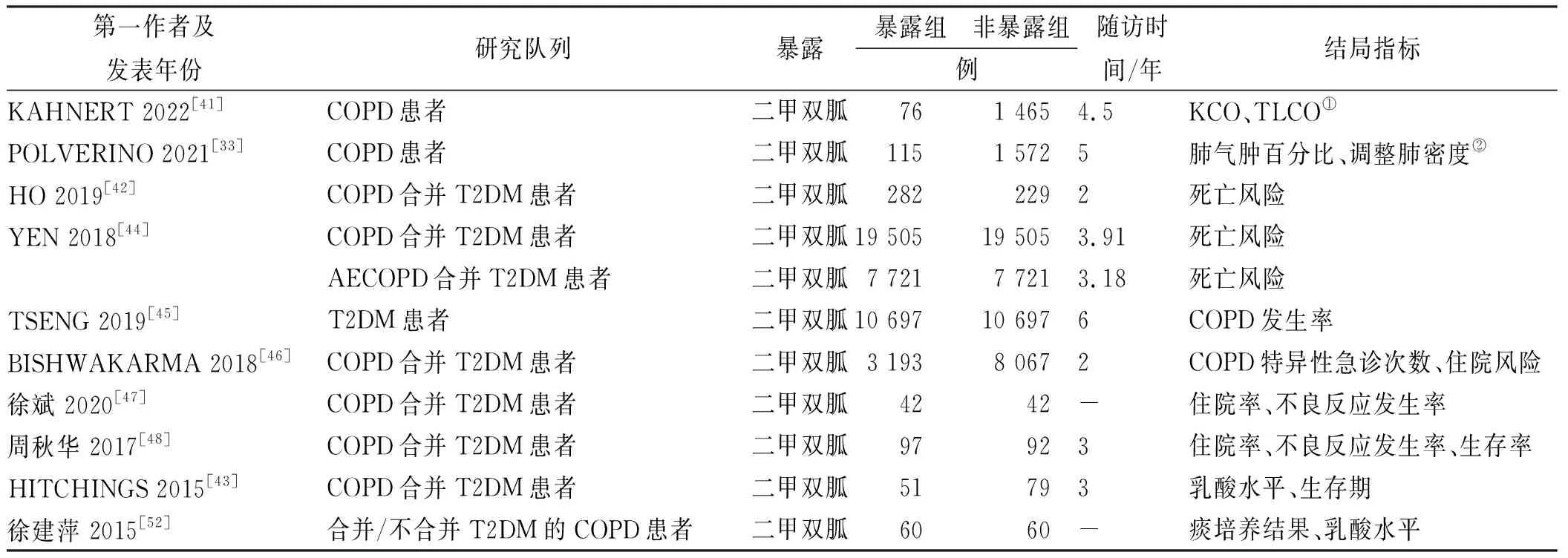
表1 二甲双胍治疗COPD合并T2DM的观察性研究相关数据Tab.1 Relevant data in the observational studies of metformin in the treatment of COPD with T2DM
队列研究和病例对照研究的整体结果表明,二甲双胍对COPD及伴有T2DM并发症患者的肺功能改善、疾病缓解、死亡风险降低和生存期延长均有一定益处。但分析上述队列研究可发现部分不足。首先,部分研究队列的暴露组与非暴露组人数存在极不均衡现象,必要时使用了倾向评分匹配进行调整;尽管多数研究对变量进行了调整,得到一致的结论,但影响COPD进展的混杂因素较多,如健康生活方式、其他药物使用等,仍然难以足够全面地排除其他混杂因素的干扰;此外,目前使用肺功能评估作为结局指标研究虽然表现出差异,但研究较少,将来需要考虑范围更加全面、样本量更广、随访时间更长的的观察性研究进行进一步验证。
当前国内外相关随机对照试验开展较少,仅有两项RCT研究了其潜在益处。戴海燕等[49]选取了AECOPD合并T2DM患者,分为试验组(常规治疗+二甲双胍)和对照组(常规治疗)各70例,有效性结局指标为APACHE II评分及1年后生存率。结果显示二甲双胍组7 d内APACHE II评分降低速度较快,评分低于对照组,二者差异有统计学意义(F=98.416,P=0.000),且二甲双胍组1年生存率较高[OR=2.486,95%CI=(0.994,6.218)],但该研究中未提及盲法、随机分配等实验方法,对于实验的内部偏倚尚无法进行评估。HITCHINGS等[50]针对AECOPD非糖尿病患者进行的一项随机、双盲、安慰药对照试验表明,二甲双胍组与安慰药组间对于毛细血管血糖水平的降低以及C反应蛋白、果糖胺水平的改善差异无统计学意义,推测在短时间内二甲双胍针对AECOPD所致血糖水平升高没有获益,但该研究主要集中在二甲双胍能否降低AECOPD非糖尿病患者高血糖的问题,有关AECOPD中高血糖的发病机制尚未证实,加之AECOPD复杂的全身性致病反应,二甲双胍在其中是否直接发挥降糖作用还无法确定。此外,该研究对于呼吸系统方面的结局指标也未进行深入研究。今后,仍需要有证据等级更高、实验设计更严谨的随机对照试验对当前结果进行进一步探索。
3.2安全性研究 由于COPD患者呼吸功能受损,可造成供氧不足,导致乳酸积蓄,而二甲双胍已被证明存在高乳酸血症的不良反应,主要是通过抑制线粒体呼吸链中的复合物1,从而导致氧化磷酸化受损及有氧呼吸抑制[51],关于二甲双胍用于T2DM合并COPD的安全性,还有待评估。徐建萍[52]研究结果显示,共病患者使用二甲双胍后,乳酸水平显著下降,组间存在差异,徐斌[47]研究发现,使用了二甲双胍的共病患者高乳酸血症、呼吸性酸中毒、总不良反应发生率均低于未使用二甲双胍的共病患者,而周秋华等[48]的研究中,两组高乳酸血症、呼吸性酸中毒的发生率并未表现出明显差异。HITCHINGS等[43]的研究中,二甲双胍组乳酸水平略有升高;中位数(四分位距)为1.45(1.10,2.05) mmol·L-1,而非二甲双胍组为1.10(0.80,1.50) mmol·L-1,P=0.012,但并未发生乳酸酸中毒,但该研究并未排除混杂因素对实验结果的影响。此外,戴海燕等[49]进行的RCT研究中,纳入的AECOPD并发症患者,约50%存在血氧过低,超过30%存在呼吸衰竭(但非呼吸性酸中毒),尽管处在慢性缺氧的呼吸困难状态,但二甲双胍组与对照组在12个月内乳酸水平呈下降趋势,无乳酸酸中毒情况发生,观察终点也未表现出差异(F=1.929,P=0.063);在HITCHINGS等[50]进行的RCT研究中,AECOPD患者也未出现酸中毒症状。当前的研究表明,二甲双胍用于治疗COPD合并T2DM可能致使乳酸升高,但整体升高幅度不大,且不良反应发生率较小。由于研究所得到的结果参差不齐,无法给出明确结论,还需要在后续究中进一步评估。
4 结束语
目前虽然已存在多种药物(如支气管舒张剂、GC等)用于治疗COPD,且患者的生活质量得到明显改善,但尚无一种治疗方法可以有效减缓疾病进展或降低死亡率。慢性共病患者通常同时患有2种及以上慢性病,对多种疾病同时起效的药物,可有效减少合并用药的复杂性并减轻对身体的负担,这将是慢性共病患者的福音。二甲双胍存在多种治疗COPD的潜在机制,可为COPD及合并有T2DM患者的治疗提供一个崭新的思路,未来仍需要更多高质量的研究进一步证实。

