超声指导冠脉旋磨术和药物洗脱支架植入术治疗冠脉内膜严重钙化的价值
班 雷
(本溪市中心医院心内科 辽宁 本溪 117099)
经皮冠状动脉(简称冠脉)介入术是治疗冠心病的主要方法,能够迅速恢复冠脉血液循环,增加心肌供血和供氧量,改善心功能,但冠脉严重钙化病变会增加介入治疗难度,容易出现血管夹层、支架膨胀不全等并发症,增加支架内血栓或再狭窄风险[1-2]。目前根据钙化病变分布部位可分为冠脉内膜钙化、外膜钙化和混合型钙化,其中内膜严重钙化病变部位靠近内膜交界侧和血管管腔,会导致冠脉管腔不规律狭窄和管壁粗糙,使球囊无法通过或通过后难以充分扩张,支架植入后膨胀不良,影响患者预后。因此在支架植入前需对钙化病变进行旋磨预处理,以获得良好的血管内腔,达到理想的支架贴壁以及展开效果,最终为介入治疗创造良好的手术条件。而血管内超声可以明确病变性质,量化钙化程度,为旋磨术的处理提供指导。研究发现,血管内超声指导下冠脉旋磨术和药物洗脱支架植入术治疗冠脉内膜严重钙化可以提高介入治疗手术成功率,改善患者预后[3]。本研究回顾性分析了本院60 例冠脉内膜严重钙化患者经超声指导旋磨术和药物洗脱支架处理的效果,报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2018 年2 月—2023 年2 月在本溪市中心医院行超声指导冠脉旋磨术和药物洗脱支架植入术治疗的60 例冠脉内膜严重钙化患者临床资料,包括年龄、性别、吸烟史、高血压史、病变血管分布等。纳入标准:①临床资料完整,无缺失;②经血管内超声检查显示沿着血管壁分布强回声光团伴声影,内膜最大钙化弧度>270°,确诊为冠脉内膜Ⅳ级钙化;③均符合旋磨术和药物洗脱支架治疗指证。排除标准:①存在旋磨易引发血栓栓塞现象的病变,如退行性变的大隐静脉桥病变;② 存在内膜撕裂病变,旋磨能够加重撕裂;③严重成角(>60°)病变;④急性心肌梗死急性期(≤7 d);⑤合并重要脏器如肝、肺、肾等严重功能不全。
1.2 方法
完善血常规、肝肾功能、血糖、血脂、感染四项、凝血功能、心电图、胸片等检查。Seldlinger 法常规穿刺桡动脉或股动脉后置入血管鞘,注入肝素100 IU/kg,行冠脉内超声检查。将pilot50 导丝送至病变血管远端,超声导管沿pilot50 导丝送入至靶病变远端,然后应用自动回撤装置,以0.5 mm/s 速度将超声导管自动回撤到靶病变近端,若自动撤回受阻,可手动撤回,无法通过最狭窄处时,按照探头所能达到的血管最远处计算,记录并分析图像,观察狭窄和钙化程度、最小管腔直径和管腔有效面积,有无钙化结节、病变形态改变等。依据超声测量的管腔直径、病变程度选择合适大小的旋磨头和药物洗脱支架,一般旋磨头/管腔直径为0.5 ~0.6,支架多在管腔截面积最小病变处植入。
选用Boston Scientific 公司的旋磨治疗仪进行治疗,将旋磨导丝送入到钙化血管的远端,送入过程中始终保持其头部摇摆样以确定进入冠脉真腔。连接好旋磨推进器、高压输液器、氮气瓶等各部件,然后固定旋磨导丝远端,术中始终保持旋磨导丝的“同轴性”,旋磨导管穿入旋磨导丝进行体外测试,保持旋磨头转速70 000 ~180 000 r/min,经旋磨导丝将旋磨头送入体内,按照“逐步推进,分段磨除”的原则,135 000 ~180 000 r/min的转速、平均0.50 mm/s 的推进速度逐步推进旋磨,遇到阻力时快速撤回正常血管内,每次旋磨时间和间隙时间分别为10 ~15 s、30 s,每处病变旋磨2 ~3 次,若是旋磨3 次仍然无法通过病变则逐渐加大旋磨头转速。旋磨终点旋磨头推进顺畅无阻力,声音轻柔,转速无衰减,病变血管光滑。通过旋磨术使钙化血管明显开通,冠脉相对光滑后,旋磨导丝撤出冠脉,送入普通工作导丝,经非顺应性球囊扩张,然后植入药物洗脱支架,开通病变,再次进行超声检查,评价支架植入效果,检测最小管腔直径、管腔有效面积、狭窄率等。
1.3 观察指标
①收集患者一般资料,包括性别、年龄、体质量指数、吸烟情况、合并疾病等,并整理临床资料包括病变血管分布、左心室射血分数、入院诊断疾病。②观察患者超声图像,并比较干预前后最小管腔直径、狭窄程度以及管腔有效面积。③统计术后即刻成功手术率以及并发症发生情况。
1.4 统计学方法
采用SPSS 24.0 统计软件分析数据,符合正态分布的计量资料以均数±标准差(± s)表示,采用t检验;计数资料以频数(n)、百分率(%)表示,采用χ2检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 患者基本资料
60 例患者中男性35 例,女性25 例;年龄50 ~75 岁,平均(65.20±6.13)岁;体质量指数18.0 ~26.3 kg/m2, 平均(22.38±2.10)kg/m2; 吸烟有25 例,饮酒有22 例;合并2 型糖尿病5 例、高血压病43 例、高脂血症5 例;病变血管分布:三支病变22 例、双支病变29 例、单支病变9 例;病变血管狭窄程度(75.34±6.79) %;左心室射血分数(64.56±5.10)%;入院诊断稳定型心绞痛38 例、不稳定型心绞痛16 例、急性心肌梗死6 例。
2.2 患者手术情况
60例患者旋磨前降支44例、回旋支5例、右冠脉11例;49 例使用1 个旋磨头,11 例使用2 个;旋磨头大小(1.45±0.29)mm;植入支架直径(2.83±0.56) mm,旋磨头/靶血管直径比值为(0.51±0.09),植入支架直径(2.83±0.56)mm,最小支架面积(5.90±1.15) mm2,见表1。
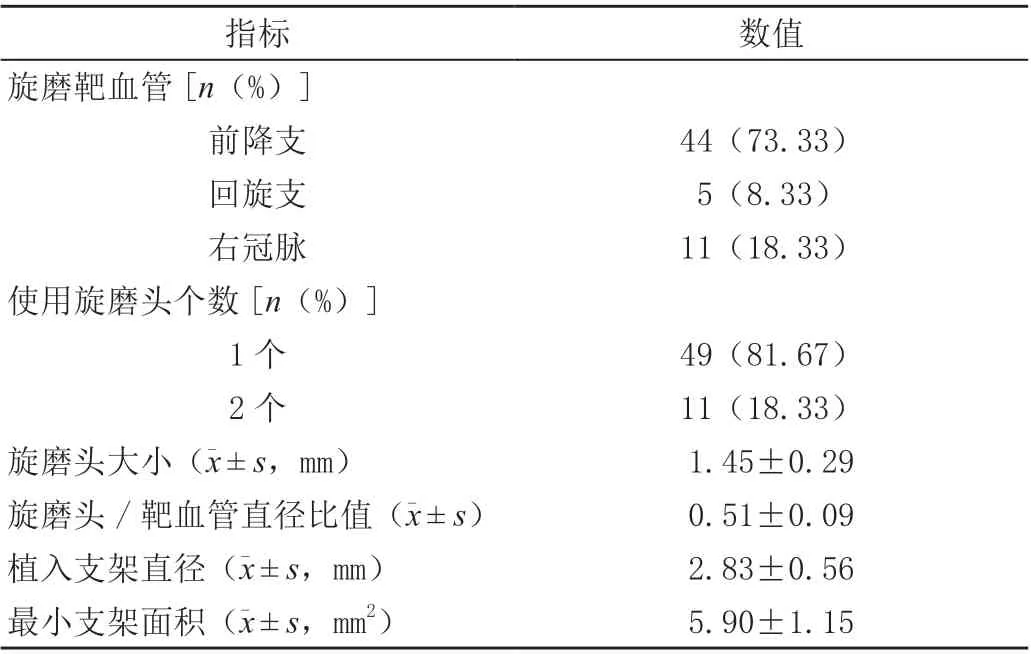
表1 患者手术情况
2.3 干预前后超声检查结果比较
干预后超声检查结果显示最小管腔直径、狭窄程度以及管腔有效面积均较干预前明显改善,差异具有统计学意义(P<0.05),见表2。
表2 干预前后超声检查结果比较(± s)

表2 干预前后超声检查结果比较(± s)
时间点 例数 最小管腔直径/mm 狭窄程度/% 管腔有效面积/mm2干预前601.98±0.5675.34±6.794.56±1.14干预后602.70±0.7710.10±2.437.10±1.88 t 5.85870.0738.949 P<0.001<0.001<0.001
2.4 患者超声图像情况
图1 是59 岁男性患者,临床诊断为稳定型心绞痛的超声图像。
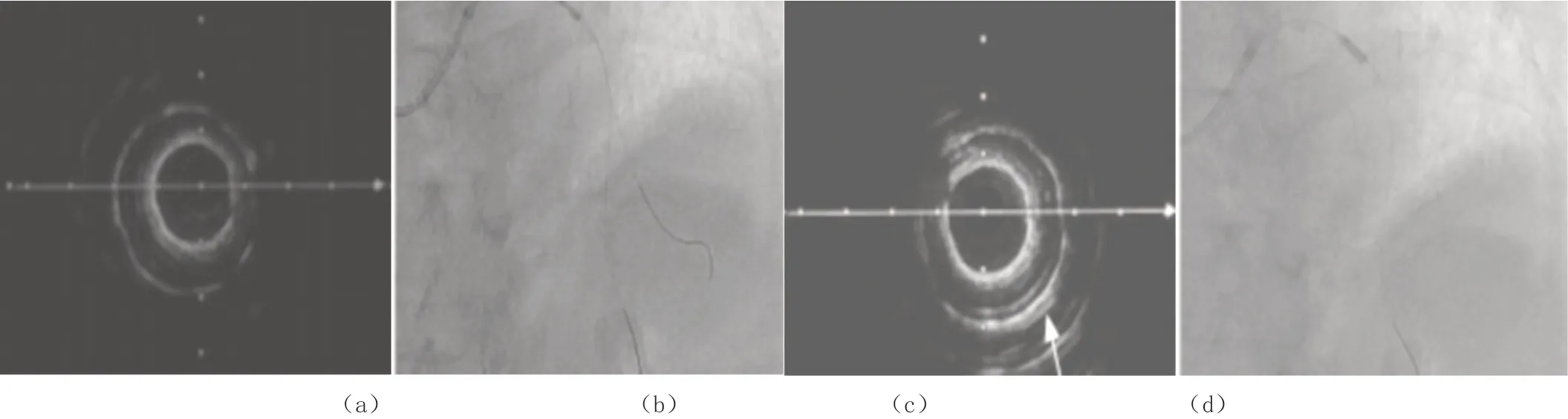
图1 患者血管内超声音图
2.5 相关并发症统计
经统计60 例患者术中均无冠脉夹层、穿孔、慢血流、急性血栓等情况出现,术后即刻手术成功率为100%。
3 讨论
冠脉钙化病变由钙盐在冠脉粥样硬化斑块沉积所致,可以导致血管顺应性下降,舒缩功能障碍和心肌灌注损伤[4]。相比冠脉外膜面钙化,严重内膜面钙化对介入治疗的影响要大很多,一般情况下外膜钙化无需特殊处理,常规操作即可,但是严重内膜钙化会直接导致球囊和支架无法通过病变处,即使勉强通过也容易出现球囊无法充分扩张,支架植入后膨胀不良问题,影响手术治疗效果[5-6]。冠脉旋磨术是对钙化病变进行磨除处理,以开扩冠脉管腔,提高血管顺应性,从而顺利、优质地植入药物洗脱支架,保证介入治疗的顺利开展。
本研究对60 例行超声指导冠脉旋磨术和药物洗脱支架植入术治疗的冠脉内膜严重钙化患者进行了回顾性分析,结果显示与术前相比,术后最小管腔直径、狭窄程度以及管腔有效面积均明显改善(P<0.05),术后即刻手术成功率达100%,表明超声指导冠脉旋磨术和药物洗脱支架植入术治疗冠脉内膜严重钙化效果显著,与有关报道相符[7]。张健等[8]通过给予冠脉内膜中度钙化患者旋磨术联合药物洗脱支架术治疗,发现手术成功率达97.26%,再狭窄率为4.11%,佐证了上述方法治疗的有效性。有研究发现,旋磨在切割物质时,可以保持邻近组织的完整性,椭圆形的旋磨头能够区分健康的血管壁和斑块[9-10]。健康的血管组织富有弹性,旋磨头高速通过时会被自然弹开,因此不会出现损伤,而缺乏弹性的、坚硬的钙化组织会被优先处理,被研磨成小于红细胞直径的微粒,然后被吞噬系统清理,一般不会引起微血管堵塞[11]。但在实际旋磨操作中应间隔一定时间,保证这些颗粒能够被充分清除[12]。
通过上述这种对钙化组织的处理,开扩了钙化的冠脉管腔,能够使球囊顺利通过病变部位和充分扩张,球囊扩张后能在钙化薄弱的部位打开缝隙,在植入药物洗脱支架时使支架扩张更充分,降低了因支架膨胀不全导致的远期再狭窄的发生风险[13]。而血管内超声能够直接显示血管腔的形态结构,精准测量血管直径,实时观察钙化斑块范围和程度,为旋磨术处理提供更多有用信息,有利于指导治疗和评估旋磨效果[14]。本研究还对并发症进行了统计,结果显示未出现冠脉夹层、穿孔等与旋磨有关的并发症,表明该治疗方法安全性好,但胡司淦等[15]应用血管内超声指导旋磨预处理,发现与之相关的并发症发生率为17.3%,可能与本研究所选病例较少有关。尽管如此,冠脉旋磨术还存在一定不足,比如当旋磨头与靶血管管腔直径的比值>0.8 时,容易损伤血管壁,导致冠脉穿孔、夹层、内膜撕裂或者无复流等。此外,还受操作技巧、经验影响,因此在实际工作中需注意加强技巧练习。
综上所述,超声指导冠脉旋磨术和药物洗脱支架植入术治疗冠脉内膜严重钙化临床效果显著,安全性较好,能够为后续手术治疗提供良好条件。由于是回顾性分析,尚未随访观察远期疗效,今后还需开展前瞻性随机对照试验,更深入了解该方案的效果。

