单侧甲状腺乳头状癌中央区淋巴结转移的临床预测模型构建
李 佳,宋 杨,汤 铜
甲状腺乳头状癌(papillary thyroid carcinoma,PTC)是甲状腺癌中最常见的病理类型,占70%~80%,目前其发病率不断增加,淋巴结转移率也较高[1]。尽管大多数PTC病人病程缓慢,在初期治疗后20~30年复发,但淋巴结转移和局部复发仍是临床工作中的重点、难点[2]。20%~40%的PTC病人在诊断时即发现区域淋巴结受累,但多数在临床中表现为隐匿性淋巴结疾病,最常表现为仅在术后病理中发现中央区淋巴结转移[3]。目前,国内外指南中对于临床淋巴结阴性(cN0)的病人,是否行预防性中央区淋巴结清扫术(prophylactic central lymph node dissection,PCLND)仍存在很大争议[4-5]。由于中央区淋巴结的清扫会增加甲状旁腺及喉返神经损伤的风险[6],根据美国甲状腺协会的指南和日本内分泌外科协会的专家共识,不常规推荐临床或放射学淋巴结阴性PTC病人行PCLND。然而在临床工作中,由于PCLND能提供准确的术后分期以指导后续治疗,并可能降低复发率,故在东亚地区国家仍较常采用PCLND[5]。我们在临床工作中发现cN0 PTC病人术后病理证实隐匿性中央区淋巴结转移较为常见。因此,本研究旨在探讨单侧cN0 PTC病人发生中央区淋巴结转移的危险因素,并以此为依据构建预测模型,为合理、全面的术前评估提供决策依据。
1 资料与方法
1.1 一般资料 选取2019年在安徽医科大学第二附属医院甲状腺乳腺外科的183例行单侧PTC切除的病人作为研究对象。纳入标准:(1)初次手术,且术前影像学评估未发现淋巴结转移;(2)经术后病理证实为PTC者;(3)术前有完整的影像学及实验室检查结果。排除标准:(1)既往曾行甲状腺手术者;(2)术后病理非PTC者;(3)术前影像学资料及实验室资料不全者;(4)术前检查存在可疑淋巴结转移者。
1.2 方法 收集纳入的183例行单侧PTC切除的病人的相关资料包括(1)人口学资料:年龄、性别;(2)术前资料:收集超声报告及术前甲状腺功能全项化验,依据术前促甲状腺激素(TSH)水平是否偏离正常参考值范围判断是否升高,依据超声及甲状腺功能全项报告甲状腺球蛋白抗体(TgAb)及甲状腺过氧化物酶抗体(TPOAb)升高判断是否合并桥本甲状腺炎,超声评估病灶位置是否紧贴包膜以及是否伴有钙化;(3)术后病理资料:病灶大小、个数、淋巴结转移情况及个数,依据术后病理报告中病灶的个数判断其是否多灶。
1.3 统计学方法 采用χ2检验、 ROC 曲线、二元logistic回归分析及多因素 logistic 回归分析,并构建中央区淋巴结转移的预测模型。
2 结果
2.1 病人基本信息 183例PTC病人中,男46例,女137例,年龄(44.75±11.88)岁,肿瘤最大径(1.17±0.78)cm(0.3~5.5 cm),中央区淋巴结转移者占52.5%(96/183)(见表1)。
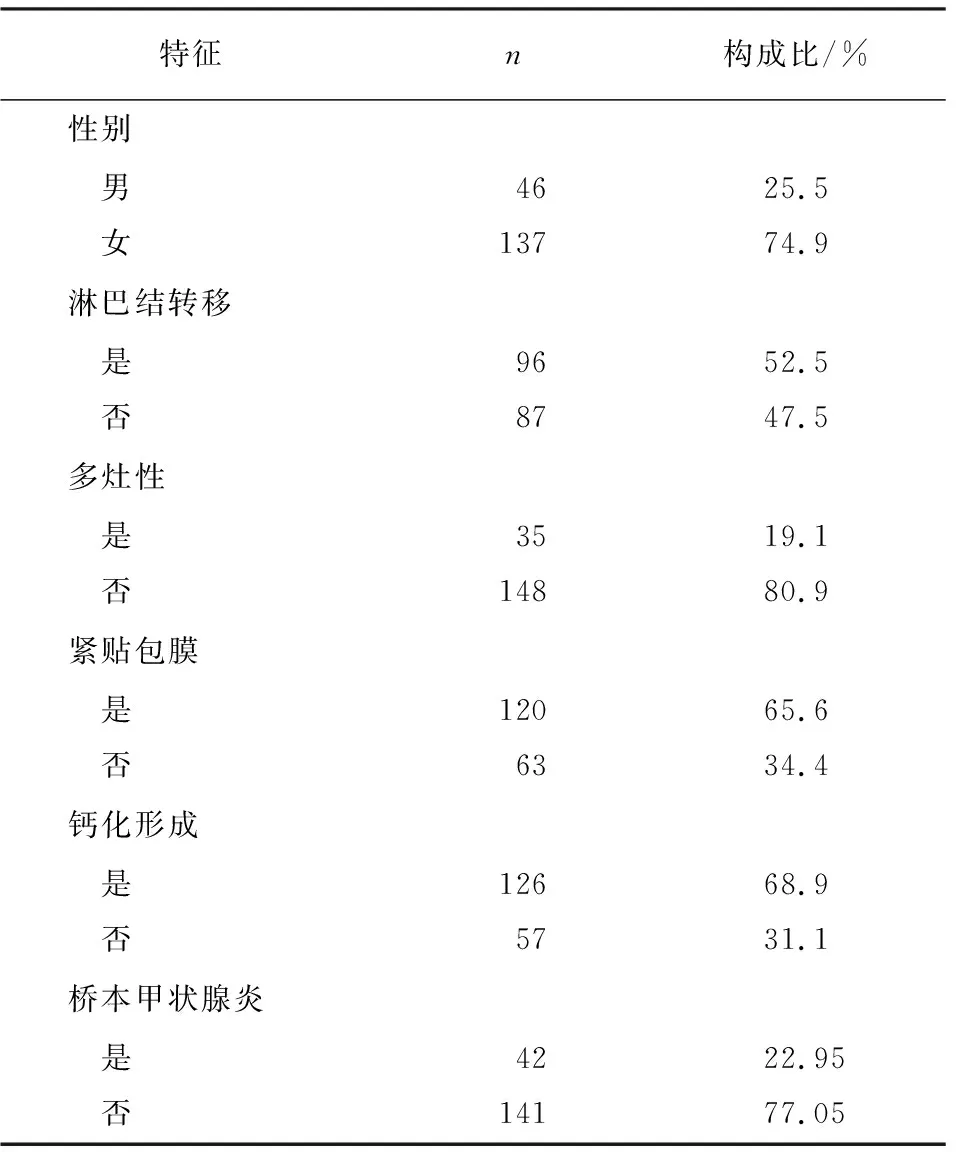
表1 183例PTC病人基本信息
2.2 PTC病人发生中央区淋巴结转移的单因素分析 中央淋巴结转移的PTC病人中男性、年龄<55岁、肿瘤最大径>1 cm、多灶性、紧贴包膜和钙化形成的比例均高于无转移病人(P<0.05~P<0.01),是否合并桥本甲状腺炎、术前TSH以及TPOAb是否升高与无转移病人的差异均无统计学意义(P>0.05)(见表2)。
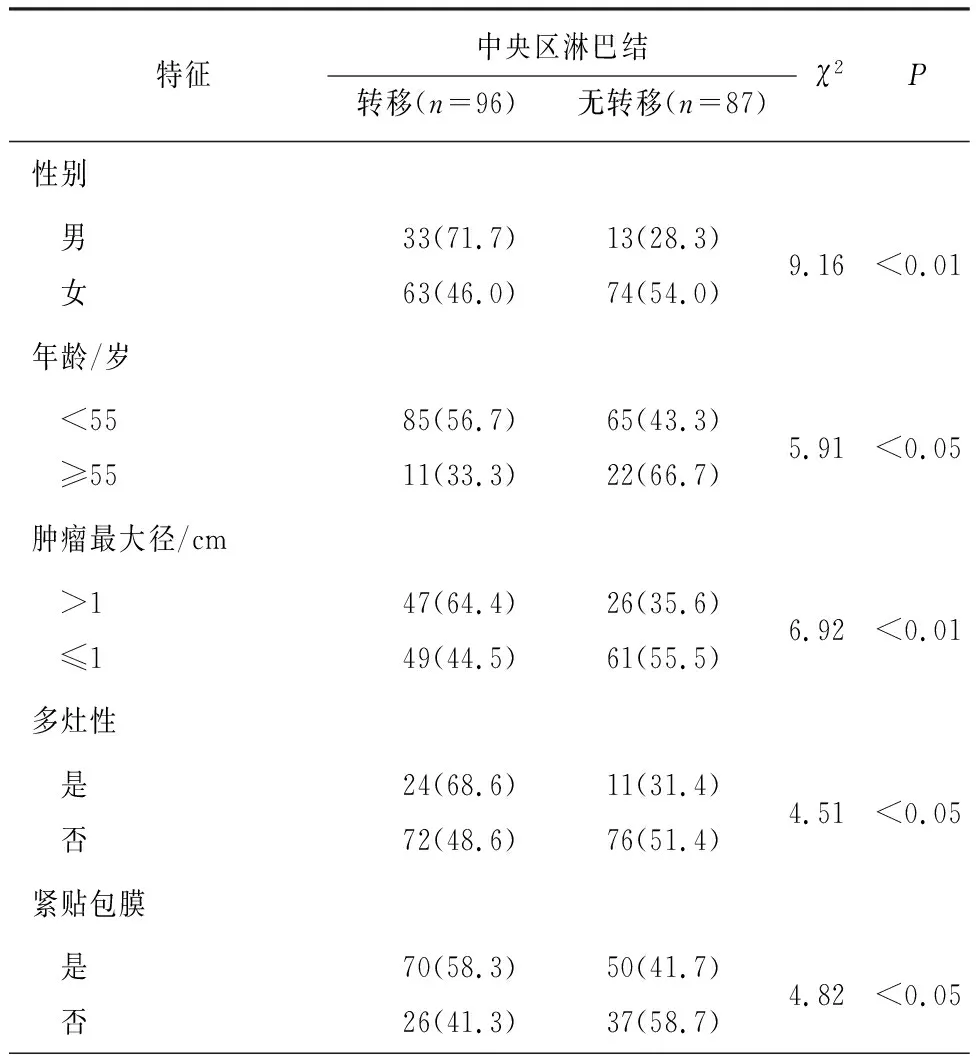
表2 PTC病人发生中央区淋巴结转移的单因素分析[n;构成比(%)]
2.3 PTC病人发生中央区淋巴结转移的多因素logistic回归分析 以中央区淋巴结是否发生转移作为因变量,纳入性别、年龄<55岁、肿瘤最大径>1 cm及钙化形成进行多因素回归分析。结果显示,男性、年龄<55岁、肿瘤最大径>1cm及钙化形成是PTC发生中央区淋巴结转移的独立危险因素(P<0.05~P<0.01)(见表3)。
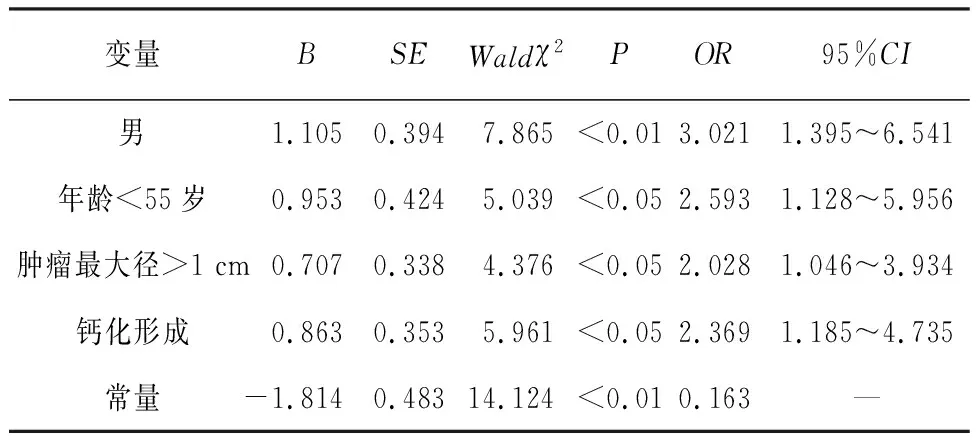
表3 中央区淋巴结转移的多因素logistic回归分析
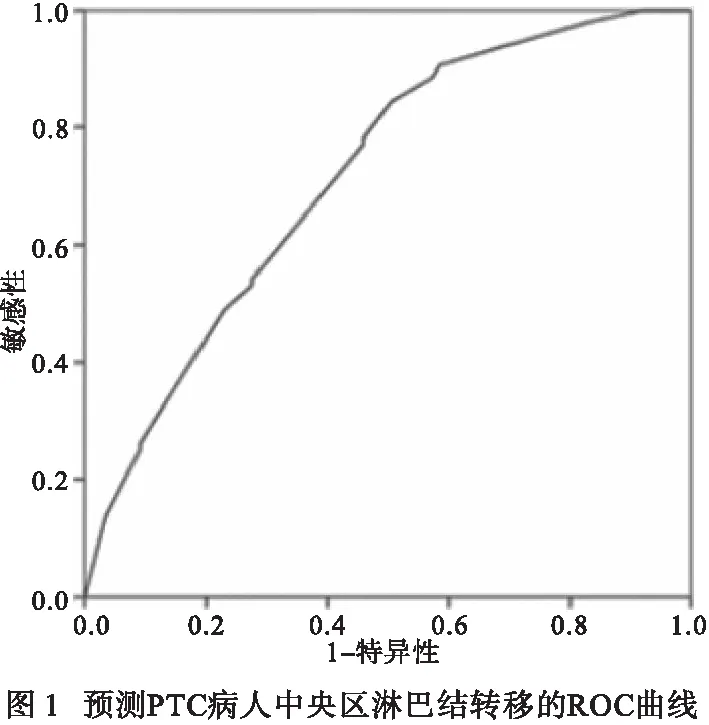
2.4 临床预测模型的构建 根据多元分析结果建立逻辑回归模型:Logit(P)=-1.814+1.105×性别+0.953×年龄+0.707×肿瘤最大径+0.863×钙化形成。将预测概率和真实值构建ROC曲线(见图1),计算出ROC曲线下面积(AUC)为0.716(95%CI:0.641~0.790),说明该模型对于中央区淋巴结转移有较好的预测效果。根据其灵敏度和特异度计算约登指数为0.338,最佳分界点为0.450。
3 讨论
PTC大多预后良好,但常伴有颈部淋巴结转移,尤其是中央区淋巴结转移。其中术前分期为cN0的早期PTC,手术切除被普遍认为是PTC最有效的治疗方法,但PCLND的应用价值仍存在争议[7],其对病人长期预后的影响尚不清楚。研究[8]认为PCLND不会改变病人的预后但可能影响复发率,由于PTC复发后的再次手术难度显著增加,可能会增加神经损伤及甲状旁腺受损的概率,影响病人的生活质量。理论上来说,PCLND可以消除隐匿性转移降低复发率,同时可以帮助术后肿瘤分期,且准确判断是否发生中央区淋巴结转移,有助于指导放射性碘治疗,降低术后血清甲状腺球蛋白,减少再次手术的可能性及并发症[9]。然而亦有研究[10]表明PCLND术后并发症的风险相对较高,如低钙血症。美国和日本专家对临床或放射学淋巴结阴性PTC病人不推荐预防性清扫,根据2015美国甲状腺协会的指南,手术干预并不被认为是PTC病人可用的唯一方式,而主动监测逐渐被认可为是更优化的策略,是低风险人群PTC(cT1N0M0)的最佳替代策略[11]。因此,术前评估预测颈部淋巴结情况对个体化选择PTC病人的治疗方案具有重要意义。
本研究表明,男性、年龄<55岁、肿瘤最大径>1 cm、多灶性、紧贴包膜和钙化形成对单侧cN0 PTC的病人中央区淋巴转移的影响具有显著的差异性。多因素logistic分析表明,男性、年龄<55岁、肿瘤最大径>1 cm、钙化形成是中央区淋巴结转移的危险因素。通过多因素分析结果建立了单侧cN0 PTC中央区淋巴结转移的预测模型,经验证该模型具有较好的预测效果和实用价值。
鉴于中国甲状腺癌负担的日趋严重和性别-年龄的异质性,加强一级预防,探索其潜在危险因素应作为重中之重[12-13]。在一项回顾性分析[14]中,纳入SEER数据库的21 972例病人中,病人性别、年龄、种族、肿瘤大小、甲状腺外侵犯以及多灶性被证实与颈部淋巴结转移相关。在我们的研究中,男性是中央区淋巴结转移的危险因素,这也与以往研究[14]结论一致,表明中央区淋巴结转移具有性别倾向。对于男性病人,外科医生术前应更加重视颈部淋巴结状况的检查和影像学评估。有研究[15]报告年龄<55岁是中央区淋巴结转移的危险因素,也有报道说年龄<45岁是中央区淋巴结转移的危险因素[16]。在我们的研究中,年龄<55岁是中央区淋巴结转移的独立危险因素,提示年轻病人更应注意中央区淋巴结转移。肿瘤大小一直被认为是PTC中央区淋巴结转移的重要预测因素,LIU等[17]的研究根据AJCC分期系统和PTMC的定义将肿瘤大小分为4组,分析结果显示肿瘤大小>1.0 cm是中央区淋巴结转移的独立危险因素,也有研究[18]报道颈部淋巴结转移与原发肿瘤的大小呈正相关关系,随着肿瘤大小的增加,颈部淋巴结转移的发生概率增加。我们的研究结果表明肿瘤最大径>1 cm是单侧cN0 PTC的独立危险因素,提示应注意肿瘤最大径>1 cm的病人中央区淋巴结转移的风险。研究[19]表明,微钙化是由于血管和纤维组织增殖引起的钙盐沉积,微钙化反映了癌组织快速生长的特征。有研究[20]回顾性分析PTC病人的病理特征,探讨PTC不同病理类型钙化的临床意义,发现沙砾体和间质钙化病人癌症分期较高,淋巴结转移较多。本研究中通过多因素分析表明,PTC中钙化形成是中央区淋巴结转移的独立危险因素。
许多甲状腺肿瘤被发现为多灶性肿瘤,报道的发病率范围为18%~87%[20],且多灶性肿瘤的中央区淋巴结转移风险更高[21]。在我们的研究中也发现多灶性肿瘤是与中央区淋巴结转移相关的高危因素。此外,以往有研究[22]得出结论,桥本甲状腺炎也与颈部的区域淋巴结转移有关,但亦有研究[23]表明桥本甲状腺炎与PTC的颈部淋巴结转移无相关性。本研究亦显示桥本甲状腺炎与单侧cN0 PTC的中央区淋巴结转移无相关性。
综上所述,通过多因素分析建立单侧cN0 PTC中央区淋巴结转移预测模型Logit(P)=-1.814+1.105×性别+0.953×年龄+0.707×肿瘤最大径+0.863×钙化形成,AUC为0.716,说明此模型有较好的预测效果和应用价值。在临床诊断中使用该预测模型计算隐匿性中央区转移的概率,P值越大,淋巴的结转移风险越高,应行PCLND。同时通过优秀的手术团队并进行充分的术前评估进而降低病人再手术以及复发转移率。

