离子液体在湿法冶金浸出和电沉积中的应用进展
王府倩, 卢明辉, 汪淑娟, 王 飞, 夏雪雯,耿淑华, 邹星礼, 鲁雄刚
(上海大学材料科学与工程学院, 省部共建高品质特殊钢冶金与制备国家重点实验室, 上海 200444)
离子液体(ionic liquids, ILs) 是一种由阴离子和阳离子组成, 在室温或接近室温下为液态的有机化合物. 通常情况下, ILs 中的阳离子为1,3-二烷基咪唑、N-烷基吡啶、季铵等有机阳离子,阴离子为[Al2Cl7]-、[Al3Cl10]-、[BF4]-、[PF6]-、[PO4]-、[SO4]-、[Tf2N]-、[CF3COO]-等无机或有机阴离子. ILs 的熔点一般低于100°C, 因此又被称为室温离子液体或者室温熔盐[1]. 离子液体的历史最早可追溯到1914 年, 第一个离子液体硝酸乙基铵([EtNH3]NO3) 由Walden 意外制备合成, 其熔点低至12°C, 由于其在空气中存在很大的爆炸危险性, 当时并未引起人们的关注. 1951 年Hurley 等[2]发现了一种可用于金属电沉积的透明溶液, 即溴化N-乙基吡啶-三氯化铝(EtPyBr-AlCl3), 由此开创了第一代离子液体. 1975 年Osteryong 等[3]发现N-乙基吡啶四氯铝酸电解液具有电化学窗口较宽、液相线范围宽且能与有机物混溶等特点, 但因其稳定性较差, 遇水易分解, 对空气非常敏感, 这种烷基吡啶类离子液体的应用受到很大限制. 1982 年, Wilkes 等[4]发现1-乙基-3-甲基咪唑基氯铝酸盐离子液体([EMIm]Cl-AlCl3) 具有更宽的液相线范围和电化学窗口(>3.0 V),这极大促进了人们对离子液体的系统性研究.随后,Wilkes 等[5]又利用[BF4]-和[MeCO2]-阴离子取代[EMIm]Cl-AlCl3离子液体中的[AlCl4]-阴离子, 制备出了2 种对空气和水更稳定的新型低温熔盐([EMIm]BF4和[EMIm]MeCO2),这种溶剂易于制备、种类多样且较为廉价, 具有较好的化学和电化学稳定性. 这类新型的咪唑基系列离子液体被称为第二代离子液体. 自此以[Tf2N]-、[CTf3]-、[C3F7COO]-等作为阴离子的一系列二烷基咪唑类离子液体相继问世, 被广大研究学者研究并应用至今. 目前人们已经研发出第三代离子液体, 该类离子液体是在二烷基咪唑的侧链上引入不同种类的官能团, 使其具有特定的性质及功能, 因此又被称为功能化离子液体. 随着化学种类增加, 功能更加分化, 离子液体进一步分为多种类型, 如室温离子液体、任务特异性离子液体、聚合离子液体等, 这将是未来发展的热门方向[6]. 图1 为离子液体发展过程示意图.
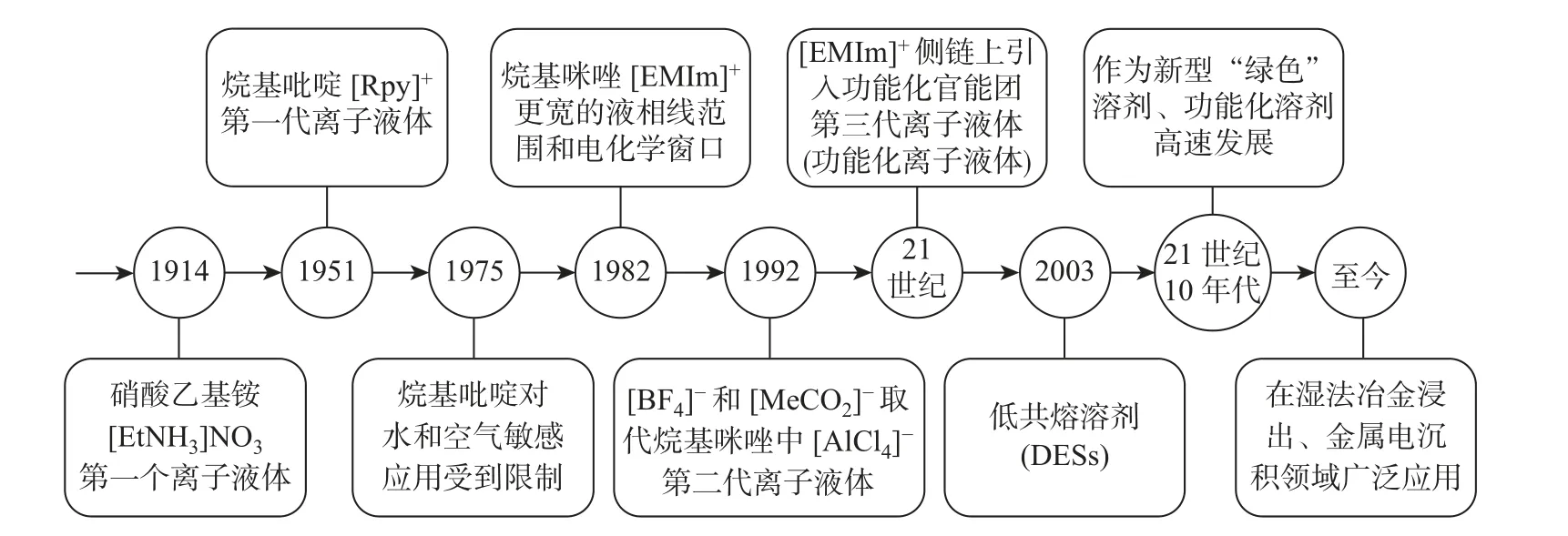
图1 离子液体发展过程示意图Fig.1 Schematic diagram of the developments of ionic liquids
离子液体的有机离子杂化特性和由此产生的分子间相互作用使其具有独特的物理化学性质[7-8], 例如: ①蒸气压低, 在储存和使用过程中不易蒸发; ②热稳定性和化学稳定性好; ③离子电导率高、电化学窗口大, 可作为多种物质研究的电解质; ④可重复使用, 易于再生; ⑤具有熔盐的极性及其离子特性; ⑥较宽的液相线温度范围; ⑦黏度、沸点、水溶性和电化学窗口可根据阴离子和阳离子的合理组合设计, 实现多功能性; ⑧可避免有毒挥发性有机化合物的产生. 在许多物理和化学过程中, 离子液体具有非分子溶剂的特殊特性, 通常表现出“绿色” 和“可设计” 的性质, 因此被越来越多地应用于分离过程、生化过程、有机合成过程、催化反应和材料工程等领域. 此外, 离子液体在溶解性、腐蚀性、环保性及操作温度等方面优于传统强酸强碱溶剂和其他有机溶剂, 因此在冶金领域表现出很好的应用前景[9].
离子液体作为一种“绿色” 溶剂得到了非常广泛的关注. 2003 年Abbott 等[10]首次发现了一种新型溶剂, 并命名为低共熔溶剂(deep eutectic solvents, DESs). DESs 的物理化学性质与传统离子液体类似, 通常由季铵盐与金属盐或氢键供体络合而成. DESs 理论上不完全由离子物质组成, 但通常被认为是一类特殊的离子液体, 因为它们具有许多相同的特性, 包括高黏度、高热稳定性、低挥发性、低蒸气压和溶解性强等. 此外, DESs 还具有易合成、成本低、易回收、无毒、对水和空气不敏感等独特优势[11]. 因此, DESs 从第三代功能化离子液体中脱颖而出, 成为离子液体溶剂更为经济的替代品. 相比传统的离子液体而言, 人们对DESs 的研究还处于起步阶段, 目前越来越多的研究工作集中在这一新兴领域[12-13].
离子液体在金属及其氧化物的溶解浸出、复杂矿物湿法冶金及活泼金属电沉积方面的应用非常广泛, 关于该领域的研究进展前人也有综述[14-15], 本工作在此基础上侧重于近10 年的研究现状, 对其研究进展进行归纳总结, 另综述了利用离子液体从电子废弃物中浸出回收金属、从金属氧化物和多种复杂矿物直接电沉积金属及其合金等方面的应用, 突出了离子液体在湿法冶金中的可能性、挑战性以及未来的发展趋势.
1 湿法冶金浸出
随着电子、交通、石油化工等行业的快速发展, 金属消耗量不断增加, 由此带来的金属资源枯竭问题也日益严重. 从低品位原料中高效地提纯回收金属成为了人们追求的目标. 湿法冶金浸出是提取金属过程中最为常用的方法之一. 利用酸、碱、盐等无机水溶液进行金属回收的冶金工艺相对常见, 但该工艺对金属往往表现出较差的选择性, 且浸出过程中存在废水循环利用困难、能耗高、溶剂消耗量大、环境污染大及对设备腐蚀性很强等问题. 为缓解现有金属提取技术产生的环境和能源问题, 开发新型、对环境友好、低能耗且操作简便的冶金方法迫在眉睫. 离子液体的出现为实现这一目标提供了可能性. 离子液体可以溶解大部分的有机物、无机物、聚合物, 且溶解度较大, 体现出很高的应用价值. 目前, 离子液体已被引入到多种金属的溶解浸出过程中, 成为传统湿法冶金介质的良好替代品.
1.1 金属及其氧化物的溶解和提取
离子液体作为一种节能环保的绿色溶剂, 具有很多传统溶剂所不具备的优势, 如对金属选择性高、可循环使用及对设备腐蚀性小等. 在冶金浸出过程中, 金属氧化物(metal oxides,MOs) 的溶解是大多数金属加工的核心步骤, 也是金属提取、资源回收的关键[16]. 虽然金属氧化物不易溶解, 但是离子液体具有很强的溶解能力(见图2). 大多数金属、金属离子和金属氧化物可以在单一离子液体或适当的离子液体组合中溶解和提取, 因此, 离子液体是环保且可持续提取有价金属、实现冶金资源综合回收利用的良好浸出介质.
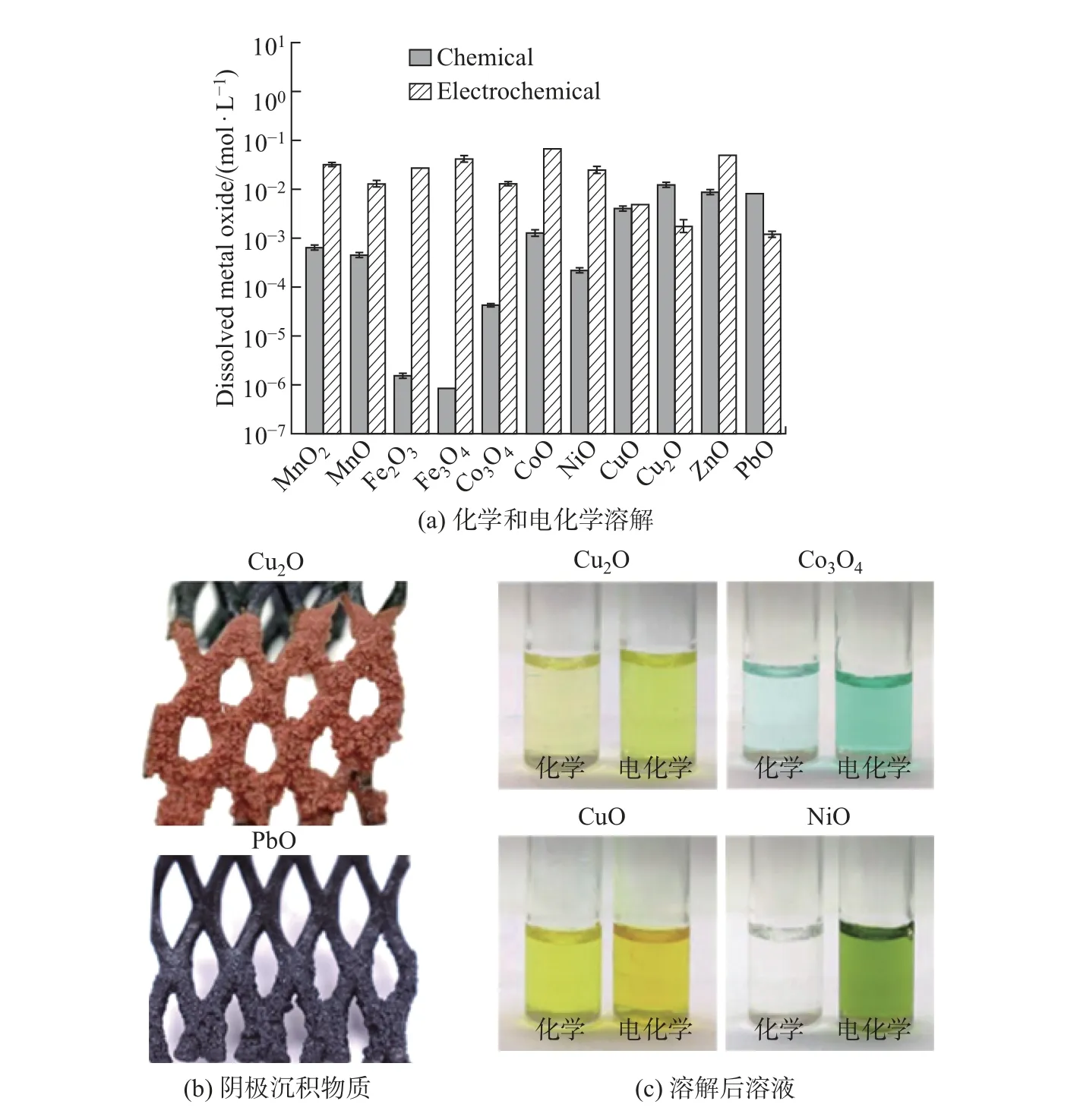
图2 多种金属氧化物在氯化胆碱-乙二醇中的化学和电化学溶解[16]Fig.2 Chemical and electrochemical dissolution of various metal oxides in choline chloride-ethylene glycol[16]
1998 年Behl 等[17]报道了铝(Al) 在室温条件下会溶解于1-乙基-3-甲基咪唑-双三氟甲磺酰亚胺盐([EMIm]Tf2N), 人们逐渐认识到采用离子液体作为溶剂去溶解浸出金属及其氧化物是可行的, 并由此开展了一系列的研究工作. 金属及其氧化物的溶解度与离子液体种类及组成物质比例有关, 大部分金属及其氧化物能够在离子液体中溶解, 而不同阴阳离子结构组成的离子液体可以选择性溶解不同的金属. 铜(Cu)、Al、铂(Pt) 和钛(Ti) 等大部分金属可溶解于含氯化物的离子液体中, 其中氯离子作为很好的配位体来溶解金属, 形成的金属配合物取决于金属的路易斯酸度和离子液体的路易斯碱度[18]. 此外, Abbott 等[19]研究了50°C 下多种金属氧化物在不同离子液体和水溶液中的溶解情况, 得到了不同金属氧化物在离子液体中的具体溶解度数值(见表1), 研究发现金属氧化物溶解后在离子液体中的赋存状态与氧化物及离子液体种类有关, 如ZnO 溶解在n(ChCl)∶n(尿素)=1∶2 的离子液体中时, 氧(O) 仍附着在金属中心, 尿素(urea) 作为配体, 以[ZnClO·urea]-络合物的形式存在于离子液体中; 而在n(ChCl)∶n(丙二酸)=1∶1 的离子液体中, 一些金属氧化物溶解后会以卤金属酸络合物存在,例如CuO 会生成Cu. 多种金属氧化物在不同离子液体中溶解的存在形式如表2 所示.
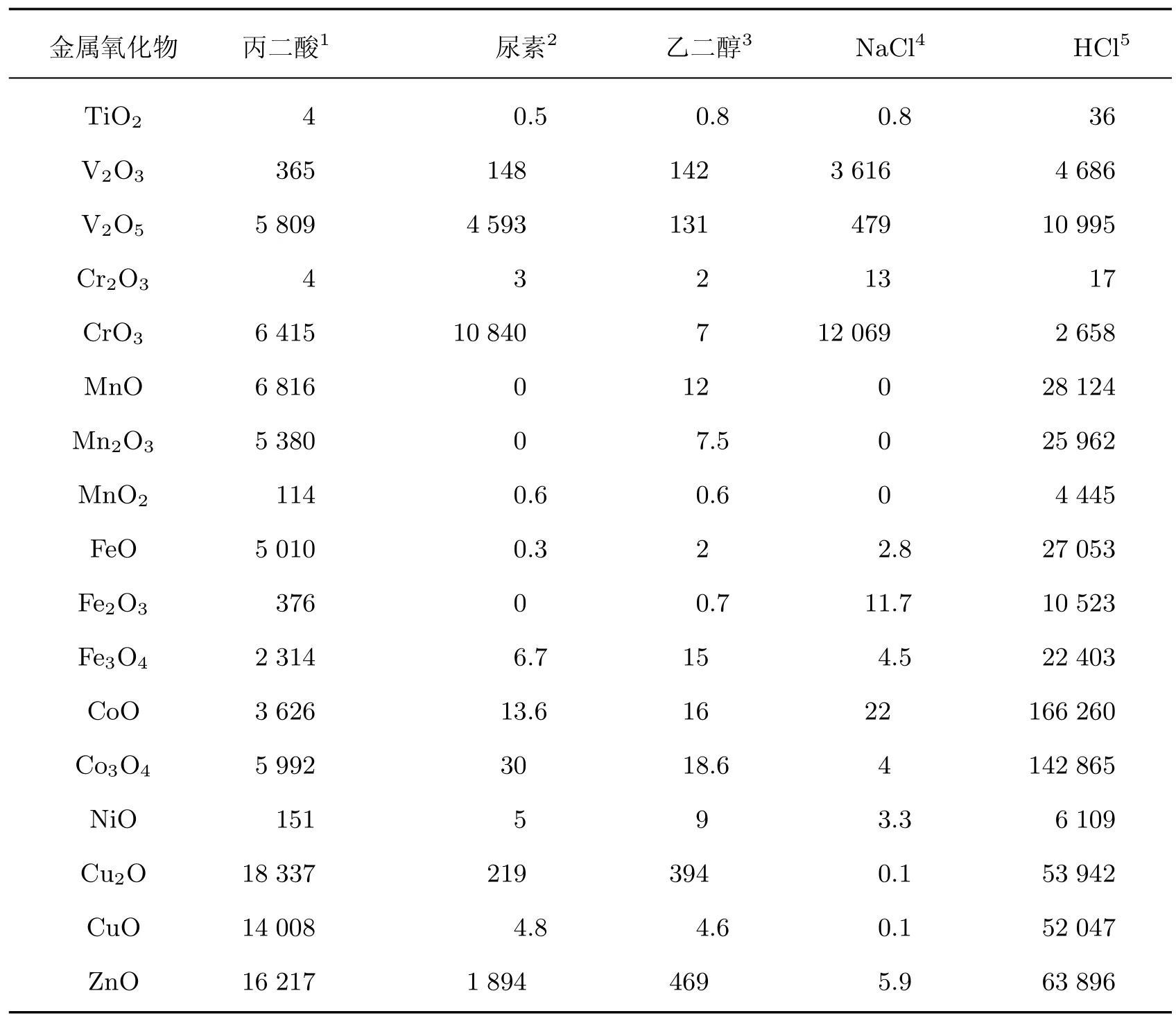
表1 金属氧化物在氯化胆碱(ChCl) 与丙二酸、尿素和乙二醇低共熔溶剂、NaCl 和HCl 水溶液中的溶解度比较(50 °C, 2 d)[19]Table 1 Solubility of metal oxides in eutectic mixtures of choline chloride (ChCl) with malonic acid, urea and ethylene glycol compared to solubilities in aqueous NaCl and HCl solutions(50°C, 2 d)[19](mg·L-1)
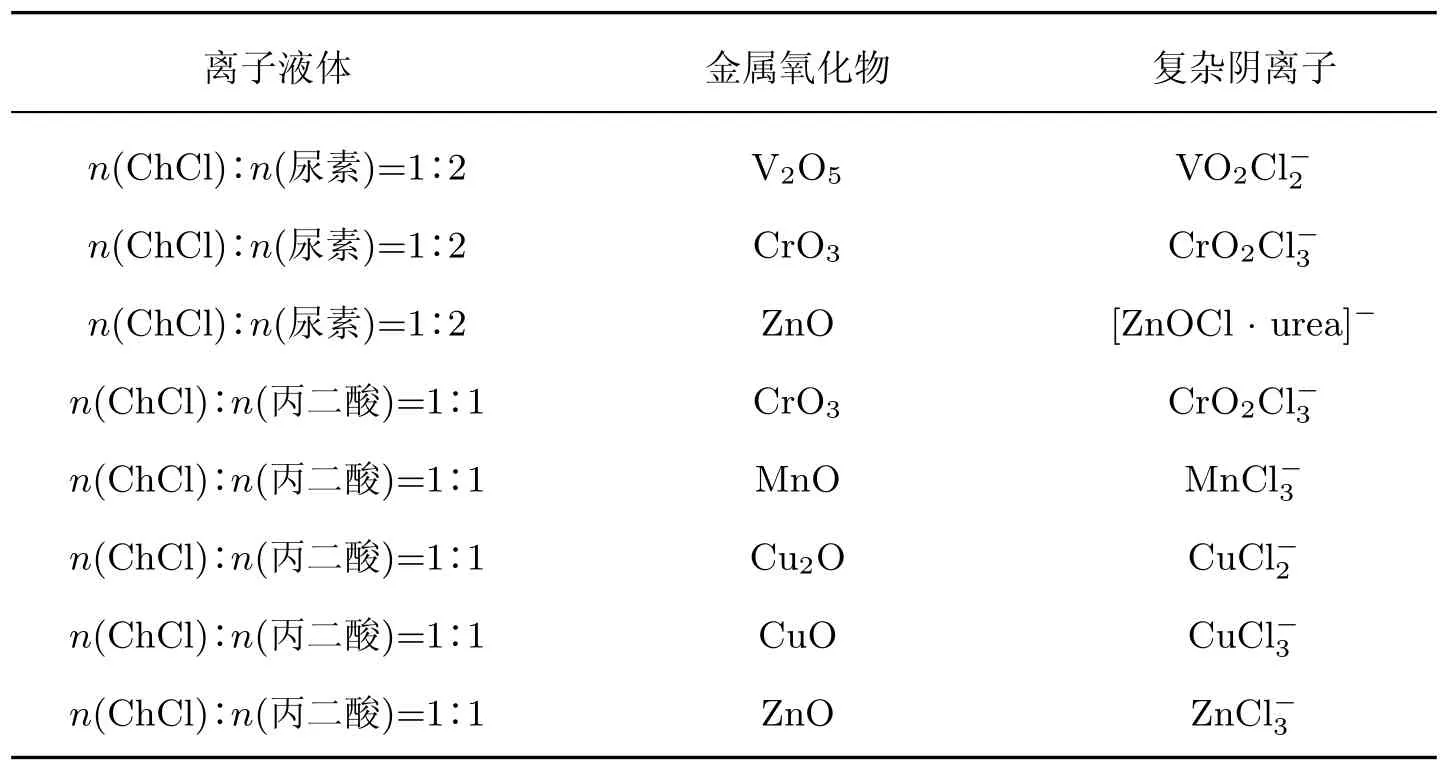
表2 金属氧化物在离子液体中溶解后的复杂阴离子存在形式[19]Table 2 Complex anion forms of metal oxides dissolved in ionic liquids[19]
Nerea 等[20]用对甲苯磺酸一水合物(p-toluenesulfonic acid monohydrate, PTSA) 与氯化胆碱组合形成低共熔溶剂, 测定了MnO、MnO2、Fe2O3、Fe3O4、Co3O4、CuO、ZnO 等多种金属氧化物在不同物质的量比溶剂中的溶解度, 发现ChCl 物质的量分数较高时有利于金属氧化物溶解. 此外, 该研究还比较了金属氧化物在多种ChCl 基低共熔溶剂和3.14 mol/L HCl水溶液的溶解度, 发现MnO2、Fe2O3、Fe3O4和CuO 在n(PTSA)∶n(ChCl)=1∶2 低共熔溶剂中的溶解度大于在HCl 水溶液中的溶解度. 对某些金属氧化物而言, DESs 比HCl 水溶液具有更强的选择性, 这主要是由于所选择的溶剂中氢键受体(hydrogen bond acceptor, HBA)与氢键供体(hydrogen bond donor, HBD) 物质的量比不同(见图3). 综上所述, 离子液体易于制备、易于处理, 为金属及其氧化物的溶解提供了一种无毒且可再生的反应介质, 利用新型离子液体可为湿法冶金中金属氧化物的溶解和提取提供新的可能性.
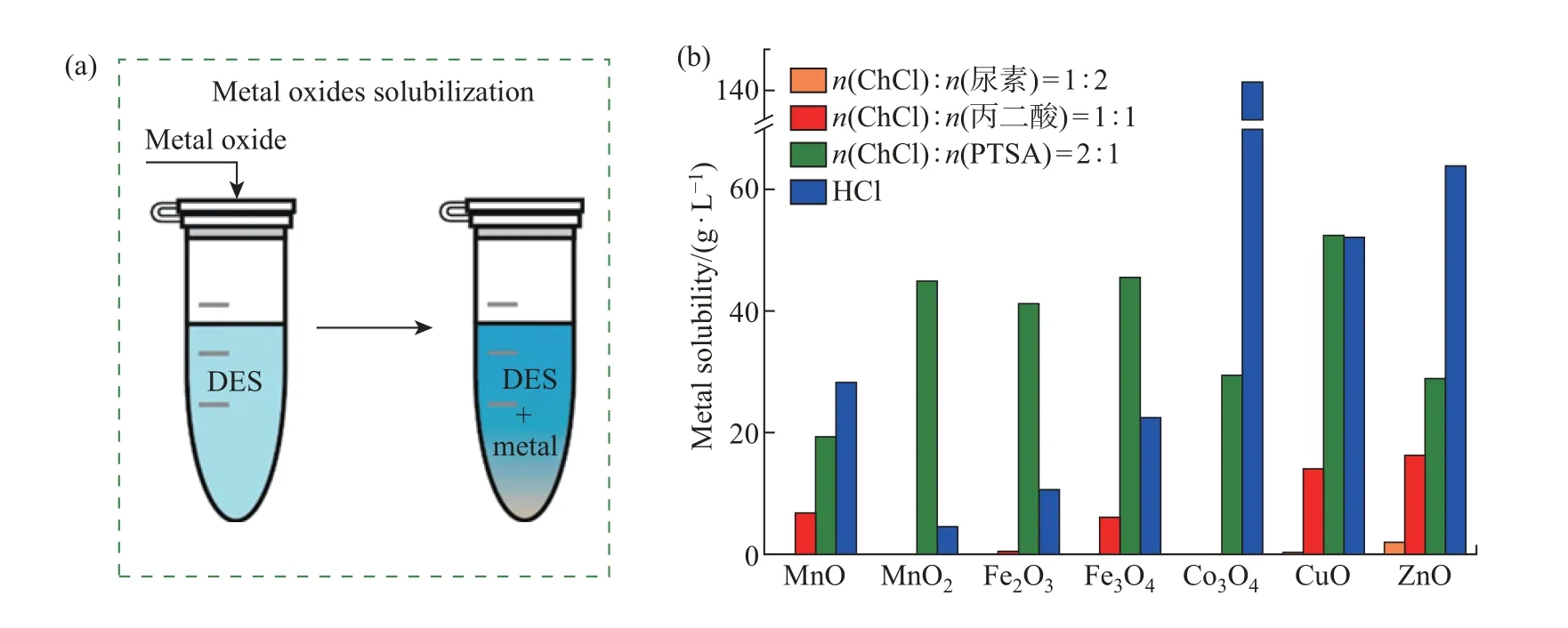
图3 金属氧化物在不同DESs 和HCl 溶液中的溶解[20]Fig.3 Solubility of metal oxides in different DESs and HCl solution[20]
1.2 金属矿物的浸出
湿法冶金处理矿石的第一步是浸出. 离子液体作为浸出剂是一种绿色高效的新方法, 尤其是对于低品位的黄铜矿(CuFeS2)、闪锌矿、黄铁矿等复杂硫化物矿石, 离子液体表现出非常显著的优势. 在大多数情况下, 矿物在离子液体中浸出主要形成氯配合物, 避免了水溶液中产生不溶性沉淀物阻碍进一步反应的情况发生. 虽然目前已经在一系列样品中进行了离子液体浸出试验, 但大多数研究主要集中在黄铜矿和含稀土矿物的浸出. 黄铜矿等硫化矿是湿法冶金中一种常见的矿石, 其浸出过程存在较大难度, 对酸浸具有很大的挑战性. 将离子液体作为传统盐酸浸出剂、高温/高压浸出或生物浸出技术的替代浸出介质来处理矿石, 具有非常好的应用前景. 2004 年Whitehead 等[21]首次报道了离子液体浸出矿石的情况, 采用1-丁基-3-甲基咪唑硫酸氢盐([BMIm]HSO4) 离子液体作为溶剂浸出以黄铜矿/黄铁矿/磁黄铁矿/闪锌矿为主的粉状矿石, 在室温下可选择性提取金(提取率≥85%) 和银(提取率≥60%), 均高于在H2SO4溶液中的提取率. 此外, 在活性炭上选择性地剥离金银后, 离子液体可以循环利用. Jenkin等[22]利用n(ChCl)∶n(EG)=1∶2 的离子液体溶解金矿石(主要由银金矿、黄铁矿、方铅矿和黄铜矿组成), 研究了多种矿物在该溶剂中的溶解行为(见图4), 发现不同矿物的溶解速率不同, 其中银金矿的溶解速率最快, 黄铜矿的溶解速率最慢, 且与目前工业氰化工艺相比, 该工艺浸出速率较快. 2019 年, Anggara 等[23]证明了在低共熔溶剂中可以溶解并直接从天然铜蓝中回收高纯铜, 反应装置示意图如图5 所示. 研究发现, 采用20% (质量分数) 氯化胆碱-草酸和80% (质量分数) 氯化胆碱-乙二醇混合得到的低共熔溶剂从矿石中能获得99% (原子分数) 铜回收率. Hartley 等[24]研究了一系列矿物(白铁矿、黄铁矿、砷黄铁矿和斜方砷铁矿) 在n(ChCl)∶n(EG)=1∶2 低共熔溶剂中的溶解情况(见图6), 发现白铁矿溶解最快, 而含砷矿物溶解较慢, 据此提出了矿物在离子液体中浸出的电化学溶解动力学受砷或硫部分的控制, 而不是简单地将Fe(Ⅱ) 氧化为Fe(Ⅲ). 近年来, 许多学者利用多种离子液体作为介质浸出多类矿物, 并研究了氧化剂的添加对矿石浸出的影响, 这为矿物冶金提供了新的研究思路和方法. Hu等[25]研究了以过氧化氢(H2O2) 为氧化剂, 利用[HMIm]HSO4、[EMIm]HSO4、[BMIm]HSO4和[OMIm]HSO4离子液体在常温下浸出黄铜矿, 结果表明, 以[HMIm]HSO4作为溶剂在最佳条件下铜的浸出率可达98.3%. Abbott 等[26]研究了以碘(I) 作为电催化氧化剂, 利用n(ChCl)∶n(EG)=1∶2 从复杂混合物(Cu/Zn、Ga/As、Au/Ag/硫化矿) 中溶解浸出和选择性回收元素, 发现碘在DES 体系中比在水中具有更大的溶解度, 在保持高氧化还原电位的同时显示出可逆的氧化还原行为.

图4 50 °C 下金矿石与低共熔溶剂反应10 min 前后的反射光图像[22]Fig.4 Reflected light image of gold ore before and after 10 min reaction with deep eutectic solvent at 50 °C[22]
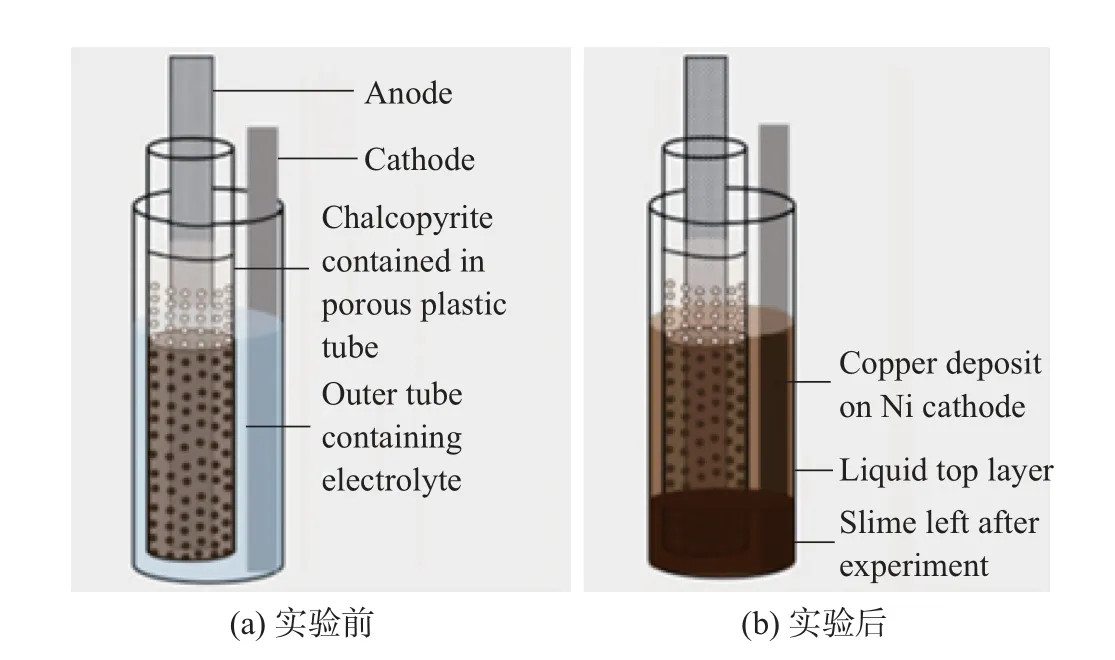
图5 实验中使用的装置设计[23]Fig.5 The device design used in the experiment[23]

图6 4 种矿粉在DES 中24 h 内阳极溶解后的溶液颜色[24]Fig.6 Solution color of four kinds of mineral powder after anodic dissolution in DES within 24 h[24]
传统湿法冶金技术的主要缺点是酸和有机溶剂消耗量大、废水产量大、完全回收稀土的工艺步骤复杂, 这既违背了可持续发展的原则, 也不符合严格的排放要求. 因此, 开发一种可替代的溶剂来回收稀土元素(rare earth element, REE) 是非常重要的. 而离子液体除上述用于黄铜矿、闪锌矿等矿物中有价金属的浸出以外, 还可以用来提取复杂矿物中的稀土元素(见图7)[27], 这为稀土金属的提取提供了一条绿色环保的技术路线. 例如, Davris 等[28]研究了使用带有羧基的功能化离子液体[Hbet]Tf2N 浸出铝土矿渣以实现有价元素的选择性溶解, 结果表明, 提高温度和增长时间可使稀土元素的提取率达到70%~85%. Davris 等[29]还用同种离子液体浸出低品位稀土矿石“R¨odberg” 中的镧(La)、铯(Ce)、钕(Nd) 等稀土元素. 研究表明, [Hbet]Tf2N 及其类似衍生物可溶解一系列金属氧化物和金属氢氧化物, 实现稀土元素的回收, 浸出过程可使轻稀土的回收率达65%~100%, 重稀土的回收率达40%~60%. 此外, 矿石中80%~90% (质量分数) 的钙(Ca) 和锰(Mg) 也会溶解于离子液体, 而铁(Fe)、硅(Si) 和铝氧化物不会溶解, 最终形成富Fe/Si 残留物. 因此, 将浸出后溶解在[Hbet]Tf2N 中的金属用酸性水溶液洗涤分离, 可使离子液体再利用(见图8).
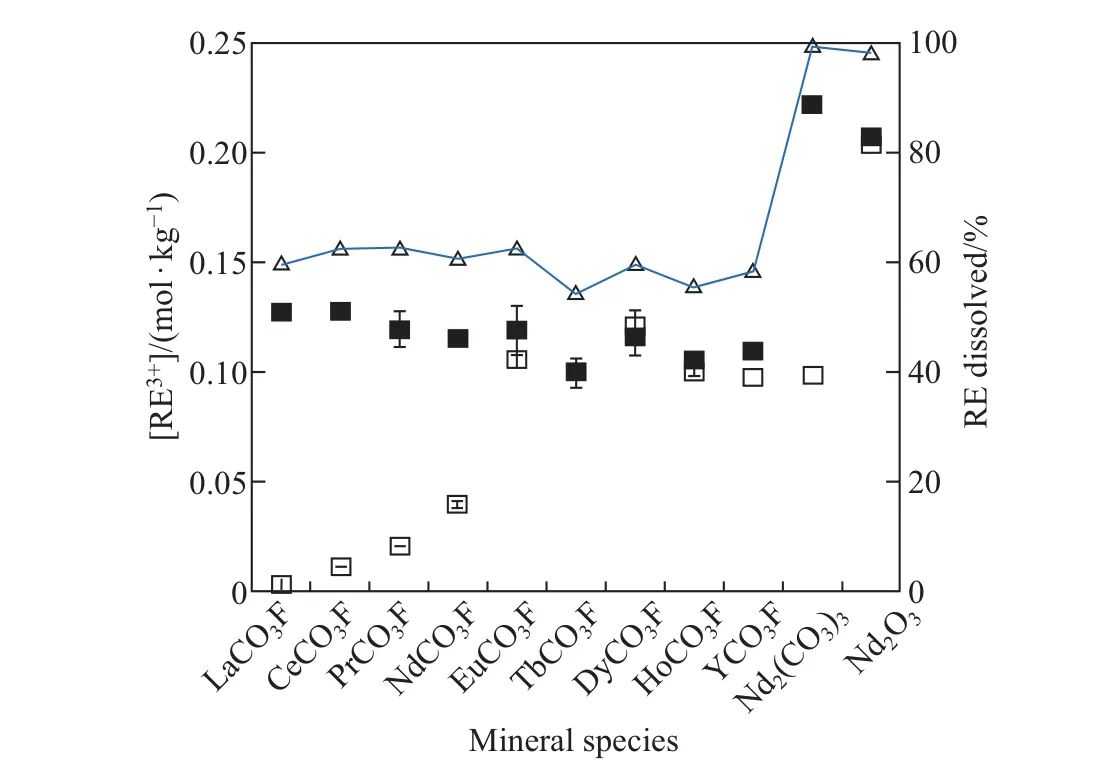
图7 120 °C 和1 000 rad/min 条件下, 在2 mol/kg[DMAH]Tf2N 和[BMIm]Tf2N 中溶解稀土矿物[27]Fig.7 Rare earth minerals are dissolved in 2 mol/kg [DMAH]Tf2N and [BMIm]Tf2N at 120 °C and 1 000 rad/min[27]

图8 盐酸反萃前后的离子液体溶液[29]Fig.8 Ionic liquid solutions before and after hydrochloric acid stripping[29]
从上述研究工作可以看出, 在离子液体中浸出金属矿物能够在较短时间内获得较高的金属浸出率, 尤其对金和银等贵金属还具有较好的选择性. 使用后的离子液体经简单处理之后还可以进行循环使用, 对有价元素的浸出效果几乎不会产生负面影响, 浸出的金属可通过后续电沉积直接提取, 这项技术有可能很好地解决现阶段在提取、分离贵金属中严重污染环境的问题. 由于离子液体蒸气压低, 几乎不会挥发, 可循环使用, 这使得离子液体浸出矿物的方法有望开发成为零排放的绿色湿法冶金新技术.
1.3 电子废弃物的浸出
随着科技的不断发展, 电子废弃物的绿色高效回收利用成为社会普遍关注的问题. 从电子废弃物中回收金属常见的湿法冶金方法可以概括为3 个主要阶段: 原材料预处理、金属离子浸出和分离、产品精炼到纯金属或纯金属化合物. 由于这些金属的溶解性差和难熔性, 其浸出过程通常需要HCl、HNO3或H2SO4等强无机酸, 这会导致严重的环境问题. 近年来, 离子液体作为绿色溶剂为电子废弃物中有价金属的回收利用提供了一条高效、环保的途径. 酸性离子液体如[BMIm]HSO4、[Hbet]Tf2N、[CM-MIm]HSO4、[BSO3HPy]HSO4等, 已被研究用于从废旧电池、废印刷线路板(waste printed circuit board, WPCB) 等电子废弃物中溶解浸出铜、钕、镝和钴等金属. 近年来, 在锂离子电池回收技术中, 使用温和条件和提供高回收效率的工艺越来越受到人们的关注. Rold´an-Ruiz 等[30]采用PTSA-H2O-ChCl 低共熔溶剂回收废弃锂离子电池中的钴(Co) 和锂(Li) 金属, 回收过程不使用任何额外的还原剂, 在浸出温度低至90°C、溶解时间短至15 min 的条件下, Co 的回收率可以达到94%. Chen 等[31]使用离子液体([BSO3HPy]OTf、[BSO3HMIm]OTf、[BSO4HPy]HSO4、[BSO4HMIm]HSO4和[MIm]HSO4)从WPCB 中浸出回收金属铜, 结果表明, 这些离子液体均能成功浸出铜, 且回收率接近100%.Zhang 等[32]以酸性离子液体[CM-MIm]HSO4为浸出试剂, 研究了铜在WPCB 中的浸出行为, 且比较了离子液体法、机械法、火法、生物法和超临界流体法下铜的回收效率、环保性、毒性和反应条件. 实验结果表明, 离子液体浸出反应条件相对温和, 易于实施, 使用离子液体从废电路板中回收铜的最快时间为2.5 h, 其浸出率可达94.3%. 与火法冶金分离相比, 离子液体的消耗相对较低、分离时间更短、效率更高、能耗更低. 因此, 利用离子液体从废印刷线路板中浸出铜是一种更加环保和高效的方法.
综上所述, 离子液体是一种很有前途的绿色浸出介质, 具有对特定金属的高溶解性、高选择性和高回收能力, 能够在低温下较短时间内得到很好的浸出效果, 加入氧化剂还可以进一步提高金属浸出率. 此外, 对于复杂矿物中稀土金属的提取以及电子废弃物的回收利用, 离子液体具有非常大的应用优势. 离子液体不仅稳定性好, 而且浸出后的离子液体经简单处理之后还可以进行循环使用, 浸出的金属可通过其他技术(如电化学技术) 提取出来. 通过离子液体浸出和新提取技术的结合方式可以很好地降低成本、简化工艺流程和减少环境污染. 因此, 利用离子液体浸出矿物的方法有望成为零排放的绿色冶金新技术, 具有非常重要的科学意义和应用前景.
2 电沉积
电沉积是指金属或合金从其化合物的水溶液、有机溶液或熔盐中电化学沉积的过程, 它是金属电解精炼、电镀、电铸等过程的基础, 也是获得金属及合金普遍使用的方法. 由于Li、Na、Mg、Al 等活泼金属的还原电位较负, 难以在水溶液中电沉积出来. 目前, 活泼金属大多采用高温熔盐电解或热还原法制备, 但其工艺流程复杂, 且操作温度高, 对设备腐蚀性大, 能耗很高. 随着科技的不断进步和发展, 人们越来越重视节约资源和保护环境, 绿色环保的电沉积方法成为未来的发展趋势. 许多研究者尝试使用有机溶剂(如芳烃或醚等) 在室温下电沉积活泼金属, 但有机溶剂仍然存在电化学窗口窄、电导率低、挥发性强、易燃烧等缺点, 很大程度上限制了其应用范围[33]. 近些年来, 离子液体的快速发展为电沉积提供了一种更优的途径.离子液体融合了高温熔盐和水溶液的特点, 相较于传统电解液具有更为优越的性能, 是一种新兴的“绿色溶剂”, 能在室温条件下电沉积得到多种金属及其合金, 整个冶金过程可以避免氢气析出、试剂毒性等问题, 对设备腐蚀性小, 且能循环使用, 可真正实现绿色生产. 自从20 世纪50 年代Hurley 等[2]第一次报道了离子液体电沉积铝的相关研究后, 广大学者陆续开展了离子液体中多种金属的电镀和电沉积研究, 并取得了一定进展.
2.1 电沉积制备单金属
随着电沉积技术的不断发展, 离子液体被广泛应用于从金属氯化物等前驱体中直接电化学制备镍(Ni)、Co、铬(Cr)、锌(Zn) 等多种金属. Abbott 等[34]对比研究了水溶液和n(ChCl)∶n(EG)=1∶2 低共熔溶剂下电沉积后的金属Ni 层, 其中离子液体中形成的镍沉积层具有相当低的表面粗糙度, 而水溶液中形成微晶沉积层且表面粗糙无光, 二者的扫描电镜(scanning electron microscope, SEM) 图像如图9 所示. 此外, DES 镀镍层的硬度值比Watts 镍高100 HV 以上, 表明其具有不同于传统镍板的力学性能. Elena 等[35]研究了1-丁基-1-甲基吡啶烷二氰胺([BMP][DCA]) 离子液体中Cr 在Au(111) 和Pt(111) 单晶电极上的电沉积行为, 发现Cr 的沉积过程是不可逆的, 沉积的Cr 钝化层阻碍了Cr 离子进一步还原. Hsu 等[36]发现在离子液体1-乙基-3-甲基咪唑双氰胺([EMI][DCA]) 中电沉积制备纳米结构的Sn 电极材料比在常规水溶液中沉积得到的电极具有更好的储锂性能, 且沉积过电位越高, 锡电极的电化学性能越好(见图10). Shimul 等[37]以无水CdCl2为镉源, 研究了离子液体1-丁基-1-甲基吡咯烷双酰胺([BMP]TFSA) 中Cd 的电沉积过程, 发现CdCl2在含氯离子液体BMPCl/[BMP]TFSA 中形成四氯镉络合物[CdCl4]2-, 25°C 时[CdCl4]2-可以在玻碳(glassy carbon, GC) 电极上电化学还原沉积得到金属Cd.

图9 去离子水和离子液体中电沉积得到的Ni 的SEM 图像[34]Fig.9 SEM images of Ni after electrodeposition in deionized water and ionic liquid[34]

图10 -2.4 V 电压下离子液体镀液中电沉积得到的Sn 电极的SEM 图像[36]Fig.10 SEM image of Sn electrodes electrodeposited at -2.4 V in IL plating solution[36]
离子液体也可用于轻金属、碱金属及稀土金属的电沉积制备. 轻金属在传统水溶液中电沉积会先发生严重析氢的反应故而无法获得, 离子液体以其宽的电化学窗口和良好的热稳定性成为电沉积此类金属的理想电解质, 许多学者对此进行了大量探索. Tang 等[38]用1-乙基-3-甲基咪唑-氯化铝(AlCl3-EMIC) 离子液体在镁合金AZ91D 上电沉积Al 镀层, 发现Al镀层与基体的结合强度很好(高于11 MPa). 目前, 利用离子液体在金属基体上电镀铝膜以提高其耐腐蚀性能的应用非常广泛, 与高温熔盐电沉积铝相比, 该方法优势在于可以在低温进行且得到的铝镀层更为致密(见图11).

图11 IC = -25 mA·cm-2, rC = 0.2 条件下采用双极电流脉冲极化法在镀锌AZ91D 表面电沉积Al的场发射扫描电镜(field emission scanning electron microscope, FE-SEM) 图像[38]Fig.11 FE-SEM image of the Al surface electrodeposited on zincated AZ91D by using the bipolar current pulse polarization method at IC =-25 mA·cm-2, rC =0.2[38]
Pieter 等[39]研究了3 种新型镁基溶剂化离子液体([Mg(G1)3][Tf2N]2、[Mg(G2)2][Tf2N]2和[Mg(G3)2][Tf2N]2) 的物理化学性质, 在80°C 条件下从这些离子液体与四丁基氯化铵(TBACl) 的混合物中进行可逆电沉积并剥离出Mg 金属. 碱金属在离子液体中的电沉积可追溯到20 世纪90 年代, 1992 年Scordilis-Kelley 等[40]利用AlCl3-MEIC 离子液体探究了碱金属(Li、Na、K、Rb 和Cs) 在汞电极上的电化学还原行为, 实现了碱金属的电沉积. 随后越来越多的学者开展了碱金属的电沉积研究. 近年来, Andrew 等[41]在N-丙基-N-甲基吡咯烷双(氟磺酰) 亚胺([Pyr13]FSI) 离子液体中, 用LiFSI、LiTFSI、LiBF4、LiPF6或LiAsF6盐在Pt和Li 电极上电沉积制备出金属Li. 研究发现, 碱金属的电沉积在多种离子液体中均可进行,这为低温获得碱金属提供了良好的可行途径. 同时, 碱金属在离子液体中的沉积/溶出具有很高的可逆性, 使得离子液体作为电解液在二次电池、电容器等领域具有广阔的应用前景. 目前,稀土金属一般采用熔盐电解法合成, 在较低温度下从溶液中沉积稀土金属的尝试较少, 利用离子液体通过电沉积制备稀土金属是一种非常新颖的技术. 例如, Abderrahman 等[42]在室温下利用三氟甲基吡啶([BMPy]OTf) 离子液体电沉积得到了镧系稀土金属镝(Dy), 并研究了三氟甲基磺酸镝(Dy(OTf)3) 配合物在[BMPy]OTf 离子液体中的电化学还原过程, 揭示了溶剂中配位相互作用对离子液体中稀土电沉积过程的影响(见图12). 这一研究使得高效回收稀土金属迈出了非常重要的一步, 实现了在较低温度下高效电沉积获得稀土资源, 提供了一种可替代高温熔盐电解的可持续的绿色电化学方法.
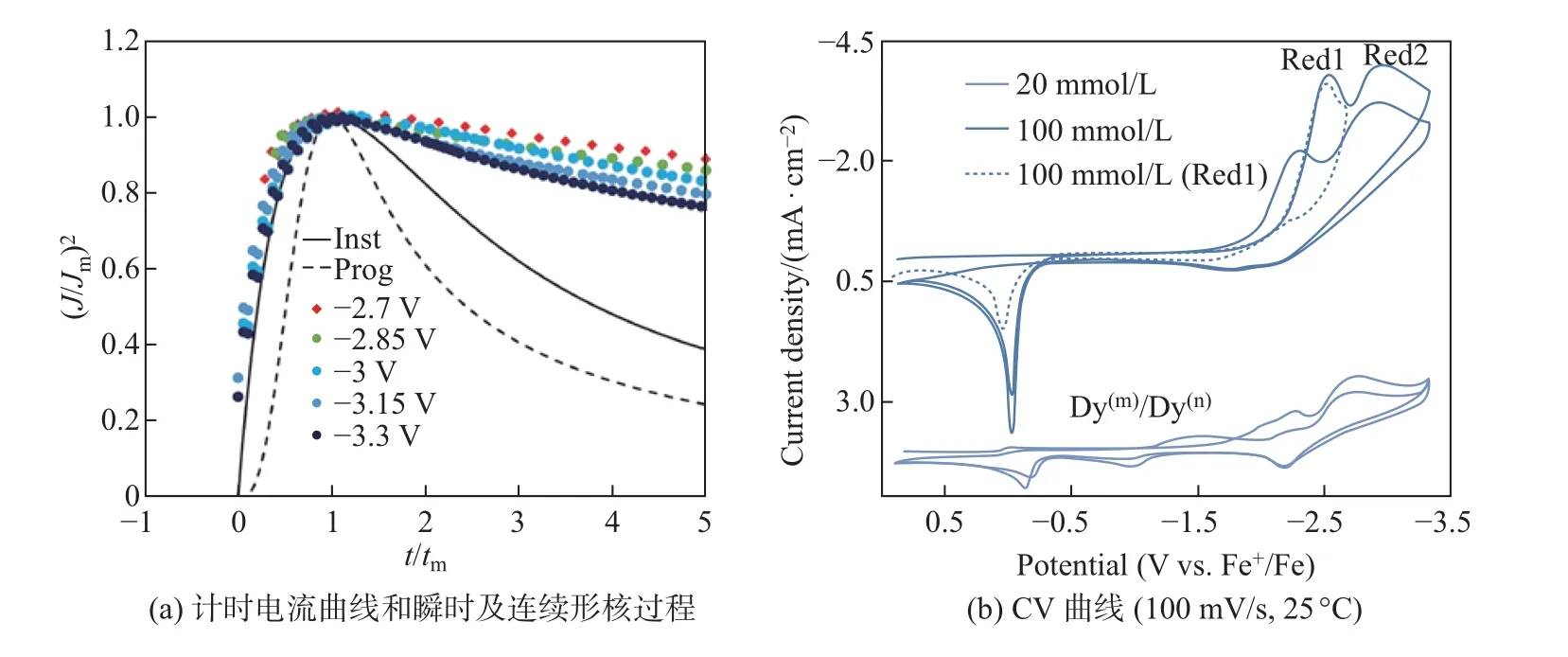
图12 稀土金属镝在[BMPy]OTf 离子液体中的电化学还原过程Fig.12 Electrochemical reduction process of rare earth metal Dy in [BMPy]OTf ionic liquid
2.2 电沉积制备金属合金
除了电沉积纯金属外, 离子液体也被广泛用于二元或多元合金材料的制备. 离子液体具有较宽的电化学稳定窗口, 能够在水溶液中电沉积得到的金属, 往往也能够在离子液体中电沉积得到. 对于用于电沉积活泼金属和稀土金属的电解质, 离子液体比水溶液更具优势, 且电沉积过程中一般不产生副反应. 离子液体中制备合金更易于实现, 由于合金共沉积通常要求2 种金属的沉积电位必须相近或者一致, 沉积电位相差较大的金属进行合金共沉积非常困难, 使用离子液体进行电沉积的优势就得以突显, 部分金属在水系溶剂氧化还原电位差异较大, 而离子液体能够适当调节共沉积金属的氧化还原性质的能力, 使其在水溶液中无法共沉积的金属具有共沉积的可能[8]. 在离子液体中通过调节沉积电位还可以实现对一些合金的晶粒尺寸形貌和成分组成进行调控. Abbott 等[43]用n(ChCl)∶n(EG)=1∶2 和n(ChCl)∶n(尿素)=1∶2 低共熔溶剂在室温条件下成功地电沉积出Cu-Sn 合金, 并对其成分进行了分析(见图13), 研究发现电流密度和原料的物质的量比共同影响了合金中的铜锌比例. Xu 等[44]利用含TiCl4的AlCl3-BMIC 离子液体中在低碳钢基体上电沉积得到均匀致密的Al-Ti 合金镀层, 其耐蚀性优于纯铝镀层和高温熔盐中得到的Al-Ti 合金镀层, 表明离子液体体系合成耐蚀镀层比高温熔盐更具优势. Gao 等[45]在n(ChCl)∶n(EG)=1∶2 低共熔溶剂中采用恒电位电沉积技术在Cu 基底上直接制备出了纳米片状的多孔Ni-Cu 合金薄膜, 与传统的水溶液相比, DES 中得到的Ni-Cu 合金在碱性介质中具有较高的析氢电催化活性. Abhishek 等[46]利用0.1 mol/L 的SbCl3-[Py1,4]TFSI 离子液体在锗电极表面沉积了GexSb1-x镀层进行修饰, 提高了钠离子电池高电流密度下充放电的容量和稳定性(见图14). 这种基于电化学沉积的离子液体表面修饰策略为开发卓越的储能器件开辟了新的范例. 吴青华等[47]采用n(ChCl)∶n(尿素)=1∶2 离子液体制备了Co-Cr 合金, 并将其与水溶液中沉积的Co-Cr 合金及离子液体中沉积的纯Co、纯Cr 电极进行析氢性能测试, 发现离子液体中电沉积Co-Cr 合金具有最高的析氢活性, 钴和铬之间的协同作用最好, 稳定性可达到80%. Lei 等[48]用碳酸丙烯酯改性后的低共熔溶剂n(ChCl)∶n(EG)=1∶2 电沉积合成出了Zn-Ni 合金, 表明该方法可以在低碳钢基体上制备致密且厚的γ相Zn-Ni 合金镀层, 且该镀层具有更高的耐蚀性、更好的力学特性和更高的热稳定性. Wang 等[49]在没有添加剂的情况下利用n(ChCl)∶n(EG)=1∶2 制备了纳米Fe-Cr 合金镀层, 该镀层具有致密且晶粒分明的表面, 平均晶粒尺寸约为1.53 nm, 在近室温下具有优异耐腐蚀性能(见图15). Fashu 等[50]首次在氯化胆碱基离子液体中电沉积成功合成了Zn-Mn-Sn三元合金, 研究表明镀液成分和沉积电位对Zn-Mn-Sn 合金的合金含量、形貌和腐蚀性能有显著影响, 与二元Zn-Mn 和Zn-Sn 镀层特性相对比, Zn-Mn-Sn 合金镀层在腐蚀环境中具有较低的溶解速率和钝化行为. 以上研究说明利用离子液体作为电解质制备金属合金也是可行的,且不同金属在离子液体中的沉积过程的差异也值得进一步探索.

图13 不同电流密度和Cu/Sn 比下Cu-Sn 合金成分沉积率[43]Fig.13 The percentage of Cu-Sn alloy composition deposition at different Cu/Sn ratios with different current densities[43]

图14 0.1 mol/L SbCl3-[Py1,4]TFSI 中在Ge 上沉积Sb 的SEM 图像[46]Fig.14 SEM image of deposited Sb on Ge from 0.1 mol/L SbCl3-[Py1,4]TFSI[46]
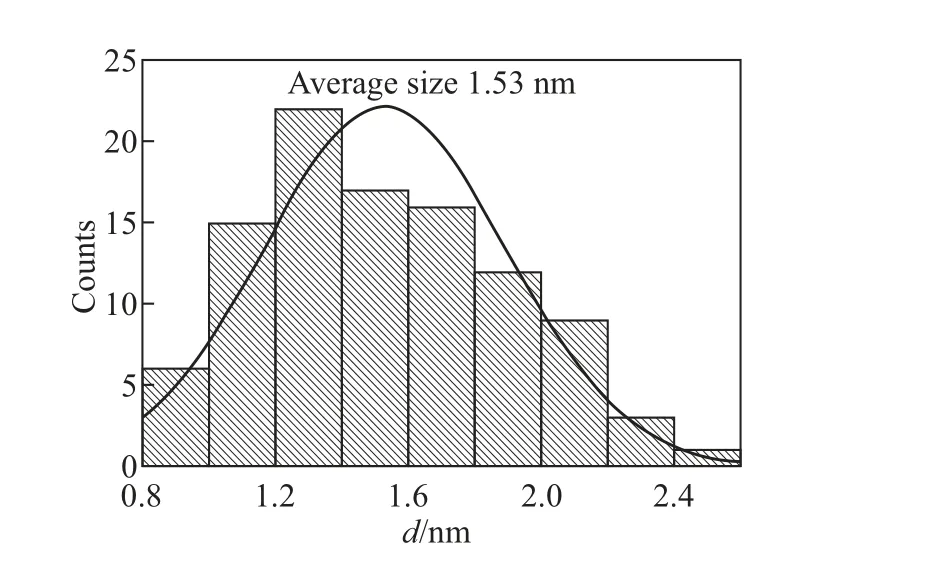
图15 2.8 V、333 K 条件下电沉积1 h 所得Fe-Cr 合金的粒径直方图[49]Fig.15 The particle size histogram of Fe-Cr alloy obtained at 2.8 V and 333 K for 1 h[49]
2.3 金属氧化物的电沉积
近年来, 随着离子液体的发展, 人们尝试将其应用到金属氧化物中, 使难以溶解的金属氧化物也能被直接电沉积进行金属回收. 金属氧化物先在离子液体中溶解形成络合物离子, 后可通过电化学还原反应沉积阴极基底上, 从而得到高纯度的金属及合金, 并且通过控制电化学沉积参数, 还可对产物组成进行精准调控, 得到性能更优的产物. Ru 等[51]采用n(ChCl)∶n(尿素)=1∶2 低共熔溶剂溶解PbO, 在不锈钢基体上电沉积制备亚微米Pb 丝, 并采用循环伏安法、阴极极化法和计时安培法研究了离子液体中Pb(Ⅱ)/Pb(0) 在不锈钢电极上的电化学行为. Ren 等[52]以ZnO 和NiO 为前驱体, 在ChCl-urea-EG 低共熔溶剂中成功电沉积了具有单γ相的Zn-Ni 合金, 实验表明, 该合金的电沉积为反常共沉积型, 这与以金属氯化物为前驱体在类似低共熔溶剂中正常的Zn-Ni 合金共沉积不同. 本课题组也对这一领域进行了探索, 例如Xie 等[53]利用CuO 和ZnO 前驱体在n(ChCl)∶n(尿素)=1∶2 中电沉积得到Zn 和Cu-Zn 合金(见图16), 发现在较低温度和较高正电位条件下可以形成致密的锌镀层, 证明了该方法的可行性. 此外, Xie 等[54]还对比研究了CuO 在n(ChCl)∶n(EG)=1∶2 和n(ChCl)∶n(尿素)=1∶2低共熔溶剂中电沉积Cu 的过程(见图17), 发现电沉积过程主要包含溶解反应和阴阳极电化学还原反应(式(1)~(4)), 且在ChCl-urea 体系中获得的Cu 镀层微观结构更加均匀. 随后Xie 等[55]在n(ChCl)∶n(尿素)=1∶2 中以CuO 和ZnO 为前驱体直接电沉积出了微/纳米结构的Cu-Zn 合金薄膜, 并研究了其电化学反应机理和形核过程(见图18), 发现所制得的铜锌合金膜在质量分数为3% 的NaCl 水溶液中具有较好的耐蚀性. 此外, 不仅可以利用离子液体从金属氧化物前驱体直接电沉积制备金属, 还可以利用离子液体制备出金属氧化物. Eneko等[56]在[Pyr14]TFSI 离子液体中采用一步电沉积成功制备了NiO 薄膜, 被认为是首次明确证明了在离子液体中可以电沉积得到金属氧化物, 且没有金属氢氧化物形成作为中间相. 研究表明, 水溶液阴极电化学沉积金属氧化物(ZnO、Nb2O5等) 是基于还原含氧前驱体(式(5)) 以增加阴极周围的局部pH 值, 通过沉淀诱导金属氧化物沉积(式(6)), 其中金属氢氧根的参与可能会干扰甚至阻碍直接的金属氧化物电沉积, 而在非质子离子液体中的氧还原(式(7)~(8))过程中不形成氢氧根离子, 这为金属氧化物的直接阴极电沉积提供了广泛的可能性(式(9)).Rita 等[57]以4 种离子液体[CnMIM]TFSI(n=2, 4, 8, 10) 作为电解液在FTO 镀膜玻璃衬底上电沉积了致密稳定的ZnO 薄膜, 发现阳离子烷基链越长, 薄膜厚度越厚, 且在离子液体中电沉积的ZnO 薄膜比在水介质中得到的更为坚固(见图19). 由上述研究可知, 利用离子液体提取金属和金属氧化物是一种很便捷有效的方法, 对于利用更多种类的离子液体进行复杂原料电沉积在未来有待拓展研究.
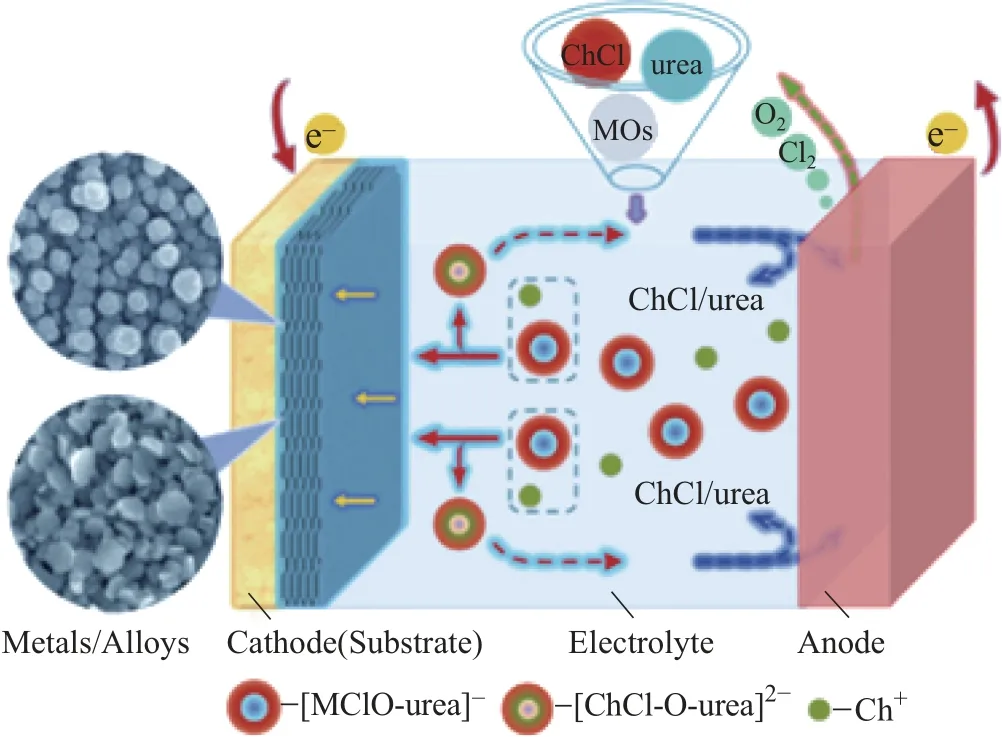
图16 n(ChCl)∶n(尿素)=1∶2 离子液体中由金属氧化物ZnO 和CuO 为前驱体电沉积Zn 和Cu-Zn 合金薄膜的示意图[53]Fig.16 Schematic diagram of electrodeposition of Zn and Cu-Zn alloy films using metal oxides ZnOand CuO as precursors in n(ChCl)∶n(urea)=1∶2 ionic liquid[53]
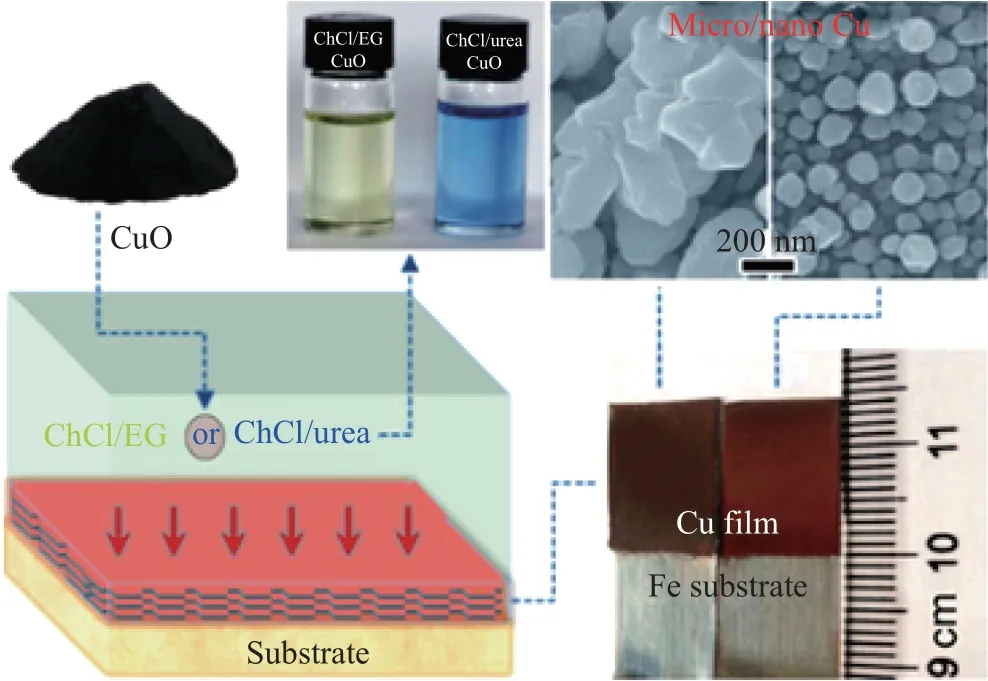
图17 n(ChCl)∶n(EG)=1∶2 或n(ChCl)∶n(尿素)=1∶2 离子液体中以CuO 为前驱体在Fe 基体上可控电沉积Cu 膜的示意图[54]Fig.17 Schematic diagram of controllable electrodeposition of Cu films on Fe substrate with CuO as precursor in n(ChCl)∶n(EG)=1∶2 or n(ChCl)∶n(urea)=1∶2 ionic liquids[54]
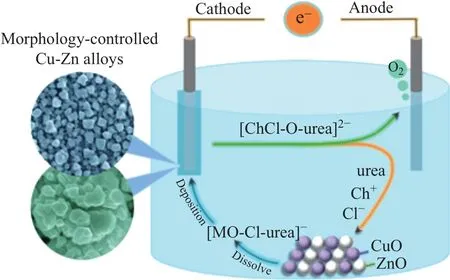
图18 n(ChCl)∶n(urea)=1∶2 离子液体中以CuO 和ZnO 为前驱体电沉积了微/纳米结构的Cu-Zn 合金薄膜示意图[55]Fig.18 Schematic illustration of electrodeposition of micro/nano structured Cu-Zn alloy films in n(ChCl)∶n(urea)=1∶2 ionic liquid using CuO and ZnO as precursors[55]

图19 离子液体[C4MIM]TFSI 和水电解质中电沉积得到的ZnO 薄膜及其在水中浸泡12 h 前后的SEM 图像[57]Fig.19 SEM images of ZnO film electrodeposited in [C4MIM]TFSI ionic liquid and aqueous media,before and after 12 h in water[57]
溶解反应:
阴极反应:
阳极反应:
综上所述, 水溶液的电沉积存在电化学窗口较窄、阴极析氢反应、金属钝化、废水处理等问题, 通过电沉积手段很难从水溶液中得到碱金属和一些稀土金属, 且电沉积过程耗能高, 污染大, 应用受到一定程度的限制. 离子液体具有电化学窗口宽、挥发性小、稳定性好、选择溶解性强、无毒环保、结构和功能可灵活设计等特点, 显示出了水系和非水系的优点, 能够有效避免析氢反应等副反应的影响, 减少氢脆现象, 提高镀层的性能, 是一种很有前景的金属电沉积电解质体系. 由于离子液体电化学窗口和液相范围更宽, 在电沉积时可以避免金属超电势的限制, 得到碱金属以及稀土金属. 此外, 一些以高温熔盐为电解质且需要在较高温度下才能电沉积得到的活泼金属和合金(如Al、Mg、Ti、Al-Mn 合金等), 通过采用离子液体作为电解质在室温条件下就能得到. 作为湿法冶金过程采用的电解质, 离子液体制备金属材料的冶金方法普遍适用于氯化物、氧化物、复杂矿物及电子废弃物等多种原料, 离子液体制备金属材料的冶金方法普遍适用于氯化物、氧化物、复杂矿物及电子废弃物等多种原料, 制备过程更加安全,制备的金属及合金种类不断增加且得到的镀层物理化学性能更为优异. 随着材料科学的不断发展与实际应用的需求, 该制备方法覆盖范围更加广泛, 为材料冶金中金属提取及新能源材料合成等多个领域奠定了研究基础, 在金属材料研究进展中具有重要的应用潜力.
3 结论与展望
离子液体兼具水系和非水系溶剂的特性, 有望成为传统溶剂的良好替代者. 除溶解性好、离子电导率高外, 离子液体还具有独特且优良的理化性质, 如电化学窗口更宽、挥发性小、热稳定性和化学稳定性好、易于再生且功能可设计等, 被称为新型“绿色溶剂”. 本工作介绍了离子液体发展的简要历程, 重点综述了离子液体在湿法冶金浸出提取有价金属以及电沉积制备多种金属材料中的应用现状.
(1) 离子液体对Cu、Zn、Al、Li 等多种金属及其氧化物、复杂矿物及电子废弃物有很强的溶解浸出能力, 特别是对Au、Ag 等贵金属具有较好的选择性, 使资源回收更加方便快捷.目前, 大多数离子液体成本较高, 要达到工业应用仍具有一定的局限性, 但深入研究金属、金属氧化物及复杂矿物在离子液体中的存在形式、相互作用及浸出机制对于材料化冶金的发展具有重要意义.
(2) 离子液体电化学窗口宽且具有适当调节共沉积金属氧化还原性质的能力, 在室温下电沉积出活泼金属、稀土金属以及沉积电位相差大的合金方面具有巨大优势, 为Al、Mg、Ti、Cu、Zn、Ni、Sn、Cr、Dy 等多种金属及其二元或三元合金的电化学沉积提供了新的思路和途径. 目前, 许多金属的电沉积过程从传统离子液体拓展到新一代低共熔溶剂体系, 原料从氯化物拓展到氧化物, 产物从宏观镀层拓展到了微观纳米材料, 在金属防腐、新能源材料与器件制备等方面都展现出优于常规电解质的巨大发展前景.
离子液体在冶金及及其衍生应用的研究探索还处于初期阶段, 机遇与挑战并存, 在这个迅速发展的领域, 还存在很大的突破空间, 需要持续加大基础探索研发力度, 在新型离子液体设计合成、性能调控、机理探索、工艺优化等方面进一步深入, 从而逐步探索实现离子液体在冶金新技术及新材料合成方面的广泛应用.

