胎盘植入剖宫产术中出血量与胎盘血管的MRI 分析
王亚 刘清华 李晔 王强 王忠
胎盘植入是临床最常见的产科重症之一,生产过程或产后发生大出血为其严重并发症,可造成围产期子宫切除,严重者甚至危及母体生命[1,2],因此在产前预测可能的出血量是临床期待的有重要意义的工作。有文献报道产妇的血清学改变与胎盘植入、产后出血相关[3],也有报道认为胎盘植入、前置胎盘是产妇出血极危险因子,并推测是由于胎盘附着处血管丰富,同时邻近子宫平滑肌收缩乏力影响血管闭合所致[4,5]。这说明胎盘植入患者产程和产后出血与胎盘的血管构成存在关系。笔者在临床工作中也观察到胎盘下血管增多、粗大,发生产时大出血几率较高。本文旨在探讨剖宫产术中出血量与胎盘植入及血管征象的关系,为临床预防胎盘植入剖腹产时大出血,以及制定治疗方案提供依据。
1 资料与方法
1.1 一般资料
均为育龄期女性单胎自然妊娠,共109 例,所有患者均经剖宫产手术分娩,其中经剖宫产手术记录和/或病理证实的粘连型植入55 例、植入型54 例,无一例子宫切除,均保全子宫。年龄25~45岁,中位年龄34 岁,孕周28~38 周,中位孕周34周。患者MRI 检查前签署了知情同意书,本研究经医院伦理委员会审查通过[伦审批2021 第(43)号]。回顾性纳入标准:胎龄28 周及以上,临床资料完整,剖宫产手术记录完整,产前胎盘MRI 图像清晰,技术规范。MRI 诊断经过手术记录和/或病理证实。排除标准:MRI 图像质量影响观察,缺乏详细的剖宫产手术记录和/或病理诊断者,产前有糖尿病、高血压和凝血功能异常者、术前行介入球囊封堵术者均不纳入本研究。
1.2 MRI 检查方法
采用GE HDX 3.0 T 磁共振仪,8 通道体部线圈,非增强扫描。孕妇仰卧足先进,膀胱为半充盈状态。分别采集矢状、冠状位T2WI 图像;FIESTA 序列;DWI 横断位与矢状成像。具体扫描序列与参数:1)矢状位和冠状位FSE T2WI 序列:TR/TE 2900 ms/80 ms,层厚6.0 mm,矩阵320×256,翻转角90°,视野34 cm×30 cm。2)FIESTA 序列扫 描参数:TR/TE 3.4 ms/1.5 ms,层厚6.0 mm,矩阵320×256。3)DWI:SE-EPI序列,b 值0、800 s/mm2,TR/TE 4200 ms/66 ms,层厚6.0 mm,矩阵96×130,翻转角90°。
1.3 研究方法
术中出血量及胎盘植入分组术中出血情况按美国妇产科医师学会指南[6]、中国2014 版产后出血指南[7]及临床实际工作分三组,常量组出血量(≤500 mL),中量组(>500~1000 mL),大量组(<1000 mL)。
剖腹产出血计量方法:产妇娩出胎儿后,去除羊水,使用负压瓶收集出血,测量血量。手术单上血迹采用面积估算,纱布血迹采用称重法。将所有出血量相加记录术中出血量。高年资主治妇产科医师记录术中出血量,同时手术副主任医师或主任医师核对并记录术中出血量。手术由3 组产科医生执行,分别为A 组、B 组、C 组,三组医师均为副主任医师及以上资质产科医生,持有医院手术授权同意书,分析各组在术中出血量的差异及一致性。
胎盘植入根据侵入深度分为粘连型(胎盘绒毛浸入到子宫浅表肌层)、植入型(胎盘绒毛植入子宫肌层)、穿透型(绒毛组织穿透整个子宫壁到浆膜层和侵入比邻组织器官者)3 种类型[8],粘连型植入定义为浅植入,植入型与穿透型定义为深植入(本组未将穿透型纳入研究)。
手术及病理记录:剖宫产时胎盘不能自娩,徒手剥离胎盘能剥脱,母体面受损、出血,受损创面深度浅,临床记录为胎盘浅植入或病理记录为粘连型植入;胎盘不能自勉,徒手剥离时不能剥离或不能完全剥离,剥离面粗糙、出血,受损母体创面深,临床记录为胎盘植入或病理为胎盘植入。临床手术第一助手按产科常规记录主任医师术中的胎盘植入部位。
胎盘植入面积测量及血管影像的观察:结合手术证实的植入部位,确定MRI 图像上胎盘植入处,植入处最大垂直径线相乘得到植入面积[9,10](植入最大层面)(图1、2)。观察及计数植入处血管结构,计数血管数目,测量血管最大管径。具体为:观察植入处是否存在圆形、类圆形、曲线型的流空低信号血管结构并计数与测量最大管径。植入处可视异常血管:FSE 序列上表现圆形或卵圆形条状或迂曲的低信号区,从肌层横跨交界面进入胎盘,同时在FIESTA 序列上观察呈明显高信号。血管数目分为:小于等于2 根、大于2 根小于等于5 根,大于5 根;血管最大径分为:≤2 mm和>2 mm(图3~5)。由高年资主治医师记录血管数目及管径,如果有异议,与副主任医师共同协商后确定记录。
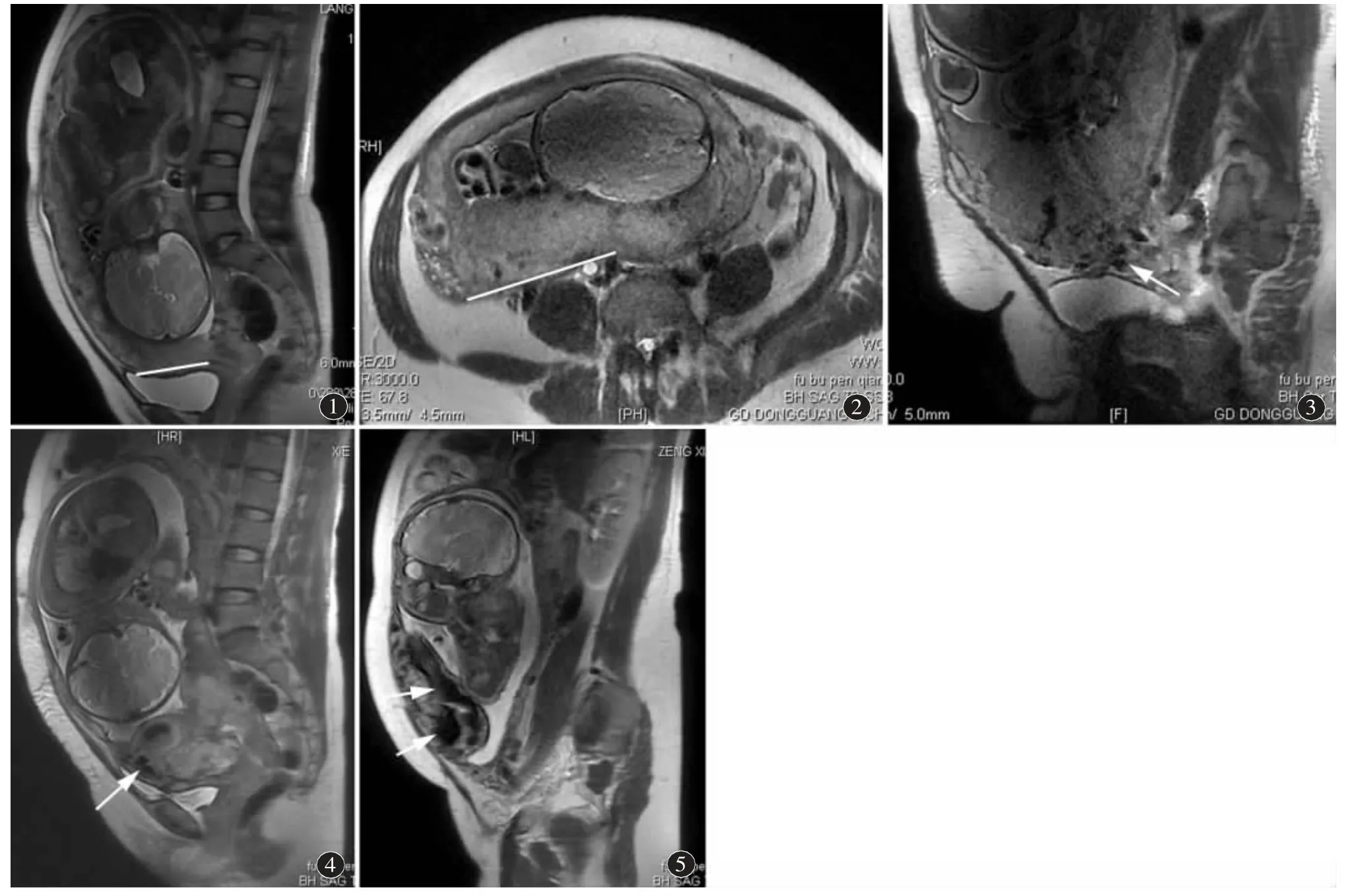
图1 胎盘粘连,女,28 岁,孕33 周,先兆流产。矢状位T2WI,胎盘粘连于子宫前壁下段,白线代表在矢状位上测量植入处最大长度。图2 胎盘粘连,女,31 岁,孕34 周,先兆早产。横断位T2WI,胎盘粘连于子宫后壁下段,白线代表在横断位上测量植入处最大长度。图3 胎盘植入,女38 岁,孕36 周,凶险性前置胎盘不伴出血,妊娠期糖尿病。矢状位T2WI,胎盘植入于子宫前壁下段,植入处血管数目(箭)。图4 胎盘植入,女,38岁,孕35 周,胎动异常数日,羊水过多。矢状位T2WI,胎盘植入子宫前壁下段,植入处圆形流空低信号为血管影像(箭)。图5 胎盘植入,女,35 岁,孕35 周,先兆早产,妊娠合并重度贫血,凶险性前置胎盘伴出血1 d。矢状位T2WI,胎盘内血管迂曲扩张呈低信号改变(箭)。
1.4 数据分析和统计学分析
通过分析组内相关系数(intraclass correlation coefficient,ICC)评估两名妇产科医师对出血量的组内一致性。观察和分析各出血组与植入类型、MRI上的植入面积、可视胎盘植入交界面血管数量、血管最大径,并进行比较。采用Spearman 分析计算出血量与植入类型、MRI 上的植入面积、可视交界面血管数量、血管最大径的相关性。计量资料采用平均数±标准差表示,采用秩和检验进行比较;计数资料采用χ2检验,采用SPSS 22.0 统计学软件,取P<0.05 为差异有统计学意义。
2 结果
2.1 患者剖宫产术后出血量分组
109 例患者剖宫产术中出血量300~4200 mL。对每组内两名产科医师测量出血量进行一致性检验结果显示为0.92,故采用手术副主任医师或主任医师核对并记录术中出血量。常量组(术中出血量≤500 mL)42 例;中量组(出血量>500~1000 mL)28 例;大量组(出血量>1000 mL)39 例。常量组植入处异常血管发生率5 例(5/42)、中量组11例(11/28)、大量组24 例(24/39)。手术由3 组产科医生执行,各组在术中出血量无统计学差异(表1)。

表1 术中手术能力一致性分析
2.2 各组在测量植入面积、植入深度、病变处血管征象比较
植入面积:常量组、中量组、大量组的植入面积依次增大。植入深度:常量组、中量组及大量组的浅植入例数逐渐减少,而深植入例数逐渐增多。以上各组间数据均具有统计学差异(P<0.01)。血管征象:常量组和中量组血管数量明显少于大量组,常量组和中量组血管最大径明显小于大量组(P<0.01)(表2)。

表2 手术出血组手术记录胎盘植入面积、产前MRI 测量面积、术中出血量及植入处界面血管数目和管径
术中出血量与胎盘植入类型、面积、血管数量、血管最大径的Spearman 相关性分析,均具有不同程度的正相关,相关系数分别为0.59、0.89、0.72、0.55(表3)。
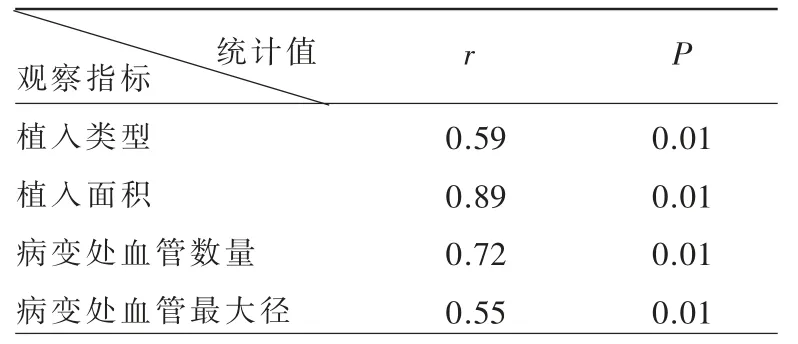
表3 手术出血量与胎盘植入类型、面积、植入界面血管数量、管径的相关性
2.3 出血量与血管数目及血管最大径程度的分析
常量组、中量组及大量组植入处血管数量例数逐渐增多,血管管径逐渐增大。术中出血大量组的血管数目及管径明显高于其他两组(P<0.01),但是出血常量组与中量组无显著性差异(P>0.05)(表4)。
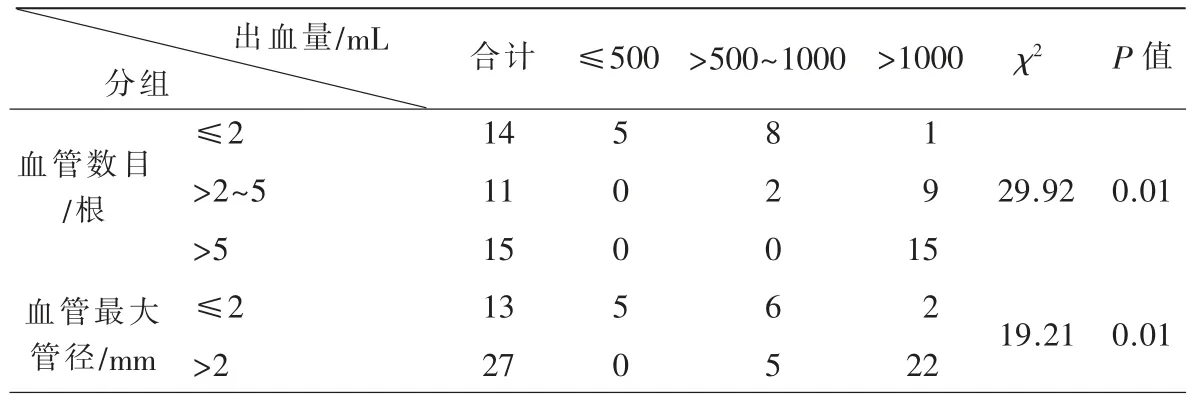
表4 出血量与病变交界面MRI 血管征象的关系
3 讨论
胎盘植入最严重的并发症是生产过程或产后发生大出血,本文旨在探讨剖宫产术中出血量与胎盘植入及血管征象的关系。按出血量分成3 组,每组内2 名产科医师测量出血量进行一致性检验结果为0.92(>0.8)一致性极好,数据较可靠。手术由3 组产科医生执行,各组在术中出血量无统计学差异,说明三组医生手术能力一致。结合手术证实的植入部位,确定MRI 图像上胎盘植入处血管征象。T2WI 能显示母胎结合部的血管影像,表现为圆形、卵圆形条状或迂曲的低信号,胎盘植入的诊断也以T2WI 为主[11,12],以上均得到专业认可。有研究[13]认为子宫浆膜面异常血管会增加产时大出血的风险,故本文选择T2WI 序列为主,观察血管征象和胎盘植入的表现。FIESTA T2WI 作为辅助序列以鉴别血管影像与纤维组织[13,14]。
本文结果显示:相对于常量组及中量组,大量组植入处交界面血管显示率最高,提示胎盘植入处血管显示率可能与大出血存在一定关系,有望产前能根据胎盘植入界面血管征象对术中可能的出血量进行预测,由于病例数较少,仍需要大宗病例验证。
从出血量多少与植入类型征象上看,随着出血量增多,植入面积逐渐增大,植入深度也依次加深;在血管征象方面,出血大量组血管数量、血管管径明显多于其他2 组,各组间数据均具有统计学差异。本结果也提示胎盘植入面积、深度与交界面的血管数目、管径呈正比。文献报道胎盘MRI表现能准确识别胎盘植入深度和广度(面积)[9,15,16],植入型胎盘子宫下段及宫颈血管丰富者大出血概率较大[11,17],植入深度亦是产后大出血重要风险因素[9,10,18],但是未见像本文以出血量为标准,对植入面积及深度进行分析,说明本研究更加深入。从病理及解剖学分析,胎盘植入越深,交界面处螺旋动脉与小静脉增多、扩张,血管壁薄,血流丰富[19,20],同时植入面积增大,造成剥离胎盘时大出血的发生率升高,说明本研究结果与病理改变一致,具有一定临床价值。
在以上结果基础上进一步分析术中出血量与胎盘植入面积、植入类型、交界面可视异常血管数目、血管最大径的相关性,呈不同程度的正相关,相关系数分别为0.89、0.59、0.72、0.55,其中植入面积和植入处血管数目与术中出血量的相关系数均大于0.6,说明上述2 个征象与术中出血量发生的相关性值得术前高度关注。
按血管数目的多少分为3 组,血管最大径分2组,进行分析。常量及中量出血组植入处血管数目少,管径小,出血量多在1000 mL 内。大量出血组植入处血管数目多,血管管径也粗,术中出血量多大于1000 mL,提示血管增多、增宽与交界处血管结构重构发生有关,血管分布弥漫迂曲者,术中存在大出血风险[15,20,21],进一步支持本研究结果。如本组4 例胎盘或子宫内血管异常密集,成血窦样改变,血管管径较宽,均在3.5 mm 以上,患者剖宫产出血量记录均高达4000 mL 以上。3 例深植入处未见流空血管影,术中出血500 mL。2 例浅植入患者术中出血1200 mL,其植入交界面血管数目达3 根,且血管管径均大于2 mm。Bourgioti 等[14]认为胎盘血管直径大于等于2 mm 能够预测胎盘植入患者剖宫产大出血,AUC 为0.80,准确度较高。目前鲜有报道交界面处血管管径与术中出血关系,笔者尝试在矢状位上测量交界面血管最大径,结果显示大量出血组管径多大于2 mm。故本研究提示植入交界面血管征象可能是剖腹产大出血的密切关联的风险因子,据此能对可能的出血量做出预测。
本研究不足之处:1)样本量偏少;2)对于植入面积测量,采用植入最大层面最大径乘积,但实际上植入面积的形状是不规则的;3)未对胎盘内及子宫肌层血管影像进行分析。
综上所述,剖宫产术中出血与植入处血管数目及最大管径、胎盘植入面积、植入类型相关,植入界面的血管征象值得关注。依据胎盘植入的这些表现,术前能预测可能的大出血发生,从而为胎盘植入剖宫产术前、术中预防大出血,以及制定治疗方案提供依据。