犬博卡病毒流行病学调查及基因序列分析
程 群,韩宏晓,郁达义,赵秋华,孙安帮,马福余,陈美松,王海根,孙 清
(上海市闵行区动物疫病预防控制中心,上海 201109)
博卡病毒(Bocavirus,BoV)为无囊膜的线性单链DNA病毒,属于细小病毒亚科(Parvovrinae)。博卡病毒最初于20世纪60年代在犬中发现,随后在人、大猩猩、猪、奶牛、猫等多种哺乳动物中检测到博卡病毒的存在[1-6]。博卡病毒感染后能引起呼吸道和消化道症状,其中消化道的症状以引起人或动物的腹泻为主,博卡病毒的流行与传播对人或其他哺乳动物的健康构成较大的威胁。
犬博卡病毒(Canine bocavirus,CBoV)属于博卡病毒亚家族的成员之一,其基因组大小约为5.4 kb,含有3个开放阅读框,分别编码NS1、NP1和VP1/2蛋白[7]。近年来,中国、德国、美国、意大利、韩国和日本等多个国家相继报道了犬博卡病毒的存在,并发现犬博卡病毒包含CBoV1、CBoV2和CBoV3三种基因型[8-10]。然而,犬博卡病毒的流行情况及遗传演化情况仍不清楚,因此,我们对上海地区犬粪便中的犬博卡病毒感染及病毒的遗传演化情况进行分析,揭示犬博卡病毒在上海犬中的存在情况,为犬博卡病毒的致病性相关研究及潜在的犬博卡病毒传染病的预警和防控提供科学依据和理论参考。
1 材料与方法
1.1 粪便样品采集 自2019年6月至2019年12月,从上海市分别采集犬新鲜粪便206份,粪便样品冻存于-80℃备用。
1.2 主要试剂 PBS磷酸盐缓冲液购自Thermo公司;DNA提取试剂盒TIANamp Virus DNA/RNA Kit购自天根生化科技(北京)有限公司;PCR所用试剂购自TaKaRa公司;胶回收试剂盒Gel Extraction Kit购自OMEGA公司。
1.3 粪便样品处理 取-80℃保存的粪便样品置于冰上融化,按照质量体积比为1∶10的比例加入PBS磷酸盐缓冲液,粪便悬液于涡旋仪剧烈震荡5 min,然后4℃条件下12 000 ×g离心5 min,吸取200 μL上清液置于新的无菌1.5 mL离心管中,以备后续提取核酸使用。
1.4 DNA提取及反转录 粪便样品按照DNA提取试剂盒TIANamp Virus DNA/RNA Kit试剂盒说明书提取病毒DNA,提取出的DNA用60 μL的无RNase水溶解,-20℃保存备用。
1.5 PCR扩增 根据参考文献[8]合成能够特异性扩增CBoV1、CBoV2和CBoV3三种基因型的通用引物,CBoV-F:5'-AARAGRAARCTYTATTTTGC-3',CBoV-R:5'-TGCCAGTCTTGWGGHGARAA-3'。以粪便cDNA样品为模板对CBoV片段进行扩增,扩增CBoV1、CBoV2和CBoV基因片段大小分别为377、386、404 bp。PCR反应体系(50 μL)为:dNTP Mixture(2.5 mmol/L)8 μL,10× LATaqbuffer 5 μL,LATaq0.5 μL,cDNA 1 μL,上、下游引物各1 μL,ddH2O 33.5 μL。PCR反应条件为:94℃预变性3 min;94℃变性30 s,56℃复性30 s,72℃延伸30 s,共32个循环;72℃再延伸10 min。PCR扩增产物经琼脂糖凝胶电泳进行纯化,胶回收产物送生工生物工程(上海)有限公司测序鉴定。
1.6 CBoV全基因扩增 根据NCBI公布的基因序列(GenBank登录号:KY038922)设计特异性扩增引物(表1),扩增阳性样品中CBoV的全基因序列。根据SMART RACE cDNA Amplification Kit试剂盒说明书扩增CBoV基因组的5' RACE和3' RACE。PCR扩增产物经琼脂糖凝胶电泳进行纯化,胶回收产物送生工生物工程(上海)有限公司测序鉴定。
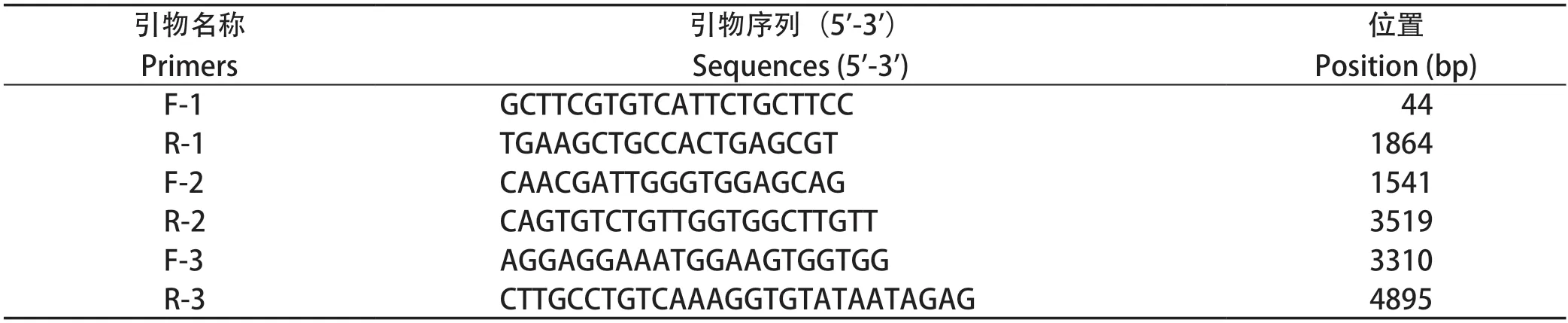
表1 PCR扩增引物Table 1 The primers of the PCR amplification
1.7 序列分析 PCR扩增序列经SeqMan软件组装成完整的CBoV基因组,利用NCBI的ORF Finder(https://www.ncbi.nlm.nih.gov/orffinder/)查找病毒基因组开放阅读框,通过MEGA 5.0软件构建系统进化树。
2 结果与讨论
2.1 CBoV PCR检测 采集的206份粪便处理后经PCR扩增后发现其中有3份样品呈现CBoV阳性,对扩增出的PCR产物进行测序,结果显示扩增出的核酸片段为CBoV序列。对序列进行分析发现,3条序列间的同源性为94.5%~99.9%,由此推测扩增出的3种CBoV属于同一种属。以上结果表明所采集的犬粪便中含有CBoV,CBoV的阳性率约为1.5%。
2.2 CBoV全基因扩增 为了进一步了解CBoV基因组特性,我们根据NCBI公布的基因序列(GenBank登录号:KY038922)设计并合成了3对特异性扩增引物,扩增CBoV的全基因序列。扩增的PCR序列经3次重复验证无误后,利用SeqMan软件组装成完整的CBoV基因组。经分析发现CBoV基因组全长5246 bp,包含249 bp的5' UTR,4853 bp的开放阅读框和144 bp的3' UTR(图1)。CBoV基因组中A+T的含量占50.3%,G+C的含量占49.7%。通过ORF Finder查找CBoV的主要开放阅读框发现,CBoV主要编码三种蛋白:非结构蛋白(non-structural protein,NS)编码基因位于基因组250~2631 bp,核衣壳蛋白(nucleoprotein,NP)编码基因位于基因组2396~2983 bp,病毒衣壳蛋白(VP1/2)编码基因位于基因组2967~5102 bp。
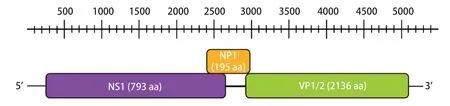
图1 CBoV基因组结构示意图Fig.1 Schematic representation of CBoV genome organization
2.3 CBoV基因进化树分析 为了进一步比较检测出的CBoV与其他种属CBoV的系统发育关系,我们把CBoV基因组全长、NS1基因、NP1基因和VP1基因分别与已报道的其他博卡病毒基因组进行比对分析,结果发现,扩增出的CBoV基因型属于CBoV2(图2)。从系统进化树中可以看出扩增出的CBoV与香港(JQ692591)、韩国(KP281720)和广州(KY038922)等亚洲分离株亲缘关系较近,处于同一个分支,同属于CBoV2。
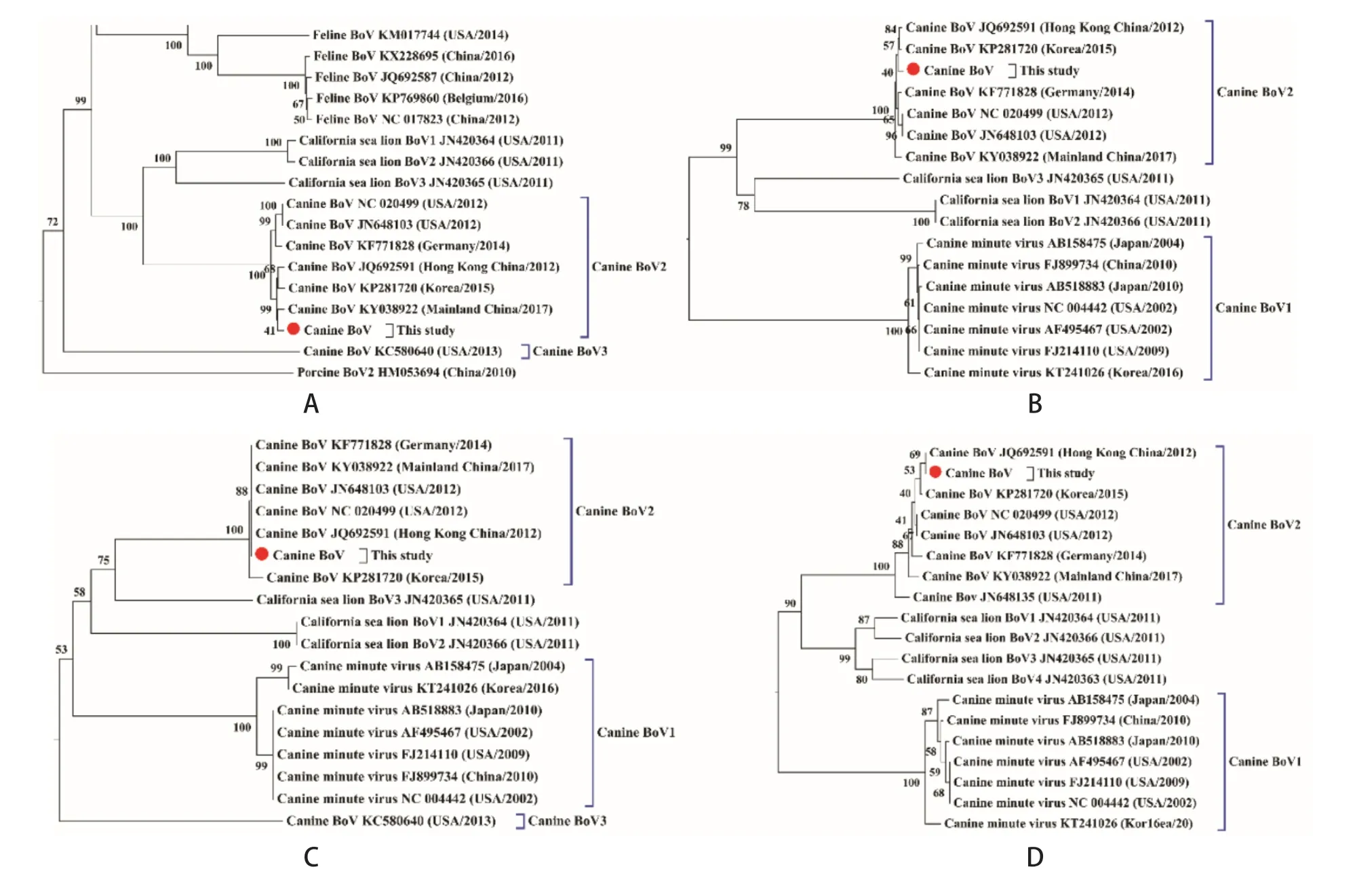
图2 CBoV进化树分析Fig.2 Phylogenetic analysis of CBoV
近年来,新发和再现的病毒性传染病不断出现,严重威胁着人类与动物的健康,逐渐成为全球关注的重要公共卫生问题。尤其是近几年对人类健康造成重大威胁的人类免疫缺陷病毒(Human immunodeficiency virus,HIV)、埃博拉病毒(Zaire Ebola virus,EBOV)、严重急性呼吸综合征(severe acute respiratory syndrome coronavirus-2,SARS-CoV)、中东呼吸综合征病毒(Middle East respiratory syndrome coronavirus,MERS-CoV)以及2019年底暴发的新型冠状病毒SARS-CoV-2等[11-13],这些病毒性传染病的最初宿主都是动物,病毒在其不断的遗传演化过程中逐渐突破物种屏障,通过与人类接触,最终感染人类。犬作为人类的伴侣动物,与人接触比较频繁,其携带的病原体容易对人的健康造成潜在的威胁,因此及时对犬携带病毒进行调查,掌握病毒的遗传变异情况,能够为防控潜在的犬源传染病提供参考。
博卡病毒能够感染人、犬、猫、猪、牛和大猩猩等多种哺乳动物,感染宿主较为广泛。人博卡病毒的感染与呼吸道症状相关,在2016—2018年广州地区急性呼吸道感染(acute respiratory tract infection,ARTIs)儿童中的调查发现,博卡病毒的总检出率为4.24%,而≤2岁患儿感染率为86.98%,表明了博卡病毒是诱发部分婴幼儿喘息性疾病的重要病原体[14]。2014—2015年黑龙江牡丹江地区腹泻犬粪便样品中CBoV的阳性率高达20%,推测犬博卡病毒可能与犬病毒性腹泻相关[15],然而也有学者从健康犬中检测到CBoV的存在[8],因此对于犬博卡病毒的流行情况与治病情况还有待于进一步研究。我们在上海地区犬粪便样本中检测到CBoV,通过基因组比对分析发现检测出的CBoV属于CBoV2,与其他亚洲分离株亲缘关系较近,处于同一个分支。CBoV的流行病学调查和基因组特征分析有助于监测CBoV在犬中的流行情况,评估对于犬健康的潜在威胁,为CBoV的致病性研究及潜在的传染病预警和防控提供科学依据和理论参考。

