葡萄糖酸钙注射液中细菌内毒素的定量检测
朱文娟,李锦妹,翁 嘉,陈文静,林凤屏,李红静,黄永德
(惠州市食品药品检验所,广东 惠州 516003)
葡萄糖酸钙注射液临床主要用于治疗人畜钙缺乏症及过敏性疾病,也可用于镁、氟离子引起的中枢抑制的中毒解救[1-2]。微量动态显色法(microkinetic chromogenic method)是一种新型内毒素定量检测方法,具有灵敏度高、检测范围宽和鲎试剂用量少等优点,近年来受到越来越多的关注[3]。该方法使用酶标仪,通过检测鲎试剂与内毒素反应产生的凝固酶使特定底物释放出的对硝基苯胺(呈色团)的数量,依据呈色团的吸光度和内毒素浓度间对应关系,计算样品中的内毒素含量[4-5]。微量动态显色法不需要凝固蛋白原形成凝胶,直接通过仪器读取结果,实现精准定量;实验操作、数据记录实现了从手工到自动化,保障了实验过程的完整性和结果数据的可溯源性;96孔反应板可同时检测多个浓度样品,省时省力;此外,微量动态显色法灵敏度比凝胶法高,适用于内毒素限值低的样品的检测,能较好地消除实验中的干扰[6]。
本研究采用微量动态显色法对葡萄糖酸钙注射液进行内毒素定量检测,同时与传统的凝胶法进行比较,建立该品的细菌内毒素定量检测方法,实现在线实时记录生产各环节样品内毒素含量的动态变化,有助于及时发现和分析潜在的污染来源,实现无菌药品安全生产的全过程控制,更好地保障临床安全用药。
1 仪器与试药
1.1 仪器
Multiskan ET内毒素检测仪(美国赛默飞);BioProbe生物探针5.2系统(湛江安度斯);MS3漩涡混匀器(美国IKA);TAL-96G试管恒温仪(湛江安度斯)。
1.2 试药
葡萄糖酸钙注射液6批(规格为10 ml:1 g×5支,其中焦作市民康药业有限公司3批,批号:21060403,21060502,22061903;常州兰陵制药有限公司3批,批号:12104090,12104210,12104130);细菌内毒素工作标准品(CSE,中国食品药品检定研究院,批号:150601-201987,规格:80 EU/ml;湛江安度斯生物有限公司,批号:2201260,浓度范围为0.02~2.0 EU/ml);动态显色法鲎试剂(批号:2202230,规格:0.35 ml,定量范围:10~0.01 EU/ml,湛江安度斯生物有限公司);凝胶法鲎试剂(TAL,批号:2204190,规格:0.65 ml/支,灵敏度:0.25 EU/ml,湛江安度斯生物有限公司);细菌内毒素检查用水(BET水,批号:2002260,湛江安度斯生物有限公司)。
2 方法与结果
2.1 细菌内毒素的限值
2020年版《中国药典》第二部品种项下规定:每1 mg葡萄糖酸钙中含内毒素的量应小于0.17 EU[7]。
2.2 微量鲎试剂动态显色法标准曲线可靠性试验及凝胶法鲎试剂灵敏度复核
按使用说明,取3支湛江安度斯细菌内毒素工作标准品,浓度分别为0.02,0.2,2.0 EU/ml,用BET水复溶,并在漩涡混匀器上充分混匀30 s,同时用BET水作为阴性对照管。吸取上述系列浓度细菌内毒素标准溶液各25 μl至96孔反应板中;取动态显色法鲎试剂,加BET水0.35 ml,充分复溶后吸取25 μl,分别加入标准溶液进行反应,每个浓度平行3管。预设吸收度(A)值为0.1,反应时间T为3600 s,温度37 ℃,检测波长405 nm,以T的对数为横坐标,浓度(C)的对数为纵坐标,得出标准曲线和相关系数(r)值。回归方程为lgT=2.8974-0.29133lgC,相关系数│r│=1.0000>0.980,变异系数(CV)值均<10 %,阴性对照反应时间>3600 s,标准曲线可靠性试验各数据符合要求,结果见表1。
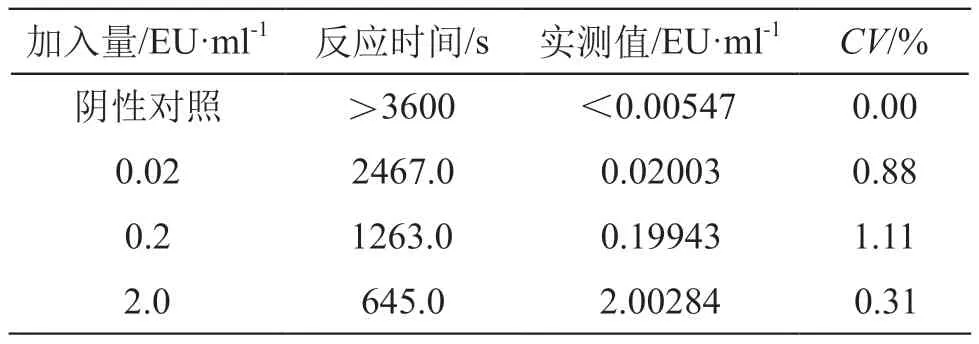
表1 标准曲线的可靠性试验结果(n=3)
凝胶法鲎试剂按2020年版《中国药典》第四部通则1143要求进行灵敏度复核[8],灵敏度为λ,符合规定。
2.3 两种检测法最大有效稀释倍数(MVD)的确定
根据MVD=cL/λ,c为样品溶液浓度(100 mg/ml),L为葡萄糖酸钙注射液细菌内毒素限值(0.17 EU/mg);微量动态显色法中λ为0.02 EU/ml,凝胶法中λ为0.25 EU/ml,计算出MVD在动态显色法中为850,在凝胶法中为68。
2.4 预干扰试验
分别选取2个厂家各1批样品,用BET水依次稀释至25,50,100,200倍(浓度分别为4,2,1,0.5 mg/ml),作为供试品溶液。按使用说明,吸取不同稀释倍数的供试品溶液各700 μl,加入浓度为0.2 EU/ml的CSE干粉中,涡漩混匀30 s使其充分复溶,作为供试品阳性对照溶液。取上述制备的各溶液和标准曲线可靠性试验中的0.02,0.2,2.0 EU/ml系列浓度CSE溶液各25 μl,加入96孔反应板,每个浓度平行2份;取BET水作为阴性对照。最后每孔加入25 μl 动态显色法鲎试剂,用内毒素检测仪测定。不同的稀释倍数,样品回收率均在50 %~200 %范围内,见表2。在稀释25倍时,不同样品的回收率分别为64.46 %和56.13 %,由于56.13 %较低且接近最低限值,故选择50倍稀释的样品进行正式干扰试验。
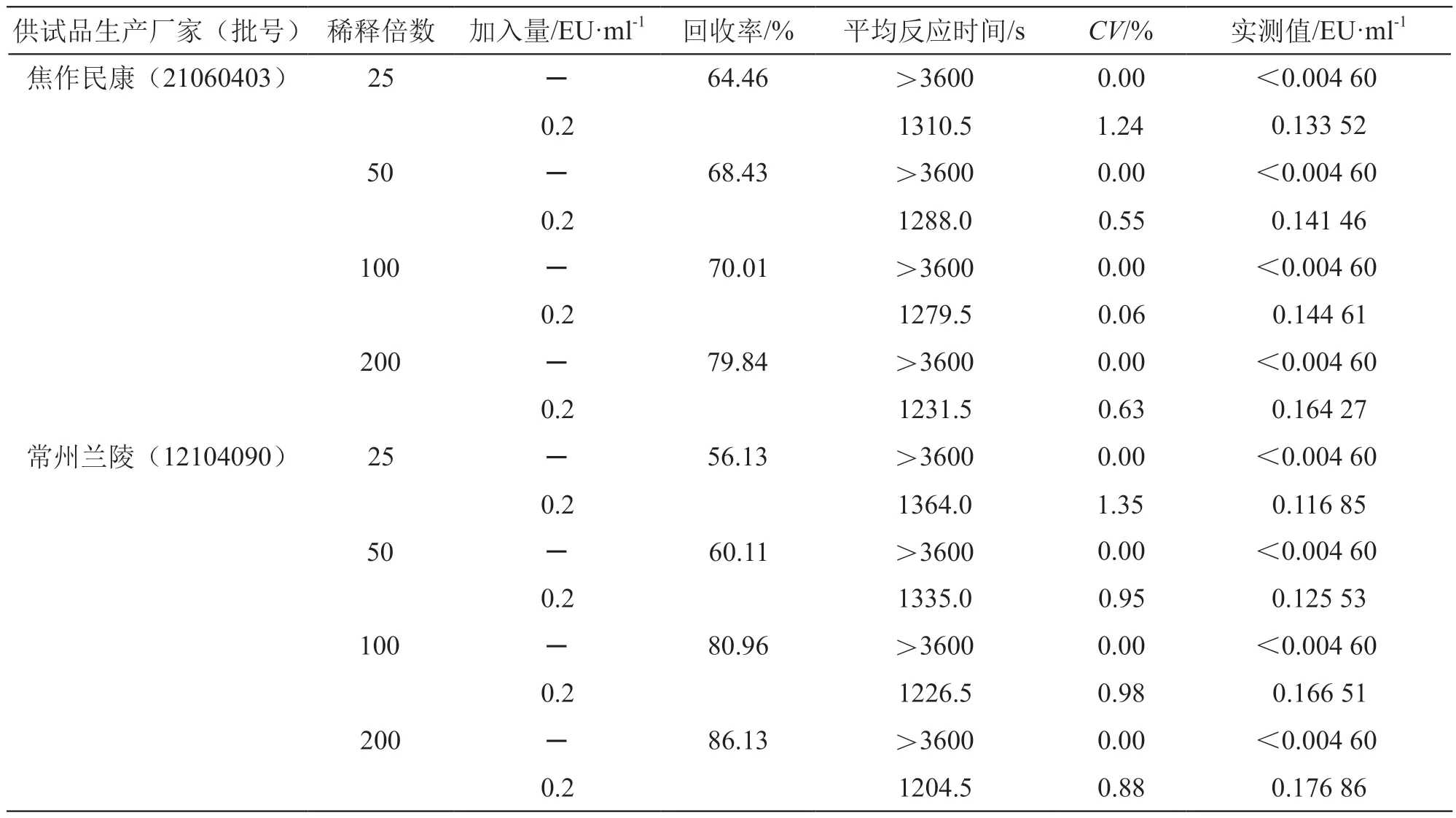
表2 预干扰试验结果(n=2)
2.5 正式干扰试验
为确证葡萄糖酸钙注射液50倍稀释的有效性,进行2个不同厂家各3个批号样品的正式干扰试验。样品稀释50倍后,按预干扰试验的方法进行测定,计算样品内毒素加标回收率和本底内毒素含量。实验的回收率范围在63.49 %~69.55 %,符合药典要求,结果见表3。结果显示,样品在50倍稀释下不存在抑制或增强的干扰作用;各试验组平行管的CV值均<1.5 %;供试品的平均反应时间均>3600 s,实测值均<0.00391 EU/ml。标准曲线的最小浓度为0.02 EU/ml,稀释倍数为50,因此6批葡萄糖酸钙注射原液内毒素结果均<1.000 EU/ml,结果最后换算为<0.01 EU/mg,符合药典规定的<0.17 EU/mg。在本试验条件下,葡萄糖酸钙注射液的最大无干扰稀释倍数为50倍。如果采用的鲎试剂灵敏度不同,需按本试验方法重新确认稀释倍数。
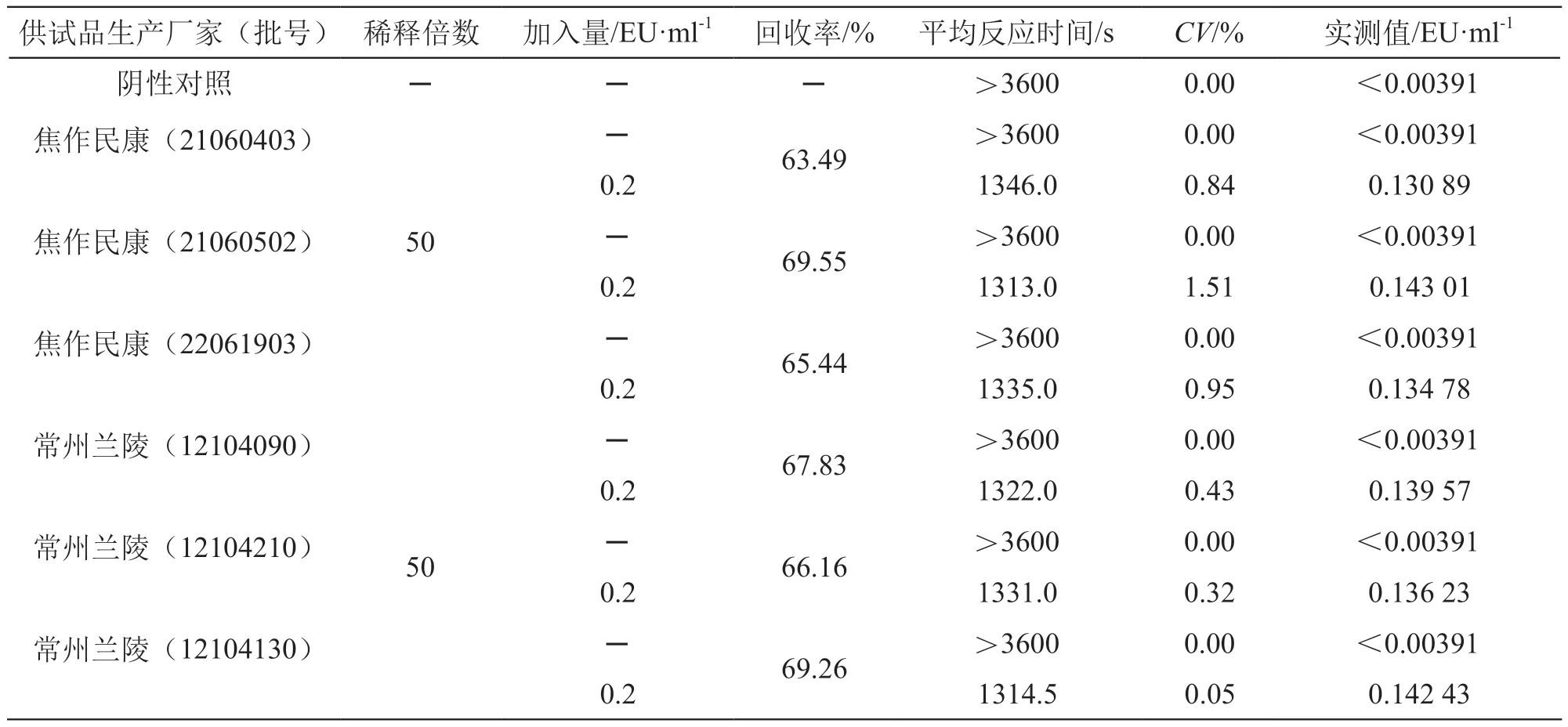
表3 正式干扰试验结果(n=2)
2.6 凝胶法检测
用BET水将样品依次稀释至34,68倍,作为2倍供试品溶液和供试品溶液。用BET水将CSE标准品(80 EU/ml)稀释至1.0,0.5 EU/ml,作为4λ,2λ阳性对照溶液。取等量2倍供试品溶液和4λ阳性对照溶液充分混匀,作为供试品阳性对照溶液(2λ)。吸取0.05 ml鲎试剂溶液至各小试管,分别加入0.05 ml供试品溶液、供试品阳性对照溶液(2λ)、阳性对照溶液(2λ)、阴性对照溶液,每种平行两管,轻摇混匀,放入试管恒温仪中,37 ℃孵育60 min后取出,观察凝胶成像结果。结果均符合规定,详见表4。
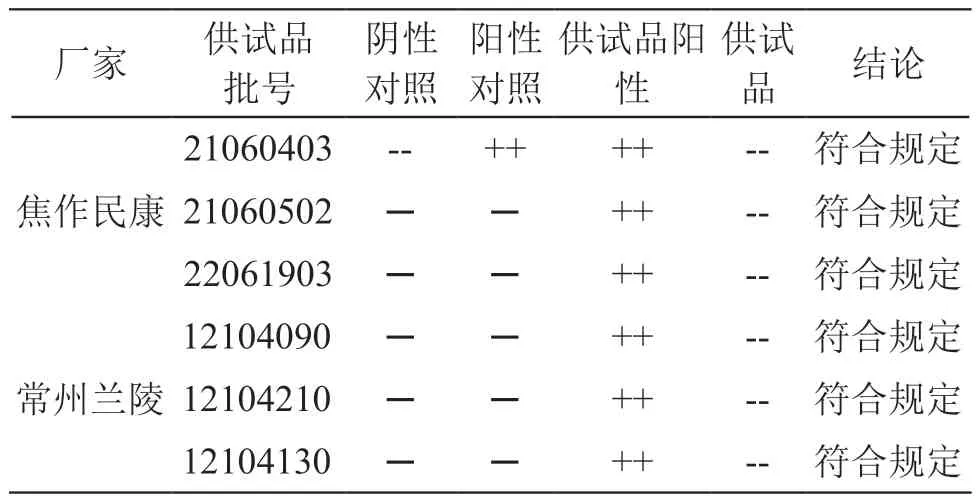
表4 凝胶法检测结果
3 讨论
葡萄糖酸钙注射液细菌内毒素检测结果,微量动态显色法与凝胶法一致,均符合《中国药典》2020年版品种项下规定[7]。相较凝胶法,微量动态显色法有以下优势:一是鲎试剂的使用量仅为凝胶法的1/4,可大大减少对国家二级保护动物鲎资源的需求;二是微量动态显色法的检测限宽,有利于一次性对各种潜在干扰浓度进行筛选,大幅减少鲎试剂的用量,实现大范围快速筛查;三是可实现实时定量检测,灵敏度高[9],检测结果可以精确的数值表示,生产质控人员可了解产品中内毒素含量的变化趋势,有利于注射液生产全过程中的关键风险控制点的安全监控[10-13];四是检测过程和数据处理皆由仪器自动化控制,可实时观察和监控动态反应,避免主观判断影响结果,实现数据的可溯源。除此之外,基于显色基质颜色的变化速率来定量检测内毒素的微量动态显色法,不受凝胶形成和浊度测定的的干扰因素影响[14-15],同时具备动态浊度法和终点法的优点。
葡萄糖酸钙注射液的临床用途和适用人群广泛,内毒素限值较低,更应严控质量,降低风险。本实验建立的微量动态显色法,实现了过程的可控和结果的精确定量,操作简便,可用于大批量检测,能更好地保障临床用药和药品的安全生产。

