胰腺癌术后子宫复发转移一例
李张辉,李格辉,刘烨磊,傅俊辉,陆才德,黄静
宁波大学附属李惠利医院 肝胆胰外科,浙江 宁波 315000
胰腺癌是一种进展迅速的消化道恶性肿瘤,研究表明胰腺癌倾向于转移至腹部淋巴结、肝脏、肺以及腹膜[1],而子宫受累很少报道。源于胰腺癌的子宫转移病例在临床实践中非常有限,我们报道一例胰腺癌子宫转移的诊治情况。
病例
患者女性,66 岁,2015 年5 月18 日因“体检发现胰腺占位20 d”收入宁波大学附属李惠利医院肝胆外科。患者因“肺部感染”于外院就诊,查胸部CT发现胰腺体部占位,于我院住院治疗完善相关检查,血糖苷抗原CA199 0.9 U/mL。腹部B超:胰腺体部见约3.0 cm×2.2 cm囊实性混合回声,边界清。腹部CT:胰腺体部占位(胰腺癌考虑),胰腺尾部萎缩(图1~2)。临床考虑:胰腺恶性肿瘤。2015年5月21日于我院行胰腺体尾部癌根治术,术中见肿块位于胰颈体部,约4.0 cm×3.0 cm,质地硬,术中诊断“胰腺癌”,遂决定行胰腺体尾部癌根治术(胰腺体尾部切除+脾脏切除+周围淋巴结清扫)。
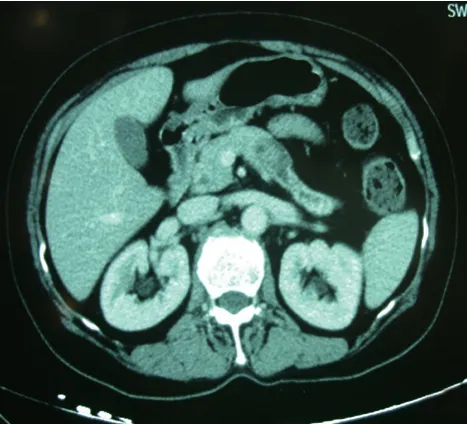
图2 胰腺体部占位伴胰尾部萎缩
手术顺利,胰腺标本见胰体部最大径约3.0 cm肿瘤,质硬(图3)。术后病理:胰腺导管内乳头状黏液性肿瘤伴浸润,浸润成份为导管腺癌,高-中分化,肿块约3.5 cm×2.5 cm×2.0 cm,脉管未见明确侵犯,神经可见侵犯,胰腺肿块旁淋巴结1枚,可见癌转移(图4)。
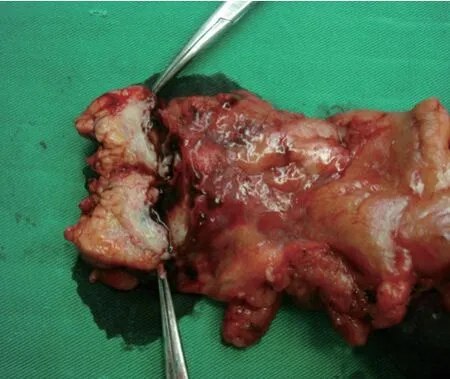
图3 胰腺体尾部癌根治术标本(黑色箭头所指为肿瘤)
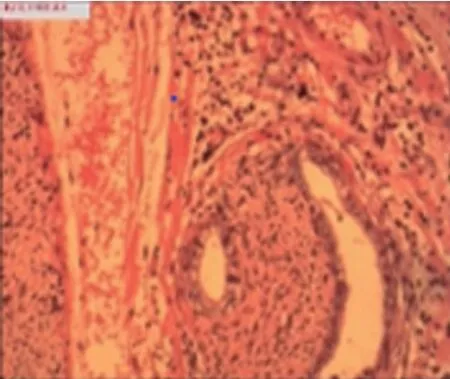
图4 肿瘤组织病理(HE,×10)
术后患者恢复良好,于2015 年5 月29 日出院。后于我院行吉西他滨化疗方案,分别在第1、8、15天静脉滴注1.6 g/m2吉西他滨,28 d为1个疗程,连续治疗4个疗程;后分别于第1、8天静脉滴注1.6 g/m2吉西他滨,21 d为1 个疗程,连续治疗3 个疗程;患者无明显化疗反应。2015年6月30日至2021年4月9日期间,患者每3个月至半年定期于我院门诊复查,血肿瘤指标、腹部CT均未见明显异常。
2021年7月28日患者于宁波市妇女儿童医院体检发现宫腔占位,全麻喉罩下行宫腔镜宫腔占位电切术。术后病理:(宫腔占位)结合组织学形态、临床病史首先考虑胰腺癌子宫转移,后患者转入我院完善相关检查以及PET-CT示:胰腺癌子宫转移,经MDT讨论为宫腔内单发转移,首先考虑为胰腺癌子宫寡转移,遂行全子宫+双侧附件切除术。
手术顺利,术后剖检子宫,宫腔内未见明显赘生物,子宫左侧后壁肌壁间、右侧壁肌壁间见肌瘤样结节,突向浆膜面,切面见不规则螺旋纹(图5)。术后病理:恶性肿瘤,约5.0 cm×3.5 cm×3.0 cm,符合腺癌(结合组织学形态、临床病史,首先倾向考虑胰腺癌转移),累及宫体肌壁全层(未达浆膜层)及左侧卵巢;脉管癌栓(+),神经侵犯(-);左宫旁(-),右宫旁(-)(图6~7)。
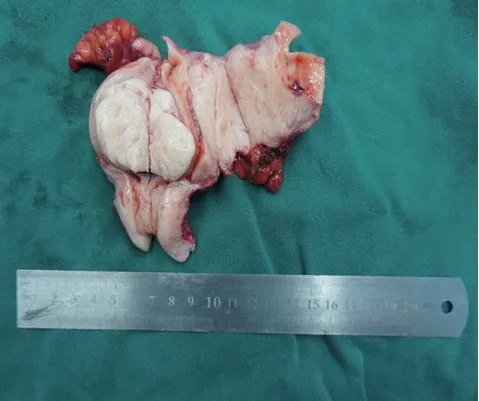
图5 子宫+双侧附件切除术后标本(黑色箭头所指为子宫肌瘤样结节)
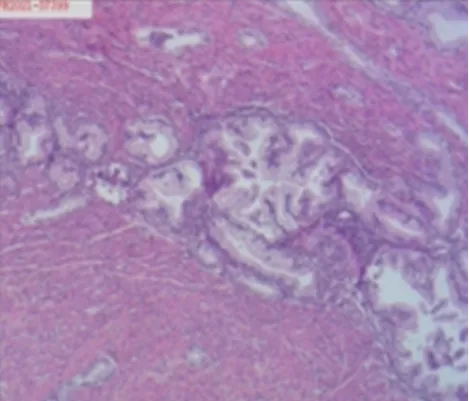
图6 肿瘤细胞排列符合腺癌特征(HE,×10)
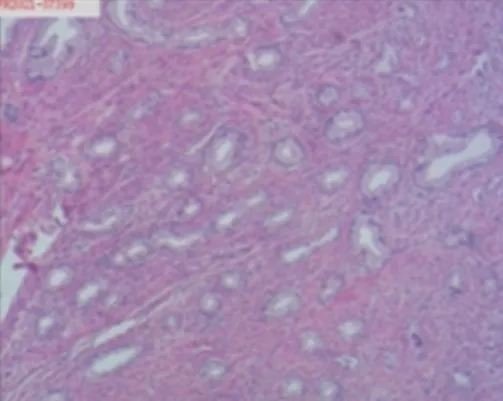
图7 子宫肿瘤组织形态与胰腺癌相似(HE,×10)
术后患者于我院行吉西他滨+白蛋白联合紫杉醇(AG)化疗并联合放射治疗的方案,先分别于第1、8 天静脉滴注吉西他滨1.4 g/m2+白蛋白联合紫杉醇150 mg/m2,20 d为1 个疗程,连续治疗6 个疗程;术后50 d开始联合行95% PTV给5 200 cGy/26f放射治疗;后单独予以静脉滴注白蛋白联合紫杉醇180 mg/m2,20 d为1个疗程,连续治疗5个疗程。患者无明显化疗放疗反应。随访至2023 年5 月30 日,患者未见明显异常。
讨论
胰腺癌是一种发病率和病死率均较高的恶性疾病,根据美国2021年癌症统计年报数据,胰腺癌新发病例数在男性和女性中均列第10位,在恶性肿瘤病死率中列第4位[2]。大多数胰腺癌患者早期没有典型临床表现,由于肿瘤高度侵袭性,诊断时多处于晚期或已有远处转移,5年生存率不足10%。早期诊断困难、手术切除率低,以及术后高复发高转移风险,使得胰腺癌预后极差[3]。手术治疗是唯一可能治愈胰腺癌的手段。手术的目的是实现R0切除,相比于R1切除,R0切除可以大大提高患者生存时间[4]。根据胰腺肿瘤的位置,手术方式包括胰十二指肠切除术、全胰切除术,以及胰体尾切除术等。当前,术后的辅助化疗已被证明对胰腺癌患者有明确的疗效,可以延缓肿瘤复发,提高患者生存率[5]。胰腺癌主要的一线化疗方案包括吉西他滨+白蛋白结合型紫杉醇、FOLFIRINOX等。对于局部晚期胰腺癌患者可以通过放疗实现缓解压迫或以疼痛为目的的对症治疗。对于无法手术或放化疗的胰腺癌患者,中医中药可以增强胰腺癌患者机体免疫力,但具体疗效缺乏客观依据。
胰腺癌术后远处转移较为常见,转移的方式主要包括直接浸润、种植转移、淋巴结转移及血行播散等,单纯表现为子宫转移者少见。转移的形成是一个极其复杂的过程,可以从概念上分为三个主要阶段:(1)癌细胞从原发肿瘤内渗入进入循环;(2)循环肿瘤细胞在血液中的传播和存活;(3)远处部位播散细胞的存活和定植[6]。在胰腺癌中,肝脏是最常见的转移部位(占60%以上),其次是肺和腹膜转移(约30%),骨和肾上腺继发性肿瘤约占10%[1]。既往研究表明,胰腺癌术后复发的主要因素包括淋巴结转移、病理分期、肿瘤分化程度等病理学特征[7]。监测术后CA199水平有助于在得到临床或影像学证据之前更早地监测胰腺癌复发的倾向。Li等[8]研究认为,在大多数胰腺癌患者中,CA199 升高可先于影像学检查证实的复发,肿瘤标志物引导的挽救治疗可以显着延长胰腺癌切除术后受监测患者的无瘤生存期和总生存期。在本病例报道中,患者术前术后的CA199水平均在正常范围内,影像学检查也未提示肿瘤复发迹象,第一次术后无瘤生存时间6年。患者第一次术后病理提示神经侵犯以及淋巴结转移,可能的转移方式为侵犯淋巴结入淋巴管再经胸导管入血转移至子宫,进而出现子宫转移。胰腺癌术后单发子宫转移曾有病例报道[9],在该报道中,患者是术后2 年子宫单发转移。子宫转移是否是肿瘤转移的一种特殊状态,或多发转移的早期表现,值得讨论,需要引起重视。本病例报道中,患者二次术后无瘤生存时间2 年以上,各项化验及检查结果均未提示有肿瘤复发转移迹象,说明根治性手术是其复发转移后的治疗重要手段之一。