中印药品专利标准、许可及侵权救济比较研究
李昱良 代水平
《我不是药神》这部电影曾引发社会的广泛关注,其中中印两国在涉及药品专利方面的法律制度存在差别,甚至对同一种专利药品产生截然不同的法律效果。就此,本文拟对其中反映中印两国药品专利的标准、许可及侵权规制问题进行对比分析,以期能明晰中印两国药品专利法律制度的差异,从而更加理性化地了解印度仿制药产业发达背后的制度逻辑,以供我国涉及药品专利的相关立法参考。
一、中印药品专利标准之比较及其相关问题分析
事实上,在《我不是药神》这部电影中,因为情节需要所塑造的制药公司,存在利用“专利常青”来获得市场垄断地位的嫌疑。所谓“专利常青”,是指由原研药厂商申请的新专利(通常是一些药物改进型专利)仅对已有药物作出较小的修改,以期延长其药物产品的专利期来寻求垄断地位,并获取超额经济利益的现象。[1]但是常青专利通常并没有任何治疗优势。因此,遏制高价专利药问题首先应当关注的就是对改进型药品专利的授予标准,它是影响专利药物可及性的一个重要因素。
(一)改进型药品专利的授予标准比较
我国对药品及其生产方法的保护开始于1992年,主要参考AGREEMENT ON TRADE-RELATED ASPECTS OF INTELLECTUAL PROPERTY RIGHTS(以下简作《TRIPS 协议》)第二十七条的相关规定,①即:被授予专利的发明创造应该具有新颖性、涉及发明性的步骤,并可进行工业应用。我国将“发明性步骤”定义为创造性,我国《专利审查指南(2020)》对“创造性”进一步解释,指只要产生的技术效果“预料不到”即具备“创造性”。②同时,该指南对化合物(涉及药物制品等)的创造性又进一步细化,即:与已知化合物在结构上接近的化合物,必须对其某一已知效果有改进或提高,并且这种改进或者提高必须是“实质性的”才可具有创造性。③然而,这些对“创造性”的解释仍然无法满足实践操作的需求,例如,如何判断“预料不到的效果”?究竟是指疗效上的?还是物理性质?抑或化学性质上?缺乏统一的标准,进而引发学界争议,如有部分学者就认为,只要产生物理或者化学性质上的不同就具备可专利性[2]。由于标准缺乏统一认证,导致我国对改进发明型药品专利审查处于比较宽松的状态。
印度直至2005 年才引入对药物制品的专利保护,其对改进型药品发明授予专利规定了严苛的法定条件。根据《印度专利法》第三条之规定,仅发现已有物质的新形式,而该新形式并没有增强其已知效果,不可专利;并进一步对“已知物质”进行解释,即:已知物质的盐、脂类、醚类、异构体、混合物以及其他衍生物等应视为相同物质,除非它产生了特别明显的功效④。《印度专利审查指南》对化学物质的“可专利性”又进一步解释,即已知物质的新形式;对其已知功效未增强的,不可专利,同时明确指出,药物的“功效”指的是“疗效”。[3]可见,对于药物这类化学制品而言,如果没有“疗效”上的增强,印度是不予专利的,而不论其是否产生“预料不到的效果”。事实上,《我不是药神》这部电影中所涉及的抗癌药“格列卫”,在2005年《印度专利法》修正案公布之后,印度专利管理部门就以“已有药物的新品型在未增强其已知效果的情况下不可专利”的理由,驳回了诺华公司的专利申请;而其拒绝授予改进型药品专利的做法直接导致了诺华公司与印度专利部门旷日持久的诉讼,直至2013 年,印度最高法院才作出了驳回诺华公司诉讼请求的最终判决。可见,印度立法排除了围绕基础专利产生的衍生物的可专利性,对未明显提升药物治疗效果的改进型药品不授予专利。
(二)改进型药品专利相关问题的分析
由于中印两国对改进型药品专利的授予条件具有不同的规定,使得两国药品生产企业在改进型药品研发投入上存在巨大差异:根据我国各中医药企业2022年三季报的数据,我国国内研发投入排名前五的中医药企业,分别为白云山(0.98亿美元)、天士力(0.87亿美元)、以岭药业(0.81亿美元)、康缘药业(0.64亿美元)、华润三九(0.52亿美元),其研发投入占营业收入比例分别为:白云山(1.21%)、天士力(9.69%)、以岭药业(6.94%)、康缘药业(13.99%)、华润三九(2.91%)。综合计算,2022 年前三季度我国研发投入排名前五的中医药企业平均投入为7600万美元,平均研发投入比例为6.95%。反观印度排名前五的医药巨头研发投入情况,2021年太阳制药(3亿美元)、Aurobindo(2.12亿美元)、瑞迪博士(2.35亿美元)、鲁宾(1.54 亿美元)和西普拉(1.27 亿美元),平均值为2.06 亿美元;其研发投资占营收的比例分别为太阳制药(5.6%)、Aurobindo(6.7%)、瑞迪博士(8.1%)、鲁宾(6.9%)和西普拉(4.3%),平均值为6.32%。[4]虽然本文受限于境外数据展示的滞后性,但从印度2021年数据,仍然可以明显看出,印度的大型制药公司在药品研发投入总额方面远超我国相关的投入。
综上分析可以看出,印度对于改进型药品授予专利的标准明显高于我国相关标准,而这种对改进型专利设置高标准准入门槛的做法,在一定程度上保护了印度制药业,避免国际医药巨头通过专利常青和技术优势对其本土医药产业的冲击和打压,但增加了其本土医药企业的技术创新压力;大型医药企业欲通过专利保护获得技术优势,则需要进行高额的研发投入来进行原始创新,如此操作,带动了整个行业的技术水平,为印度仿制药市场的蓬勃发展提供了条件。反观我国,因为对改进发明型药品专利审查较为宽松,国内医药企业往往缺乏原始创新压力,以致近年来申报和上市的具有中国原创意义的专利新药,很多其实还是从已有药物有效成分提取而来,或是根据有效成分结构优化合成的思路而“研发”所得[5],其技术创新程度和水平都有待加强;且医药企业如此这般地不需要进行原始创新就可以获得专利保护,导致一些大型医药企业的研发投入长期处于较低水平,例如国内知名药企云南白药2022 年三季报公布的研发投入,就仅有3000 万美元,再如华北制药、山东新华等老牌药企很少有研发的项目,不少制药企业甚至没有设立研发部门[6]可见,改进型专利准入门槛低,是我国药品专利质量提升速度慢的主要原因之一。
二、中印药品专利许可制度对比及相关问题的剖析
针对《我不是药神》这部电影里所反映的专利药品售价过高的问题,还可以通过专利强制许可制度对其进行规制,即:相关的单位或者个人通过向专利主管部门申请药品专利的强制许可,可以不经过药品专利权人的许可而实施其专利,从而有效降低专利药品的价格。因此,专利的强制许可制度也是抑制“高价专利药”、维护公共健康利益的有效措施。
(一)药品专利强制许可制度对比
我国有关专利强制许可的条件和申请主体,集中规定在《专利法》第五十三至五十六条中;申请强制许可的事由则主要分为专利未实施或未充分实施、为消除垄断的可能、为实施“从属性”专利、国家出现紧急状态或为了公共利益这四类。根据我国《专利法》第五十三条的规定,对于单位或者个人,必须具备“实施条件”时才可申请强制许可。
印度的《专利法》对强制许可的申请条件,主要规定如下:一是该发明不能满足公众合理的需求;二是该专利产品未能以合理价格向公众销售;三是该发明专利没有在印度域内实施。⑤对于其“合理需求”“合理价格”以及本土实施的定义,印度专利管理部门有较大裁量权,这一点,可以从“2012年印度对拜耳公司的抗癌药索拉非尼(多吉美)作出强制许可的案例”管窥一斑:一是对于“法定条件一的合理需求”,印度专利部门是根据由世界卫生组织(WHO)公布的癌症患者的统计数据和拜耳公司的索拉非尼销售数据进行比对,从而作出“未满足合理需求”的判断;二是对于“法定条件二的合理价格”,印度专利部门认为必须以消费者为主要参考对象而非以药物研发成本为参考;对于“法定条件三规定的没有在印度域内实施”,拜耳公司所主张的“实施行为包括生产、销售和进口”的观点被印度专利部门驳回,并认为必须是“在本国制造”才满足条件。[7]此外,在印度,强制许可的申请主体可以是“任何利益相关人”。
(二)药品专利强制许可之相关问题的剖析
通过上述比较,不难看出中印两国在强制许可的条件方面存在很大的差异性——我们国家所规定的强制许可条件比印度的类型多,但是可操作性不强,基本上是照搬《TRIPS协议》的内容,主要体现在两个方面:一是“国家出现紧急状况”和“为了公共利益”的具体情形,缺乏细化规定;二是申请主体要求具备“实施条件”,进而将一般申请主体(例如普通患者)排除在外。相比之下,《印度专利法》将强制许可的申请事由规定为“未满足公共需求”“未以合理价格销售”“未在本土实施”,并赋予某些行政管理部门对这些条件判断的自由裁量权,更有利于强制许可制度的实施与运用;同时,印度立法将强制许可申请主体规定为“任何利益相关人”,这种规定更符合强制许可维护公共利益的内在属性。
三、中印药品专利侵权救济模式之比较分析
从《我不是药神》这部电影里,我们还可以看到,中印两国行政机关对药品专利侵权所秉持的态度迥然不同。事实上,两国涉及药品专利侵权救济的法律制度的确存在较大差异。药品专利侵权救济模式的不同,一定程度上也影响了两国仿制药市场的发展。
(一)药品专利侵权救济模式之差异性分析
根据我国《专利法》和《刑法》的相关规定,针对专利侵权的救济有民事责任、行政责任以及刑事责任。其中,关于专利侵权民事责任主要规定了一般赔偿数额和惩罚性赔偿数额的确定方式,前者按照权利人因被侵权所受到的实际损失或者侵权人因侵权所获得的利益确定,权利人的损失或者侵权人获得的利益难以确定的,参照该专利许可使用费的倍数合理确定⑥;后者规定对故意侵犯专利权,情节严重的,可以在按照上述方法确定数额的一倍以上五倍以下确定赔偿数额,权利人的损失、侵权人获得的利益和专利许可使用费均难以确定的,人民法院可以根据专利权的类型、侵权行为的性质和情节等因素,确定给予三万元以上五百万元以下的赔偿。
此外,我国《专利法》第七十七条还规定了专利侵权赔偿的豁免事由:一是侵权对象是未经专利权人许可而制造并售出的专利侵权产品;二是侵权人的行为限于使用、许诺销售和销售三种实施行为;三是能证明该产品合法来源。只有同时满足上述三个条件,才会免去专利侵权人的民事赔偿责任。
至于专利侵权的行政责任,主要规定在《专利法》第六十八条中,即:行政执法机关可以对专利侵权人实施责令改正、没收违法所得以及进行罚款等具体行政行为。⑦本条款中亦涉及了专利侵权的刑事责任,根据其规定,假冒专利构成犯罪的,应当依法追究刑事责任;我国《刑法》第二百一十六条又进一步规定:“假冒他人专利,情节严重的,处三年以下有期徒刑或者拘役,并处或者单处罚金。”
反观印度关于药品专利侵权救济的法律,专利侵权只允许获得行政救济和民事救济,胜诉的原告可以获得如下救济:一是禁止令;二是补偿性损害赔偿;三是交付或销毁侵权物品;四是承担诉讼成本。但是在印度的司法实践中,原告请求专利侵权人支付实际诉讼成本的请求几乎不会得到支持,印度法院对专利权侵权案件也几乎不会支持惩罚性赔偿,印度法官一般也不支持高额的损害赔偿金。可以说,在印度的司法实践中,对于专利侵权案件已经形成了补偿损失的惯例。[8]对于专利侵权的免责事由,印度《专利法》规定,在专利侵权诉讼中,被告证明其在侵权期间不知道也没有合理的理由认为该专利权存在的,即可免除赔偿责任。简单来说,专利侵权人只要证明其主观上不知道专利权的存在,即可得到赔偿豁免的机会。[9]最为关键的是,在印度,专利侵权不用承担刑事责任。[10]
(二)药品专利侵权救济模式的思考
通过上述制度比较可以看出,印度对专利的保护力度较低,对专利侵权的救济也乏善可陈,其对于专利侵权秉持的是“填平损失”而非“惩罚侵权”的态度。客观来说,印度较为粗放的专利侵权救济保障制度在一定程度上促进了其仿制药产业的蓬勃发展,这一点可以通过下表管窥一斑。
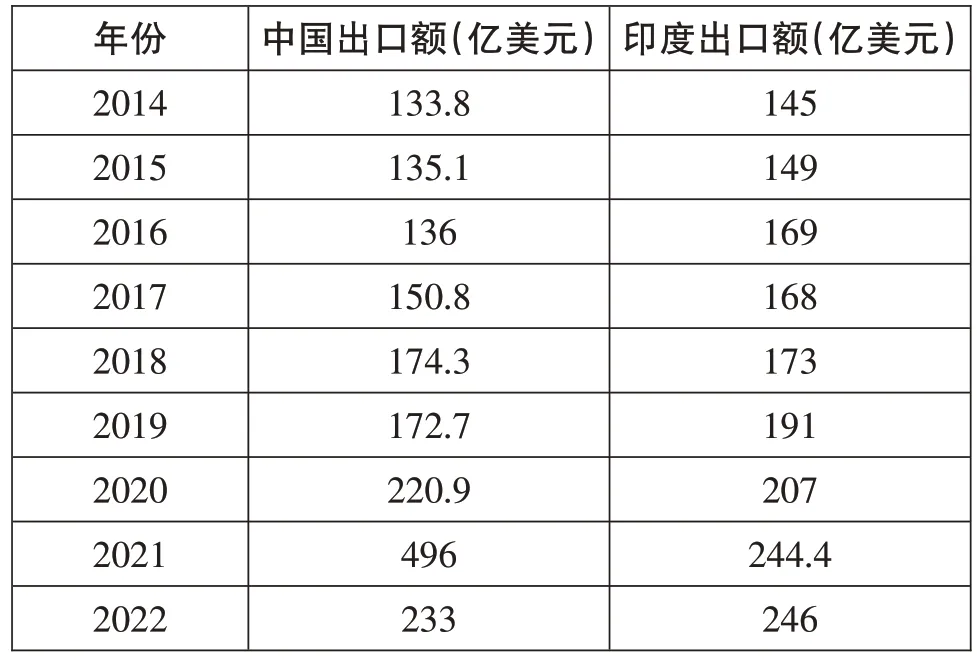
表 2014-2022年中印两国医药品出口金额统计
对上表“2014-2022 年中印两国医药品出口金额统计”的对比可以看出,在2019年之前,印度的医药品出口额始终高于我国,并且一度在2016年左右与我国达到了33 亿美元的差值,直至2020 年,我国医药产品出口金额首次超过印度,并在2021年对其完成了大幅度的反超(这里做出合理的推测,是因为新冠疫情暴发后,我国医药工业迅速恢复,大量出口医药产品,因此反超印度),但在2022 年度,我国医药产品出口额又出现了回落,印度则与上年度出口额实现持平。[11]总的来看,印度的医药产品在出口金额方面长期超过我国同期水平,其“世界药房”之称名副其实。
通过上述对比可见,中印两国针对药品专利侵权的救济模式不尽相同,我国的救济模式有民事、行政以及刑事救济三种途径,而印度只有民事以及行政救济模式,两国相关法律制度在具体的救济措施方面也存在较大不同。在民事救济方面,我国立法秉持的是补偿被侵权人损失和惩罚专利侵权并行的态度,立法详细规定了补偿赔偿金的具体计算方式,而印度立法则以补偿被侵权人损失为原则,并且由于立法缺乏具体细节,印度法院对补偿金数额拥有较大裁量权;在行政救济方面,我国立法对专利侵权行为,不仅要阻止侵权还要对其进行惩罚性的打击,而印度立法则较为消极,只是规定了一些消除侵权影响、防止侵权扩大的行政措施;在刑事救济方面,我国将专利侵权行为纳入了刑事打击的范围,而印度刑事法律则将专利侵权排除在外。此外,我国专利制度规定的专利侵权赔偿责任豁免的条件明显比印度更高。
四、我国药品专利标准、许可及救济模式之完善的思考
通过上述对中印两国改进型药品的可专利标准、药品专利的强制许可制度以及药品侵权救济模式进行分析,可以发现我国现行的法律制度还存在改进型药品专利授予标准不够清晰、强制许可制度的启动条件过高,以及专利侵权救济模式有待进一步完善等问题。结合上述分析,本文提出一些具体的法律建议,以期通过法律制度的完善促进我国药品专利产业的发展。
(一)提高改进型药品专利授予标准以提升我国药品专利的授予质量
截至目前,根据我国最新的《专利审查指南(2020)》,针对改进型专利的授予和限制等条款并没有明显的变化,也就是说,我国仍存在“专利常青”的风险。应当指出,对于中国和印度这种医药产业起步较晚的发展中国家,在医药产业进行完全的原始创新还存在很大的技术难度,因此,鼓励改进型药品创新则是发展中国家踏入创新体系入口的关键性步骤。改进型创新专利和常青专利的界限看似很模糊,实际上还是有较大差异的,前者往往是开发具有突破性的原始创新药品的基石,而常青专利则仅仅是为了阻碍仿制药品上市,维持垄断利益的产物。[12]不能增强已知疗效的药物新物理或者化学形式如果被囊括进可授予药品专利的范畴,那么其被利用来申请常青专利的风险性就很高,并且也不利于鼓励医药企业加大研发投入,进行技术创新。
从《专利法》的角度来看,医药专利有其特殊性,往往需要明确对不同种类药物的专利审查标准,因此,建议未来我国可以从药品专利的授予标准着手,提高药品专利特别是改进型药品专利的授予标准,细化对药品等特殊产品的专利审查规则,至少要排除对药物疗效无明显提升的改进型药品的可专利性,降低在医药领域出现“专利常青”现象的可能性。通过这种方式,也可以加大我国药企的原始创新的压力,促使其加大研发投入进行技术创新,从而带动整个医药产业的高质量发展。
(二)放宽申请强制许可的主体条件并细化规定“为了公共利益”
强制性许可制度从设立之初就天然带有维护公共利益、防止专利权滥用的反垄断属性。因此,要遏制医药巨头滥用市场支配地位销售天价专利药的行为,有效实施强制许可当然是其制度的应有之义。从法理逻辑来看,一切权利皆有边界,如果说《专利法》赋予了专利权人“有期限的合法垄断”的权利,那么强制许可制度则对这种权利的边界进行了调整[13];从维护公共健康利益、防止专利权滥用的知识产权法范畴的角度来看,我国专利立法所参照的《TRIPS协议》等文件中有关强制许可的规定,我们应当理解为一种兜底性条款而非一种应当严格遵循的限制性标准,这一点也在我国参加并通过的《多哈宣言》第四条第二款和第五条(a)(b)款得到了确认⑧,根据该《宣言》,各成员其实是可以自由规定强制许可申请事由的;从现实状况来说,在《宣言》颁布后的2006年到2013年,全球对非传染性疾病药品作出的专利强制许可数量(8个)超过对传染性疾病药品作出的强制许可(4 个)。[14]综上所述,我国不论是针对“为了公共利益”进行细化规定,还是像印度一样另外设置一般性条款,使天价抗癌药被纳入可以被申请实施强制许可的范围,在法理逻辑、立法目的以及国际上的司法实践中都是站得住脚的。
综合上述分析,本文建议我国适当探索药品专利的强制许可制度,放宽对申请主体的要求,例如,参考印度经验,将申请主体范围改为“任何利益相关人”,赋予普通患者申请强制许可的主体资格。此外,针对我国《专利法》第五十四条有关“为了公共利益”启动强制许可的条件上,可以在司法解释或者正式的法律文件中做出进一步的细化规定,或者参考印度经验,赋予相关行政部门一定对药品专利强制许可实施条件的自由裁量权,使强制许可的申请更具有操作性。涉及公共健康利益的药物往往是治疗癌症等重大疾病的品牌药物,如果其技术含量仍然很高,则利用强制许可制度进行“高水平仿制”本质上其实也是一种自主创新。
(三)继续完善药品专利侵权救济制度
应当指出,印度对专利侵权的救济秉持的是一种消极的态度,这种做法尽管能在一定时期内凭借规模效应获得竞争优势,但却不利于医药产业的长期健康发展。考虑到西方在国际谈判和贸易中常常对我国知识产权保护横加指责,印度我行我素的做法当然不能照搬,因此,我国应当继续加强对药品专利侵权民事、行政救济的力度,并保持将情节严重的专利侵权行为纳入刑事打击范围的做法,以威慑恶意的专利侵权行为。
与此同时,我们也应当看到,我国较为严苛的专利侵权赔偿豁免制度,在保护专利权人利益的同时,还存在国际医药巨头利用其所持有的大量专利独享垄断利益的风险。在我国,启动赔偿豁免的主体不仅要证明主观上不知道专利权的存在,还要证明药物的来源合法,并且仅限于使用、许诺销售和销售三种实施行为才可以豁免赔偿责任,相较于印度仅仅要求行为人证明主观上不知道专利权存在即可申请专利侵权赔偿豁免,我国的规定使得专利药品的可及性大大降低,也容易增加行政执法机关的工作量以及法院讼累。因此,本文建议我国适当放宽药品专利侵权赔偿豁免制度的启动条件,扩宽赔偿豁免实施行为的情形,只要能够证明行为人主观上不知道专利权存在,药物的来源合法,排除了破坏正常市场竞争秩序,恶意侵权的可能,即可启动赔偿豁免制度。
我们态度鲜明地地保持“惩罚侵权”的态度确有必要,但是打击专利侵权的行为与反对专利垄断、维护公共健康利益的主张并不矛盾,只有将二者结合,才能更好地为医药产业的高质量发展保驾护航。
五、结语
综上分析,中印两国在药品专利授予标准、强制许可和侵权救济三方面制度存在很大的差异,并且这种制度的差异性对药品市场的发展产生了一定的影响,我国的相关制度还需要在借鉴印度相关法律制度的基础上,结合我国药品专利发展实践进行相应的改进,进而通过“适切的法律制度”促进我国药品质量的提升,以优质药品来保障人们的健康。
注释
①《TRIPS协议》,即《与贸易有关的知识产权协议》,是世界贸易组织(WTO)的重要文件,加入世贸组织的国家和地区都有义务遵守该协定的内容,该协定于1994年与世贸组织及其他协定一并缔结,是迄今为止在知识产权法律和制度影响最大的国际公约。
②参见《专利审查指南》(2020)第二部分第四章之四:几种不同类型发明的创造性判断。
③参见《专利审查指南》(2020)第二部分第十章之六:化学发明的创造性,第二段。
④India. The Patents Act,Section 3,non patentable inventions(d).
⑤India. The Patents Act,1970,Chapter XVI Working of Patents,Compulsory Licences ,Licences of Right and Revocation Article 84;India. The Patents(Amendment)Act,2002,Section 39.
⑥参见《中华人民共和国专利法》第七十一条。
⑦有关专利侵权的行政责任,参见《中华人民共和国专利法》第六十八条:假冒专利的,除依法承担民事责任外,由负责专利执法的部门责令改正并予公告,没收违法所得,可以处违法所得五倍以下的罚款;没有违法所得或者违法所得在五万元以下的,可以处二十五万元以下的罚款;构成犯罪的,依法追究刑事责任。
⑧《多哈宣言》是指2001 年11 月在多哈召开的WTO 第四届部长级会议上发表的《TRIPS 与公共健康多哈宣言》,根据上述《宣言》,WTO就公共健康问题开始谈判,计划于2002年12 月31 日就实施专利药品强制实施许可制度、解决发展中国家成员方公共健康危机达成一致意见。2016 年5 月12日,中国外交部长王毅出席在多哈举行的中阿合作论坛第七届部长级会议,中阿合作论坛第七届部长级会议通过了《多哈宣言》。

