润肠通秘茶的超高效液相色谱指纹图谱研究及其6 种成分含量测定
马琳琳,周荻书,林瑞仪,吴明安,郑国扬,郑开荣,李伟荣,王奇,潘华峰 (. 广州中医药大学科技创新中心,广东 广州 50405;. 大兴安岭天草药业有限公司,黑龙江 大兴安岭 6599)
便秘是临床常见病、多发病,慢性便秘表现为排便次数减少、粪便干硬和(或)排便困难,病程至少为6 个月[1]。我国目前慢性便秘的发病率已高达3.19%~11.6%,尤以中老年人居多[2-3]。润肠通秘茶原名为饮益通袋泡茶,为黑龙江省中医研究院的院内制剂。处方源于《太平惠民和剂局方》的黄芪汤,由黄芪、陈皮、当归、肉苁蓉、火麻仁、蜂蜜组成,治疗气血两虚型便秘有显著疗效[4-6]。中老年人多肾阴不足、五脏虚损,尤以气血亏虚,生化乏源,肠燥津亏而致便秘多见[7]。润肠通秘茶在原方的基础上增加了当归、肉苁蓉,取其养血补肾润肠作用,共奏益气行气,养血润肠通便之功效。目前未见润肠通秘茶的质量分析研究。本实验采用超高效液相色谱(UPLC)法建立润肠通秘茶的指纹图谱,并用聚类分析(CA)及主成分分析(PCA)等进行化学模式识别,同时对润肠通秘茶所含6 种主要成分进行含量测定,以控制润肠通秘茶的质量。
1 仪器与材料
1.1 仪器 Waters ACQUITY H-CLASS 超高效液相色谱仪(美国沃特世公司);MS204 型万分之一电子天平、TLE3002 型千分之一电子天平(瑞士梅特勒托利多公司);PL-S80TX 超声波清洗机(东莞康士洁超声波科技有限公司),Eppendorf Centrifuge 5804 R 型离心机(德国艾本德公司)。
1.2 材料 橙皮苷(批号:wkq22010509)、芒柄花素(批号: wkq210615090)、 毛蕊花糖苷(批号:wkq22031108),四川省维克奇生物科技有限公司,含量均大于98%;阿魏酸(批号:G27A11L112005)、毛蕊异黄酮葡萄糖苷(批号:Y16O11H127829)、松果菊苷(批号:Y12D8H50506),上海源叶生物科技有限公司,含量均大于98%;乙腈、甲醇为色谱纯;其余试剂为市售分析纯;水为娃哈哈纯净水;11 批润肠通秘茶由大兴安岭天草药业有限公司提供,批 号(编 号):211101(S1)、211102(S2)、211001(S3)、211002(S4)、220102(S5)、220101(S6)、211201(S7)、211202(S8)、210902(S9)、210903(S10)、210801(S11)。
2 方法与结果
2.1 溶液的配制
2.1.1 润肠通秘茶的制备 精密称定润肠通秘茶1 g,置于具塞锥形瓶中;精密加入70%稀甲醇30 mL,密塞,称定质量;超声处理60 min,取出,放冷,再称定质量;用70%稀甲醇补足减失的质量,摇匀。静置后将提取液转移至离心管中,于25 ℃,以11 000 r·min-1离心15 min(离心半径:10.8 cm)。取上清液,0.22 μm 滤膜滤过,即得。
2.1.2 混合对照品溶液的制备 精密称取适量的松果菊苷、阿魏酸、毛蕊异黄酮葡萄糖苷、毛蕊花糖苷、橙皮苷、芒柄花素对照品,溶于二甲基亚砜,配制成浓度分别为1.09、1.08、1.22、1.20、1.17、0.49 mg·mL-1的混合对照品溶液。
2.2 色谱条件 色谱柱为Ultimate UHPLC AQ-C18(2.1 mm×100 mm,1.8 μm);检测器为二极管阵列检测器;流速:0.5 mL·min-1;柱温:28 ℃;检测波长:280 nm;进样量:2 μL;流动相为乙腈(A)-0.1%甲酸水(B)。梯度洗脱,洗脱程序为:0~15 min,5%→40% A;15~18 min,40%→95% A;18~23 min,95%→95% A;23~25 min,95%→5%A;25~27 min,5% A。
2.3 润肠通秘茶UPLC 指纹图谱研究 按“2.1.1”项下方法制备11 批润肠通秘茶的供试品溶液,按“2.2”项下色谱条件,进样测定,记录色谱图。将11 批润肠通秘茶的色谱图数据导入《中药色谱指纹图谱相似度评价系统》(2012 年版)进行分析。设置S2 批次为参照谱图,使用中位数进行自动匹配,时间窗宽度设置为0.1,通过多点校正法对色谱峰进行Mark 峰匹配,生成11 批润肠通秘茶的指纹图谱以及共有模式图谱,确定14 个共有峰。见图1。

图1 11 批润肠通秘茶供试品超高效液相指纹图谱(A)和共有模式图谱(B)Figure 1 UPLC fingerprint of 11 batches of Runchang Tongmi Tea samples(A)and their common mode(B)
2.3.1 精密度试验 按“2.1.1”项下方法制备供试品溶液(S6),连续进样6 次,以松果菊苷(分离度好、出峰时间及峰形稳定)为参照峰。记录润肠通秘茶样品14 个共有峰相对保留时间。结果显示,14 个共有峰相对保留时间的RSD 均小于0.21%,相对峰面积的RSD 均小于7.93%,表明仪器精密度良好。
2.3.2 重复性试验 按“2.1.1”项下方法制备供试品溶液(S6),平行6 份,进样,以松果菊苷为参照峰。记录14 个共有峰相对保留时间。结果显示,14 个共有峰相对保留时间的RSD 均小于0.20%,相对峰面积的RSD 均小于7.45%,表明方法重复性良好。
2.3.3 稳定性试验 按“2.1.1”项下方法制备供试品溶液(S6),室温下分别于0、2、4、6、8、12、24 h进样,以松果菊苷为参照峰S。记录14 个共有峰的相对保留时间。结果显示,14 个共有峰相对保留时间的RSD 均小于0.20%,相对峰面积的RSD 均小于7.91%,表明24 h 内润肠通秘茶供试品溶液稳定性良好。
2.3.4 指纹图谱相似度及相对峰面积计算 使用《中药色谱指纹图谱相似度评价系统》(2012 年版)计算11 批润肠通秘茶之间的相似度,相似度介于1~0.992。结果见表1。11 批润肠通秘茶中14 个共有峰相对峰面积的RSD 在2.60%~16.15%范围内,表明11 批润肠通秘茶之间的化学成分含量存在一定差异。结果见表2。

表1 11 批润肠通秘茶供试品指纹图谱的相似度结果Table 1 Similarities of 11 batches of Runchang Tongmi Tea samples

表2 11 批润肠通秘茶供试品共有峰的相对峰面积Table 2 The relative peak areas and RSDs of 14 common chromatographic peaks of 11 batches of Runchang Tongmi Tea samples
2.3.5 指纹图谱色谱峰指认 取供试品(S6)溶液和混合对照品溶液,按“2.2”项下色谱条件进样测定,获取对应色谱图。将两个色谱图进行比对,根据出峰时间,指认5 号峰为松果菊苷,6 号峰为阿魏酸,7 号峰为毛蕊异黄酮葡萄糖苷,8 号峰为毛蕊花糖苷,12 号峰为橙皮苷,14 号峰为芒柄花素。见图2。

图2 混合对照品(A)和润肠通秘茶供试品(B)的超高效液相色谱图Figure 2 Mixed reference(A)and UPLC fingerprint of Runchang Tongmi Tea samples(B)
2.3.6 聚类分析(CA) 将11 批润肠通秘茶的共有峰峰面积数据导入SPSS 25 软件,对峰面积进行Z-score 标准化法处理,运行系统聚类,通过欧氏距离对11 批样品进行聚类分析。结果见图3。当类间距离为10 时,可将11 批样品分为3 类:S9 自行聚为1 类;S11 自行聚为1 类;其余聚为1 类。

图3 11 批润肠通秘茶供试品聚类分析树状图Figure 3 Pheogram of hierarchical clustering analysis for 11 batches of Runchang Tongmi Tea samples
2.3.7 主成分分析(PCA) 将11 批润肠通秘茶共有峰峰面积的数据导入SPSS 25 数据分析软件,数据标准化处理之后,进行主成分分析。结果见表3 及图4。前3 个成分的累计方差贡献率大于85%,可以概括润肠通秘茶供试品数据的大部分信息;并且,在碎石图中特征值>3 曲线陡峭,特征值<3 后趋于平缓,表明提取3 个主成分合理。
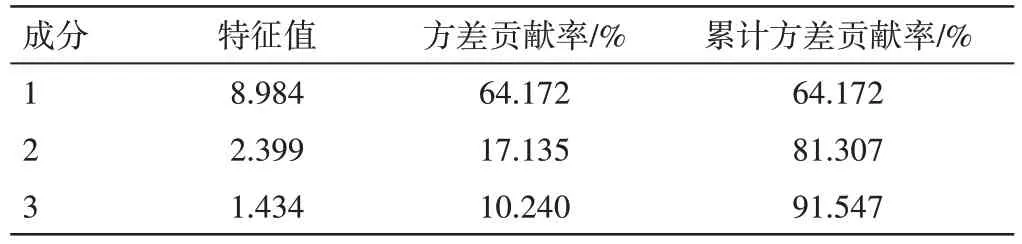
表3 11 批润肠通秘茶供试品的特征值及累计方差贡献率Table 3 Characteristic values and cumulative variance contribution rates of 11 batches of Runchang Tongmi Tea samples

图4 11 批润肠通秘茶供试品的碎石图Figure 4 Scree plot for 11 batches of Runchang Tongmi Tea samples
通过SPSS 25 分析软件将11 批润肠通秘茶共有峰峰面积标准化处理后的数据作为变量,运用SIMCA 14.1 软件得到11 批润肠通秘茶的PCA 得分图。见图5。结果显示所有样品均在95%可信区间内,且分为3 类:S9 自行聚为1 类;S11 自行聚为1 类;其余聚为1 类,与CA 分析结果一致。

图5 11 批润肠通秘茶供试品主成分分析得分图Figure 5 Plot of PCA scores for 11 batches of Runchang Tongmi Tea samples
2.4 润肠通秘茶的含量测定
2.4.1 线性关系考察及检测限、定量限 精密量取“2.1.2”项下混合对照品溶液500 μL,加入等量甲醇,逐级稀释成10 个浓度。按“2.2”项下色谱条件进样测定,记录峰面积。以浓度为横坐标(X),对应的色谱峰面积(Y)为纵坐标,绘制标准曲线,得各成分的线性回归方程。结果见表4。

表4 各成分的回归方程、线性范围和相关系数Table 4 The regression equation,linear range and correlation coefficient of each component
逐级稀释标准品溶液,按照信噪比(S/N= 3)计算松果菊苷、阿魏酸、毛蕊异黄酮葡萄糖苷、毛蕊花糖苷、橙皮苷、芒柄花素最低检测限,结果分别为:0.266、0.132、0.179、0.220、0.143、0.120 μg·mL-1。按照信噪比(S/N= 10)计算定量限,结果分别为:0.639、0.264、0.447、0.703、0.286、0.359 μg·mL-1。
2.4.2 精密度试验 精密量取适量混合对照品溶液,加入适量甲醇稀释,连续进样6 次,记录各成分峰面积。结果松果菊苷、阿魏酸、毛蕊异黄酮葡萄糖苷、毛蕊花糖苷、橙皮苷、芒柄花素峰面积的RSD分别为:0.35%、0.58%、0.41%、0.43%、0.39%、0.45%,表明仪器精密度良好。
2.4.3 重复性试验 按“2.1.1”项下方法制备供试品溶液(S6),平行6 份,进样,记录各成分峰面积。结果松果菊苷、阿魏酸、毛蕊异黄酮葡萄糖苷、毛蕊花糖苷、橙皮苷、芒柄花素峰面积的RSD 分别为:3.81%、3.55%、5.62%、7.02%、6.95%、3.15%,表明供试品制备方法重复性良好。
2.4.4 稳定性试验 按“2.1.1”项下方法制备供试品溶液(S6),分别于0,2,4,6,8,12,24 h 进样,记录各成分峰面积。结果松果菊苷、阿魏酸、毛蕊异黄酮葡萄糖苷、毛蕊花糖苷、橙皮苷、芒柄花素峰面积的RSD 分别为:0.36%、6.07%、7.65%、1.70%、0.39%、2.02%,表明24 h 内供试品溶液稳定性良好。
2.4.5 加样回收率试验 取润肠通秘茶供试品(S6)溶液9 份,分成3 组,每组3 份,按相当于供试品中成分含量80%、100%和120%加入各对照品。按“2.2”项下色谱条件进样测定,计算平均加样回收率。结果松果菊苷、阿魏酸、毛蕊异黄酮葡萄糖苷、毛蕊花糖苷、橙皮苷、芒柄花素分别为:102.35%、105.03%、85.86%、96.70%、103.44%、97.37%;RSD 分别为:1.78%、5.89%、7.63%、5.61%、1.98%、6.78%。
2.4.6 样品含量测定 按“2.1.1”项下方法制备11 批润肠通秘茶供试品溶液,按“2.2”项下色谱条件进样测定。计算11 批润肠通秘茶中松果菊苷、阿魏酸、毛蕊异黄酮葡萄糖苷、毛蕊花糖苷、橙皮苷、芒柄花素的含量。结果见表5。

表5 11 批润肠通秘茶供试品含量测定结果(mg·g-1,n=3)Table 5 Determination results of 6 constituents in 11 batches of Runchang Tongmi Tea samples(mg·g-1,n=3)
3 讨论
比较了回流和超声两种方法提取,由于回流提取所需时间较长,故本研究选择超声提取[8]。分别使用水及甲醇作为提取溶剂,发现用甲醇提取时出峰较多,故确定以甲醇为提取溶剂。在参考已有研究[9-10]的基础上,考察提取时间(30、45、60 min)、甲醇浓度(50%、70%、90%)、料液比(1∶30、1∶40、1∶50)3 个因素,用正交试验进行评价,最终确定70%甲醇、料液比1∶30、超声60 min 时,样品的色谱图中色谱峰峰形、分离度、峰高最佳。
关于测定成分的选择,主要参考《中国药典》(2015 年版)对制剂中各中药含量测定的要求进行确定[11]。《中药药典》中黄芪项下要求检测的成分有黄芪甲苷和毛蕊异黄酮葡萄糖苷,但黄芪甲苷的检测波长与其他成分的波长相差大,故参考相关研究[12-13]将黄芪甲苷更换为芒柄花素。经预试验,最终确定以毛蕊异黄酮葡萄糖苷、芒柄花素、阿魏酸、松果菊苷、毛蕊花糖苷、橙皮苷6 种成分作为含量测定指标。
对指纹图谱进行相似度分析及模式识别,发现11 批润肠通秘茶色谱图相似度大于0.991,且大部分的相似度结果为1,表明不同批次润肠通秘茶所含成分相似度高,质量稳定。聚类分析和主成分分析结果显示,11 批润肠通秘茶主要成分可分为3 类,批间成分差异较小。
综上所述,本实验建立了润肠通秘茶UPLC 指纹图谱及6 种成分含量测定方法,对其质量进行了整体评价,本方法快速、简单、准确,对润肠通秘茶质量标准的提升具有重要意义。

