基于炎症模型大鼠建立穿心莲内酯抗炎作用的PK-PD 模型
姚媛,廖琼峰,陈国平,孙旭,苏芬丽 (. 广州中医药大学第一附属医院,广东 广州 50405;. 广州中医药大学中药学院,广东 广州 50006)
穿心莲内酯是中药穿心莲的主要有效成分之一,具有抗炎、抗菌作用[1],对诸多炎症性疾病和感染性疾病有良好疗效,已被开发成为多种制剂应用于临床,如喜炎平注射液可用于治疗新冠病毒感染重症患者[2]。穿心莲内酯口服制剂因其疗效确切,安全性高,使用方便,被临床广泛用于治疗上呼吸道感染、细菌性痢疾等。然而以往的研究[3]发现,在正常动物体内,穿心莲内酯口服生物利用度低。这一特点无法解释穿心莲内酯在临床上高效的抗炎作用。在疾病条件下,药物在体内的药效学和药动学行为可能发生改变。基于药物本身是作用于疾病状态下的机体,本研究通过大鼠炎症模型,研究穿心莲内酯血药浓度与对炎症因子的作用关系,旨在建立穿心莲内酯在体内炎症状态下的药代动力学-药效动力学(PK-PD)结合模型,客观阐明穿心莲内酯发挥抗炎作用的量效关系和作用时间窗,以期为其临床治疗提供参考。
1 材料与方法
1.1 仪器 BS224S 万分之一电子天平,德国Sartorius公司; HH-6 数显恒温水浴锅,金坛市富华仪器有限公司;3K30 离心机,德国Sigma 公司;5424 型小型高速离心机,德国Eppendorf 公司; Varsoskan Flash 多功能酶标仪,美国Thermo 公司;Thermo Scientific Ultimate 3000 液相系统、TSQ Endura 三重四极杆质谱仪、Thermo Fisher 和Thermo Scientific Xcalibur 数据采集和处理系统,美国Thermo 公司。
1.2 药物与试剂 穿心莲内酯对照品,中国药品生物制品研究院,批号:110797-201609,纯度≥98%;白术内酯对照品,上海诗丹德生物技术有限公司,批号:4030,纯度≥98%;穿心莲内酯供试品,西安美禾生物技术有限公司,批号:2021040301,纯度≥98%;脂多糖(LPS),美国Sigma-Aldrich 公司,批号:12181202,纯度≥98%;大鼠TNF-α、IL-1β及IL-6 酶联免疫检测试剂盒,天津安诺瑞康生物技术 有 限 公 司, 批 号: 596210720、 310210720、385210720;甲醇、甲酸,色谱纯,德国Merck 公司;实验用水为去离子水。
1.3 动物 SPF 级SD 大鼠,180~220 g,由广东省医学实验动物中心提供,实验动物生产许可证号:SCXK(粤)2018-0002,实验动物质量合格证号44007200090193。动物实验环境:广东省中医药工程技术研究院SPF 级动物实验室。动物饲养于温度(22±2)℃、相对湿度(60±10)%的环境中,饲养管理均按照实验动物的要求及规则执行。动物实验经广东省中医药工程研究院动物伦理委员会审批,审批号:048889。
1.4 大鼠炎症模型的建立 选取雄性SD 大鼠10 只,体质量(250±20)g,适应性饲养7 d。按10 mg·kg-1给予大鼠腹腔一次性注射LPS 溶液,注射后正常饮食,备用[4]。大鼠腹腔注射麻醉后仰卧位躺立,对右颈部进行皮肤消毒后剪开,钝性分离颈静脉,将此静脉的远心端结扎,在血管上剪一小切口;然后沿切口处向心脏方向插入连接1 mL 注射器,观察出血是否顺畅,后拔掉注射器,将聚乙烯管的末端固定在颈部的皮肤上,缝合开口处。
1.5 药液的制备 先称取穿心莲内酯0.080 g,置研钵中,先加一滴乙醇充分研磨,再用0.5%CMC-Na配制成穿心莲内酯质量浓度约为11 mg·mL-1的混悬药液。药液现配现用,并超声充分混匀。
1.6 穿心莲内酯在炎症模型大鼠体内的药物代谢动力学研究 取炎症模型大鼠,按84.70 mg·kg-1灌胃穿心莲内酯,于给药前及给药后5、15、30 min,1、1.5、2、3、4、6、8、10、12 h 各采血0.45 mL,置于肝素化的离心管中,以3 500 r·min-1离心15 min(离心半径13.5 cm),分离血浆,取血浆样品100 μL于-80 ℃下保存,用于药效学考察。
取血浆样品50 μL,置于1.5 mL 高速离心管中。精密加入4.0 μg·mL-1内标溶液白术内酯50 μL,甲醇100 μL,涡流混合1 min,离心10 min(15 000 r·min-1,离心半径7.7 cm),取上清液10 μL 进样分析。采用LC-MS/MS 测定不同时间点血浆中穿心莲内酯的质量浓度,按非房室模型计算穿心莲内酯主要的药代动力学参数。
1.7 穿心莲内酯干预后的药效动力学考察 取“1.6”项下的血浆样品,按酶联免疫检测试剂盒说明书操作,测定不同时间点血浆中IL-6、IL-β 和TNF-α 的含量,结合“1.6”项下样品的血药浓度数据,分别绘制穿心莲内酯的质量浓度-时间和效应浓度-时间曲线。
1.8 穿心莲内酯在效应室质量浓度的拟合 将“1.7”项下穿心莲内酯的质量浓度-时间及效应浓度-时间数据导入到Phoenic 8.1 软件,通过半房室模型工具对上述数据进行拟合,获得穿心莲内酯在效应室的质量浓度-时间数据,进而绘制穿心莲内酯效应室的质量浓度-效应曲线(以IL-6、IL-β 和TNF-α 为药效指标)。
1.9 穿心莲内酯PK-PD 结合模型的建立 固定“1.6”项下穿心莲内酯的相关药代动力学参数,采用Phoenic 8.1 软件中的Phoenic model 项下的“PK”模型进行拟合,获得PK 参数;采用Phoenic model 项下的“PD”模型,对“1.8”项下效应室浓度-效应关系(分别以IL-6、IL-β 和TNF-α 为药效指标)进行拟合,得相关PD 参数;进而获得穿心莲内酯的PKPD 结合模型的参数,建立其PK-PD 结合模型。
2 结果
2.1 穿心莲内酯在炎症模型大鼠体内的药代动力学研究 炎症模型大鼠灌胃给予穿心莲内酯后,大鼠血浆中穿心莲内酯的血药浓度-时间关系经一、二、三房室模型拟合后,以负2 倍对数似然函数值(-2LL)、最小化信息量(AIC)、贝叶斯信息准则(BIC)为主要拟合优度参数的标准,发现二房室模型拟合优度最高。通过模型计算后发现血药浓度的实测值与预测值基本一致。穿心莲内酯的主要药代动力学参数:吸收速率常数(Ka)=0.045 08 min-1,表观分布容积1(V1)=1 290 L,表观分布容积2(V2)=3 733 L,清除率1(Cl1)=9.40 L·min-1,清除率2(Cl2)=37.82 L·min-1,分布半衰期(t1/2)=15.37 min。
2.2 穿心莲内酯干预后的药效动力学研究 分别以IL-6、IL-1β 和TNF-α 为药效指标,穿心莲内酯在炎症模型大鼠体内的血药浓度-时间和效应-时间之间的变化见图1。

图1 穿心莲内酯在炎症大鼠体内的血药浓度-时间和效应-时间曲线(n=10)Figure 1 Plasma concentration-time and effect-time profiles of andrographolide in inflammatory model rats(n=10)
2.3 穿心莲内酯在效应室浓度(Ce)的拟合 以IL-6、IL-β 及TNF-α 为药效指标,可得穿心莲内酯在效应室的效应-浓度变化,如图2 所示。

图2 穿心莲内酯在炎症模型大鼠体内的效应室质量浓度-效应曲线(n=10)Figure 2 Concentration in effect compartment and effect profiles of andrographolide in inflamatory model rats(n=10)
2.4 穿心莲内酯的PK-PD 模型的建立 分别以IL-6、IL-β、TNF-α 为药效指标时,利用Phoenic model 项下的“PK-Emax”模型进行拟合计算,得到穿心莲内酯的PK-PD 参数。见表1。根据穿心莲内酯的PK-PD参数,以IL-6 为药效指标时,可得穿心莲内酯的PK-PD 模型为:E=55.004-20.544 5×Ce/(1.680 23+Ce)。最终模型拟合的-2LL 为78.83,AIC 值为100.83,BIC 值为114.68,说明该模型拟合度较精确。
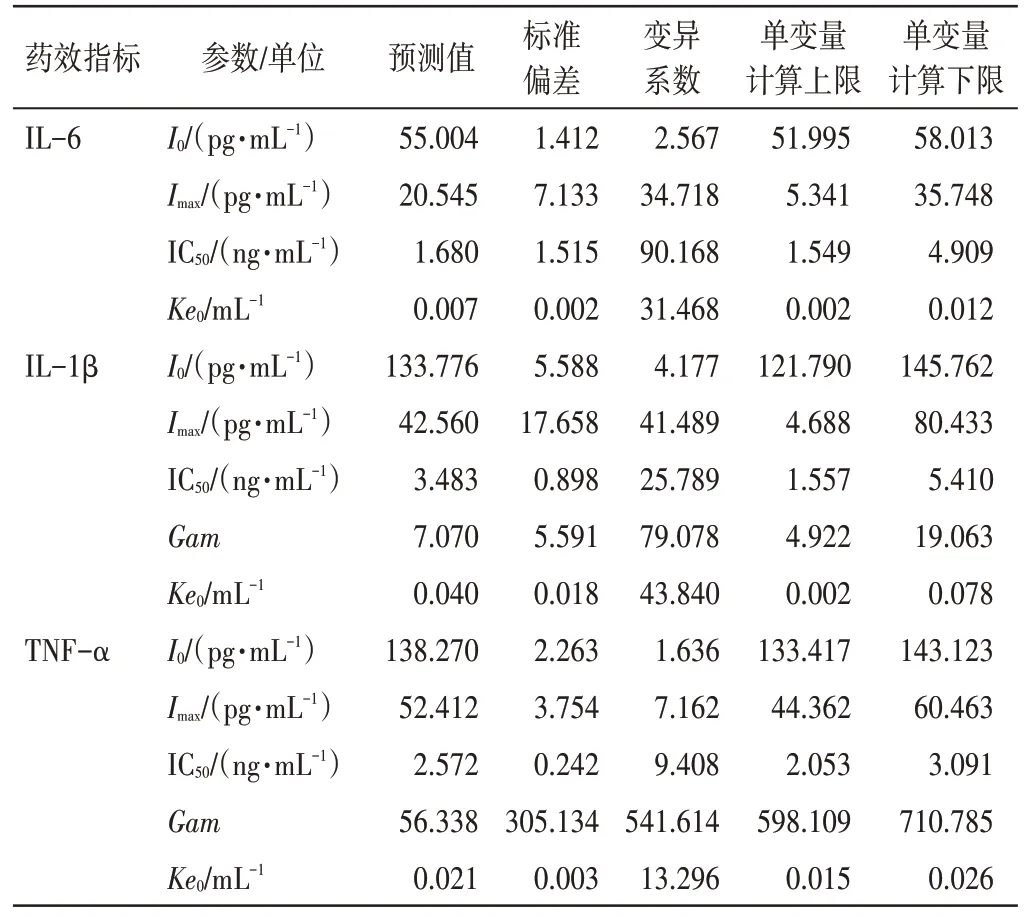
表1 穿心莲内酯以IL-6、IL-1β 和TNF-α 为药效指标的PK-PD 参数Table 1 PK-PD parameters of andrographolide when using IL-6,IL-1β and TNF-α as pharmacodynamic indexes
以IL-1β 为药效指标时,可得穿心莲内酯的PK-PD 模型为:E=133.776-42.560 3×Ce/(3.483 03+Ce)。最终模型拟合的-2LL 为132.40,AIC 值为156.40,BIC 值为171.50 ,说明该模型拟合度较精确。
以TNF-α 为药效指标时,可得穿心莲内酯的PK-PD 模型为:E=138.27-52.412 2×Ce/(2.571 69+Ce)。最 终 模 型 拟 合 的-2LL 为109.73,AIC 值 为133.72, BIC 值为148.82,说明该模型拟合度较精确。
式中E为效应值。由上述PK-PD 模型可以根据穿心莲内酯的浓度推算出相应的药效值,也可以根据药效值推算相对应的浓度。
3 讨论
以往对穿心莲内酯的药动学研究多在正常机体条件下进行,未考虑炎症状态下药物在体内的药动学行为可能发生变化,从而导致药物治疗效果的差异。对于临床而言,病理状态下获得的药效指标更有意义[5]。因此,在疾病状态下进行穿心莲内酯的PK-PD 研究,可客观评价穿心莲内酯在机体内的药动学行为和产生药理效应的动态变化,为科学预测其在感染性疾病中的作用机制提供参考[6-7]。
本研究主要是以大鼠炎症模型为研究对象,观察穿心莲内酯的血药浓度-时间曲线以及效应-时间曲线。结果发现,在大鼠给药后,随着穿心莲内酯的血药浓度的提高,炎症因子表达缓慢下降,给药30 min 后血药浓度达峰,而IL-6、IL-1β 和TNF-α在给药后90 min 才基本达到最大下调值,提示药物在作用部位的效应变化滞后于血药浓度变化,药物分布至靶点的延迟、通过间接机制产生活性、受体激活时间的延长和耐受现象的产生等[8]均可能是导致滞后现象产生的原因。根据这种变化关系宜采用间接效应连接模型建立PK-PD 模型。因此以Phoenic 8.1 软件中的半房室模型法对血药浓度-效应浓度-时间数据进行拟合,获得穿心莲内酯在效应室的质量浓度-效应浓度数据,采用效应室间接连接模型拟合,进而呈现穿心莲内酯与药效指标之间的量效关系,最终建立穿心莲内酯的PK-PD 结合模型。
穿心莲内酯的PK-PD 模型结果表明,IL-6、IL-1β、TNF-α 的浓度与穿心莲内酯的质量浓度存在一定的相关性。由此可推测穿心莲内酯通过抑制促炎性细胞因子IL-6、IL-1β、TNF-α 的表达发挥抗炎作用。通过对炎症状态下穿心莲内酯的PK-PD 模型建立,可准确地评价穿心莲内酯在炎症状态下体内的动力学过程和产生药理效应的动态变化,为揭示中药穿心莲及穿心莲内酯制剂的清热解毒的药效物质基础及作用机制提供参考。

