艾滋病合并巨细胞病毒感染患者1例抗病毒药物的合理性分析
潘 瑛 曹 辉
南京市第二医院药学部,江苏南京 210003
艾滋病(acquired immune deficiency syndrome,AIDS)是指人类免疫缺陷病毒(human immunodeficiency virus,HIV)侵犯人体免疫系统后,导致人体免疫系统功能进行性下降,从而产生各种机会性感染,是累及全身多器官多系统的疾病。人类β 疱疹病毒5 型,即巨细胞病毒(cytomegalovirus,CMV)作为AIDS 患者常见的机会性感染之一,CMV 感染最常累及视网膜,还可累及肺、胃肠道、脑、肝脏和食管等组织,可作为AIDS 患者死亡的独立预测因素,加快AIDS 患者的发病及病死[1-2]。AIDS 患者由于自身基础免疫力低下,容易造成多种机会性感染,病情复杂多变,治疗难度大,预后不确定。基于此类复杂情况,要求在治疗过程中诊断及时准确,用药合理有效,同时保证最大的安全性。现结合1 例AIDS 患者合并CMV 感染的药物合理选择的治疗经过,探讨临床药师对于此类患者进行药学监护的工作重点,希望能为临床治疗提供有效的参考。
1 病例资料
患者,男,50 岁,因胸闷气喘1 月余,加重半月,伴纳差、乏力,于2020 年12 月26 日就诊于南京医科大学第四附属医院,胸部CT 示双肺广泛感染性病变,且病程中出现腹泻、便血症状,查HIV 抗体阳性,未启动抗HIV 治疗,于2020 年12 月31 日转至南京市第二医院(我院)ICU 治疗。
入院查体:体温37.2℃,脉搏110 次/min,呼吸23 次/min,血压148/83 mmHg(1 mmHg=0.133 kPa),精神萎靡,呼吸急促、费力,双肺呼吸音粗,双下肺闻及散在湿啰音;全身皮肤黏膜无黄染,无瘀点瘀斑,无出血点,全身浅表淋巴结无肿大。查血常规:中性粒细胞绝对值1.83×109/L,白细胞6.78×109/L,红细胞3.6×1012/L,血红蛋白109 g/L,血小板205×109/L;查肝肾功能:谷丙转氨酶18.8 U/L,谷草转氨酶42.0 IU/L,白蛋白29.4 g/L,肌酐154.2 μmol/L,尿素17.95 mmol/L;查免疫功能:CD4+T 细胞13 个/μl;血浆超敏HIV:<1.20E+05,提示HIV 感染;查大便常规:隐血实验阳性。
据以上初步诊断,高度怀疑卡氏肺孢子虫肺炎(pneumocystis Carinii pneumonia,PCP)感染,且不排除病毒性肺炎,故经验性予以注射用醋酸卡泊芬净(美国默沙东药厂,H20171218,规格:50 mg),用法:首剂70 mg,后改50 mg,qd,19 d,加复方磺胺甲恶唑片(SMZ)(华中药业股份有限公司,H42022487,规格:0.48 g),用法:4 片,qid,19 d,联合抗PCP;予以注射用哌拉西林钠他唑巴坦钠(4 ∶1)(瑞阳制药股份有限公司,H20110134,规格:2.5 g)抗阴性菌,用法:2.5 g,q12 h,19 d;予以更昔洛韦注射液(ganciclovir,GCV)(辰欣药业股份有限公司,H20051042,规格:0.25 g/5 ml)抗病毒,用法:0.25 g,q12 h,15 d;辅以激素抗炎,同时监测相关指标,结果见图1。于2021 年1 月2 日和1 月6 日行肺泡灌洗液和全血基因测序检查,确诊PCP、CMV 及细菌感染,结果见表1,加利奈唑胺葡萄糖注射液(正大天晴药业集团股份有限公司,H20163338,规格:0.2 g/100 ml)抗阳性菌,用法:0.6 g,q12 h,14 d,其余治疗同前。
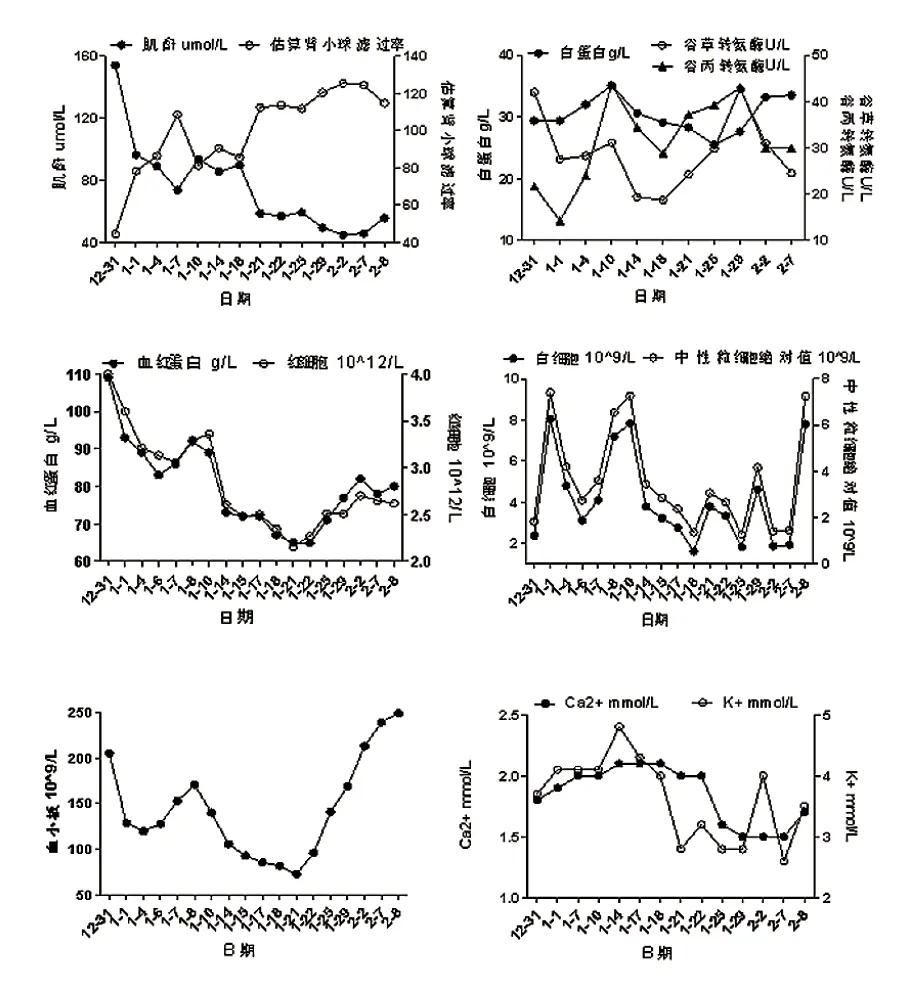
图1 相关指标变化趋势图
患者肠腔胀气,便血,予以艾速平+硫糖铝+整肠生+新络纳+保留灌肠治疗,并进行肠内营养支持。治疗3 d 仍便血,加康复新液促进胃肠溃疡黏膜愈合,于1 月6 日行肠镜检查,示结肠多发溃疡伴出血,肠镜活检组织免疫组化结果:CMV(+),确诊CMV 肠炎。经过积极治疗,1 月10 日血便停止,腹胀好转,抗CMV 治疗同前。
1 月15 日复查CT 改善不明显,但考虑影像学变化的滞后性,且患者总体病情明显好转,于1 月18 日转入感染科继续治疗,改以注射用醋酸卡泊芬净(美国默沙东药厂,H20171218,规格:50 mg),用法:50 mg,qd, 8d,磷酸伯氨喹(上海上药中西制药有限公司,H20059843,规格:13.2 mg),用法:3 片,qd,14 d,注射用拉氧头孢钠(浙江惠迪森药业有限公司,H20083977,规格:1.0 g),用法:2 g,q12 h,18 d,盐酸克林霉素注射液(重庆莱美药业股份有限公司,H20020513,规格:0.6 g/8 ml),用法:0.6 g,qd,3 d,后改0.6 g,q8 h,14 d,继续联合抗PCP、抗菌治疗,注射用醋酸卡泊芬净使用28 d 后停用,其余不变,同时继续监测相关指标,结果见图1。
于1 月25 日和2 月2 日分别复查CT,肺部病灶均较前吸收。转科后继续予以GCV(辰欣药业股份有限公司,H20051042,规格:0.25 g/5 ml)抗CMV,用法:0.25 g,q12 h,共18 d。 于1 月20 日查血CMV-DNA 5.61×103copies/ml,示单用GCV 效果不佳,加用膦甲酸钠氯化钠注射液(foscarnet,FOS)(正大天晴药业集团股份有限公司,H20000441,3.0 g/250 ml)联合抗CMV,用法:3g,q8 h,18 d。后多次测CMV-DNA,结果均阴性,结果见表1,于2 月4 日停用GCV,2 月7 日停用FOS。患者不适症状逐渐缓解后,各项指标均有好转,结果见图1,于2 月3 日开始口服抗HIV 药物治疗,并于2 月9 日出院,嘱其坚持治疗并定期复查。
2 结果
2.1 抗CMV结果
由表1 可知,患者入院之初两次测CMV-IgM抗体均在正常范围之内,有所上升,但考虑从CMV感染到产生抗体被检测到一般需要2 周左右的“窗口期”,结果存在滞后性。患者病情危重需尽快明确感染源,故对肺泡灌洗液和全血进行基因测序,测得CMV 序列数分别为317 和84,提示患者CMV感染。单用GCV 抗CMV 治疗18 d,仍测得CMVDNA:5.61×103copies/ml,示单用GCV 疗效不佳,进而联用FOS 抗CMV,后续考虑基因检测费用较高、取样操作性要求高、患者不配合等限制因素,故选CMV-DNA 为抗CMV 治疗的监测指标。联合用药后两次测得血浆CMV-DNA 阴性,且考虑CMV可侵袭脑部,故测脑脊液CMV-DNA 为阴性。
2.2 相关指标变化结果
由图1 可知,肝功能指标谷丙转氨酶和谷草转氨酶变化趋势一致,基本处于正常范围之内;入院查白蛋白29.4 g/L,低于最低值37.0 g/L,随着治疗深入,白蛋白水平存在下降趋势,一直低于最低值,故予以人血白蛋白纠正低蛋白血症。白蛋白合成分泌主体为肝脏,肝功能受损肝细胞数量下降,白蛋白分泌水平降低,其减少程度与肝炎的严重程度平行[3]。综合整个疗程,患者肝功能受损较小,基本维持正常功能。
从图1 可知,入院时肾功能指标肌酐水平偏高,估算肾小球滤过率低于最低值,表现出肾功能受损,治疗后肌酐恢复至正常水平,但呈现下降趋势,于1 月21 日较前下降约1/3,而滤过率则恢复至正常水平。GCV 和FOS 联合用药期间,肌酐水平略低于最低值,但总体水平较为稳定,滤过率处于正常范围,肾功能基本正常。
以血红蛋白、红细胞、血小板、白细胞和中性粒细胞绝对值(以下简称“中粒值”)作为骨髓抑制的指标,由图1 可知,5 个指标的变化趋势基本一致,在1 月6 日左右均有一个明显的下降,此时GCV 用药1 周,从血常规指标显示已有骨髓抑制发生的趋势,入院初期血红蛋白和红细胞水平就较为低下,已存在贫血症状,推测为患者有痔疮史,且近期便血,造成慢性失血。前期患者已在外院接受治疗,入我院时处于危急状态,抢救1 周左右才脱离生命危险,后续指标有一段上升趋势,表示患者治疗有效,感染得到了一定的控制。随着治疗深入,用药时间延长,指标均开始下降,到1 月20 日左右降至最低值,血小板下降约2/3,血红蛋白和红细胞下降至最低值的1/2 左右,白细胞和中粒值也低于最低值。后采取纠正措施,血小板恢复至正常水平,血红蛋白和红细胞也处于上升状态,而白细胞和中粒值虽予以纠正却始终处于较低水平,考虑除GCV 的影响外,患者自身免疫缺陷,以及克林霉素和拉氧头孢的使用也有一定影响,当抗菌药和抗病毒药停用后,继续辅以纠正,白细胞和中粒值均恢复至正常水平。
患者入院前反复腹泻一月有余,入院后动态监测电解质水平,其中以钾离子(K+)和钙离子(Ca2+)的变化最为明显。由图1 可见,K+前期处于正常范围,而Ca2+入院时即略低于最低值,二者到1 月21 日均出现下降趋势,均低于最低值,出现了低钾血症、低钙血症的副反应,故予以氯化钾颗粒和钙剂进行纠正。FOS 于2 月7 日停药后,二者水平均有上升。
3 讨论
3.1 抗CMV药物的合理性应用分析
临床常用抗CMV 药物有GCV 和FOS,GCV 为核苷类药物,抗病毒感染范围广泛,为抗CMV 首选药物,静脉和口服均有疗效,可同时用于诱导治疗和维持治疗,且价格低廉,其主要副反应为中性粒细胞减少症,贫血和血小板减少症等骨髓抑制反应[4]。有报道称在血常规正常的患者中,GCV 较之FOS有起效较快,较短的输注期,中枢治疗作用和不需要水化等优势[5]。FOS 作为二线抗病毒药物,除能抗疱疹病毒外,对HIV 感染后并发的病毒感染也有抑制作用,在对所有抗逆转录病毒药物产生耐药性的AIDS 突变患者中,FOS 可显著降低血浆HIV 载量并改善免疫状态,常作为耐GCV 患者治疗的首选,口服生物利用度低,常静脉给药,其主要副反应为肾功能损害、电解质紊乱和胃肠道反应等[6]。
本例在综合考虑药物特性,患者病情及经济因素,先用GCV 抗CMV,给药方案为0.25 g,q12 h,共15 d,并监测血常规。经过治疗,患者腹胀好转,血便停止,1 月15 日复查CT 示肺部感染改善不明显,故于1 月18 日采样查血浆CMV-DNA 5.61×103copies/ml,示该患者单用GCV 疗效不佳,于1 月21 日加用FOS 联合抗CMV,患者肝肾功能基本正常,故给药方案为3 g,q8 h,共18 d,联合用药15 d。后查血浆和脑脊液CMV-DNA 均<500 copies/ml,显示联合用药有效。据报道,FOS 与GCV 联合使用具有多种优势,如二者抗病毒机制不同,联用时可能会产生协同效应,也可能会减少药物毒性反应,或是当一种药物必须中断时,另一种药物可以继续控制病情发展直到恢复联用等,当然联用也存在频繁输液和长时间静脉水化等缺点[7]。
药师建议抗CMV 治疗需足量足程,治疗2 ~3 周后需再给予维持量,同时监测CMV-DNA 情况决定后续疗程,在感染症状消失或体温正常1 周,CMV-DNA检测阴性后停药较为妥当[8]。本例患者在抗CMV治疗过程中,以CMV-DNA 为指标监测CMV 治疗效果,及时调整治疗方案,直至CMV-DNA 转阴,后考虑到CMV 感染的反复性及患者自身低下的免疫力,开具更昔洛韦胶囊口服给药作为序贯治疗,减少治疗成本[9]。本例患者整体的抗CMV 用药选用合理,给药剂量准确有效,疗程切合患者实际病情发展,治疗效果达到预期水平。
3.2 抗CMV 药物不良反应分析
FOS 主要经肾脏排泄,半衰期约3 ~4 h,故需增加给药频率(8 ~15 g/d)才能达到抑制CMV复制所需的血药浓度[10],且该药可螯合二价金属离子,形成难溶性配合物,而该类配合物的存在也是其肾毒性的原因之一,约1/3 患者在使用该药时肾功能显著下降[11]。基于此,在用药时需开具中药制剂补益肝肾,且后期治疗需综合评价CMV 治疗疗效和肾功能指标以判断是否需要调整给药剂量。FOS 的肾毒性会使患者肌酐升高约2 ~3 倍,一般停药后1 ~10 周内能恢复至治疗前水平或正常,但本例患者并未出现升高,反而一直下降,推测可能是患者治疗时间较长,病情复杂,长时间服用肠内营养剂,正常饮食较少,营养不良导致。另外,FOS 还可致电解质水平异常,且该类副反应多为可逆,本例患者电解质水平变化与文献报道一致[12]。
患者治疗3 周左右,血常规发生变化,推测其原因有:①AIDS 患者免疫力低下,用药疗程较长,故副反应发生率较高;②多重感染需多药联用,除GCV 发生骨髓抑制反应的概率较高需重点监控外,其他药物如SMZ、利奈唑胺和哌拉西林钠他唑巴坦钠也有一定的骨髓抑制反应[13-15];③前期用药以治疗用药为主,针对性纠正措施干预较少。故而在治疗3 周左右骨髓抑制较为明显,贫血明显,又需加用FOS 抗CMV,该药也可能导致血红蛋白降低,故为保证联合用药的安全有效,需采取输血,口服中药制剂来改善贫血状态,给予人粒细胞刺激因子升粒细胞,保证患者治疗安全。
另需注意,几乎所有的抗生素会促使梭菌过度生长,使结肠内的正常菌群紊乱,进而导致伪膜性结肠炎。本例为CMV 肠炎,治疗好转后仍需密切关注大便次数和便血状况,一旦病情发生反复,应当及时采取停用或更换抗生素,及时止血,维持体液和电解质平衡及补充蛋白质等相应措施进行干预。
综上所述,CMV 感染作为AIDS 患者常见的机会性感染之一,应当引起重视,临床药师应关注抗CMV 药物的选择、药物之间的相互作用及不良反应等,与医师形成互补团队,辅助制订个体化用药方案,为患者提供更好的药学服务。

