轻度亚低温治疗中重度成人ARDS 患者的疗效与安全性分析
段成飞
(河南省清丰第一医院重症医学科 清丰 457300)
急性呼吸窘迫综合征(ARDS)是一种以进行性低氧血症、呼吸窘迫为特征的临床综合征,多因严重创伤、感染、烧伤等因素造成肺泡上皮细胞和肺毛细血管内皮细胞受损,进而导致弥漫性肺间质和肺泡水肿[1]。ARDS 是临床常见的呼吸系统重症疾病,虽然近年来对于其的治疗取得一定进展,但其病死率仍高达四成[2]。体外膜肺氧合是临床治疗重症ARDS的有效措施,采用人工肺完成体外呼吸与循环,但并发症、费用等因素限制了其临床应用[3]。因此积极寻求安全、有效的治疗方案对于重症ARDS 患者来说具有重要意义。亚低温治疗是临床治疗新生儿缺血缺氧性脑病、重型颅脑损伤等脑疾病的常见治疗方案,其脑保护作用已得到广泛证实[4~5]。有学者指出,亚低温状态不仅可减缓机体代谢速率,还可抑制炎症反应,可有效治疗ARDS[6]。但由于临床将亚低温应用于ARDS 患者的研究鲜少开展,其有效性、安全性尚缺乏足够的证据支撑。基于此,本研究探讨轻度亚低温治疗中重度ARDS 的疗效及对氧代谢、血流动力学等指标的影响。现报道如下:
1 资料与方法
1.1 一般资料 选取2020 年12 月至2022 年11月清丰第一医院收治的78 例中重度成人ARDS 患者,按随机数字表法分为对照组和研究组,各39 例。对照组男 21 例,女 18 例;年龄 46~70 岁,平均年龄(52.87±6.16)岁;APACHEⅡ评分(18.62±3.24)分;氧合指数(PaO2/FiO2)(112.15±11.28)mm Hg。研究组男22 例,女17 例;年龄46~70 岁,平均年龄(52.73±6.25)岁;APACHEⅡ评分(18.56±3.31)分;PaO2/FiO(2113.66±11.19)mm Hg。两组一般资料均衡性良好(P>0.05)。本研究经清丰第一医院医学伦理委员会审查批准(批准文号:清丰第一医院伦理字20200608 号)。
1.2 入组标准 (1)纳入标准:年龄≤70 岁;符合ARDS 相关诊断标准[7],且被诊断为ARDS 未超过1 d;中重度即PaO2/FiO2低于150 mm Hg,呼吸末正压(PEEP)5 cm H2O 以上,吸入氧浓度(FiO2)不低于60%;接受机械通气治疗;患者或家属知情并自愿签署同意书。(2)排除标准:合并恶性肿瘤患;合并其他肺部或呼吸系统疾病;合并心血管疾病;合并血液系统、免疫系统疾病;血压需大剂量升压药维持。
1.3 治疗方法 两组患者均根据ARDS 病因进行对症治疗,对照组在此基础上采用常规治疗方案:给予呼吸机支持、器官保护、抗感染等,并将患者的核心温度(肛温)控制在37.5℃。研究组采用轻度亚低温治疗:即采用日成RC-2000 亚低温治疗仪(购自成都柏威斯科技有限公司)控制体温,2 h 将患者核心温度降至34.0℃,48 h 后开始复温,同时逐渐减少肌松药、镇静药的剂量,控制体温每4 小时上升1.0℃,12 h 恢复至正常范围(36.5℃~37.5℃);呼吸机设置:采用容量控制模式,小潮气量通气策略,即潮气量6 ml/kg,预测体质量;PEEP 初次设定12 cm H2O,后根据P-V 曲线低位拐点调整;目标气道平台压(Pplat)低于 30 cm H2O,若 Pplat>30 cm H2O,则逐步降低(每次调整1 ml/kg)潮气量,最低至4 ml/kg;同时将呼吸频率逐渐提高,最高不超过35次/min,调节FiO2水平以维持分钟通气量,维持血氧饱和度在95%左右,呼吸机参数根据血气分析进行调整。
1.4 观察指标 (1)临床指标:比较两组通气时间、入住ICU 时间及7 d 死亡率。(2)呼吸机监测指标:记录并比较两组治疗前、脱机时呼吸机监测指标,包括呼吸系统静态顺应性(Cst rs)、气道阻力、PEEP、Pplat。其中Cst rs=潮气量/(吸气末Pplat-呼气末总PEEP),气道阻力=(气道峰值压-Pplat)/吸气流量。(3)血流动力学指标:采用Mindray 便携式彩色多普勒超声系统Z5T(购自上海聚慕医疗器械有限公司)测定心脏指数(CI);采用微创血流动力学监护仪(购自上海涵飞医疗器械有限公司)对两组患者血流动力学指标进行监测,并比较两组治疗前、脱机时 CI、平均动脉压(MAP)、心输出量(CO)、每搏输出量(SV)。(4)氧代谢指标:比较两组治疗前、脱机时 PaO2/FiO2、氧输送(DO2)、氧消耗(VO2)、氧摄取率(O2ER)。DO2=动脉氧含量(CaO2)×CI,VO2=[CaO2-静脉氧含量(CvO2)]×CI,O2ER=VO2/DO2。
1.5 统计学方法 采用SPSS24.0 软件进行数据处理。计量资料以()表示,采用独立样本t检验;计数资料用%表示,采用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组临床指标对比 研究组通气时间、入住ICU 时间均短于对照组(P<0.05);两组 7 d 死亡率相比,差异无统计学意义(P>0.05)。见表1。
表1 两组临床指标对比()

表1 两组临床指标对比()
组别 n 通气时间(d)入住ICU 时间(d)7 d 死亡[例(%)]对照组研究组t/χ2 P 39 39 4.85±1.24 4.03±1.02 3.189 0.002 5.37±1.53 4.22±1.11 3.799 0.000 5(12.82)6(15.38)0.106 0.745
2.2 两组呼吸机监测指标对比 脱机时两组Cst rs均升高,PEEP、Pplat 均降低(P<0.05),且研究组Cst rs 高于对照组,PEEP、Pplat 低于对照组 (P<0.05);脱机时研究组气道阻力与对照组相比,差异无统计学意义(P>0.05)。见表2。
表2 两组呼吸机监测指标对比()

表2 两组呼吸机监测指标对比()
注:与本组治疗前相比,*P<0.05。
Pplat(cm H2O)治疗前 脱机时对照组研究组组别 n Cst rs(ml/cm H2O)治疗前 脱机时气道阻力[cm H2O/(L·s-1)]治疗前 脱机时PEEP(mm Hg)治疗前 脱机时39 39 t P 28.56±3.46 28.15±3.52 0.519 0.605 32.25±3.57*37.15±4.02*5.692 0.000 6.83±1.59 6.78±1.64 0.137 0.892 7.37±1.85 7.46±1.88 0.213 0.832 16.94±2.16 17.07±2.13 0.268 0.790 9.13±1.46*6.26±1.39*8.891 0.000 26.48±2.24 26.75±2.29 0.526 0.600 16.54±2.03*12.25±1.96*9.494 0.000
2.3 两组血流动力学对比 脱机时两组MAP、CI、CO、SV 与治疗前相比,差异无统计学意义(P>0.05);脱机时两组 MAP、CI、CO、SV 相比,差异无统计学意义(P>0.05)。见表3。
表3 两组血流动力学对比()

表3 两组血流动力学对比()
SV(ml/beat)治疗前 脱机时对照组研究组组别 n MAP(mm Hg)治疗前 脱机时CI[L/(min·m2)]治疗前 脱机时CO(L/min)治疗前 脱机时39 39 t P 71.24±6.25 72.53±6.17 0.917 0.362 70.54±6.13 70.02±6.20 0.373 0.711 3.06±0.56 3.12±0.52 0.490 0.625 2.97±0.49 3.01±0.54 0.343 0.733 4.15±1.03 4.19±1.07 0.168 0.867 4.09±0.99 4.11±1.00 0.089 0.930 64.29±15.32 63.89±14.96 0.117 0.907 62.23±15.16 61.37±14.86 0.253 0.801
2.4 两组氧代谢指标对比 脱机时研究组和对照组 PaO2/FiO2较脱机前均升高,VO2、O2ER 均降低,且研究组 PaO2/FiO2高于对照组,VO2、O2ER 低于对照组,差异有统计学意义(P<0.05);脱机时研究组DO2与对照组相比,差异无统计学意义(P>0.05)。见表4。
表4 两组氧代谢指标对比()
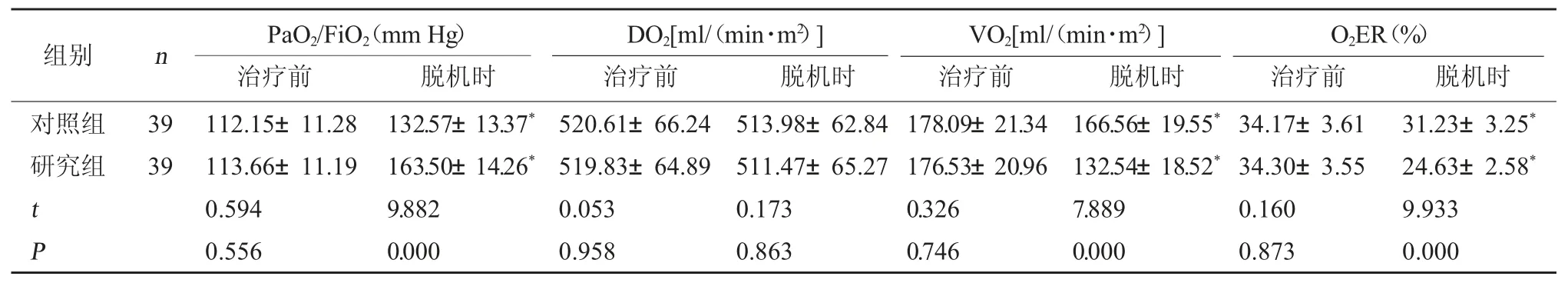
表4 两组氧代谢指标对比()
注:与本组治疗前相比,*P<0.05。
O2ER(%)治疗前 脱机时对照组研究组组别nPaO2/FiO2(mm Hg)治疗前 脱机时DO2[ml/(min·m2)]治疗前 脱机时VO2[ml/(min·m2)]治疗前 脱机时39 39 t P 112.15±11.28 113.66±11.19 0.594 0.556 132.57±13.37*163.50±14.26*9.882 0.000 520.61±66.24 519.83±64.89 0.053 0.958 513.98±62.84 511.47±65.27 0.173 0.863 178.09±21.34 176.53±20.96 0.326 0.746 166.56±19.55*132.54±18.52*7.889 0.000 34.17±3.61 34.30±3.55 0.160 0.873 31.23±3.25*24.63±2.58*9.933 0.000
3 讨论
ARDS 肺是不均质的,处于重力依赖区的肺泡大量坍陷,而处于重力依赖区外的肺泡则与之相反,发生膨胀,致使通气/血流比例失衡,因此采用间断肺复张+高PEEP 的肺开放通气策略,促使坍陷肺泡开放[8]。同时,由于ARDS 肺又称小肺或婴儿肺,为避免重力依赖区外的肺泡发生过度膨胀,需小潮气量通气,并对Pplat 进行限制。但在临床应用中,肺开放策略仅可在PEEP 和潮气量中选择一个进行设置,但无论是PEEP 还是潮气量都无法适用所有肺泡[9]。因此,常规通气策略对于临床重症ARDS 的治疗效果欠佳,其病死率仍居高不下。
基于肾脏替代疗法的理念,肺休息策略被提出并应用于临床,通过体外膜肺氧合实现体外呼吸与循环,在保证氧输送的前提下降低呼吸频率和潮气量,进而达到减轻肺负担、让肺休息的目的[10~11]。但由于并发症、费用等因素,该方法无法做到全面推广应用。近年来,有学者提出一种新型“肺休息”治疗方案,即轻度亚低温治疗,该疗法可降低机体代谢,改善肺部炎症反应状态,从而减轻肺部负担[12]。本研究结果显示,研究组通气时间、入住ICU 时间均短于对照组,脱机时研究组Cst rs、PaO2/FiO2均高于对照组,PEEP、Pplat、VO2、O2ER 均低于对照组,提示轻度亚低温治疗中重度成人ARDS 可有效缩短患者脱机时间,且有助于肺功能和氧代谢的改善。究其原因在于,机体亚低温状态可有效阻断细胞因子瀑布效应,对肺部乃至全身炎症反应都具有抑制作用;并可对肺泡上皮细胞、肺毛细血管内皮细胞通透性起到调节作用,减少渗出,避免肺泡大量塌陷,增加肺功能残气量,增强气体弥散功能,进而改善Cst rs 和PaO2/FiO2[13~14]。同时在容量控制通气模式下,维持潮气量不变而Cst rs 改善,肺应力降低,肺部炎症、重力依赖区外的肺泡过度膨胀可得到有效缓解,进而促使Cst rs、肺通气/血流比增加,形成良性循环[15]。机体在亚低温状态下代谢降低,机体耗氧量也随之降低,肺功能负担减轻,使氧的供需平衡得到优化调整,有助于改善全身微循环,也可降低呼吸机相关性肺损伤的发生风险[16~17]。
亚低温治疗可引发心律失常、肌颤、循环不稳定等并发症,且并发症风险随着温度的降低而升高[18]。本研究结果显示,脱机时两组 MAP、CI、CO、SV 差异不显著,提示轻度亚低温治疗中重度ARDS 对于血流动力学无明显影响,安全性较高,但更低温度对于ARDS 患者血流动力学是否有影响需进一步探讨。另外,本研究结果显示,两组7 d 死亡率相比差异不显著,可能与本研究样本数量过少等因素有关。
综上所述,轻度亚低温治疗中重度成人ARDS可有效缩短患者脱机时间,有助于肺功能和氧代谢的改善,且对于血流动力学无明显影响。

