昆虫细胞无血清培养的研究进展及应用
黎宏 郭清源 郭拉杨 扶星星


摘 要:随着生物工程技术的快速发展,细胞工程愈来愈受到重视。昆虫细胞培养技术作为生物工程的新领域,在现代生物学上具有重要的价值,其中以昆虫杆状病毒为载体,以昆虫细胞为受体的基因工程研究也取得了突破性的进展。体外培养的昆虫细胞可以高效地表达外源基因,且昆虫杆状病毒具有对人畜无害等特点,使得昆虫细胞培养技术广泛地应用于生物学、医药学和农业等各个领域。本文综述了昆虫细胞培养的研究进展,其中包括了体外培养昆虫细胞培养基的基础成分及无血清培养基的添加物、生物反应器大规模培养昆虫细胞和昆虫杆状病毒表达载体系统及其应用,为昆虫细胞无血清培养基的研发提供了理论依据。
关键词:昆虫细胞;杆状病毒;无血清培养;大规模培养
中图分类号:Q813.1+1 文献标志码:ADOI:10.3969/j.issn.1007-7146.2023.03.002
Research Progress and Application of Serum-free Culture of Insect Cells
LI Hong, GUO Qingyuan, GUO Layang, FU Xingxing*
(Sichuan Benoji Technology Co., Ltd., Mianyang 621000, China)
Abstract: With the rapid development of the field of bioengineering, cell engineering has been paid more and more attention. Insect cell culture technology, as a new field of bioengineering, has important value in modern biology, among which the genetic engineering research using insect baculovirus as the carrier and insect cells as the receptor has also made breakthrough progress. Insect cells cultured in vitro can express foreign genes efficiently, and insect baculoviruses are harmless to humans and animals, which makes insect cell culture technology being widely used in various fields such as biology, medicine and agriculture. In this paper, the research progress of insect cell culture is reviewed, including the basic components of insect cell culture medium in vitro, the addition of unclear medium, the bioreactor for the large-scale culture of insect cellss and the vector system of insect baculovirus expression and its application. It provides a theoretical basis for the development of serum-free culture medium for insect cells.
Key words: insect cells; baculovirus; serum-free culture; mass cell culture
(Acta Laser Biology Sinica, 2023, 32(3): 200-207)
昆蟲细胞培养始于1915年,理查德·戈德施密特[1]使用惜比古天蚕蛾(Hyalophora cecropia)的精子进行体外培养并成功保持了惜比古天蚕蛾的精子活性,但是由于没有适合的培养基用于细胞体外培养,所以没有看到细胞分裂;1962年Grace建立了世界上第一个细胞系[2],昆虫细胞系的建立工作开始在世界范围内广泛的开展。昆虫细胞体外培养越来越受到人们的重视,其原因主要在于昆虫多角体病毒(insect polyhedral virus)可以高水平地表达蛋白,也可以用其基因片段来构建重组病毒,高效表达外源基因,生产某些药用蛋白[3];此外,杆状病毒可以引起昆虫流行病,但对人畜和植物无害。所以昆虫细胞体外培养正广泛应用于疫苗开发、基因治疗、外源蛋白筛选等领域。目前已经建立了很多的昆虫细胞系,其中研究和应用最多的昆虫细胞系是草地贪叶蛾(Spodoptera frugiperda)卵巢细胞系Sf21及其分离株Sf9和粉纹夜蛾[Plusiani (Hubner)]胚胎细胞系High Five[4]。
1 昆虫细胞培养基
细胞培养基既为细胞提供了生长和繁殖的生存环境,也提供了细胞生长和增殖过程中所需的营养物质[5]。糖类是大部分昆虫细胞主要的碳源和能源物质,昆虫细胞生长虽然也能利用部分蔗糖,但是蔗糖在培养基中的主要作用是调节渗透压。维生素是维持细胞生长的一类重要生物活性物质,除了在细胞中形成酶的辅基或辅酶外,还对促进昆虫细胞生长和黏附具有积极作用。不同种类的昆虫细胞对氨基酸的需求是不一样的,其中有14种氨基酸是细胞本身不能合成,只能由培养基提供的。几乎所有的昆虫细胞对谷氨酰胺(glutamine)都有较高的要求。谷氨酰胺是细胞合成核酸和蛋白质的重要材料,但是昆虫细胞自身合成的谷氨酰胺没有直接从培养基中摄取有效,所以昆虫细胞培养基中都含有较高浓度的谷氨酰胺[6]。昆虫细胞需要较高浓度的渗透压,所以昆虫细胞培养基中的无机盐浓度较高,且各无机盐离子之间需要平衡,如某些细胞系对Na+/K+的比例有严格要求。此外,一般认为泛酸(pantothenic acid)、异己酸(isocaproic acid)、乙酸(acetic acid)、核黄素(lactochrome)对细胞的存活是有利的,而胆碱(bilineurine)、吡哆醇(pyridoxol)、维生素B1(vitamin B1)、烟酰胺(nicotinamide)可促进细胞增殖。对昆虫细胞新陈代谢的研究为设计开发适合昆虫细胞生长增殖的培养基提供了基本的理论依据,同时,设计合理的培养方案对实现高产量的杆状病毒表达是十分重要的。
2 昆虫细胞无血清培养基的添加物
昆虫细胞培养技术发展很快,在经历了天然培养基、合成培养基等阶段后,无血清培养基成为昆虫细胞培养基的发展趋势。虽然血清对细胞的生长增殖具有很好的促进作用,但是使用血清存在很多问题[7]:血清的成本高,来源有限,无法大量使用;不同批次生产的血清质量差别很大;血清的成分复杂且不明确,对后期产物的分离、提纯及检测造成一定影响;同时,血清是支原体和其他病毒污染的重要来源。而无血清培养基是不添加动物来源血清或其他生物提取液,但仍可以维持细胞在体外较长时间生长、繁殖的培养基。所以无血清培养基具有化学成分明确、较小的批间差异、减少了外源污染的风险、有利于细胞培养产物的分离纯化、降低了成本等区别于有血清培养基的优点[8]。
血清成分复杂,发展无血清培养基,必需寻找适当的具有类似于血清功能的因子,但是想要找到血清的替代物是相当困难的[9]。目前,大多数商品化的无血清培养基价格较贵,且仅有液体供应,导致此类培养基的保存和应用都受到影响;而且大多数商品化的无血清培养基都含有水解乳蛋白(hydrolyzed milk protein)、酵母提取物和脂类复合物等生物活性物质,虽然其成分相对稳定,但依然不明确,对于其中一些添加物的成分和作用机理还不够了解。因此,还需加深细胞代谢及各成分的作用机理的研究,找到适合的成分明确的替代物。迄今为止,人们已经发现许多因子单独或一起使用可以替代血清,其中水解乳蛋白和酵母提取物是昆虫细胞培养基中最常用的添加物质。水解乳蛋白是氨基酸的主要来源,酵母提取物是维生素和嘌呤碱基的主要来源。激素和生长因子有利于维持细胞生存和增殖,如雌二酮、孕酮等是无血清培养基中经常添加的补充因子,胰岛素与细胞上的胰岛素受体结合后可促进RNA、蛋白质和脂肪酸的合成,抑制细胞凋亡,是重要的培养基添加物。在培养基中添加结合蛋白也是很有必要的。经常添加的结合蛋白是转铁蛋白和白蛋白,其中转铁蛋白可以促进细胞生长,白蛋白可以结合毒素和减轻蛋白酶对细胞的影响,还可以通过与维生素、脂类、金属离子、激素、生长因子[10]结合,调节和稳定其在培养基中的活性作用。另外,微量元素也是细胞代谢所必需的,是细胞体外培养的重要添加因子,可以促进细胞黏附和增加细胞的终产量。在含有血清的培養基中,微量元素主要由血清提供,所以在研究无血清培养基时应添加适当的微量元素。昆虫细胞所需的微量元素主要包括Fe2+、Mn2+、Cu2+、Zn2+、Al3+等,其中Fe2+、Mn2+、Cu2+、Zn2+、Al3+能促进细胞黏附和增加细胞的终产量,Al3+和Zn2+可以促进病毒的感染和复制[11]。
3 生物反应器大规模培养昆虫细胞
自1956年Waytt发明昆虫组织培养液以来,昆虫细胞培养规模不断地扩大,由最开始的静止培养,发展到摇瓶培养,乃至大规模生物反应器[12]。大规模生物反应器培养细胞的两种基本培养模式是悬浮培养和固定化培养[13]。细胞培养的操作方式在很大程度上取决于生物反应器的细胞培养模式,高效的培养方法是昆虫细胞大规模培养的关键[14]。昆虫细胞的培养方法与哺乳动物细胞的培养方法基本相似,相对于哺乳动物细胞,昆虫细胞更耐剪切力,而且培养过程中不需要CO2,但昆虫细胞在培养过程中需氧量很高,大量输氧操作如搅拌、喷气等都是必需的。但这些操作产生的剪切力往往会引起细胞的损伤和死亡,并且已经成为限制昆虫细胞大规模培养的关键因素。想要提高悬浮培养的昆虫细胞密度,需要从生物反应器的设计、氧气转运、剪切力的强弱、细胞接种密度、培养基组分等多个方面考虑[15],这些敏感性问题的解决直接影响昆虫细胞的大规模培养效果。而病毒感染复数、病毒感染时间、细胞密度等则是影响杆状病毒表达系统高效表达的关键因素[16]。张艳艳等[17]在昆虫细胞-杆状病毒系统分泌表达的猪瘟病毒E2蛋白及其免疫原性的研究中,采用CSFV石门强毒株(Rb-E2)来表达CSFV E2蛋白,细胞在72 ~ 96 h发生病变,之后再按10%的比例扩增;7 d后测得病毒滴度为107.8 TCID50 /mL;用病毒感染复数为2的量进行转染,96 h收获的蛋白质量浓度为50 ?g/mL。最理想的生物反应器培养方式应既能提高细胞密度又能增加表达产物,还能够降低生产成本。
4 昆虫杆状病毒表达载体系统
昆虫杆状病毒表达载体系统是以昆虫杆状病毒为外源基因载体,以昆虫和昆虫细胞为受体的表达系统[18]。表1列举了一些杆状病毒宿主细胞的来源及应用。昆虫杆状病毒表达系统是目前国内外广泛应用的真核表达系统,是利用杆状病毒结构基因中多角体蛋白的强启动因子构建的表达系统,可以使很多真核目的基因得到高水平表达[19]。
相对于以大肠杆菌为代表的原核表达系统和包括酵母和哺乳动物在内的真核表达系统,昆虫杆状病毒作为外源基因表达载体的优势在于:杆状病毒基因组较小,分子生物学特性比较简单,并且基因组上有多种限制性内切酶酶切位点,易于操作;同时,杆状病毒的病毒粒子是杆状的,容纳外源基因的可塑性比较强,理论上它能容纳任何外源基因;此外,杆状病毒基因中p10基因和多角体蛋白基因都是极晚期基因,它们的启动子能够高效地表达目的蛋白;杆状病毒的宿主为昆虫细胞,目的蛋白可以利用昆虫细胞的翻译后修饰系统进行加工和修饰;杆状病毒表达载体特异性非常强,只能够在昆虫细胞中进行复制,安全性高。与哺乳动物细胞比较,昆虫培养细胞系相对更容易生长,而且昆虫杆状病毒表达载体系统既可采用不同的重组病毒同时感染细胞的形式,也可以采用在同一载体上同时克隆多个外源基因的形式[21]。
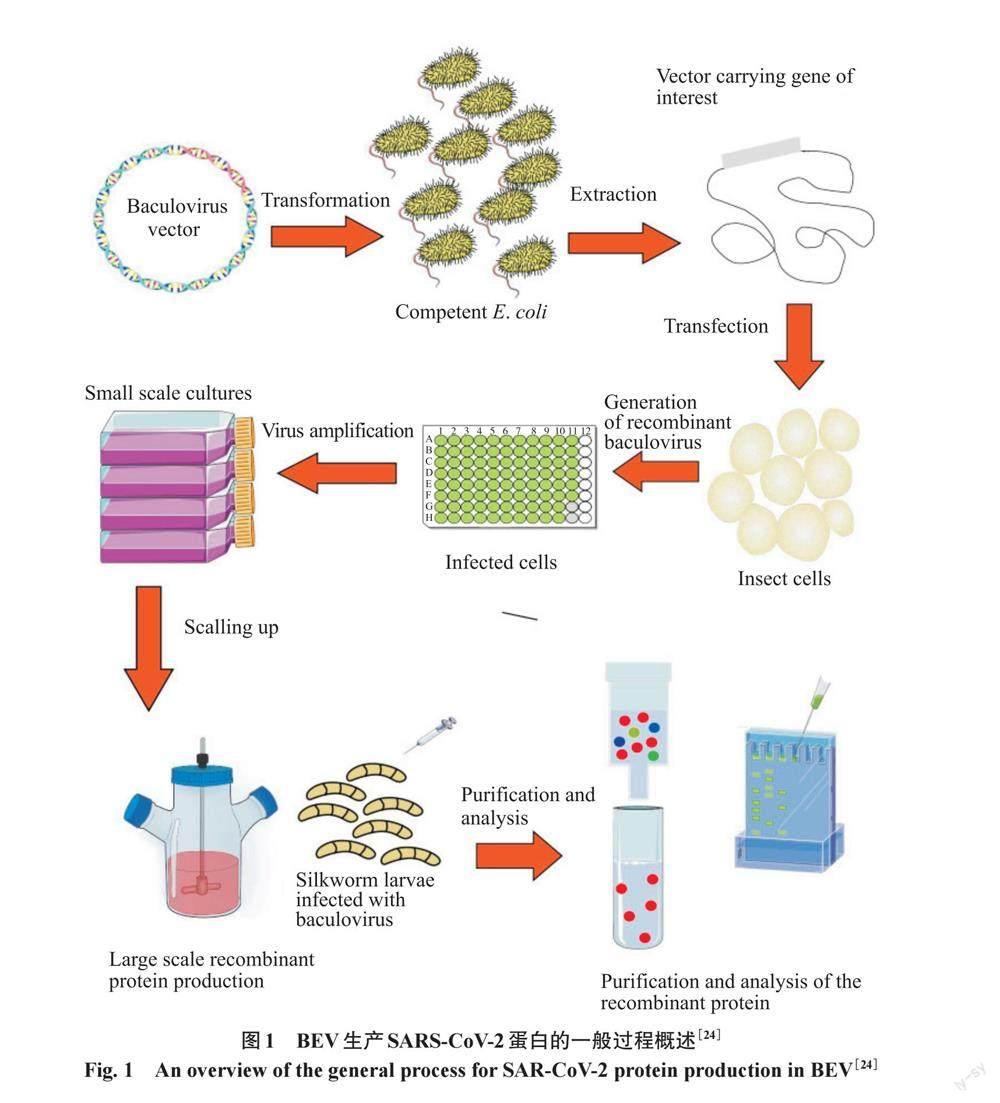
目前使用最为广泛的昆虫杆状病毒表达系统是杆状病毒-昆虫细胞系统(Bac-to-Bac系统[22-23])。该系统由美国Gibcobrl公司开发,是一个由杆状病毒表达载体和宿主两个部分组成的二元系统,其中,杆状病毒表达载体主要有两个功能:一个功能是将编码目标蛋白质的外源基因导入宿主细胞中;另一个功能是为在晚期或极晚期启动子控制下的目标基因的转录提供所需的转录复合物。宿主通常是鳞翅类昆虫细胞系,有时是鳞翅类的昆虫。Bac-to-Bac杆状病毒表达载体系统需要先在大肠杆菌系统中生产重组病毒,筛选纯化后再转染昆虫细胞。如图1所示:杆状病毒载体系统(baculovirus expression vector system,BEV)生产SARS-CoV-2蛋白的过程中,编码SARS-CoV-2蛋白的杆状病毒载体被转化至感受态大肠杆菌,在大肠杆菌中发生了易位,编码SARS-CoV-2蛋白的基因从供体质粒转移到宿主质粒,而该质粒从大肠杆菌中提取,用于转染昆虫细胞,生成重组杆状病毒;重组杆状病毒进一步扩增,扩大重组蛋白的产量,在生物反应器或蚕幼虫中生产大量的蛋白质,最后在对蛋白质进行纯化和分析之后进行各种应用。
与其他3种传统的基因工程表达系统相比(表2),昆虫细胞杆状病毒表达系统虽然有自己的特点和优势,但仍存在不足:昆虫细胞表达系统是一个瞬时表达系统,且表达载体的启动子为晚期启动子,表达时限是从感染后的22~24 h开始到宿主细胞死亡,蛋白高水平表达时间很短;昆虫细胞一般不提供复杂的N-糖基化,虽然这种类型的N-糖基化通常足以提供有生物活性的蛋白产物,但是末端缺乏复杂糖基化有可能影响蛋白的溶解性和稳定性;杆状病毒高水平表达蛋白的同时会致使细胞翻译后修饰的速度跟不上表达的速度,可能会降低产生表达后修饰蛋白;目前昆虫细胞多采用无血清培养基培养,但由于没有血清蛋白的保护,产物水解问题严重。
5 昆虫杆状病毒表达系统的应用
基于昆虫杆状病毒表达系统[26]自身的特点和优势,它被广泛应用于药物研发、疫苗生产、重组病毒杀虫剂等众多领域(图2为杆状病毒技术的主要应用示意图)。
由于昆虫杆状病毒表达载体系统具有重组蛋白表达量高、适合大规模生产等优势,其在疫苗研发领域也获得了广泛应用[27]。已有批准文号的相关疫苗产品有猪瘟E2蛋白重组杆状病毒灭活疫苗、兔病毒性出血症杆状病毒载体灭活疫苗、猪圆环病毒2型猪肺炎支原体二联灭活疫苗、猪圆环病毒2型杆状病毒载体灭活疫苗和水貂肠炎病毒杆状病毒载体灭活疫这5种,其具体申报的厂家和批准时间如表3所示。
正在申报临床的相关疫苗产品有32个,其中包括:瑞普生物申报的猪圆环病毒2型杆状病毒载体、猪肺炎支原体、副猪嗜血杆菌三联灭活疫苗;齐鲁动保申报的兔病毒性出血症病毒杆状病毒载体、多杀性巴氏杆菌病二联灭活疫苗;齐鲁动保、天康生物、吉林和元、华威特和大北农申报的猪圆环病毒2型杆状病毒载体灭活疫苗等疫苗产品(表4)。
另一方面,由于昆虫杆状病毒对许多害虫比较敏感,将其作为微生物杀虫剂具有优越的性能。其作用机理如图3所示:通过线粒体途径诱导细胞凋亡,通过DNA损伤诱导细胞周期阻滞,通过mTOR途径诱导自噬或诱导昆虫细胞坏死。将昆虫杆状病毒作为杀虫剂具有以下2点优势:1)对人畜、环境等其他非目标昆虫的影响很小,是生产绿色食品必不可少的生物农药;2)昆虫杆状病毒产生的包含体具有侵染性病毒颗粒,不仅对环境中的生物稳定性具有一定的作用,而且也便于使用传统技术来制造和应用。
6 总结与展望
昆虫细胞培养基的发展相对于哺乳动物培养基起步较晚,但随着昆虫细胞培养技术、基因工程和分子生物技术突飞猛进的发展,昆虫细胞系已被越来越广泛地应用于各个研究领域。随着昆虫细胞大规模培养和无血清培养研究的不断深入,昆蟲细胞的规模化和低成本培养成为可能。昆虫无血清培养基不仅可以降低成本,还减少了异源物污染的可能性,具有很好的发展前景。要使昆虫细胞培养技术在基础研究和产业化方面得到更广泛的应用,需要从以下2个方面开展工作:其一,开发生物反应器大规模培养工艺技术,并提高产物表达量;其二,研制低成本昆虫细胞无血清培养基,进一步降低培养成本,低成本无血清培养基的设计开发要以成分明确、批间差异小、稳定性高、产物效率高、易纯化为目标,向着无蛋白、无动物源组分、广谱的细胞应用范围的方向发展。
参考文献(References):
[1] 李守信, 李长友, 郑桂玲, 等. 昆虫细胞培养研究进展[J]. 西北农业学报, 2005, 14(3): 41-48.
LI Shouxin, LI Changyou, ZHENG Guiling, et al. Progress in insect cell culture[J]. Journal of Northwest Agriculture, 2005, 14(3): 41-48.
[2] SMAGGHE G, GOODMAN C L, STANLEY D. Insect cell culture and applications to research and pest management[J]. In vitro Cellular & Developmental Biology-Animal, 2009, 45(3/4): 93-105.
[3] 刘春菊, 任炜杰, 王志亮. 杆状病毒表达系统在兽用亚单位疫苗领域应用的研究进展[J].中国畜牧兽医, 2013, 40(9): 101-105.
LIU Chunju, REN Weijie, WANG Zhiliang. Progress in the application of baculovirus expression system in the field of veterinary subunit vaccine[J]. Chinese Animal Husbandry and Veterinary Medicine, 2013, 40(9): 101-105.
[4] 李雪菲, 袁琳, 胡海斌, 等. 杆状病毒表达系统研究进展[J]. 生物学杂志, 2005, 22(6): 8-10.
LI Xuefei, YUAN Lin, HU Haibin, et al. Progress in baculovirus expression system[J]. Journal of Biology, 2005, 22(6): 8-10.
[5] 张松, 乔自林, 王家敏. 无血清培养基的研究进展[J]. 江西畜牧兽医杂志, 2018(1): 4-8.
ZHANG Song, QIAO Zilin, WANG Jiamin. Advances in serum-free media [J]. Jiangxi Journal of Animal Husbandry and Veterinary Medicine, 2018(1): 4-8.
[6] 馬伟, 王家敏, 令世鑫, 等. 昆虫细胞无血清培养基研究进展[J]. 动物医学进展, 2016, 37(2): 101-104.
MA Wei, WANG Jiamin, LING Shixin, et al. Progress in serum-free medium of insect cells[J]. Advances in Animal Medicine, 2016, 37(2): 101-104.
[7] 张佑红, 朱雄伟, 陈燕. 昆虫细胞培养及其应用进展[J]. 武汉化工学院学报, 2006, 28(3): 20-24.
ZHANG Youhong, ZHU Xiongwei, CHEN Yan. Progress in insect cell culture and its application[J]. Journal of Wuhan University of Chemical Technology, 2006, 28(3): 20-24.
[8] 曹翠平, 吴小锋, 鲁兴萌. 昆虫细胞无血清培养[J]. 细胞生物学杂志, 2005, 27: 127-132.
CAO Cuiping, WU Xiaofeng, LU Xingmeng. Serum-free culture of insect cells [J]. Journal of Cell Biology, 2005, 27: 127-132.
[9] 顾涵英, 冯佑民. 无血清培养基及其主要补充因子[J]. 生物化学与生物物理进展, 1990, 17(4): 255-259.
GU Hanying, FENG Youmin. Serum-free medium and its main supplementation factors[J]. Biochemical and Biophysical Progress, 1990, 17(4): 255-259.
[10] HALTOM A R, JAFAR-NEJAD H. The multiple roles of epidermal growth factor repeat O-glycans in animal development[J]. Glycobiology, 2015, 25: 1027-1042.
[11] 余泽华, 刘冬连, 陈曲侯. 昆虫细胞无血清培养基的研究进展[J]. 生物工程进展, 1995, 39(11): 45-47.
YU Zehua, LIU Donglian, CHEN Quhou. Progress in serum-free medium of insect cells[J]. Bioengineering Progress, 1995, 39(11): 45-47.
[12] 赵利民, 蒋天华, 罗乃杰. 应用激流式生物反应器大规模悬浮培养昆虫细胞sf9的工艺研究[J]. 山东畜牧兽医, 2012, 33(8): 12-13.
ZHAO Limin, JIANG Tianhua, LUO Naijie. Process research of large-scale suspension culture of insect cells sf9 using torrent bioreactor[J]. Shandong Animal Husbandry and Veterinary Medicine, 2012, 33(8): 12-13.
[13] MEGHROUS J, AUCOIN M G, JACOB D, et al. Production of recombinant adeno-associated viral vectors using a baculovirus/insect cell suspension culture system: from shake flasks to a 20 L bioreactor[J]. Biotechnology Progress, 2005, 21(1): 154-160.
[14] THOMPSON C M, MONTES J, AUCOIN M G, et al. Recombinant protein production in large-scale agitated bioreactors using the baculovirus expression vector system[J]. Methods in Molecular Biology, 2016, 1350: 241-461.
[15] ELIAS C B, JARDIN B, KAMEN A. Recombinant protein production in large-scale agitated bioreactors using the baculovirus expression vector system[J]. Methods in Molecular Biology, 2007, 388: 225-246.
[16] MOTOHASHI T, SHIMOJIMA T, FUKAGAWA T, et al. Efficient large-scale protein production of larvae and pupae of silkworm by Bombyx mori nuclear polyhedrosis virus bacmid system[J]. Biochemical and Biophysical Research Communications, 2005, 326: 564-569.
[17] 张艳艳, 张静远, 廖发明, 等. 重组杆状病毒高效表达猪圆环病毒型蛋白及其免疫特性分析[J]. 中国生物制品学杂志, 2019, 32(1): 40-45.
ZHANG Yanyan, ZHANG Jingyuan, LIAO Faming, et al. Analysis of swine circovirus type 2 Cap protein by recombinant baculovirus and its immune profile[J]. Chinese Journal of Biological Products, 2019, 32(1): 40-45.
[18] CHAMBERS A C, AKSULAR M, GRAVES L P, et al. Overview of the baculovirus expression system[J]. Current Protein & Pepeide Science, 2018, 91: 541-546.
[19] 凌同. 昆蟲杆状病毒表达系统的研究进展与应用[J]. 微生物学免疫学进展, 2014, 42(2): 70-78.
LING Tong. Progress and application of the insect baculovirus expression system[J]. Progress in Microbiology Immunology, 2014, 42(2): 70-78.
[20] 荣芮, 李婷婷, 张玉云, 等. 昆虫杆状病毒表达载体系统在疫苗研究中的应用进展[J]. 生物工程学报, 2019, 35(4): 577-588.
RONG Rui, LI Tingting, ZHANG Yuyun, et al. Progress in the application of insect baculovirus expression vector system in vaccine research[J]. Journal of Bioengineering, 2019, 35(4): 577-588.
[21] TROMBETTA C M, MARCHI S, MONTOMOLI E. The baculovirus expression vector system: a modern technology for the future of influenza vaccine manufacturing[J]. Expert Review of Vaccines, 2022, 21(9): 1233-1242.
[22] 于永利. 昆虫杆状病毒表达载体系统与疫苗研制的年回顾[J]. 微生物学免疫学进展, 2015, 43(4): 1-15.
YU Yongli. A 30-year review of insect baculovirus expression vector systems and vaccine development[J]. Progress in Microbiology and Immunology, 2015, 43(4): 1-15.
[23] YE B, ZHAO Z, YUE D, et al. Construction of the antheraea pernyi (Lepidoptera: Saturniidae) multicapsid nucleopolyhedrovirus bacmid system[J]. Journal of Insect Science, 2020, 20(5): 5.
[24] AZALI M A, MOHAMED S, HARUN A, et al. Application of baculovirus expression vector system (BEV) for COVID-19 diagnostics and therapeutics: a review[J]. Journal of Genetic Engineering and Biotechnology, 2022, 20(1): 98.
[25] PIDRE M L, ARRIAS P N, AMOR?S MORALES L C, et al. The magic staff: a comprehensive overview of baculovirus-based technologies applied to human and animal health[J]. Viruses-basel, 2022, 15(1): 80.
[26] FELBERBAUM R S. The baculovirus expression vector system: a commercial manufacturing platform for viral vaccines and gene therapy vectors[J]. Biotechnology Journal, 2015, 10: 702-714.
[27] TARGOVNIK A M, SIMONIN J A, GREGORIO J M C, et al. Solutions against emerging infectious and noninfectious human diseases through the application of baculovirus technologies[J]. Applied Microbiology and Biotechnology, 2021, 105(21/22): 8195-8226.
[28] HE X, LU L, HUANG P, et al. Insect cell-based models: cell line establishment and application in insecticide screening and toxicology research[J]. Insects, 2023, 14(2): 104.

