酶联免疫捕获法检测耳鼻喉科患儿血清过敏原特异性IgE的价值
陈昕谊 彭东正
变态反应性疾病的诊断是治疗的依据。对普通的吸入性变应原,根据临床病史,结合皮肤测试和(或)过敏原特异性IgE(specific immunoglobulin E,sIgE)的测定,可以作出特异的变应原诊断[1]。sIgE 法是一种安全的检测指标,它不受患者的皮肤状况、药物使用历史的影响,能检出多种变态反应原,并在临床上得到广泛的应用[2]。长期以来,在临床上很少有可用于 sIgE 的定量测定,目前国内只有 Immuno CAP 系统。本系统应用荧光酶联免疫吸附测定(enzyme linked immunosorbent assay,ELISA)技术,是目前世界上对变应原sIgE 的“金标准”[3]。但是,由于采用的是进口设备,价格昂贵,难以在我国大规模推广。酶联免疫捕获法是一种全自动的全定量的变应原免疫吸附检测系统,它与传统的固相包被致敏原不同,它首先将血清中的 IgE 抗体被包覆于固相载体上的抗IgE 抗体捕获,在此基础上,添加了液相的变应原,以消除非 IgE 抗体的干扰,提高了检测的敏感性[4]。本研究选取广州市中西医结合医院2019 年3 月—2022 年2 月收治的耳鼻喉科患儿血清样本300 份,旨在探讨酶联免疫捕获法检测对耳鼻喉科患儿血清过敏原特异性IgE(sIgE)水平分析的价值。
1 资料与方法
1.1 一般资料
选取2019 年3 月—2022 年2 月广州市中西医结合医院收治的耳鼻喉科患儿300 例,纳入标准:(1)于本院耳鼻喉科就诊,且需进行过血液生化检验。(2)临床资料完整。(3)年龄≤18 周岁。排除标准:(1)入组前1 周有免疫抑制剂应用史。(2)因精神疾病或其他原因无法配合完成。本研究经医院伦理委员会审批,批准免除知情同意(批号20220132)。取患儿临床血液生化检验剩余血清进行过敏原特异性IgE 检测。基本资料中,患儿年龄2 ~18 岁,平均(11.5±2.4)岁。病程0.5 ~5 年,平均(2.3±0.4)年。
1.2 方法
取已知粉尘螨、户尘螨、狗毛屑、猫毛屑、艾蒿花粉、链格孢sIgE 抗体阳性血清高、中、低浓度各3 份,每份200μL,分装好后保存在-20℃冷冻,用前复溶。样品稀释液则不含任何过敏原的sIgE 抗体,保存在2 ~8 ℃冷藏。另取前述患者血清样本300 份,保存在2 ~8 ℃冷藏待用。
分别使用酶联免疫捕获法和Immuno CAP 系统对sIgE水平进行检验。其中,酶联免疫捕获法sIgE 抗体检测试剂盒购自苏州浩欧博生物医药有限公司,广州市中西医结合医院检验科全自动酶免仪则由深圳爱康生物科技有限公司生产。Immuno CAP 系统则由瑞典Phadia AB 公司生产的试剂盒以及全自动荧光免疫分析仪组成。相关操作均严格按照产品说明书进行。
1.3 观察指标
比较两种系统检验sIgE 水平的精密度、灵敏度、线性范围,并进行方法学对比。其中,精密度评价依据CLSIEPl5-A2 文件进行[5],酶联免疫捕获法检测对血清样本上述过敏原sIgE 分别检测,4 次/d,连续5 d,计算批内变异系数(coefficient of variation,CV)以及总CV%。灵敏度评价则对稀释液样本进行上述过敏原sIgE 分别检测,同一批内进行连续20 次测定,得到吸光度平均值以及标准差结果,使用定标曲线方程计算定量下限(limit of quantitation,LOQ)。线性范围评价则依据张秀明的方法进行[6],2 种方法对血清样本的过敏原sIgE 检测后,使用线性回归对定量结果进行分析,依照国际惯例,0.35 kU/L 作为结果阈值,小于该结果则判定为阴性,大于等于该结果则判定为阳性[5]。使用Kappa 分析对定性结果进行评价,同样依照上述国际标准。
1.4 统计学方法
研究数据全部导入SPSS 20.0 统计学软件包进行整理和分析,计量资料以(±s)表示,进行t检验;计数资料用n(%)表示,行χ2检验。定量数据使用线性回归分析,定性数据使用Kappa 一致性分析,以α=0.05 为检验标准,Kappa 分析标准为0.75。P<0.05 为差异有统计学意义。
2 结果
2.1 精密度比较
酶联免疫捕获法检测6 种过敏原sIgE 的批内CV 值均<7%,而总CV%<8%,根据产品说明书,以上指标均低于不精密度标准,酶联免疫捕获法检测的精密度可满足临床应用。见表1。
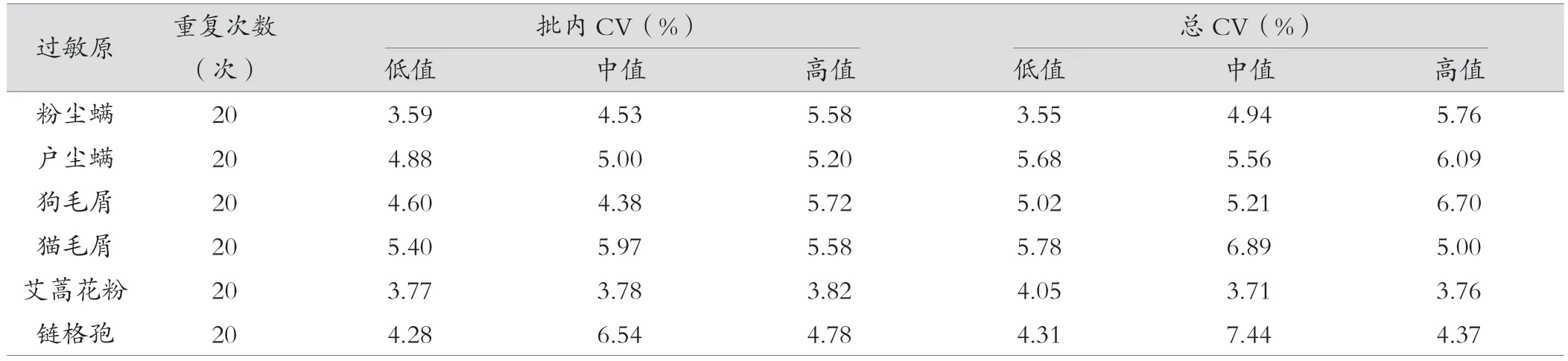
表1 酶联免疫捕获法检测的精密度
2.2 灵敏度比较
6 种过敏原的LOQ 值均<0.35 KU/L,均为阴性。见表2。
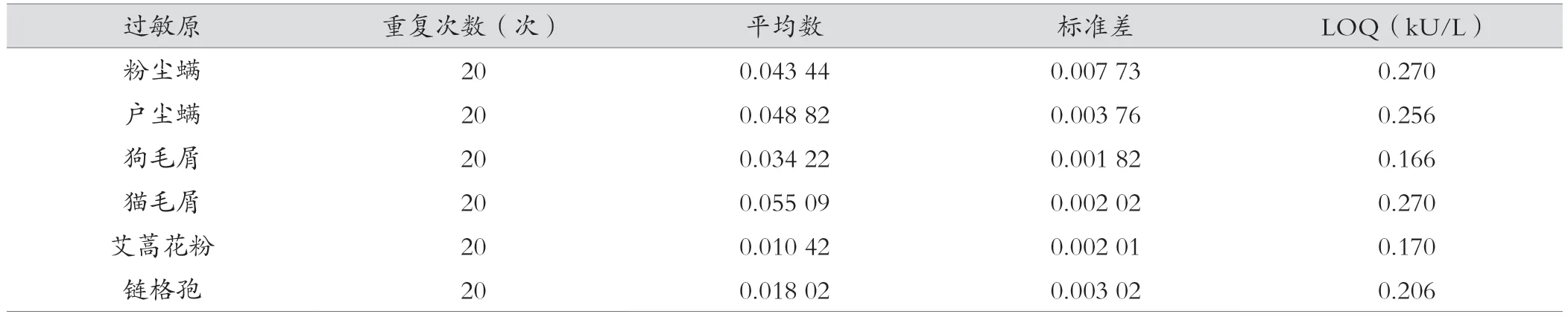
表2 酶联免疫捕获法检测的灵敏度(%)
2.3 线性范围比较
粉尘螨、户尘螨、狗毛屑、猫毛屑、艾蒿花粉、链格孢的样品范围浓度依次分别为:0.37 ~94.34 kU/L,0.35 ~89.43 kU/L,0.36 ~91.23 kU/L,0.35 ~93.35 kU/L,0.33 ~95.32 kU/L,0.36 ~85.64 kU/L,检测结果均无明显离群值。粉尘螨的相关系数为0.998,户尘螨的相关系数为0.999,狗毛屑的相关系数为0.986,猫毛屑的相关系数为0.991,艾蒿花粉的相关系数为0.990,链格孢的相关系数为0.989,均大于产品说明书的阈值0.975,线性范围良好。
2.4 两种检测方法比较
2.4.1 定量结果比较
不同过敏原的回归方程斜率差异均有统计学意义(P<0.05),两系统定量检测结果相关性较强。见表3。
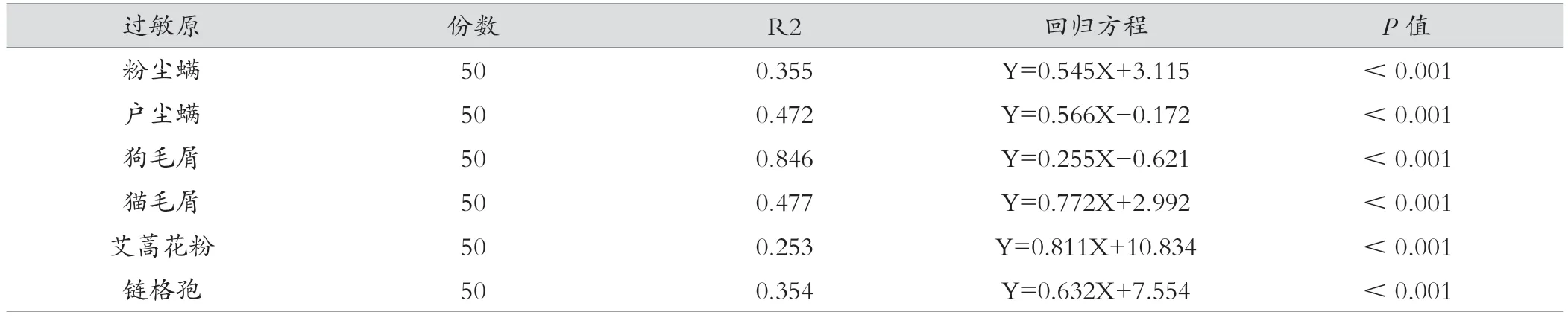
表3 两种检测方法定量结果比较
2.4.2 定性结果比较
两种检测方法的定性结果显示,阳性符合率均低于90%,其中以粉尘螨的阳性符合率最高,为86.00%,粉尘螨、猫毛屑和艾蒿花粉的阴性符合率并列第一,均为100%。综合来看,两种检测方法的阳性符合率为77.33%,阴性符合率为98.67%,Kappa 值为0.833,P<0.05。见表4。
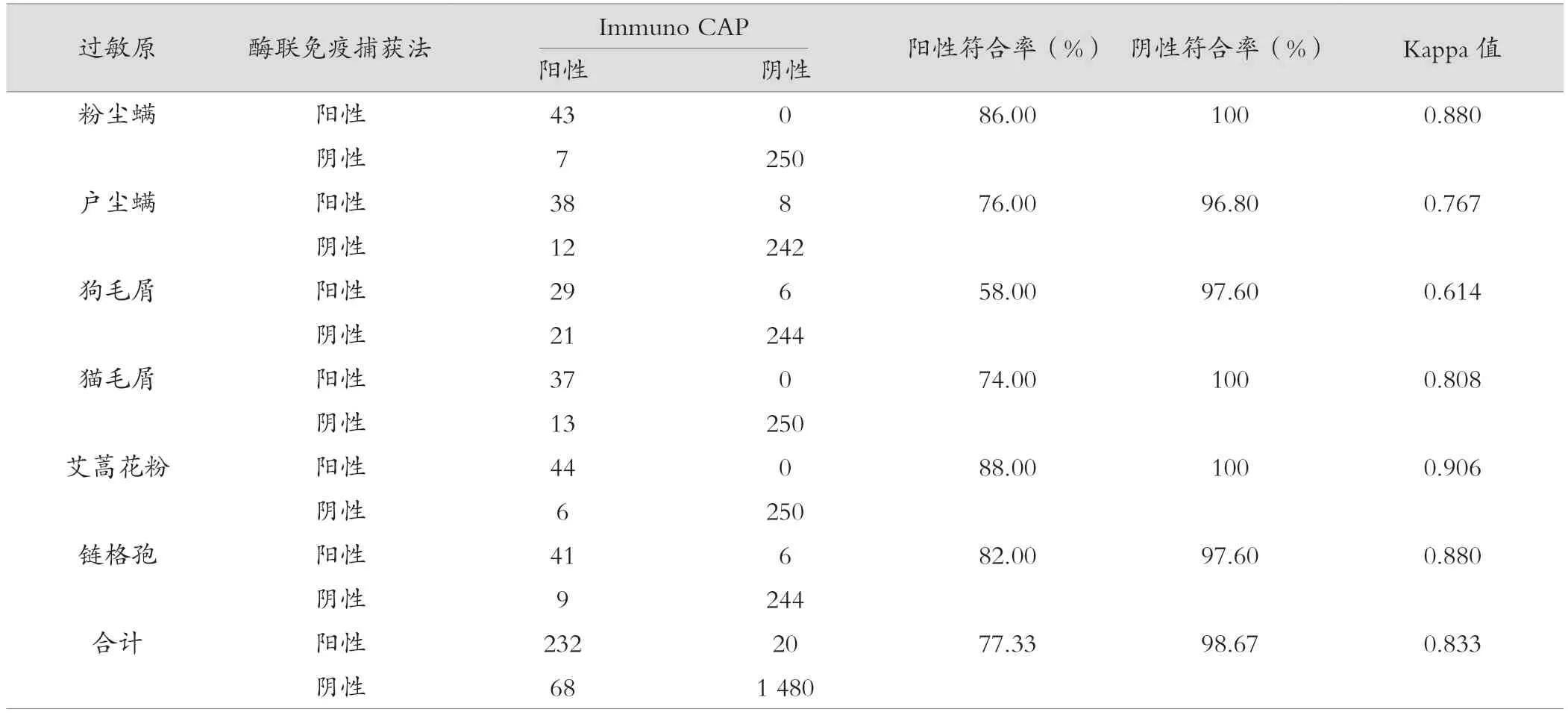
表4 两种检测方法定性结果比较
3 讨论
IgE 是一种特异的变应原诊断指标。长期以来,我国对过敏性原 sIgE 的测定大都是半定量的,不仅不能全面、准确地给出准确的诊断结果,而且大部分都是人工进行的;由于难以进行品质控制,难以确保试验结果的准确性和可靠性[7]。Immuno CAP 是目前世界上对过敏性原 sIgE 定量测定的“金标准”,国内20 多年前就引进了 Immuno CAP,本系统应用ELISA 技术,是目前世界上对变应原sIgE 的“金标准”。但是,由于采用的是进口设备,价格昂贵,难以在我国大规模推广。因此,在临床上,急需一种低成本的全自动定量分析方法[8]。酶联免疫捕获法是一种能够国产的全自动、全定量变应性 IgE 检测系统,同样采用 ELISA 技术,与传统的固相包被致过敏原不同,它首先将血清中的 IgE抗体被包覆于固相载体上的抗IgE 抗体捕获,在此基础上,添加了液相的变应原,以消除非 IgE 抗体的干扰,提高了检测的敏感性,以微孔板为固相载体,将抗人 IgE抗体引入到受检者的体内;充分捕获检测血清中 IgE 抗体,清除游离抗体,如 IgG,防止其他抗体与变应原发生竞争;然后,在液体中添加生物素变态反应源,将其与固定载体上的 sIgE 结合,形成“抗人IgE-sIgE-过敏原”这类免疫复合物,最后添加到链霉亲和素化的辣根过氧化物酶,并与底物进行显色反应。结果表明,样品中 sIgE 水平较高[9]。采用捕捉技术,不仅能有效地消除非 IgE 的干扰,而且能减少变态反应的用量,降低试剂的费用;利用生物素亲和素体系,可以有效地提高检测的敏感性[10]。
本研究对酶联免疫捕获法的性能进行了初步评价。对于6 种常见吸入物过敏原,低、中、高值样本的批内和总CV%均低于试剂盒标示不精密度。各种过敏原的定量测定下限不等,但均低于分析下限0.35 kU/L,符合厂商标示灵敏度。粉尘螨、户尘螨、狗毛屑、猫毛屑、艾蒿花粉、链格孢过敏原的相关系数均大于0.975,说明线性范围良好。
国际上对 sIgE 的定性标准是0.35 kU/L,在此数值以下时敏感性高于90%,但特异性却相对较低[11]。血清中 sIgE值>0.35 kU/L,说明患者对变应原的耐受性降低,暴露于变应原的发生率也会增加。本研究结果表明,6 个变应原的阴性符合率均大于阳性符合率,其中粉尘螨、猫毛屑和艾蒿花粉的阴性符合率并列第一,均为100%。阳性符合率粉尘螨最高,为86.00%;狗毛屑最低,为58.00%。
以上结果表明,Immuno CAP 与酶联免疫捕获法的预测值具有较好的相关性,但也存在一些差异。国外也有一些关于不同检测体系的 sIgE 测试结果的一致性,分析表明,主要是因过敏原原料的差异引起的[12]。过敏原的主要成分是过敏性提取物,主要由各种致敏性的蛋白质组成。笔者认为,在过敏原的选用上以主要致敏蛋白为主,其次是次要致敏蛋白;所有敏感蛋白均无组分丢失,并以合适的浓度保证了所有过敏患者的检测,并且量化的结果具备一定的临床相关性[13]。但由于植物、动物、微生物等来源因素的影响,其致敏性成分的含量和活性也因地理位置的不同与自然环境的改变而发生改变。目前,国内尚无完全变态反应原的标准,所有的原材料及诊断试剂制造商,均依靠自己的实验室对照品来进行品质管理。因此,不同的过敏原sIgE 检测体系难以取得完全一致的结果,需要临床医生对自己的测试体系有足够的认识,并根据临床情况做出适当的解释[14-15]。
综上所述,酶联免疫捕获法检测对耳鼻喉科患儿血清过敏原特异性IgE 水平的评价效能,具有较好的精密度与灵敏度,且与Immuno CAP 系统的相关性较好,作为一种自动化全定量检测手段,能够满足临床耳鼻喉科常见过敏原检验的要求,具有使用价值。此文的研究结果为儿童耳鼻喉科常见过敏性疾病的诊断和鉴别诊断后期标准制定提供了借鉴内容。

