盐酸达泊西汀片的体外溶出曲线相似性评价
郭巧兰 陈良梅 安 明
1.包头医学院药学院,内蒙古包头 014040;2.天士力研究院江苏天士力帝益药业有限公司,天津 300410
盐酸达泊西汀是用于治疗早泄的短效的5-色胺再摄取抑制剂[1],通过减少神经元对血清素的吸收[2]以及神经递质对细胞突触前和突触后受体之间电位差的影响来延缓早泄症状[3]。盐酸达泊西汀具有pH依赖性(pKa=8.6)[4],在中性溶液中的溶解度较低[5],在生物药剂学分类系统中属于Ⅳ类药物,溶出度成为药物吸收的限制环节[6],这类药物的体外溶出至关重要[7]。同时普通口服固体制剂给药后,药物在体内的溶解和释放对于药物的吸收起重要作用[8]。本研究考察盐酸达泊西汀片在不同溶出介质中的体外溶出曲线[9],并通过相似因子(ƒ2)法与参比制剂的溶出曲线进行相似性评价[10],为后续相关研究提供数据支持。
1 材料
1.1 仪器
7080DS自动溶出度仪(美国安捷伦科技有限公司);Cary60紫外分光光度计(美国安捷伦科技有限公司);XS105DU十万分之一电子天平[梅特勒-托利多仪器(上海)有限公司];S220 pH计[梅特勒-托利多仪器(上海)有限公司];TS-100C恒温摇床(上海天呈实验仪器制造有限公司)。
1.2 试药
盐酸达泊西汀原研片60 mg(德国美纳里尼集团杨森公司,批号:1800101);盐酸达泊西汀自制片60mg(天士力研究院,批号:D03、D04、D05、D06);盐酸达泊西汀原料药[广州市同晖化工有限公司,批号:2DPH(M)0060820];盐酸达泊西汀对照品(杭州国瑞生物科技有限公司,批号:WR20211202);甲醇(美国Supelco公司,色谱纯,批号:1148507118)
2 方法与结果
2.1 溶出介质制备
按照《普通口服固体制剂溶出度实验技术指导原则》[11]配制9种介质,分别为pH 1.0盐酸溶液、pH 4.5醋酸盐缓冲溶液、pH 5.0醋酸盐缓冲溶液、pH 5.5醋酸盐缓冲溶液、pH 5.8磷酸盐缓冲溶液、pH 6.0磷酸盐缓冲溶液、pH 6.4磷酸盐缓冲溶液、pH 6.8磷酸盐缓冲溶液及水。
2.2 对照品溶液的制备
精密称取27 mg盐酸达泊西汀对照品置于10 ml容量瓶中,加入甲醇稀释至刻度并摇匀,作为储备液。精密量取1 ml储备液置于100 ml容量瓶中,加相应溶出介质稀释至刻度,摇匀得到对照品溶液。
2.3 溶解度的测定
根据摇瓶法分别测定达泊西汀原料在pH 1.0、pH 4.5、pH 5.5、pH 5.8、pH 6.8和水6种介质中的饱和溶解度并绘制曲线,结果见图1。溶出介质pH在1.0~4.5时,达泊西汀呈现较高溶解度,该pH区间不同处方工艺自制片的体外溶出度较快,难以反映不同制剂工艺导致的自制片溶出度差异。溶出介质在pH 4.5~6.8时,原料药溶解度显著降低,因此可选择具有区分力的溶出条件以区分不同制剂工艺片剂对体外溶出度的影响。

图1 达泊西汀原料药的pH-溶解度曲线
2.4 方法学考察
2.4.1 检测波长的确定 精密称量处方中可能使用的辅料,分别加6种介质充分溶解并过滤,得到空白辅料溶液。在200~400 nm内对空白辅料溶液、空白溶剂和对照溶液进行紫外扫描。结果表明,盐酸达泊西汀在292 nm处有最大吸收峰,而空白溶剂和空白辅料溶液在292 nm处无明显吸收,所以选择292 nm为测定波长。
2.4.2 线性关系考察 精密量取适量的盐酸达泊西汀储备液置于100 ml量瓶中,用6种溶出介质稀释至刻度,分别配制成15、20、30、40、45 μg/ml的不同浓度对照品溶液。根据紫外分光光度法,测定不同浓度溶液在292 nm处的吸光度。以盐酸达泊西汀的质量浓度(x)为横坐标,吸光度(y)为纵坐标绘制标准曲线,得到回归方程,结果见表1,在15~45 μg/ml内呈良好线性关系。
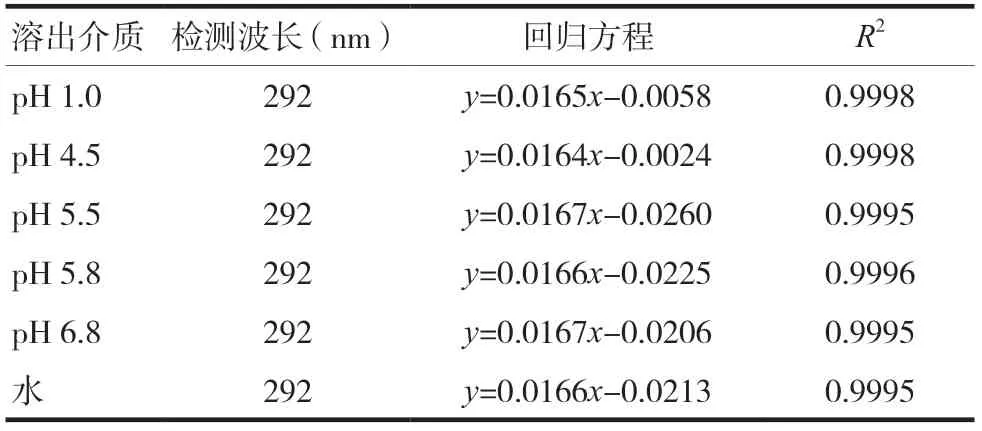
表1 不同溶出介质线性回归方程
2.4.3 精密度实验 取适量对照品溶液,用紫外分光光度法重复测定6次。RSD分别为0.29%、0.45%、0.36%、0.55%、0.63%和0.61%。结果表明,该仪器具有良好的精密度。
2.4.4 稳定性实验 取适量6种介质的对照品溶液,置于室温下0、2、4、6、8、12和24 h并测量吸光度。RSD分别为0.54%、0.38%、0.59%、0.41%、0.51%和0.46%,表明盐酸达泊西汀室温下24 h内在6种介质中具有良好的稳定性。
2.4.5 回收率实验 分别精密称取约21.6、27.3、30.0 mg的盐酸达泊西汀原料并置于10 ml容量瓶中,加甲醇稀释至刻度,摇匀并作为储备液。分别精密量取1 ml储备液放入100 ml容量瓶中,加入处方辅料,分别加入6种介质稀释至刻度,摇匀并过滤。根据紫外分光光度法测定292 nm处的吸光度值,计算盐酸达泊西汀回收率和RSD。3个浓度样品(80%、100%、120%)中的盐酸达泊西汀平均回收率在99.4%~99.7%,RSD分别为0.70%、0.48%、0.20%、0.28%、0.19%、0.32%,表明在6种介质中的盐酸达泊西汀回收率均良好。
2.5 溶出度测定
按《中华人民共和国药典》2015年版第4部分通则0931[12],溶出介质900 ml,取样时间为5、10、15、20、30、45和60 min,根据紫外分光光度法测定3批不同处方(批号:D03、D04、D05)自制片吸光度,计算平均累积溶出度并绘制溶出曲线,结果见图2~7。
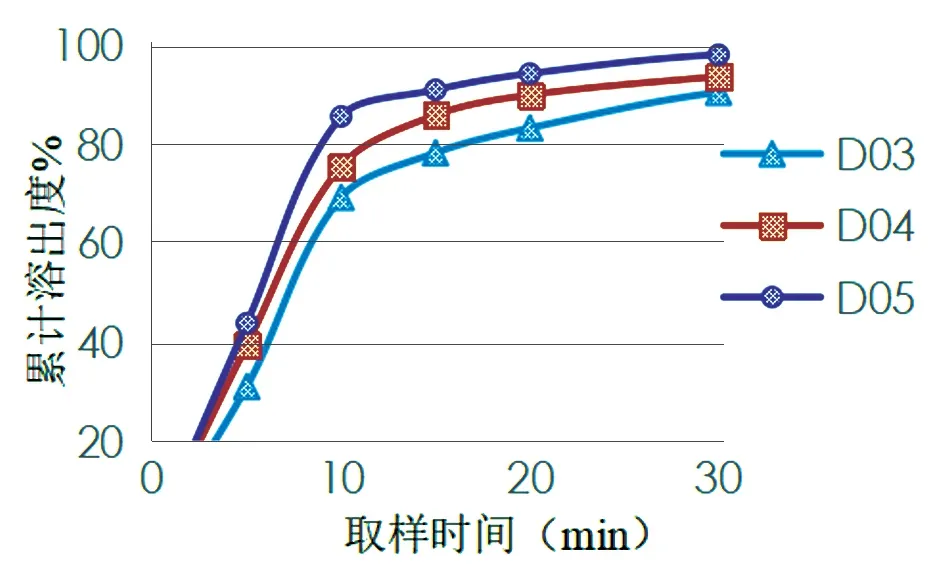
图2 pH 1.0介质中的3批自制片溶出曲线
2.6 溶出介质的区分力考察
为进一步考察溶出介质的区分力,在常见的4种介质评价中,加入了pH 5.5、pH 5.8两种介质,考察了3批工艺参数不同的自制片的溶出曲线相似性,结果见表2。由表可知6种介质均表现出D03批与D05批自制片溶出曲线的不相似以及D04批与D05批的溶出曲线相似性。自制片D03和D04批在pH 5.5批和pH 5.8两种介质中的溶出曲线明显不相似,表明两种介质具有一定区分力。
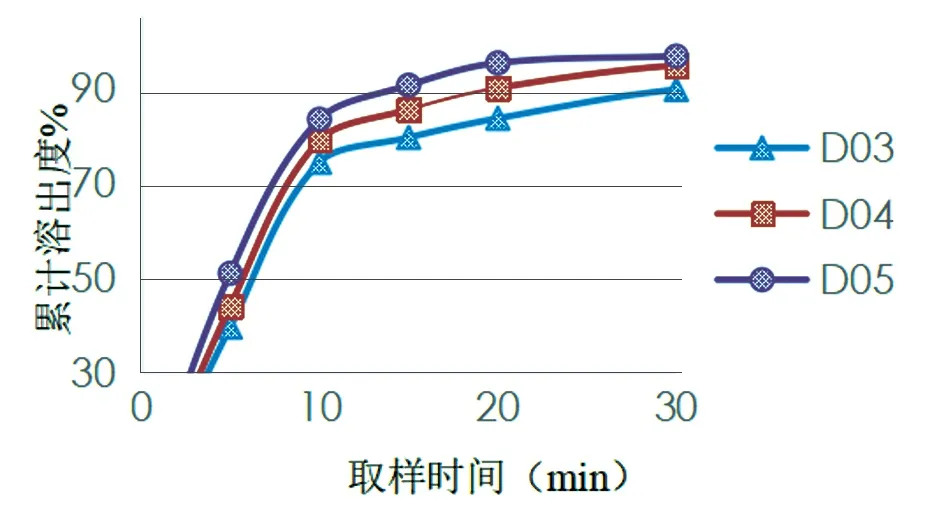
图3 pH 4.5介质中的3批自制片溶出曲线

图4 pH 5.5介质中的3批自制片溶出曲线
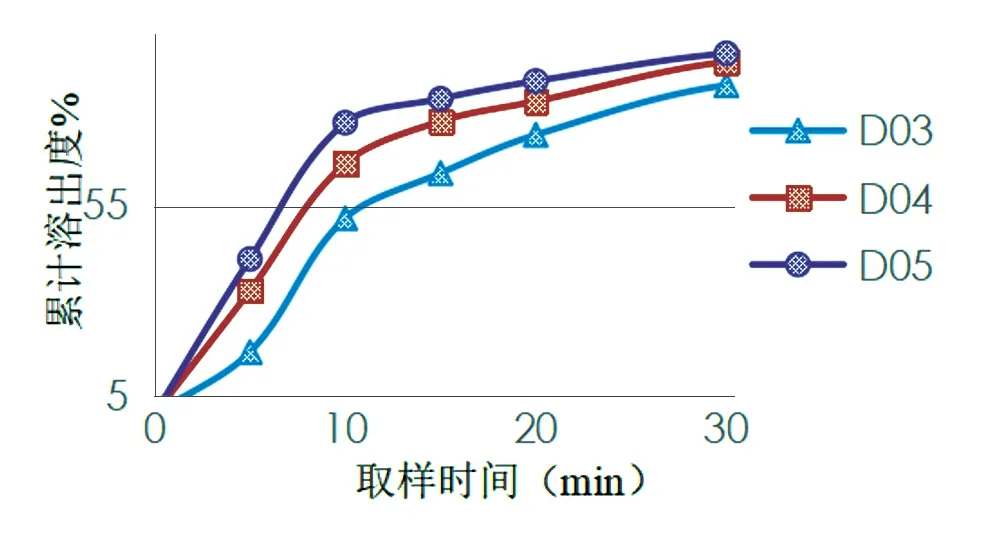
图5 pH 5.8介质中的3批自制片溶出曲线

图6 pH 6.8介质中的3批自制片溶出曲线

图7 水中的3批自制片溶出曲线

表2 ƒ2结果统计表
2.7 溶出曲线相似性评价
通过该6种介质评价经处方优化的自制片D06与原研片的溶出曲线相似性,结果见图8。结果显示,与 原 研 片 的ƒ2分 别 为69.9、67.5、67.9、68.9、68.3、67.0,结果均大于50,表明自制片D06与原研片在6种介质中的溶出曲线相似。
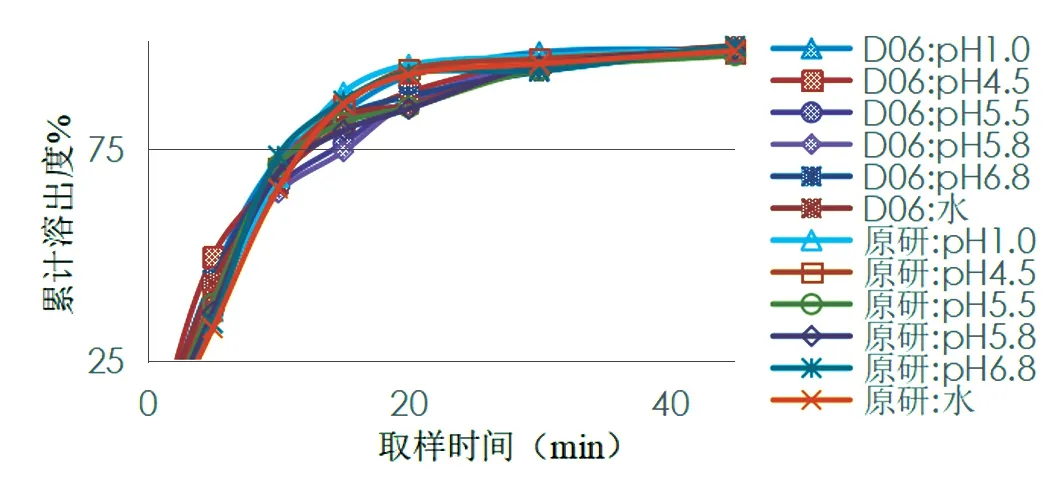
图8 自制片D06与原研片在6种不同介质中的溶出曲线
3 讨论
具有区分力的溶出方法在固体制剂的处方工艺中发挥重要作用,可以区分出不同处方药物的内在质量属性[13]。本文阐述了具有区分力的溶出方法的筛选和验证思路[14],为固体制剂的处方工艺研发提供了参考。对于仿制药,与原研片具有相似的体外溶出曲线,虽不能完全证明具有和原研片的生物等效性,但可大大提高生物等效性(BE)的通过率。
各国普遍使用ƒ2法虽计算简便,但也存在局限性[15]。为进一步的体内外相关性评价,需要在此基础上通过其他模型类拟合统计法进行综合评价,掌握体外溶出评估体系,才能在仿制药的再评价和质量标准的建立提供便利[16]。

