贝伐珠单抗联合卡培他滨 奥沙利铂对晚期结直肠癌患者临床疗效及免疫功能的影响


【摘要】 目的 探讨贝伐珠单抗联合卡培他滨、奥沙利铂治疗晚期结直肠癌的临床效果。方法 选取2019年5月—2022年5月铅山县人民医院收治的60例晚期结直肠癌患者作为研究对象,按治疗方式的不同将患者分为2组,各30例。对照组予以卡培他滨、奥沙利铂治疗,观察组在对照组的基础上加用贝伐珠单抗治疗,2组均持续治疗2个疗程。比较2组临床疗效、免疫功能、肿瘤标志物水平、生存质量及不良反应。结果 观察组客观缓解率较对照组高,治疗后CD3+、CD4+、CD4+/CD8+水平高于对照组,CD8+水平低于对照组(P<0.05);观察组治疗后糖类抗原19-9(carbohydrate atigen 19-9,CA19-9)、糖类抗原125(carbohydrate antigen 125,CA125)、肿瘤相关黏液抗原(carbohydrate atigen 242,CA242)、癌胚抗原(carcinoembryonicantigen,CEA)水平较对照组低(P<0.05);观察组治疗后世界卫生组织生存质量测定简易量表(world health organization on quality of life brief scale,WHO QOL-BREF)中各领域评分均较对照组高(P<0.05);2组不良反应发生率相比,差异无统计学意义(P>0.05)。结论 贝伐珠单抗联合卡培他滨、奥沙利铂可提高晚期结直肠癌治疗效果,加快肿瘤标志物复常,减轻免疫功能损害,改善患者生存质量,且安全性良好。
【关键词】 晚期结直肠癌;贝伐珠单抗;卡培他滨;奥沙利铂
中图分类号:R735.3+5 文献标识码:A
文章编号:1672-1721(2023)35-0045-03
DOI:10.19435/j.1672-1721.2023.35.015
结直肠癌是主要发生于结肠或直肠的恶性肿瘤,常发于40岁以上中老年群体。结直肠癌早期症状不明显,肿瘤进展过程中可逐渐出现便血等症状,但特异性欠佳,不易引起重视,多数患者就诊时已进展至中晚期[1-2]。目前,临床对于早期结直肠癌患者以手术治疗为主,但晚期结直肠癌患者因肿瘤扩散、机体耐受性差等,已失去手术最佳时机,仅可依靠放化疗抑制肿瘤进展,延长生存时间。卡培他滨、奥沙利铂为当前晚期结直肠癌化疗常用方案,二者可从不同作用机制下促进肿瘤细胞凋亡,抑制肿瘤生长,延缓疾病进
展[3-4]。常规化疗整体效果有限,部分患者会出现耐药现象,导致抗肿瘤效果减弱。随着分子靶向药物的应用,抗肿瘤治疗出现新的选择,抑制与肿瘤关系密切的特异性因子可辅助增强抗肿瘤效果。贝伐珠单抗为靶向药物,可阻断肿瘤血供及新生血管形成,抑制肿瘤生长[5]。本研究分析了贝伐珠单抗联合卡培他滨、奥沙利铂治疗晚期结直肠癌的临床效果,报告如下。
1 资料与方法
1.1 一般资料 选取2019年5月—2022年5月铅山县人民医院收治的60例晚期结直肠癌患者作为研究对象,按治疗方式的不同将患者分为2组,各30例。对照组男性17例,女性13例;年龄45~72岁,平均年龄(60.24±4.38)岁;肿瘤类型,结肠癌18例,直肠癌12例;肿瘤分期,Ⅲ期16例,Ⅳ期14例;体质量指数(body mass index,BMI)19~28 kg/m2,平均BMI(24.16±1.52)kg/m2;肿瘤最大径3.8~6.5 cm,平均肿瘤最大径(4.48±0.42)cm;转移部位,肺转移10例,肝转移12例,其他8例。观察组男性16例,女性14例;年龄47~75岁,平均年龄(60.29±4.42)岁;肿瘤类型,结肠癌17例,直肠癌13例;肿瘤分期,Ⅲ期18例,Ⅳ期12例;BMI 19~28 kg/m2,平均BMI(24.23±1.55)kg/m2;肿瘤最大径3.7~6.6 cm,平均肿瘤最大径(4.52±0.45)cm;转移部位,肺转移11例,肝转移12例,其他7例。2组基线资料对比差异无统计学意义(P>0.05),具有可比性。本研究经医院医学伦理委员会审批。
1.2 入选标准 纳入标准:符合《中国结直肠癌诊疗规范(2017版)》[6]中晚期结直肠癌诊断标准;经病理检查确诊,且肿瘤分期Ⅲ期—Ⅳ期;卡氏功能状态评分(karnofsky performance status,KPS)≥70分;预计生存期≥3个月;患者及其家属知情同意并签署知情同意书。
排除标准:肝肾衰竭;合并其他恶性肿瘤;对本研究用药存在禁忌证;伴有急性心脑血管疾病。
1.3 方法 对照组予以卡培他滨(齐鲁制药有限公司,国药准字H20143365)、奥沙利铂(先声药业有限公司,国药准字H20093899)治疗,第1天静脉注射奥沙利铂130 mg/m2;第1~14天口服卡培他滨治疗,
1 000 mg/m2,2次/d。观察组在对照组基础上加用贝伐珠单抗(齐鲁制药有限公司,国药准字S20190040)治疗,第1天静脉滴注5 mg/kg。3周为1个疗程,2组均用药2个疗程。
1.4 观察指标 (1)临床疗效。病灶消失,肿瘤标志物正常为完全缓解;病灶缩小≥50%,肿瘤标志物水平明显下降为部分缓解;病灶增大≥25%,或新的病灶出现为病情进展;处于部分缓解及进展间为病情稳定。客观缓解率=完全缓解率+部分缓解率+病情稳定率。(2)免疫功能。治疗前及治疗2个疗程后分别采集2组3 mL空腹血,采用流式细胞仪测定CD3+、CD4+、CD8+、CD4+/CD8+水平。(3)肿瘤标志物水平。治疗前及治疗2个疗程后分别采集2组3 mL空腹血,离心处理后,以酶联免疫法测定糖类抗原19-9(CA19-9)、肿瘤相关黏液抗原(CA242)、糖类抗原125(CA125)、癌胚抗原(CEA)水平。(4)生存质量。治疗前及治疗2个疗程后,以世界卫生组织生存质量测定简易量表(WHO QOL-BREF)评价2组生存质量,包括生理、心理、社會及环境4个领域,各100分,评分越高提示患者生存质量越好。(5)不良反应。记录2组手足综合征、骨髓抑制、恶心呕吐、肝肾损伤等发生情况及不良反应发生率。
1.5 统计学方法 采用SPSS 22.0统计学软件分析数据,计量资料以x±s表示,行t检验,计数资料以百分比表示,行χ2检验,P<0.05为差异有统计学意义。
2 结果
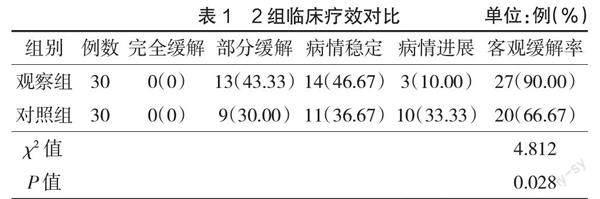
2.1 2组临床疗效对比 观察组客观缓解率较对照组高(P<0.05),见表1。
2.2 2组免疫功能对比 2组治疗前免疫功能指标水平相比,差异无统计学意义(P>0.05);观察组治疗后CD3+、CD4+、CD4+/CD8+水平较对照组高,CD8+水平较对照组低(P<0.05),见表2。
2.3 2组肿瘤标志物水平对比 2组治疗前肿瘤标志物水平相比,差异无统计学意义(P>0.05);观察组治疗后CA19-9、CA125、CA242、CEA水平均较对照组低(P<0.05),见表3。
2.4 2组治疗前后生存质量对比 2组治疗前WHO QOL-BREF评分相比,差异无统计学意义(P>0.05);观察组治疗后WHO QOL-BREF各領域评分较对照组高(P<0.05),见表4。
2.5 2组不良反应发生率对比 2组手足综合征、骨髓抑制、恶心呕吐、肝肾损伤等不良反应发生率相比,差异无统计学意义(P>0.05),见表5。
3 讨论
结直肠癌病因复杂,临床认为可涉及饮食、遗传、化学致癌物质接触、消化道疾病等多个方面。在多种因素长期相互作用下,体内致癌物质无法及时代谢出体外,延长与肠道接触时间,从而持续刺激肠道黏膜细胞,使肠道黏膜细胞产生恶性变化并过度增殖,最终形成肿瘤组织[7-8]。结直肠癌早期常无明显症状,随着肿瘤不断生长,可引起肠道功能障碍,从而诱发便血、腹泻等症状。该类症状与多种胃肠道疾病相似性高,特异性有限,使得患者未能得到早期诊治,较多患者明确诊断后进入晚期,导致整体预后偏差。如何改善晚期结直肠癌患者预后成为临床研究重点。
化疗为当前晚期结直肠癌主要治疗手段之一,选取适宜的化疗药物治疗能够阻止肿瘤生长。卡培他滨联合奥沙利铂较为常用,卡培他滨口服吸收快,可经肝脏转化为5'-脱氧-5-氟胞苷,再经肝脏、肿瘤组织胞苷脱氨酶、胸苷磷酸化酶后,转化为氟尿嘧啶以抗肿瘤[9-10]。奥沙利铂以DNA为作用靶点,铂原子可与肿瘤细胞DNA交叉联结,抑制肿瘤细胞DNA复制、转录,以阻止肿瘤细胞增殖。两药联合后可进一步发挥协同作用,从不同机制阻止肿瘤增殖,改善患者预后。但长期联合应用两药发现,仍有部分患者肿瘤控制欠佳,易再次进展。免疫功能与肿瘤发生及发展存在密切关系,一旦机体免疫功能下降,则难以阻止肿瘤细胞增殖。CD3+、CD4+、CD8+、CD4+/CD8+是反映免疫功能的重要指标。当机体免疫功能低下时,则表现为CD3+、CD4+、CD4+/CD8+水平下降,CD8+水平异常升高。CA19-9、CA125、CA242、CEA为常见肿瘤标志物,正常情况下在血清内含量极低,恶性肿瘤患者体内该类指标水平可异常升高。本研究中,相比于对照组,观察组客观缓解率较高;治疗后CD3+、CD4+、CD4+/CD8+水平较高,CD8+水平较低;治疗后CA19-9、CA125、CA242、CEA水平较低;治疗后WHO QOL-BREF各领域评分较高(P<0.05);2组不良反应发生率相比,差异无统计学意义(P>0.05)。提示贝伐珠单抗联合卡培他滨、奥沙利铂可增强晚期结直肠癌治疗效果,降低肿瘤标志物水平,加快患者免疫功能恢复,改善生存质量,且未增加不良反应发生风险。随着临床对于结直肠癌的不断深入研究,发现血管内皮生长因子(vascular endothelial growth factor,VEGF)在肿瘤进展中具有重要作用,可加快肿瘤血管新生,为肿瘤增殖提供充足的营养物质。贝伐珠单抗具有较强靶向性,能直接与VEGF结合,阻止VEGF与其受体相结合,从而减弱VEGF诱导的肿瘤血管新生等生物学效应,减少肿瘤新生血管形成,切断肿瘤组织内血供,阻止肿瘤生长及扩散[11-12]。贝伐珠单抗还能调控内皮细胞通透性,使药物能更快渗入肿瘤深处,形成高浓度药物环境,故与卡培他滨、奥沙利铂联用后可发挥协同作用,进一步增强抗肿瘤效果。
综上所述,贝伐珠单抗联合卡培他滨、奥沙利铂可提高晚期结直肠癌治疗效果,纠正免疫功能异常,加快肿瘤标志物水平复常,安全性较高。
参考文献
[1] ZORZI M,BATTAGELLO J,SELBY K,et al.Non-compliance with colonoscopy after a positive faecal immunochemical test doubles the risk of dying from colorectal cancer[J].Gut,2022,
71(3):561-567.
[2] 周晓艳,宋晓锋,周利胜,等.甲磺酸阿帕替尼联合FOLFOX化疗方案治疗晚期结直肠癌的临床疗效[J].癌症进展,2022, 20(14):1445-1448,1452.
[3] 李振前,杨梦春,刘戎惠,等.扶正消癌汤合四君子汤联合卡培他滨治疗晚期结直肠癌临床研究[J].陕西中医,2022,43(8):1037-1040.
[4] 马骏,张玉英,陈树军,等.奥沙利铂不同给药方案联合卡培他滨对结直肠癌肝转移患者的疗效及生存率的影响[J].中国医药,2020,15(4):593-596.
[5] 易涵,古再丽努尔·如则托合提,姜明燕,等.贝伐珠单抗联合伊立替康与雷替曲塞治疗氟尿嘧啶耐药晚期结直肠癌的疗效和安全性[J].药物评价研究,2020,43(2):293-298.
[6] 国家卫生计生委医政医管局,中华医学会肿瘤学分会.中
国结直肠癌诊疗规范(2017年版)[J].中华胃肠外科杂志,2018,21(1):92-106.
[7] DUVVURI A,CHANDRASEKAR V T,SRINIVASAN S,et al.Risk of colorectal cancer and cancer related mortality after detection of low-risk or high-risk adenomas,compared with no adenoma,at index colonoscopy:a systematic review and meta-analysis[J].Gastroenterology,2021,160(6):1986-1996.
[8] 周帅,贾国战,韩伟光,等.血清G-CSF、ADPN在奥沙利铂联合卡培他滨治疗Ⅲ期结直肠癌患者术后辅助中的表达及其与肠道菌群失调的相关性[J].现代生物医学进展,2022, 22(17):3298-3302.
[9] 种王斌,朱金祥,刘佳.贝伐珠单抗联合奥沙利铂+卡培他滨化疗治疗转移性结直肠癌的疗效及安全性[J].癌症进展,2022,20(6):624-626,635.
[10] 冯禄,张艳辉,郭凯红.卡培他滨联合奥沙利铂治疗晚期结直肠癌的近远期疗效及对血清癌胚抗原、糖类抗原19-9表达水平的影响[J].癌症进展,2021,19(4):395-398.
[11] 卢元丽,张志国,张颖,等.贝伐珠单抗联合XELOX化疗方案治疗老年晚期结直肠癌肝转移患者的临床观察[J].中西医结合肝病杂志,2021,31(9):806-808,812.
[12] 王梅娟,于韶荣,黎超,等.卡培他滨和雷替曲塞分别联合贝伐珠单抗治疗晚期结直肠癌的疗效及安全性比较[J].现代肿瘤医学,2021,29(24):4362-4365.
(收稿日期:2023-10-10)
作者简介:李娟,女,本科,主治医师。

