下腔静脉滤器开放手术取出的安全性与可行性分析
李金勇,刘建龙,贾伟,田轩,蒋鹏,程志远,张蕴鑫,刘笑,田晨阳,周密
(北京积水潭医院 血管外科,北京 100035)
下肢深静脉血栓形成(deep venous thrombosis,DVT)是血管外科常见的疾病之一,其主要临床表现为肢体疼痛及肿胀。DVT 急性期引起致死性肺栓塞(pulmonary embolism,PE),仅次于心肌梗死和脑血管疾病,为心脑血管疾病死亡的第三大常见原因[1-2]。下腔静脉滤器(inferior vena cava filter,IVCF)是预防PE 发生的一种有效的手段,其适用证为存在抗凝禁忌,抗凝失败及其相关并发症,以及在抗凝基础上血栓仍进展加重的患者[3-4]。尽管滤器的置入带来了一定的获益,但是滤器的长期置入可能会产生一些并发症,比如说滤器置入时脚支或回收钩穿刺血管壁损伤血管[5],移位至心脏[6];置入后产生腹部疼痛,继发血栓形成阻塞下腔静脉,回收钩、脚支穿透十二指肠及腹主动脉引起损伤等[7-8]。因此,美国食品药品监督管理局(food and drug administration,FDA)建议当不再需要滤器发挥保护作用时需要尽快将其取出,并推荐滤器取出的最佳时间是在其置入后的29~54 d[9]。
应用IVCF 需要关注的是其回收率及相关并发症。相关文献[10]报道IVCF 平均回收率仅为34%。在美国,2012—2016 年间,滤器的年回收率由6.9%升至22.1%,表明仍有多数滤器还未取出[11]。腔内介入是IVCF 取出的主要方式,文献[12]报道其取出率高达97.6%。但是对于腔内介入无法取出或超出时间窗的IVCF,可以通过腹腔镜技术、机器人技术及开腹手术取出[13-15]。本中心先前报道了15 例全腹腔镜下IVCF 取出的临床经验[16],取得较好的效果,而该技术主要适用于回收钩穿透腔静脉壁的锥形滤器。对于回收钩贴壁的锥形滤器或梭形滤器,则需要开放手术取出,而目前关于开放手术的临床报道较少、样本量较小[17-21]。本中心收治了27 例IVCF 开放手术取出的患者,效果显著,报告如下。
1 资料与方法
1.1 一般资料
回顾性分析2019 年2 月—2022 年8 月在北京积水潭医院血管外科收治的IVCF 置入后行开放手术取出患者临床资料。纳入标准:⑴ ICVF 为回收钩贴壁滤器,经腔内介入取出失败的患者;⑵ 超出时间窗或介入无法取出的梭形滤器;⑶ 下腔静脉超声或造影明确下腔静脉通畅者;⑷ 下肢深静脉血栓稳定或陈旧患者。排除标准:⑴ 高龄患者或伴有严重内科疾病且手术风险较大者;⑵ 近3 个月出现非创伤性脑出血及消化道出血患者;⑶ 急性DVT 患者;⑷ 抗凝禁忌的患者;⑸ 资料不完整。共有27例符合条件,平均年龄为(42.30±12.12)岁,男性13 例(48.1%),女性14 例(51.9%)。所有患者术前行腹部CT 检查进行评估明确ICVF 及回收钩的位置。
1.2 治疗方法
所有患者均在全身麻醉下行经右侧腹直肌切口下腔静脉切开滤器取出术。术前准备:术前停用口服抗凝药物,改为低分子肝素皮下注射(1 次/12 h),术前晚停用;其次,术前1 d 口服20%溶液250 mL 甘露醇,直至患者出现清水样便;再次,术前需要留置胃管,并备好腹带进行腹部加压。手术过程如下:⑴ 全麻后,仰卧位,消毒铺单后,取右侧腹直肌切口,长约20 cm,切开皮肤、皮下脂肪组织,分离腹直肌,切开覆膜,进入腹腔,分离右结肠韧带及肝结肠韧带,暴露下腔静脉,分离腔静脉周围组织,注意保护输尿管及神经,完全暴露肾静脉下至髂总静脉分叉处下腔静脉,充分结扎要静脉,阻断钳分别阻断滤器近远端下腔静脉,祛血后滤器处不再有血液充盈,切开下腔静脉前壁,约4 cm,完整剥离滤器及部分增厚的内膜,为方便剥离,可剪断滤器分次剥出,彻底取出滤器后,应用不可吸收缝线,连续缝合血管壁,开放阻断钳,检查无出血,逐层关腹,腹带加压。多数肾静脉下纺锤形滤器均经此种手术方式取出(图1)。⑵ 对于锥形滤器,分离下腔静脉后,找到回收钩所在位置,留置荷包缝合线,切开静脉壁约2 mm,钳加回收钩直视下将滤器取出,收紧缝合线,无须行下腔静脉阻断(图2)。⑶ 对于肾静脉上滤器,除完整游离下腔静脉外,还需要完整游离双肾静脉及肾上下腔静脉,完全阻断血流后切开下腔静脉前壁,完整取出滤器后进行血管壁连续缝合,术中注意勿要损伤十二指肠及胰腺。⑷ 肝后下腔静脉滤器取出需要取右上腹斜行切口,进入腹腔后游离肝左叶,暴露肝后段下腔静脉及第一肝门,经膈肌下肝上缘,分离第二肝门,分别阻断第一、第二肝门及滤器远端下腔静脉,切开静脉壁,完整取出滤器后连续缝合(图3)。

图1 术中图片1 A:CT提示纺锤形滤器(28岁女性患者);B;切开下腔静脉取出滤器;C:缝合下腔静脉壁;D:取出的纺锤形滤器Figure 1 Intraoperative pictures 1 A: CT showing a spindle-shaped filter (28-year-old female patient);B: Filter removal by incision of the inferior vena cava;C: Suture of the inferior vena cava wall;D: The spindle-shaped filter after removal

图2 术中图片2 A:CT提示锥形滤器(35岁男性患者);B:切开下腔静脉取出滤器;C:取出的锥形滤器;D:缝合下腔静脉壁Figure 2 Intraoperative pictures 2 A: CT showing a conical-shaped filter (35-year-old male patient);B: Filter removal by incision of the inferior vena cava;C: Suture the inferior vena cava wall;D: The conical-shaped filter after removal
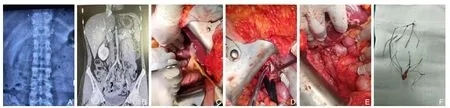
图3 术中图片3 A:腹部平片提示肝后下腔静脉纺锤形滤器;B:CT提示肝后下腔静脉纺锤形滤器;C:阻断第二肝门;D:切开下腔静脉取出滤器;E:缝合下腔静脉壁;F:取出的纺锤形滤器Figure 3 Intraoperative pictures 3 A: Plain abdominal X ray showing a spindle-shaped filter in the retrohepatic inferior vena cava;B: CT showing a spindle-shaped filter in the retrohepatic inferior vena cava;C: Occlusion of the second hepatic hilar;D: Filter removal by incision of the inferior vena cava;E: Suture of the inferior vena cava wall;F: The spindle-shaped filter after removal
术后卧床至少1 周,肠外营养支持,排气后可饮水并拔除胃管,排便后可进食,1 周后尝试下地活动。术后第2 天给予低分子肝素抗凝(1 次/12 h),出院后改为口服抗凝药物(按术前剂量口服)。伤口术后2 周拆线。
1.3 安全性及围手术期风险评价
技术成功率定义为顺利进行开腹手术且下腔静脉滤器完整取出。统计患者围手术期滤器取出率及病死率。记录患者年龄、性别、既往慢性疾病病史、血栓史、滤器置入原因、滤器取出原因、口服抗凝药物种类、滤器体内置入时间、滤器类型、滤器位置、尝试介入取出次数等一般资料。记录手术前后血红蛋白及是否输血。评价围手术期出血、感染、血栓发生率、胃肠道、泌尿道及心血管系统等相关并发症[22]。
1.4 统计学处理
2 结果
2.1 患者一般情况
所有患者中,4 例(14.8%)患者为孕产妇,12 例(44.4%)患者DVT 继发于下肢骨折或外伤,3 例(11.1%)患者DVT 继发肿物或肿瘤切除手术,8 例(29.6%)患者为原发性DVT。研究人群中3 例(11.1%)伴有高血压,1 例(3.7%)伴有糖尿病,1 例(3.7%)伴有脑出血,无冠心病患者。研究人群滤器置入前血栓情况:8 例(29.6%)为股静脉+腘静脉DVT,15 例(55.6%)为腘静脉DVT,1 例(3.7%)为髂静脉+股静脉DVT,1 例(3.7%)为肾静脉+下腔静脉DVT,2 例(7.4%)为腘静脉+肺栓塞DVT。血栓治疗方式:2 例(7.4%)给予尿激酶溶栓+口服利伐沙班片抗凝治疗,21 例(77.8%)口服利伐沙班片抗凝,2 例(7.4%)口服华法林抗凝,1 例(3.7%)口服阿司匹林,改为利伐沙班片,1 例(3.7%)口服阿司匹林,改为华法林抗凝治疗。开放手术前行介入尝试取出中位次数为1(1~2)次。术前D-二聚体为(0.52±0.82)mg/L(表1)。
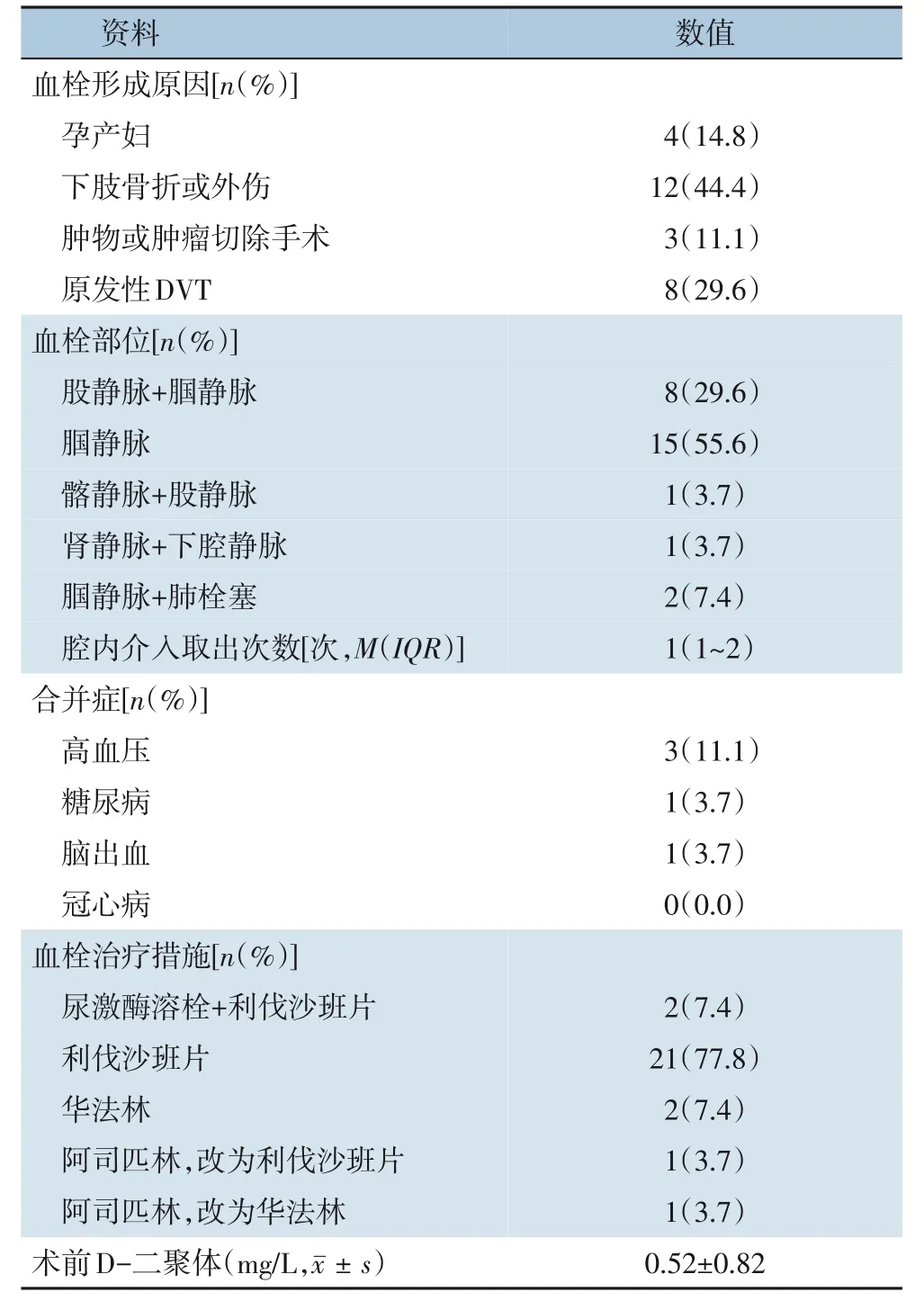
表1 27例患者一般资料Table 1 The general date of the 27 patients
2.2 滤器类型与取出原因
置入滤器中,Aegisy 滤 器8 例(29.6%),Denali 滤器1 例(3.7%),Cordis 滤器10(37.0%)例,Simon 滤 器1 例(3.7%),Celect 滤 器3 例(11.1%),Tulip 滤器4 例(14.8%)。取出滤器原因:2 例(7.4%)为滤器断裂,3 例(11.1%)为回收钩穿透血管壁,6 例(22.2%)为腹痛或腰痛,7 例(31.8%)为拒绝终生抗凝,7 例(31.8%)为心理因素强烈要求取出,2 例(7.4%)为回收钩损伤脏器(表2)。
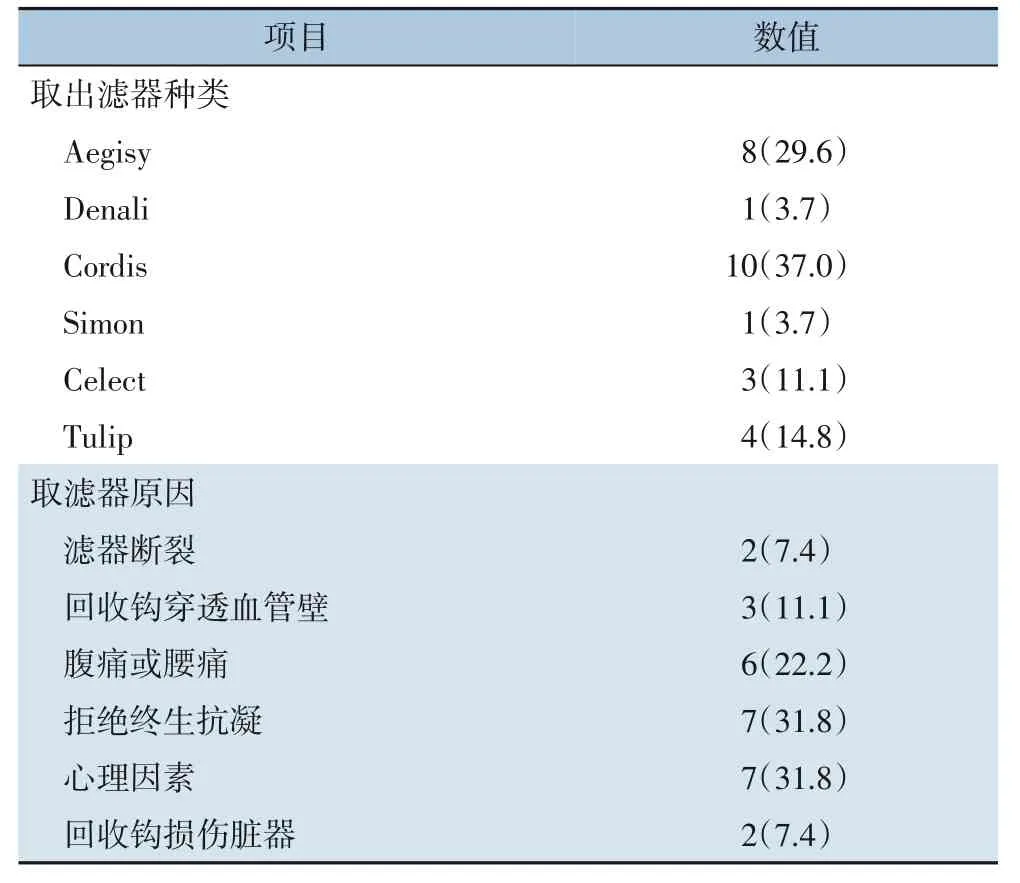
表2 27例患者滤器类型与取出原因[n(%)]Table 2 The filter type and reason for removal of the 27 patients [n (%)]
2.3 滤器取出情况
技术成功率为100%,所有滤器全部取出,置入中位时间为20(5~48)个月。1 例(3.7%)滤器位于肾静脉上下腔静脉,1 例(3.7%)位于肝后下腔静脉,25 例(92.6%)滤器位于肾静脉下下腔静脉。术中有2 例(7.4%)于滤器回收钩处留置荷包缝合线,不阻断下腔静脉血流,通过直接钳夹回收钩取出,取出后进行荷包缝合;有2 例(7.4%)未阻断下腔静脉血流,将滤器直接回收至血管鞘后行荷包缝合;1 例(3.7%)阻断双肾静脉及滤器远近端下腔静脉血流,1 例(3.7%)分别阻断滤器远端下腔静脉、第一肝门及第二肝门血流,21 例(77.8%)患者阻断滤器远近端下腔静脉血流,然后通过切开下腔静脉前壁进行滤器取出,取出后进行血管壁连续缝合。手术平均时间为(224.15±23.85)min。围手术期无PE 或DVT 发生,无心肺系统并发症,无伤口感染,1 例(3.7%)出现腹痛伴血性胃液,1 例(3.7%)出现血尿,保守对症治疗后缓解,术前血红蛋白平均为(128.59±15.05)g/L,术后为(110.56±22.15)g/L,6 例(22.2%)术后输入悬浮红细胞400 mL,未见致命性大出血及休克。术后至出院中位住院时间为9(8~12)d(表3)。
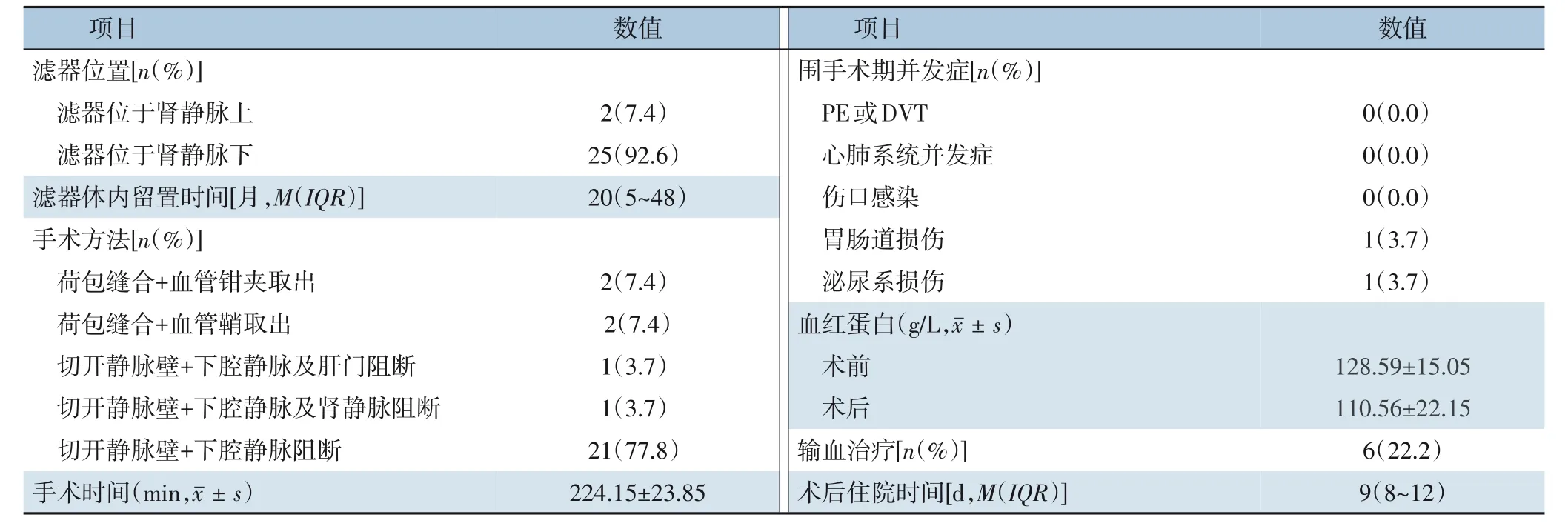
表3 27例患者手术及围手术期相关指标Table 3 Surgical variables and perioperative variables of the 27 patients
3 讨论
尽管IVCF 在预防致死性PE 方面获益,但长期置入产生的相关并发症不可忽视。IVCF 的相关并发症因类型而异,如移位至右心可引起心律失常,附壁丝断裂移位至肺,穿孔致周围脏器损伤,继发血栓阻塞下腔静脉及产生PE 等[23]。文献[8,24-25]报道严重者回收钩或脚支穿透主动脉及十二指肠致出血、栓塞,危及生命。因此,当不需要IVCF 发挥保护作用时尽可能将其取出。随着IVCF 的设计及取出方式的层出不穷,仍有约40%~60%的IVCF通过常规腔内介入技术无法取出,常见原因为回收钩贴壁或穿出、滤器移位、超出时间窗等[26]。
对于腔内介入技术无法取出的IVCF,可尝试外科手术,目前常用的有开放手术、腹腔镜辅助技术及机器人辅助技术。腹腔镜辅助技术创伤小,但适应证严格,对于回收钩穿出下腔静脉壁的患者较适宜[16,27]。达芬奇机器人辅助下手术中视野范围广,在腔静脉壁缝合上具有一定优势,但价格不菲[28-29]。目前关于上述两种手术方法仅限于病例报道,缺乏大样本数据证实其安全性及可行性。开放手术可以完全暴露滤器段下腔静脉,需要完全阻断滤器远近端血流,还需要控制滤器段腔静脉属支如腰静脉等血流,必要时结扎,在完全阻断滤器段下腔静脉血流的情况下,可切开静脉壁进行滤器取出。对于不同类型滤器取出方式有所不同,如纺锤形滤器需要切开进行剥离再缝合,而伞形滤器可切开取出,也可于滤器回收钩处留置荷包缝合,通过钳夹或回收鞘回收滤器,取出后收紧荷包线,避免了下腔静脉切开缝合。
有关开放手术滤器取出的临床病例报道较少,样本量极小[15,17-20],这些研究详尽论述了开放手术成功取出的经验,取得了一定的效果。本中心报道了27 例开放手术行IVCF 取出的患者,效果显著。所有患者IVCF 顺利取出,围手术期无严重并发症及死亡,IVCF 取出安全可行。结合本研究中心的经验,开放手术行滤器取出需要注意以下几点:首先,术前肠道的准备非常重要,术中肠道过度充气对手术视野的影响极大,建议术前严格做好肠道准备;其次,术中一定要完全游离滤器远近端下腔静脉血流,建议结扎部分汇入的腰静以便更好地阻断血流,如仍不能完全阻断血流,应考虑下腔静脉背侧有分支静脉汇入,如存在,应进行结扎,只有完全阻断血流,切开腔静脉壁才能完整取出滤器,减少出血;第三,如果滤器位于肾静脉上,还需阻断肾静脉血流,避免损伤肾静脉,本研究有1 例患者,回收钩进入右肾静脉粘连,术中切开肾静脉进行修复,术后出现肉眼血尿,保守治疗1 周后好转;本中心还报道了1 例滤器位于肝后下腔静脉的患者,术中暴露滤器远端下腔静脉,第一肝门及第二肝门,完全阻断上述血流后切开顺利取出滤器,围手术期无大出血,患者术后良好,无相关并发症,该病例目前尚无文献报道。第四,滤器置入时间较长的患者,内膜与滤器机化粘连较重,如滤器无法完整剥离,可切断脚支逐步剥离,避免强行剥离致使腔静脉壁损伤。第五,对于锥形行滤器患者,回收钩的位置非常重要,术中要精确定位,预先留置荷包线,取出滤器后要迅速收紧结扎,操作要轻柔,千万避免暴力牵拉致切开扩张致较多出血,本研究有4 例(14.8%)患者经此种方式顺利取出,无围手术期相关并发症且效果显著。
在2016—2017 年美国国家住院患者数据库中,Tanner 等[30]报道了100 例开放手术滤器取出的患者,其中45 例(45%)为开胸手术,55 例(55%)为开腹手术,围手术期有10 例(10%)患者出现呼吸系统并发症,20 例(20%)出现血栓栓塞并发症,泌尿道及胃肠道系统并发症各5 例(5%),5 例(5%)出现休克,围手术期病死率为5%,平均住院时间为6.5 d。但该研究只报道了围手术期相关并发症,未对患者滤器的性质及取出的手术方式做详尽的描述。本研究中27 例患者围手术期无PE 或DVT 发生,无心肺系统并发症,无伤口感染,1 例(3.7%)出现腹痛伴血性胃液,1 例(3.7%)出现血尿,均给予保守对症治疗后缓解,6 例(22.2%)术后输入悬浮红细胞400 mL,未见致命性大出血及休克,无死亡患者。术前的充分准备,术中的严格操作及精准手术方式,术后的精心护理,可避免相关并发症的出现,提高手术效果。但对于IVCF,仍然需要严格管理,选取合适的滤器,及时取出,避免滤器长期置入、取出复杂化及相关并发症。
全腹腔镜辅助下滤器取出是一种微创的手术方式。而本中心先前也报道了15 例全腹腔镜辅助下滤器取出的经验[16],其滤器取出率为93.3%,围手术期有1 例(6.7%)给予输血治疗,1 例(6.7%)皮肤感染,然而腹腔镜技术更适合于回收钩穿透下腔静脉壁的锥形滤器,术中无须阻断滤器远近端静脉,通过于回收钩周围留置荷包线,待滤器取出收紧荷包线即可。无论是梭形滤器还是锥形滤器均可应用开放手术进行取出,对于腹腔镜取出失败的滤器亦可开放取出,所不同的是开放手术切口较长,术中需要阻断相关血流及游离部分脏器,手术的难度大且技术十分复杂,患者术后卧床时间往往较长(至少1 周),围手术期出血较腹腔镜手术多、手术时间长,患者术后恢复时间较长。然而,无论开放手术还是腹腔镜技术,术前的充分准备、术中的精准操作及术后严格管理是降低手术风险、提高滤器取出的重要保障。
对于开放手术行IVCF 取出,术前腹部CT 的评价非常重要,CT 可以从三维的角度明确滤器在下腔静脉的位置、回收钩的位置、回收钩或脚支是否穿透周围组织及周围组织与滤器的关系等,对滤器的取出十分重要。相关文献[31-32]也报道了术前CT 对滤器取出的重要作用。因此,要重视影像学检查在开放手术滤器取出中的意义。
对于腔内技术及腹腔镜技术无法取出的滤器,本研究通过病例回顾分析提供了技术上可行且安全有效的经验。然而,本研究为病例回顾报道,样本量仍略显不足,所有患者围手术期无症状性PE,且未行肺动脉CTA 进行评价,术后未行长期随访及对滤器取出后下腔静脉通畅性进行评价。开放手术滤器取出后下腔静脉是否缩窄或闭塞及血栓后综合征(post-thrombosis syndrome,PTS)的发生是未知的,需要大样本及长期随访进一步明确及证实。尽管开放手术滤器取出手术难度大、技术复杂,但滤器取出是安全可行的。术前充分利用CT 判断滤器及其回收钩的位置,采用合适的手术方式,通过熟练的手术技巧可以提高开腹手术的安全性和成功率。未来仍需要长期随访并进行大样本研究来进一步证实开放手术的安全性及可行性。
利益冲突:所有作者均声明不存在利益冲突。

