多糖铁复合物胶囊的溶出度测定
王耀霞 孔凡强 程宏霞 范前业 朱斌 丁海燕▲
1.青岛大学附属医院药学部,山东青岛 266003;2.上海医药集团青岛国风药业股份有限公司,山东青岛 266510
铁是人体中重要的矿物质元素之一,其含量在人体中约占0.004%,它参与人体多种生命活动,对机体的代谢过程发挥着极其重要的作用,铁元素缺乏导致的贫血称之为缺铁性贫血[1]。世界上25%以上的人群患有贫血症,而缺铁性贫血是最常见的贫血症之一,占贫血症患者总数的50%以上[2-3]。其中妊娠期妇女及儿童由于对营养及微量元素需求量大,是缺铁性贫血的高发人群[4-5]。
临床上常用的口服补铁剂已发展了三代,第一代是以硫酸亚铁为代表的无机亚铁盐类;第二代是以富马酸亚铁、琥珀酸亚铁等为代表有机亚铁盐类;第三代是以大分子螯合铁为代表的新型补铁剂。第一代和第二代补铁剂由于其生物利用度较低、易产生较大的胃肠道副作用和细胞膜损伤,限制了其临床应用;第三代新型补铁剂虽然可以降低胃肠道副作用,但还存在一些铁盐螯合物体内生物利用度低,造价较高等问题[6-9]。目前以多糖铁复合物(polysaccharide-iron complex,PIC)为代表的第三代口服补铁剂,由于具有良好的溶解性及较高的体内生物利用度成为近年来研究的热点[10-11]。PIC 的合成方法以化学合成法为主[12],有研究人员采用该方法合成出孔石莼多糖铁复合物[13]、浒苔多糖铁复合物[14]、当归多糖铁复合物[15]等,进一步研究也表明PIC 的合成并非简单的物理吸附而是稳定络合反应[16]。目前市售的多糖铁复合物胶囊,元素铁含量高达150 mg/粒,在消化道能以分子形式被吸收。在临床上,由于其具有良好的有效性和安全性,常用于妊娠期女性铁缺乏症和缺铁性贫血的治疗[17-18]。临床研究数据表明,相对于其他口服铁剂,多糖铁复合物胶囊的胃肠道反应等不良反应发生率更低[19-22]。
多糖铁复合物胶囊虽上市多年,但各国药典均未收载该品种,对于口服固体制剂而言,溶出度检测是评价药物制剂剂量和日常监管的一个重要指标[23]。虽然有文献报道了该制剂溶出度的检测方法,但消解过程较为繁琐,且耗时较长[24]。本研究建立了一种邻菲罗啉法测定多糖铁复合物胶囊溶出度的方法,该方法简单、快速、准确度高。
1 仪器与试药
1.1 仪器
708-DS 型溶出仪(美国Agilent);UV-2700i 型可见紫外分光光度计(日本岛津);XS205 型电子天平[梅特勒-托利多(上海)有限公司,精密度:0.000 1 g];ME-4001 型电子天平[梅特勒-托利多(上海)有限公司,精密度:0.1g];S201 型PH 计(梅特勒);H1650-W医用离心机(湖南湘仪实验室仪器开发有限公司,离心半径为50 mm);HH 数显恒温水浴锅(常州国宇仪器制造有限公司)。
1.2 试药
多糖铁复合物胶囊(上海医药集团青岛国风药业股份有限公司,181115、181116、181117);标准铁溶液(规格:1 000 μg/ml,贮存于1.0 mol/L 硝酸介质中,国家有色金属及电子材料分析测试中心,定值日期:2018 年11 月5 日);盐酸(国药集团化学试剂有限公司,20180223);盐酸羟胺(国药集团化学试剂有限公司,20170124);1,10-菲啰啉(国药集团化学试剂有限公司,20171013);三水合乙酸钠(国药集团化学试剂有限公司,20171013);冰醋酸(国药集团化学试剂有限公司,20160728);磷酸二氢钾(国药集团化学试剂有限公司,20171107);氢氧化钠(国药集团化学试剂有限公司,20150324);十二烷基硫酸钠(天津市大茂化学试剂厂,20170901);试剂均为分析纯。
2 方法与结果
2.1 溶液的配制
2.1.1 试液1 mol/L 盐酸溶液:精密量取9 ml 浓盐酸,置100 ml 容量瓶中,用纯化水定容,摇匀,得试液Ⅰ。10%盐酸羟胺溶液:取盐酸羟胺10.0 g,精密称定,置100 ml 量瓶中,加纯化水溶解并定容,摇匀,得试液Ⅱ。pH 4.5 醋酸缓冲液:取三水合乙酸钠18.0 g,精密称定,置1 000 ml 容量瓶中,加适量水使溶解,再精密量取冰醋酸9.8 ml,置容量瓶中,加水定容,摇匀,得试液Ⅲ。0.1%菲啰啉溶液:取1,10-菲啰啉0.1 mg,精密称定,置100 ml 量瓶中,加纯化水溶解并定容,摇匀,得试液Ⅳ。
2.1.2 对照品储备液 精密量取10.0 ml 标准铁溶液,移入100 ml 容量瓶中,用纯化水定容,摇匀备用。
2.1.3 空白溶液 精密量取1 ml 纯净水,移入100 ml容量瓶中,再依次加入1 ml 试液Ⅰ、2 ml 试液Ⅱ、5 ml试液Ⅲ和5 ml 试液Ⅳ,用纯化水定容,摇匀,即得。
2.1.4 供试品溶液 在900 ml 溶出介质中加入1 粒多糖铁复合物胶囊,按照溶出度测定方法操作,即得供试品溶液。
2.2 溶出度测定方法
参考文献[24]中的溶出度试验条件,对消解方法进行研究,确立本品的溶出度测定方法:取本品置沉降篮中,按照《中华人民共和国药典》2020 版四部[25]通则溶出度与释放度测定法第二法进行,以900 ml 1%十二烷基硫酸钠的pH 7.5 磷酸二氢钾溶液为溶出介质,溶出介质温度为(37±0.5)℃,转速为100 r/min,30 min 时取溶出液5 ml 置离心管中,将离心管放入离心机中,3 000 r/min 离心10 min,精密量取离心后的上清液1 ml,移入100 ml 量瓶中,加入1 ml 试液Ⅰ,密封,置90℃水浴中加热10 min,取出,放冷,加入2 ml 试液Ⅱ,摇匀,静置10 min,再加入试液Ⅲ和5 ml 试液Ⅳ,摇匀,静置5 min,用纯净水定容,摇匀,静置10 min。按照《中华人民共和国药典》2020 版四部[25]通则0401,照紫外-可见光光度法测定吸光度,计算每粒胶囊的溶出量。
2.3 专属性试验
精密量取对照品储备液1.0 ml,置100 ml 量瓶中,按“2.2”项下方法操作,制备1 μg/ml 的对照品溶液。另取空白溶液、供试品溶液,分别在400~700 nm处进行扫描,结果显示,在510 nm 处对照品溶液和供试品溶液均有最大吸收,但空白溶液在此处无吸收,本检测方法专属性良好。
2.4 线性试验
精密量取对照品储备液0.1、0.5、1.0、1.5、2.0 ml,分别置100 ml 量瓶中,按照“2.2”项下方法,即得0.1、0.5、1.0、1.5、2.0 μg/ml 的系列对照品溶液,照紫外-可见分光光度法,在510 nm 波长处测定其吸光度。以铁离子浓度(C)为横坐标,吸光度(A)为纵坐标,进行线性回归,结果见图1。结果显示,铁离子浓度在0.1~2.0 μg/ml 范围内,吸光度与浓度具有良好的线性关系,线性回归方程为A=0.202 5C+0.000 66,(r2=0.999 9)。
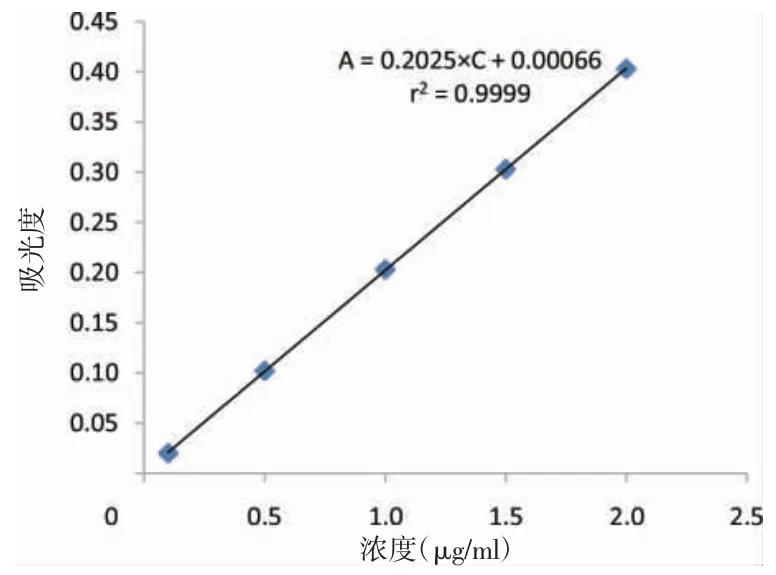
图1 对照品溶液标准曲线图
2.5 重复性试验
按照“2.2”项下方法,由同一分析人员同法制备6 份供试品溶液并对其进行紫外测定,6 次检测结果的RSD 为2.73%。
2.6 溶液稳定性
对照品溶液稳定性:按照“2.3”项下制备对照品溶液,室温下放置,分别于0.5、1.0、2.0、4.0、6.0、8.0 h依法检测,结果显示对照品溶液的RSD 为0.44%,提示室温下8 h 内,对照品溶液的稳定性良好。
供试品溶液稳定性:按照“2.2”项下方法制备供试品溶液,室温下放置,分别于5、10、20、30、60、90、120 min 依法检测,结果显示,对照品溶液的RSD 为0.55%。提示室温条件下2 h 内,供试品溶液的稳定性良好。为方便操作,本实验选择将供试品溶液放置10 min 后测定吸光度值。
2.7 回收率试验
精密称取多糖铁复合物胶囊(181115)内容物,用溶出介质配成约含铁150 μg/ml 的溶液,精密量取0.5 ml 样品溶液9 份,分别置100 ml 量瓶中,加入“2.1”项下对照品储备液0.4、0.6、0.8 ml 各三份,按“2.2”项下制备供试品溶液,依法检测,计算回收率,结果见表1。平均回收率为99.30%,平均RSD 为1.03%,提示在该溶出条件及测定条件下,方法的准确度良好。
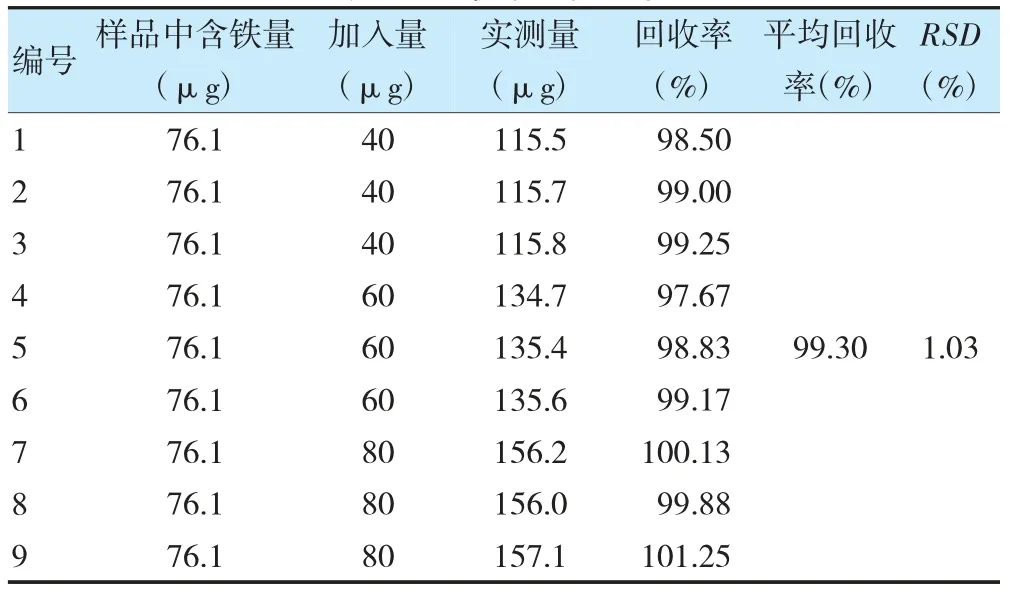
表1 回收率试验结果
2.8 样品检测
取3 批多糖铁复合物胶囊(每批各6 粒),按“2.2”项下方法进行溶出度测定,同时对应的溶出液按文献[24]中的消解方法进行,依法检测溶出度,检测结果见表2。

表2 两种方法下多糖铁复合物胶囊溶出度比较
3 讨论
本研究方法经过专属性、线性、重复性、溶液稳定性、回收率试验等方法学验证,结果良好,适合多糖铁复合物胶囊的溶出度测定。
邻菲罗啉法测定多糖铁复合物胶囊溶出度的原理是在酸性条件下,多糖铁复合物发生消解,盐酸羟胺将解离出的Fe3+还原成Fe2+,Fe2+与1,10-菲啰啉结合生成化学性质稳定的红色络合物,通过测定红色络合物的吸光度,计算多糖铁复合物胶囊的溶出量。本方法的优点在于:①在多糖铁复合物消解过程中使用盐酸替换硫酸作为消解剂,避免了浓硫酸使用过程中的危险性;②消解过程中提高反应温度至90℃,确保多糖铁复合物被完全消解的同时,缩短了反应时间,对于检测过程更具可操作性;③在Fe3+被盐酸羟胺还原成Fe2+后的溶液中加入少量的pH 4.5 醋酸缓冲液,即可使满足Fe2+与1,10-菲啰啉结合生成稳定的红色络合物的条件,避免了醋酸缓冲液的过量加入。
[通讯作者]过对3 个批次的市售多糖铁复合物胶囊溶出结果测定,本研究方法与文献方法溶出结果相当,同时本研究方法不仅操作简便、可靠,缩短测定时间,减少时间成本,而且可以大幅减少试剂的用量,降低物质成本的同时更加有利于环境保护。

