较大胃间质瘤内镜手术治疗方法的选择及疗效分析
邹 欢 何 斌▲ 屈 霄 邱洪清 李 锐
1.江苏省张家港市第一人民医院消化内科,江苏张家港 215600;2.苏州大学附属第一医院消化内科,江苏苏州 215000
胃间质瘤是全消化道常见的间叶性肿瘤,随着胃镜及超声内 镜(endoscopic ultrasonograpy,EUS)技术的不断进步,胃间质瘤检出率已呈现逐步上升趋势。计算机断层扫描(computer tomography,CT)也是诊断胃间质瘤的主要影像学方法[1],可指导临床治疗及随访。以往胃间质瘤的治疗为外科手术[2-3]和腹腔镜手术,但随着内镜技术的发展[4],采用消化内镜治疗胃间质瘤已被国内外专家认可[5-6],研究表明,对于直径3~5 cm 的较大胃间质瘤,内镜术亦是一种安全有效的治疗手段[7-8]。胃间质瘤的内镜手术方式有内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)、内镜下全层切除术(endoscopic full-thickness resection,EFR)及经黏膜下隧道内镜切除术(submucosal tunneling endoscopic resection,STER)。本研究分析了ESD、EFR、STER 治疗直径3~5 cm 胃间质瘤患者的肿瘤特征并评估手术临床疗效,旨在为较大胃间质瘤患者手术方案的选择提供参考依据。
1 资料与方法
1.1 一般资料
回顾性分析2014年1月至2019年12月在苏州大学附属第一医院、苏州大学附属张家港第一人民医院接受内镜术的51 例胃间质瘤患者的临床资料。其中男28 例,女23 例;年龄32~82 岁,平均(58.25±10.62)岁。根据手术方式不同分为ESD 组(n=25)、EFR 组(n=20)、STER 组(n=6)。ESD 组中,男14 例,女11 例;年龄32~82 岁,平均(58.24±2.28)岁。EFR组中,男10 例,女10 例;年龄42~82 岁,平均(58.90±2.43)岁。STER 组中,男4 例,女2 例;年龄47~63 岁,平均(54.42±1.65)岁。三组患者年龄、性别比较,差异均无统计学意义(P>0.05),具有可比性。纳入标准:①术前胃镜、内镜超声提示存在胃黏膜下肿瘤,经超声内镜明确病变层次[9-10];②术前CT 评估,显示无转移病灶;③肿瘤最大直径为3.0~5.0 cm。排除标准:①同时存在食管或十二指肠病灶;②有多个胃内病灶。本研究经医院医学伦理委员会审核批准(批号:20200913)。
1.2 方法
ESD 组:采用Dual Knife(Olympus,KD-650L)于肿瘤基底部边缘标记,用注射针(Olympus,NM-200L-0432)将混合稀释液(靛胭脂∶肾上腺素∶生理盐水=3~5 ml∶1 ml∶100 ml)在病灶周围黏膜下多点注射,采用Dual Knife 将肿瘤基底周围黏膜切开,在肿瘤下方剥离黏膜下层,并完整剥离肿瘤,最后对创面电凝止血。EFR 组:采用ESD 术分离肿瘤周围直至浆膜层,再采用IT Knife(Olympus,KD-611L)或Dual Knife 将部分浆膜及肿瘤完整切除,所造成的医源性胃穿孔使用钛夹、尼龙绳联合钛夹(Micro-Tech Co,ROCC-D-26-165)或耙状金属夹闭合系统(over-the-scope clip,OTSC)[11]等缝合创面。STER 组:在瘤体近端4~5 cm 处切开黏膜层,开口大小1.5~2.0 cm,在黏膜下层及肌层间建立一纵行隧道直达瘤体,暴露病灶后完整切肿瘤,用氩离子束凝固术(argon plasma coagulation,APC)(Olympus,FD-410LR)和热活检钳处理隧道内的出血灶,最后用金属夹关闭黏膜切口。所有患者在治疗后第1、6、12 个月行胃镜检查,定期复查CT判断有无转移病灶,术后均随访1年。记录随访资料。
1.3 观察指标及评价标准
①肿瘤特征:包括患者肿瘤部位、肿瘤最大长径、肿瘤起源、肿瘤生长方式。②手术资料:包括完整切除率、术后并发症(出血和穿孔)、创面完全愈合率。③随访资料: 所有患者在治疗后第1、6、12 个月行内镜检查,并进行1年随访,同时定期复查CT 判断有转移病灶。记录随访资料。
1.4 统计学方法
采用SPSS 22.0 统计学软件进行数据分析,计量资料用均数±标准差(±s)表示,多组计量资料整体比较采用方差分析,两两比较采用LSD-t 检验;计数资料用率表示,多组率的整体比较采用χ2检验,以P<0.05认为差异有统计学意义;多组率的两两比较采用Bonferroni 方法校正,以P<0.05/n 为差异有统计学意义。
2 结果
2.1 三组患者肿瘤特征的比较
三组患者肿瘤最大长径比较,差异有统计学意义(P<0.05);ESD 组与EFR 组肿瘤最大长径比较,差异无统计学意义(P>0.05);STER 组肿瘤最大长径小于ESD 组,差异有统计学意义(P<0.001);STER 组肿瘤最大长径小于EFR 组,差异有统计学意义(P<0.001)。三组患者肿瘤部位比较,差异有统计学意义(P<0.05);ESD 组肿瘤分布于胃底、胃窦、胃体、贲门,EFR 组肿瘤主要位于胃底、少见于胃体及胃窦,STER 组肿瘤位于胃体大弯侧及贲门,本研究无胃底、胃窦病例;ESD组和EFR 组肿瘤部位比较,差异无统计学意义(P=0.086);STER 组和ESD 组、EFR 组肿瘤部位比较,差异有统计学意义(P<0.017)。三组患者肿瘤起源比较,差异有统计学意义(P<0.05);ESD 组肿瘤起源于黏膜肌层、黏膜下层,且与浆膜层存在一定距离,EFR 组肿瘤全部起源于固有肌层且与浆膜层密切相连,STER组肿瘤均起源于固有肌层;ESD 组与EFR 组、STER组肿瘤起源两两比较,差异有统计学意义(P<0.017)。三组患者肿瘤生长方式比较,差异有统计学意义(P<0.05);所有患者均行腹部CT 检查以明确肿瘤生长方式,ESD 组、STER 组肿瘤均为腔内生长,EFR 组肿瘤可腔内外生长,多为腔外生长,少数腔内生长;EFR 组和ESD 组、STER 组肿瘤生长方式两两比较,差异有统计学意义(P<0.017)(表1)。
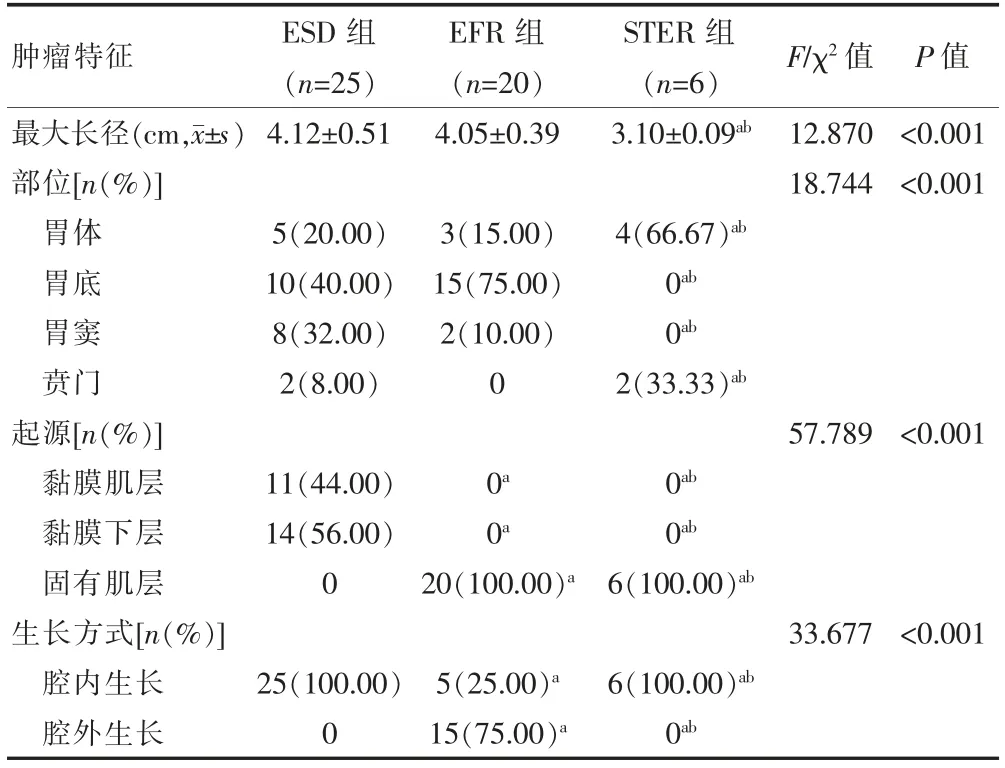
表1 三组患者胃间质瘤的肿瘤特征
2.2 三组患者手术资料的比较
ESD 组有两例患者肿瘤长径为4.0、4.6 cm 的病例未完整切除,整块切除率为92%,EFR 组、STER 组整块切除率为100%。三组患者完整切除率比较,差异无统计学意义(P>0.05)。三组患者并发症发生率比较,差异有统计学意义(P<0.05)。ESD 组有4例术后出血,无穿孔病例;EFR 组所有病例均发生主动穿孔,无术后出血病例;STER 组无并发症病例。ESD 组与STER组比较,差异无统计学意义(P=0.561);EFR 组并发症发生率高于ESD 组和STER 组,差异有统计学意义(P<0.017)。术后随访12 个月,所有患者创面均愈合良好,无一病例有病灶残留或复发(表2)。
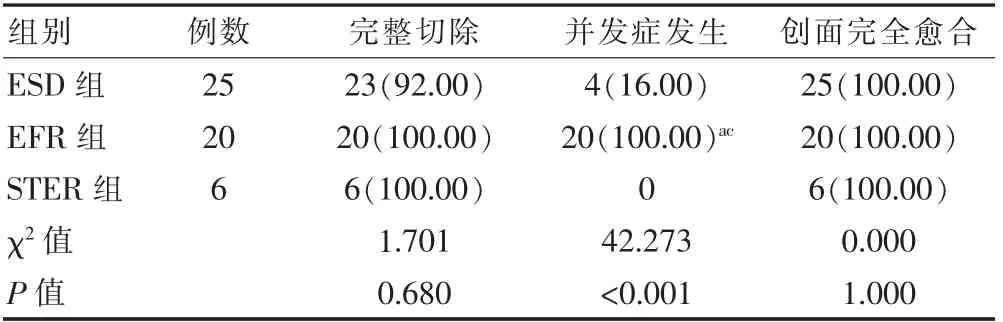
表2 三组患者手术资料的比较[n(%)]
2.3 三组患者随访资料的比较
所有患者定期复查胃镜及腹部CT,随访一年期间无患者出现复发及远处转移。
3 讨论
胃间质瘤为常见的胃黏膜下肿瘤,患者常有腹胀、腹痛、腹部肿块、呕血或便血等症状,其他症状有吞咽困难、体重下降、咳嗽、呕吐、里急后重及反复排黏液便等[12],其具有恶性倾向,难以自行消失,药物治疗无效,因此对于直径>2 cm 的胃间质瘤,主张手术切除[13]。切除肿瘤的方法有外科手术及内镜下治疗术。外科手术包括传统外科手术和腹腔镜手术,外科手术中病灶定位难度大,且术后切口感染、肠粘连等并发症发生率较高。近年来,内镜微创手术不断发展,内镜术已成为胃间质瘤的重要治疗手段,且与外科手术比较,具有一定优势。由于胃间质瘤肿瘤直径、肿瘤部位、起源层次、生长方式不同,内镜手术治疗的方式及复杂程度各有不同,故应根据肿瘤特征选择最适宜的内镜手术方式。
本研究结果显示,STER 组肿瘤部位与ESD 组、EFR 组比较,差异有统计学意义(P<0.05),提示STER更适合治疗胃体大弯侧及贲门处较大胃间质瘤。STER 组肿瘤直径小于EFR、ESD 组,差异有统计学意义(P<0.05),这是由于STER 对肿瘤直径有一定要求。ESD 组肿瘤起源于黏膜肌层和黏膜下层,EFR 组、STER 组肿瘤均起源于固有肌层,ESD 组与EFR 组、STER 组肿瘤起源比较,差异有统计学意义(P<0.05),提示ESD 适用于治疗起源于黏膜肌层和黏膜下层的肿瘤,EFR、STER 适用于治疗固有肌层间质瘤。ESD组、STER 组肿瘤均为腔内生长,EFR 组肿瘤以腔外生长为主,各组肿瘤生长方式两两比较,差异有统计学意义(P<0.05),可见ESD、STER 适用于治疗腔内生长肿瘤,EFR 可用于腔外肿瘤的治疗。
ESD 较早运用于胃黏膜下肿瘤的治疗,切除范围包括黏膜层、黏膜肌层及大部分黏膜下层,可完整切除肿瘤实现根治[14]。武育卫等[15]将ESD 用于治疗42例胃良性肿瘤,肿瘤起源于黏膜层、黏膜肌层、黏膜下层,切除肿瘤直径为1.0~4.5 cm,完全切除率为85.7%,无迟发性出血和穿孔,术后3 个月胃镜随访,无残留和复发。本研究将ESD 用于较大胃间质瘤的治疗,切除肿瘤直径为3.0~5.0 cm,适用于胃内各部位起源于黏膜肌层及黏膜下层的腔内性胃间质瘤,整块切除率高,术后随访一年无转移复发,可实现根治。EFR 为ESD 的衍生手术,可完整切除包括浆膜层在内的整个病灶,通过钛夹、尼龙绳等手段修补创面,提高手术成功率,达到安全、有效的目的,多项研究表明EFR 的安全性与其他手术方式无明显差异[16-17]。周平红等[18]将EFR 用于治疗20 例源于固有肌层的胃黏膜下肿瘤,切除病灶长径为1.8~3.5 cm,完整切除率为100%,术后随访1~12 个月无病灶残留、复发。本研究中EFR 切除较大胃间质瘤20 例,均起源于固有肌层,多位于胃底,腔外生长多见,可见更适用于胃底的腔外性较大胃间质瘤。以往研究表明,STER 治疗固有肌层肿瘤是安全有效的[19],STER 利用胃黏膜和固有肌层之间的通道进行操作,既可完整切除肿瘤,又保护消化道的完整性。徐美东等[20]用STER 治疗23 例来源于固有肌层的胃黏膜下肿瘤,瘤体直径大小为1.5~3.2 cm,贲门近胃体侧11 例,贲门近胃底侧4 例,胃体小弯5 例,胃窦大弯侧3 例,成功率为100%,随访3~18 个月,无一例病变残留或复发,同时指出由于受建立黏膜下隧道的限制(一般隧道内镜操作空间最大宽度3.5 cm),目前可采用STER 切除的黏膜下肿瘤(submucosal tumor,SMT)一般直径<3.5 cm。本研究有6 例较大胃间质瘤使用STER 术,肿瘤直径3.0~3.3 cm,位于贲门及胃体小弯侧,均为腔内生长的起源于固有肌层的胃间质瘤,切除成功率为100%。
出血和穿孔是内镜治疗的常见并发症[21]。ESD 组有4 例患者出现术后出血,均在内镜下成功止血,无一例发生大出血;EFR 组均有主动穿孔,通过内镜缝合术及术后护理均痊愈;STER 组6 例未见出血、穿孔并发症,但根据以往经验,术中一旦出现出血、穿孔并发症,则手术难度大大增加,故STER 对术者要求较高。随访结果显示,三组患者的创面愈合率100%,无患者出现局部复发或远处转移,进一步证实了内镜术治疗较大胃间质瘤的可行性。
ESD、EFR、STER 用于治疗较大胃间质瘤均可起到较好的临床效果,建议患者术前完善超声内镜及腹部CT 加以评估,根据肿瘤大小、部位、起源、生长方式选择最佳手术方式。若直径3.0~5.0 cm 的胃间质瘤为内生性、起源于黏膜肌层及黏膜下层且与浆膜层有一定距离者,可行ESD 切除肿瘤;若肿瘤起源于固有肌层并与浆膜层紧密粘连,则需行EFR,如肿瘤位于胃底,CT 提示为外生性肿瘤,则可优先考虑EFR 切除;受隧道空间限制,可用于STER 治疗的较大胃间质瘤病例较少,而且STER 手术难度相对较大,对术者要求高,同时Zhang 等[22]指出STER 治疗胃黏膜下肿瘤最佳部位为贲门,其次是胃窦大弯或胃体小弯。鉴于STER 能保持消化道完整性、避免胸腹腔感染并发症等优越性,若内生性胃间质瘤直径≤3.5 cm、位于贲门或胃体小弯侧、起源于固有肌层,在有经验丰富的术者参与手术的情况下,可尝试行STER。由于STER 受肿瘤直径、肿瘤部位等限制,因此符合本研究入组条件的病例较少。
综上所述,ESD、EFR、STER 治疗较大胃间质瘤均有较好的临床效果,可根据肿瘤部位、大小、肿瘤起源及生长方式选择不同内镜治疗术。本研究为回顾性分析,样本量较小,ESD、EFR、STER 治疗较大胃间质瘤的选择及临床疗效仍需多中心、大样本的前瞻性研究来进一步探讨。

