经后路开窗减压矫形融合内固定术治疗DLSS合并LS患者的临床疗效
田 伟,王 玺,宋泽元,寇剑铭,侯建文
(江苏省连云港市第二人民医院,江苏 连云港 222000)
退变性腰椎椎管狭窄(DLSS)是骨科常见病变类型,腰椎椎管狭窄是导致腰腿疼痛的主要原因之一,往常在行走时出现明显麻痛,间歇性跛行,部分患者可能出现偏瘫、截瘫或大小便失禁等,影响生活及工作[1]。且合并节段性腰椎不稳定(LS)会引起关节囊肥大、小关节骨质增生、椎间盘突性突出等,出现间歇性跛行或根性疼痛,严重者还可能出现马尾综合征。保守治疗仅能在短时间内缓解症状,但疗效欠佳,随后转为手术治疗。而因腰椎解剖位置特殊,选取科学、有效、安全的手术方式是临床研究重点。随着内固定技术的发展全椎板切除(LAM)椎间融合内固定手术(IF)已逐渐应用在DLSS合并LS患者中,一方面可保留传统全椎板椎管减压术较佳的减压效果,还可增强脊柱稳定性,远期效果较佳,但该术式会在一定程度上破坏脊柱后方结构,增加术后失血量,进一步增加术后并发症发生风险[2]。经后路开窗减压矫形融合内固定术(PLIF)可增强脊柱的稳定性,有效维持椎管形态及容量。当前针对到底采用何种术式对DLSS合并LS患者进行治疗尚处在研究阶段。本研究对比PLIF及LAM椎间融合IF治疗DLSS合并LS患者,并探讨对患者脊柱功能、腰椎功能障碍、疼痛程度的影响,旨在为临床治疗提供客观依据。
1 资料与方法
1.1一般资料:选取109例DLSS合并LS患者为研究对象,采用随机数字表法分为观察组(n=55)、对照组(n=54),其中观察组女32例,男23例;年龄53~78岁,平均年龄(65.44±7.33)岁;病程3~8年,平均病程(5.33±0.62)年。对照组女31例,男23例;年龄54~79岁,平均年龄(65.39±7.21)岁;病程3~9年,平均病程(5.29±0.65)年,两组一般资料有可比性(P>0.05)。
1.2纳排标准:纳入标准:①有腰痛、下肢麻木、间歇性跛行症状,且经影像学检查确诊为DLSS,且合并LS;②一般临床资料完整;③保守治疗时间在6个月以上无效者。排除标准:①合并骨质疏松患者;②因脊柱感染或肿瘤引起的椎管狭窄者;③合并严重凝血功能不全者;④对手术不耐受者;⑤有出血性疾病者。
1.3方法:对照组:LAM椎间融合IF:患者取俯卧位,全麻,去除狭窄节段全椎板、黄韧带(咬骨钳),配合影像学检查结果,咬除关节突,针对椎体不稳定者,经手术切开纤维环去除病灶,刮除软骨皮质,在椎间隙中安置椎间融合器,随后放置椎弓根钉,确保生理弧度,固定后,对病灶部位清扫。观察组:PLIF:患者取俯卧位,全麻,后正中切口,剥离棘突椎板附着肌肉,显示两侧横突、关节突、棘突椎板,止血。进针,置入椎弓根钉,在C形臂辅助下确定位置。切除病变节段部分关节突内壁及椎板,暴露椎间隙,牵开硬膜囊、神经根,扩大并松解神经根,冲洗切口。
1.4观察指标
1.4.1椎体融合情况:根据CT影片及骨痂评估两组术后3个月椎体融合情况,包括坚强:有连续骨小梁通过融合区域,且节段间相对活动度在4度以下;可能:在融合区域中出现不清晰的骨小梁,但节段间活动度在4度以下;不融合:无骨小梁通过融合区域,且节段间相对活动度在4度以上;融合率:坚强融合、可能融合例数之和占总例数比率。
1.4.2临床指标:记录两组术中失血量,手术、卧床、及住院时间,切口长度。
1.4.3脊柱矢状面形态:在术前及术后3个月确保患者无不适感情况下,采用X射线检查脊柱矢状面形态,包括腰椎前凸角(LL)、失状垂直轴(SVA)、骨盆投射角(PI)、胸椎后凸角(TK)、骨盆倾斜角(PT)。
1.4.4功能障碍程度及疼痛程度:应用ODI评估评估脊柱功能障碍,总分45分,得分越高,患者脊柱功能障碍越严重。采用JOA评估人体功能障碍性:29分满分,分数越低,患者功能障碍越严重。采用VAS评估腰背疼痛,0分为无疼痛,10分为剧烈疼痛,得分越高,患者疼痛程度越严重。
1.4.5腰椎稳定性:在术前及术后3个月确保患者无不适感情况下,采用X射线检查椎间隙高度、椎间孔高度、腰椎前凸角。
1.4.6并发症:包括神经损伤、硬膜撕裂、椎间盘炎、脑脊液漏、椎间隙感染发生情况。

2 结 果
2.1两组椎体融合率比较:观察组术后1年椎体融合情况明显高于对照组,差异有统计学意义(P<0.05),见表1。

表1 两组椎体融合率比较
2.2两组手术情况:观察组术中失血量显著低于对照组,手术时间、卧床时间、住院时间及切口长度短于对照组,差异有统计学意义(P<0.05),见表2。

表2 两组手术情况比较
2.3两组脊柱矢状面形态比较:术前两组LL、SVA、PI、TK、PT比较,差异无统计学意义(P>0.05),术后两组LL、SVA、PI、TK、PT均显著降低,两组手术前后以上指标差值均比较,差异无统计学意义(P>0.05),见表3。

表3 两组脊柱矢状面形态比较
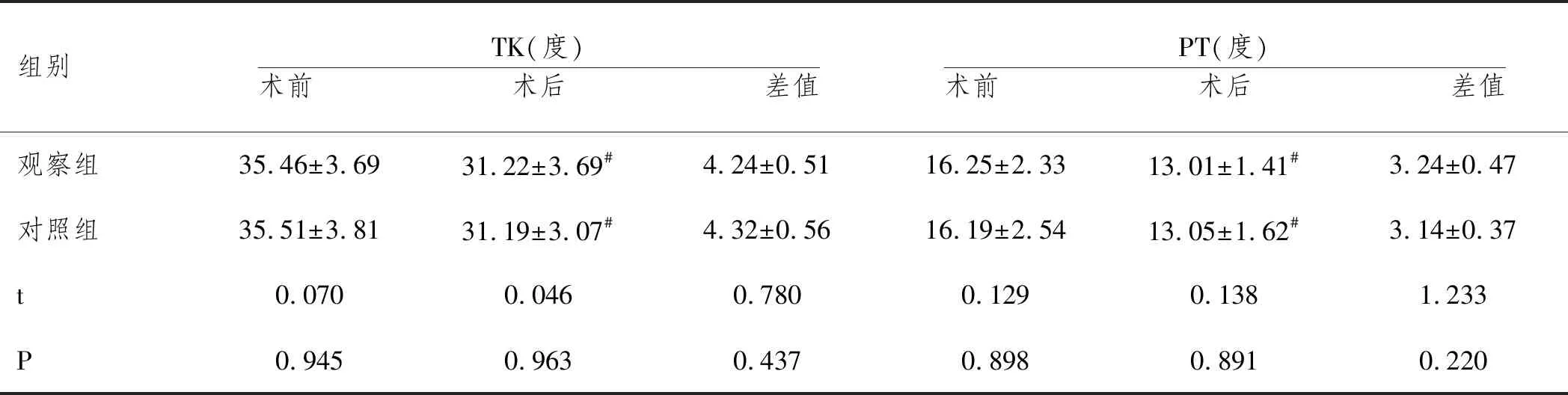
组别TK(度)术前 术后 差值PT(度)术前 术后 差值观察组35.46±3.6931.22±3.69#4.24±0.5116.25±2.3313.01±1.41#3.24±0.47对照组35.51±3.8131.19±3.07#4.32±0.5616.19±2.5413.05±1.62#3.14±0.37t0.0700.0460.7800.1290.1381.233P0.9450.9630.4370.8980.8910.220
2.4两组ODI评分、VAS评分、JOA评分比较:术前两组ODI评分、VAS评分、JOA评分比较,差异无统计学意义(P>0.05),术后两组ODI评分、VAS评分均显著降低,JOA评分升高,且两组手术前后ODI评分、VAS评分、JOA评分差值比较,差异有统计学意义(P<0.05),见表4。

表4 两组ODI评分 VAS评分 JOA评分比较
2.5两组腰椎稳定性比较:术前两组椎间隙高度、椎间孔高度、腰椎前凸角比较,差异无统计学意义(P>0.05),术后两组椎间隙高度、椎间孔高度、腰椎前凸角均显著升高(P<0.05),且两组手术前后椎间隙高度、椎间孔高度、腰椎前凸角差值比较,差异有统计学意义(P<0.05),见表5。

表5 两组腰椎稳定性比较
2.6两组并发症比较:观察组术后并发症发生率显著低于对照组,差异有统计学意义(P<0.05),见表6。
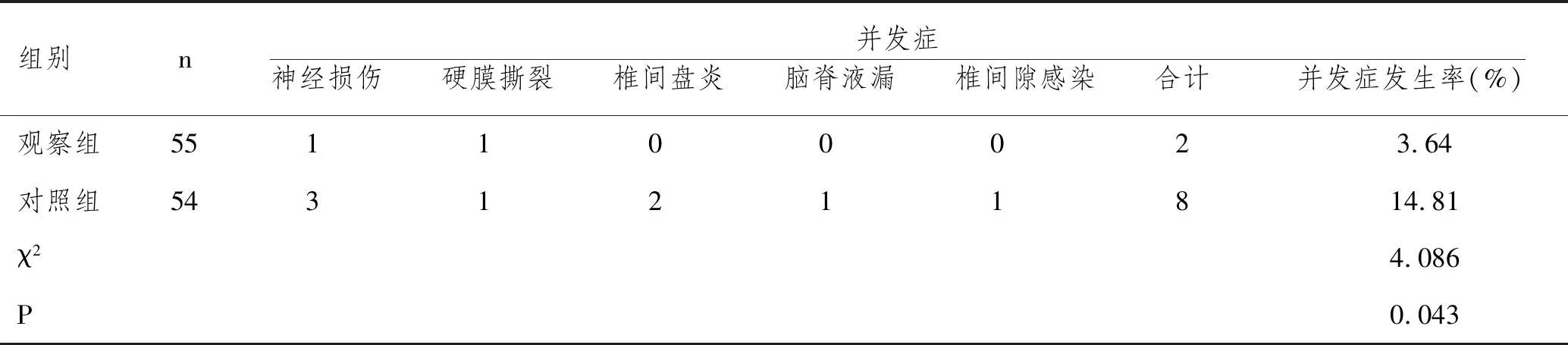
表6 两组并发症比较
2.7手术前后图片展示:①患者卞某,男性,55岁,术前诊断:L3/4、L4/5椎管狭窄合并腰椎不稳,行腰椎后路LAM减压融合IF,见图1。②患者李某,女性,67岁,术前诊断:L3/4、L4/5椎管狭窄合并腰椎不稳,行PLIF,见图2。
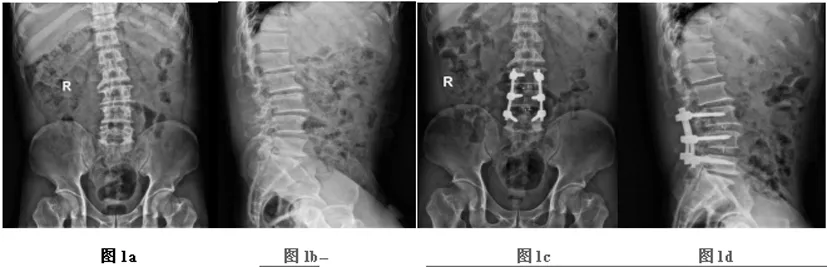
图1 患者卞某手术前后图片
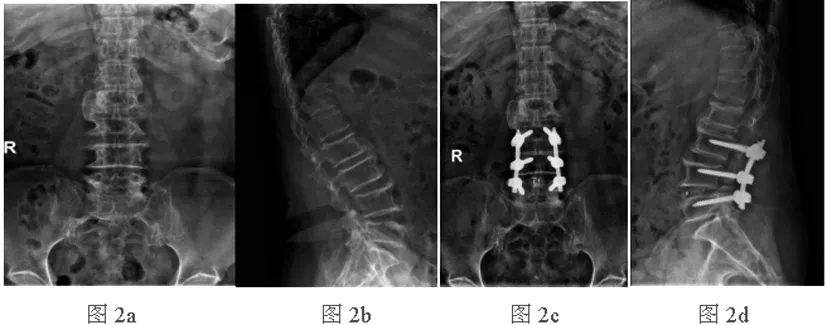
图2 患者李某手术前后图片
3 讨 论
DLSS是多种因素引起的软骨组织与腰椎骨组织、形态结构变化的疾病,患者马尾神经受到刺激后会出现出现一系列症状[3]。好发于50岁以上患者,退变多在椎间盘,压迫神经根、硬膜囊及马尾,而椎间隙变窄亦会影响椎间稳定性,增加了局部负荷,出现增生肥大,诱发反复性腰痛、椎间隙变窄等症状,患者生活及工作受到影响,因此选择科学、有效的手术方式治疗是临床亟待解决的问题[4]。
本研究发现PLIF治疗DLSS合并LS患者融合效果显著优于LAM椎间融合IF,分析可能是因为LAM椎间融合IF在术中对表面软骨刮除过多,导致融合器失去重要支撑结构,出现融合器不稳定及沉陷,最后移位[5]。而PLIF可选择性减压,并保护脊柱后部结构,在术后稳定性较强。但亦有研究提出,融合器本身形状及接触面积大小均会影响手术稳定性,提示临床在治疗中,需注意融合器的选择,必须与椎间隙高度一致,选择合适融合器[6]。本研究发现PLIF较LAM椎间融合IF治疗DLSS合并LS患者,更能促进患者术后恢复,减少术中失血量,分析可能是因为PLIF实施原理主要是经扩张椎管进行减压,开窗大小多取决于患者神经压迫范围,但切口程度总体相对较小,因此失血量较少;另外PLIF较LAM椎间创伤小,因此手术时间更短,恢复更快[7]。
本研究发现,术后两组LL、SVA、PI、TK、PT均显著降低,但两组手术前后以上指标差值均比较无显著差异,提示PLIF及LAM椎间融合IF手术,均能有效改善DLSS合并LS患者脊柱矢状面形态,且效果相当。中老年人腰椎多合并基础疾病,合并退行性改变,且部分患者还合并LS,增加了临床治疗难度。本研究发现PLIF及LAM椎间融合IF,均能有效降低机体功能性障碍程度,促进脊柱功能恢复,且前者效果更佳,分析可能是因为,后者减压彻底,可较佳恢复椎管容积,在短期内改善患者临床症状,但该术式对局部组织结构破坏较大,增加了中老年患者手术风险,融合后节段僵硬,增加了相邻节段压力,致使关节不稳,影响术后肢体功能恢复;而前者不仅可实现有效减压,还可有效保护术中组织,利于术后功能恢复[8]。本研究还发现PLIF较LAM椎间融合IF,更能降低术后疼痛程度,分析可能是因为前者创伤较小,损伤较小,且对脊柱后方组织保护作用较佳,可有效抑制瘢痕组织异常增生,降低术后疼痛[9]。本研究还发现,PLIF及LAM椎间融合IF,均能有效改善DLSS合并LS患者腰椎稳定性,且前者效果更佳,分析可能是因为前者经单侧进入病灶,切除突出椎间盘及增厚的韧带,可从根源上降低神经压力,并减少刺激、压迫神经根,改善症状,另外椎弓根螺钉的对腰椎节段病变部位进行内固定,可保证腰椎正常生理弯曲,并维持前凸,与脊柱正常功能,提高稳定性。而后者可在一定程度上减压,但会在损伤腰椎后柱张力,但不利于术后恢复,亦可能影响稳定性的恢复。本研究中PLIF及LAM椎间融合IF治疗DLSS合并LS患者均较为安全,但前者术后并发症更低,可能与创伤较小有关。
综上所述,PLIF及LAM椎间融合IF,在DLSS合并LS患者中应用较佳,在改善脊柱形态、腰椎功能稳定性方面效果相当,但前者具有失血少、创伤小,术后疼痛程度更低、更能降低肢体功能障碍等优势。

