玻璃体内注射雷珠单抗后视网膜静脉阻塞性黄斑水肿复发的预测因素分析△
梁雁雁 樊 芳 贾志旸
视网膜静脉阻塞(RVO)是继糖尿病视网膜病变后的第二大致盲性眼底病变[1]。依据发生的部位可分为视网膜中央静脉阻塞(CRVO)、视网膜分支静脉阻塞(BRVO)、视网膜半侧静脉阻塞(HRVO)[2]。BRVO和CRVO发生率较高。黄斑水肿(ME)是导致RVO患者视力下降的最主要的原因[3]。目前针对RVO性ME的治疗方式多样,其中玻璃体内注射抗血管内皮生长因子(VEGF)为一线的治疗方案[4-6]。RVO性ME作为一种慢性易复发的疾病,需长期随访评估,所以早期寻找合适的随访指标预测ME的复发以及时发现ME变化就显得尤为重要。本研究即以RVO性ME患者为研究对象,分析RVO性ME复发的可能相关危险因素。
1 资料与方法
1.1 一般资料回顾性分析2020年1月至2021年4月河北省人民医院眼科确诊的未经治疗的RVO性ME患者62例(62眼),均接受玻璃体内注射雷珠单抗治疗,治疗均按照1+PRN的方案进行,每位患者至少随访6个月。依据术后6个月内是否进行额外注射将患者分为两组,未进行额外注射的患者纳入未复发组,仍有额外注射的患者纳入复发组。ME的消退定义为玻璃体内注射雷珠单抗治疗后黄斑中央凹视网膜厚度(CRT)<300 μm 或 CRT较治疗前下降≥10%,并且无残留视网膜内囊腔或视网膜下液的证据。复发的ME定义为ME消退后再次出现 CRT>300 μm,或 CRT<300 μm但出现新的视网膜囊腔或视网膜下液[7]。比较两组患者的基线资料,分析影响ME复发的相关因素。
1.2 纳入及排除标准纳入标准:(1)OCT显示CRT>300 μm;(2)同意并接受玻璃体内注射雷珠单抗治疗;(3)能配合治疗并坚持随访者;(4)随访时间不少于6个月。排除标准:(1)合并其他眼底疾病,如糖尿病视网膜病变、年龄相关性黄斑变性、视网膜血管炎等;(2)伴有青光眼或屈光间质严重混浊的患者;(3)既往接受过玻璃体内注射、眼底激光或视网膜手术者;(4)合并视网膜功能异常的系统性疾病者;(5)不能配合检查者。本研究符合《赫尔辛基宣言》原则,通过河北省人民医院伦理委员会审批。
1.3 注射方法所有患者在行玻璃体内注射雷珠单抗前进行全身检查及眼科专科检查,排除手术禁忌证,同时告知患者及家属该治疗的目的及手术相关注意事项,并签署手术知情同意书。所有患者术前使用盐酸左氧氟沙星滴眼液滴眼,每天4次。术前使用复方托吡卡胺滴眼液散瞳,患者取仰卧位,常规消毒铺巾,开睑器开睑,50 g·L-1聚维酮碘消毒结膜囊后,生理盐水冲洗结膜囊3次,盐酸丙美卡因滴眼液对术眼进行表面麻醉。自11点钟位距离角膜缘4 mm处于睫状体平坦部垂直进针,向玻璃体内注射雷珠单抗0.05 mL(0.5 mg)。注射完毕后迅速拔出针头,并按压注射部位数秒直至无返流。结膜囊内涂妥布霉素地塞米松眼膏后包扎术眼,手术结束。术后常规使用5 g·L-1盐酸左氧氟沙星滴眼液滴眼,每天4次,持续1周。
1.4 观察指标记录患者的性别、年龄、发病眼别、病程、RVO类型、视网膜激光治疗史,及高血压病史、总胆固醇、甘油三酯情况。所有患者在术前1 d接受详细的眼科检查,包括BCVA(转换为logMAR形式记录)和眼压的测量,裂隙灯检查、散瞳眼底检查、荧光素眼底血管造影、OCT检查等。使用日本拓普康DRI OCT Triton型OCT仪评估黄斑区的结构变化,包括:(1)ME的类型:弥漫性视网膜增厚型、黄斑囊样水肿型、浆液性视网膜脱离型以及混合型[7];(2)CRT:黄斑中心凹处内界膜与视网膜色素上皮(RPE)层之间的距离,使用OCT系统自带软件自动测量;(3)视网膜下液(SRF);(4)黄斑前膜(ERM);(5)玻璃体黄斑牵拉(VMA);(6)视网膜高反射病灶(HRF);(7)视网膜内层紊乱(DRIL);(8)外界膜及椭圆体带的连续性;(9)RPE层的完整性。术后每月随访,重复所有检查项目。若需要再次行玻璃体内注射,则实行相同的随访计划,并记录注射次数。
1.5 统计学方法应用SPSS 24.0统计学软件分析数据。计量资料用均数±标准差表示,组间比较采用独立样本t检验;计数资料用率或百分比表示,组间比较采用χ2检验。多因素分析利用Logistic回归分析预测影响RVO性ME复发的独立危险因素。检验水准:α=0.05。
2 结果
2.1 未复发组与复发组基线资料比较共纳入62例RVO性ME患者,均为单眼发病,其中男30例,女32例,年龄23~83(58.16±11.47)岁;右眼39例,左眼23例。分析其ME的类型,弥漫性视网膜增厚型14例(22.6%),黄斑囊样水肿型21例(33.9%),浆液性视网膜脱离型8例(12.9%),混合型19例(30.6%)。62例患者在行第1次玻璃内注射后,CRT均下降,随访6个月期间有27例ME无复发,未再次行玻璃体内注射雷珠单抗治疗。35例患者在随访过程中因ME复发再次或多次行玻璃体内注射雷珠单抗治疗,其中注射2次者10例,注射3次者15例,注射4次者9例,注射6次者1例。将行1次注射的患者纳入未复发组,多次注射者纳入复发组,比较两组患者间的基线资料,发现复发组患者的注射次数多,CRT厚,伴有HRF者多,合并高血压者多,差异均有统计学意义(均为P<0.05);两组患者间其余观察指标相比差异均无统计学意义(均为P>0.05)(表1)。
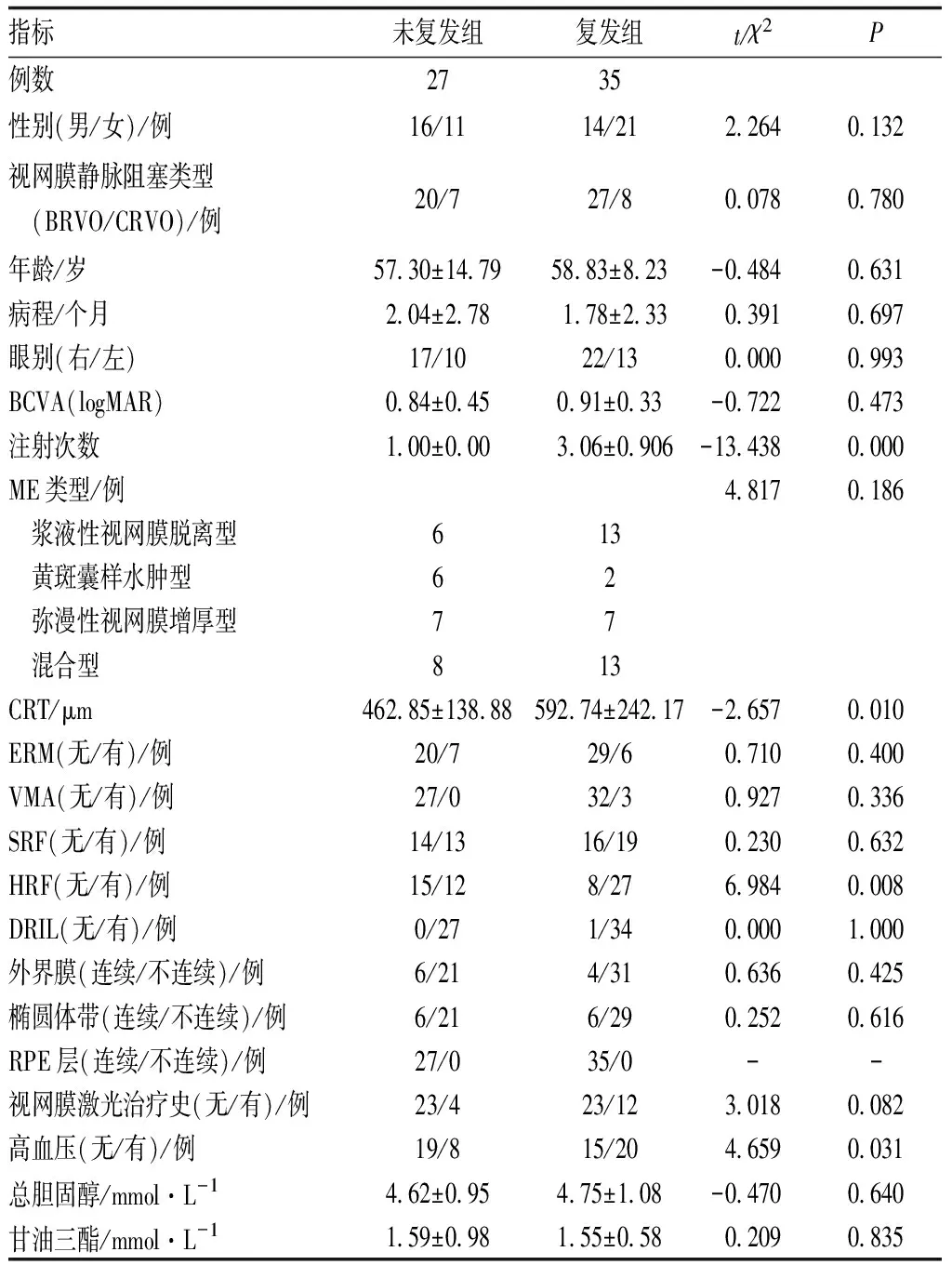
表1 RVO性ME患者基线资料
2.2 回归分析
2.2.1 二元Logistic回归分析二元Logistic回归分析多变量相互作用下RVO性ME复发的影响因素,在构建Logistic回归模型时采用逐步向前策略,将单因素分析中P<0.05的变量纳入模型。结果显示,基线CRT越厚以及伴有HRF的患者,在玻璃体内注射雷珠单抗治疗后RVO性ME复发的风险就越大(表2)。
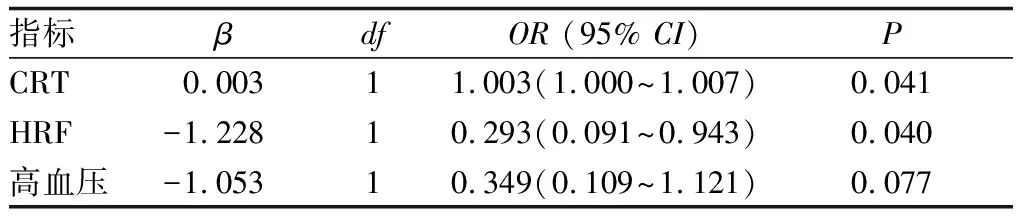
表2 RVO性ME复发影响因素的二元Logistic回归分析
2.2.2 有序Logistic回归模型分析有序Logistic 回归模型分析注射次数与影响RVO性ME复发因素之间的相关关系。以注射次数为因变量(1=注射1次;2=注射2次;3=注射3次;4=注射4次),自变量包括CRT、是否伴有HRF以及是否合并高血压。平行线检验显示有序Logistic回归模型有意义(P=0.189),CRT为影响注射次数的独立危险因素,即基线时CRT越厚则多次行玻璃体内注射的风险就越大(表3)。ROC 曲线分析显示,基线 CRT=482.5 μm(曲线下面积:0.661;灵敏度:68.6%;特异度:63.0%)是RVO性ME复发的临界值(图1)。
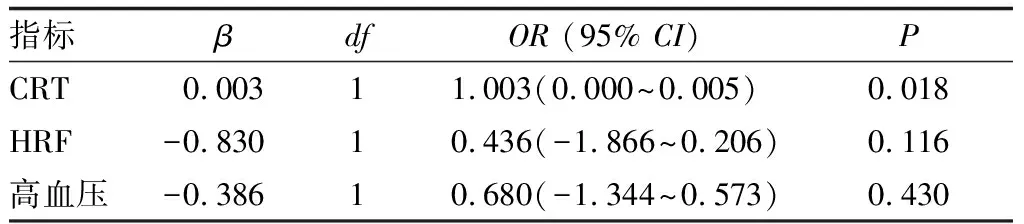
表3 注药次数的影响因素有序Logistic回归分析
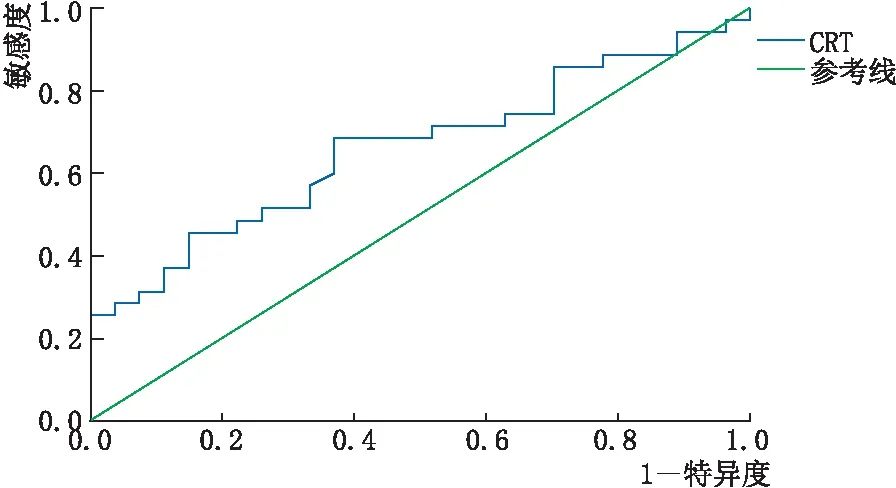
图1 基线CRT预测ME复发的ROC曲线
3 讨论
RVO发生后,静脉回流受阻、静脉血管迂曲扩张、视网膜循环障碍,沿视网膜静脉分布的区域缺血、缺氧,多种细胞及细胞因子参与,造成视网膜组织和结构的损伤,液体的进出平衡被打乱,进而发生ME等并发症。其中最重要的参与疾病发生发展过程的因子为VEGF,这使玻璃体内注射抗VEGF药物成为RVO性ME的一线治疗方式[8]。在抗VEGF治疗起始阶段,大部分的患者均会表现出积极的应答,但同时部分患者需要反复注射抗VEGF药物以阻断疾病的发展,维持视力的稳定。在临床工作中,因为RVO性ME的反复发作、复诊复查频繁以及检查治疗费用高昂,所以在治疗初期对现有的临床资料进行分析,评估预期治疗效果,进行个体化治疗成为眼科医生的重要工作。
目前,关于RVO性ME进行抗VEGF治疗后复发因素分析和预测的研究较少。国外研究结果表明,患者发病的年龄与ME的复发具有显著相关性,越高龄的患者,ME越容易复发[9]。这可能与老年患者的视网膜动静脉血管交叉处狭窄更加明显,更容易产生视网膜血流循环障碍有关[10];另外,年龄越大者视网膜血管内的血液流变学变化和血管内皮细胞退化更易发生[11]。本研究的结果也显示,复发组患者的平均年龄要稍高于未复发组患者,但两组间差异无统计学意义,可能与样本量较少有关。
以往多项研究证实,基线CRT与ME的复发呈显著正相关[7,9,12],本研究通过对患者基线时CRT的观察得出了相同的结论,复发组患者的CRT明显厚于未复发组,且差异有统计学意义(P=0.010)。多因素分析Logistic回归模型分析也显示基线时CRT厚是ME复发的一项独立危险因素,并且与玻璃体内注射次数密切相关。Tilgner等[13]发现,在接受抗VEGF药物治疗的BRVO患者中,黄斑囊性改变可作为ME复发的早期指标。本研究复发组患者的浆液性视网膜脱离型和混合型ME类型计数大于未复发组,但ME类型与复发之间未见显著联系,将各种水肿类型进行两两比较也未出现统计学差异。考虑可能与本研究样本量较少有关,后续应继续加大样本量进一步分析。
以往的研究结果也表明,DRIL以及HRF的存在是RVO性ME复发的危险因素[14-15]。DRIL定义为神经节细胞层、内丛状层复合物、内核层和外丛状层之间的界限不清,现多被认为与视网膜血流异常具有相关性[16],所以受DRIL影响的区域持续缺氧,导致VEGF的过度表达,使ME复发。由于本研究主要统计患者初发病时的OCT表现,RVO发生后,视网膜循环受阻,相关组织缺血、缺氧严重,所以多数患者均表现出DRIL,这可能是本研究中DRIL在两组患者间差异无统计学意义的原因。HRF则多被认为与视网膜的炎症反应相关[17],HRF数量的增加情况可能表明视网膜中炎症反应的过程。本研究结果显示,复发组伴有HRF的患者明显高于未复发组,二元Logistic回归分析结果显示,HRF是ME复发的危险因素。这提示我们,在发现患者存在大量HRF时,单独使用抗VEGF药物可能不能达到预想的疗效,此时应考虑多因素的作用机制。
本研究结果还表明,全身高血压病史与ME复发相关。以往的研究显示,高血压是RVO发生的危险因素[18],但很少有关于高血压与RVO性ME复发相关关系的报道。Tomita等[19]研究显示,全身高血压史与注射抗VEGF药物的次数密切相关。由于长期存在的高血压可引起全身小血管管壁发生变性,使管腔狭窄,静脉回流受阻,所以持续的高血压状态会影响视网膜血管的循环状态,导致毛细血管的不断渗漏。Kida等[20]研究表明,RVO性ME患者在治疗全身高血压后,RVO伴随的ME也随之改善。
综上所述,本研究结果发现,基线 CRT厚、伴有HRF和高血压与玻璃体内注射雷珠单抗后RVO性ME的复发具有相关性,其中基线CRT厚与伴有HRF更是ME复发显著的高危因素。在临床工作中,面临基线 CRT 较厚,伴有HRF、高血压以及全身基础疾病较多的患者,应向患者及家属说明在其诊疗过程中需要进行追加注射的可能性。本研究的不足之处是,作为回顾性研究,未能更加详细地了解患者眼底血流以及眼内细胞因子等情况是否是RVO性ME的危险因素,后期应扩大样本量深入分析。

