肝硬化门静脉高压症患者脾切除后早期血栓形成与Janus激酶-信号转导和转录激活因子信号通路的关系
王 欢, 申晓旭, 陈良琪, 龚天兰
贵州医科大学附属医院 感染科, 贵州 550002
肝硬化门静脉高压症指的是由于肝组织过度纤维化导致门静脉系统压力增加从而引发的一系列症候群,是临床肝硬化患者的常见病和多发病[1]。目前对于肝硬化门静脉高压的手术治疗方式,主要为脾切除联合贲门周围血管离断术[2]。而患者术后形成门静脉血栓是肝硬化门静脉高压患者脾切除术后发生的严重并发症之一。报道[3-4]显示,患者术后门静脉血系统血栓的发生率可高达22.2%~37.5%,但是由于大部分患者发生门静脉血栓后早期临床症状不明显,导致患者治疗不及时,治疗效果不佳,从而可能危及患者生命安全。目前,关于患者术后发生门静脉血栓的机制尚未阐明,研究患者术后门静脉血栓发生机制,对于术后门静脉血栓的预防和治疗具有着重要价值。本研究探讨分析肝硬化门静脉高压患者脾切除后血栓形成情况与Janus激酶-信号转导和转录激活因子信号通路的关系,现报道如下。
1 资料与方法
1.1 研究对象 选取2018年3月—2020年4月在本院因肝硬化门静脉高压行脾切除断流术患者198例作为研究对象,其中,男117例、女81例,年龄23~75岁,平均年龄(48.93±11.54)岁;BMI(22.97±3.16)kg/m2。乙型肝炎肝硬化患者135例、丙型肝炎肝硬化患者32例、酒精性肝硬化患者22例,原发性胆汁性肝硬化患者7例,特发性门静脉高压患者2例。
术后随访3个月,根据患者术后是否发生门静脉血栓将其分为血栓组(n=41)和非血栓组(n=157)。采用彩超检测门静脉血栓情况,采用SIEMENS ACUSON S2000彩色多普勒超声诊断仪,3.0~5.0 MHz宽频凸阵探头,清晨空腹左侧卧位,于右上腹肋间斜切面监测门静脉主干及分支血栓情况。所有患者均在术后1周、出院前行腹部彩超检测,任何一次检查出血栓均纳入血栓组。
1.2 纳入标准与排除标准 纳入标准:(1)术前均经临床诊断为肝硬化门静脉高压症,且经胃镜检查证实患者存在食管胃底静脉曲张,曲张静脉直径5 mm以上或可见红色征(曲张静脉表面出现鞭痕样、樱桃红样或血泡样改变)时行试管静脉套扎联合胃底静脉硬化剂注射;(2)消化道无出血史;(3)符合脾切除断流术手术指征,包括脾功能亢进以及脾大引起的白细胞、血小板减低,食道静脉红斑,且术前评估可耐受手术治疗;(4)肝功能Child-Pugh分级A~B级;(5)患者及其家属自愿签署知情同意书。
排除标准:(1)合并肝癌或其他恶性肿瘤患者;(2)术前合并凝血功能异常(包括凝血四项指标、血小板、血栓弹力图异常)或术前已经有血栓形成;(3)由于其他原因需要进行抗凝治疗患者;(4)术前合并机体重要器官功能障碍;(5)术后发生胰瘘、腹腔出血或合并严重感染等相关并发症患者;(6)术后3个月内因非门静脉血栓并发症死亡患者。
1.3 方法
1.3.1 术后处理方法 患者均行脾切除术,且均由本院同一组手术医护人员执行,于左肋缘下作切口切除肿大脾脏,离断食管下段至少6 cm及以上半胃浆膜层全部血供,胃冠状静脉、左膈下静脉以及胃短静脉等,包括与上述血供静脉伴行的同名动脉以及迷走神经干。用细线间断缝合胃大下弯前后壁浆膜,使其浆膜化。
术后给予患者门静脉血栓预防抗凝措施,包括术后12 h开始应用低分子肝素,200 IU/kg体质量/12 h皮下注射,连续注射5 d;进食后停用低分子肝素,改用口服华法林2.5 mg/d抗凝治疗6个月,抗凝目标为:凝血酶原活动度50%~70%,国际标准化比值1.25~1.50。当术后血小板超过正常值上限后单用或者联合使用抗血小板药物治疗,包括双嘧达莫、阿司匹林以及噻氯匹定等,直至血小板恢复正常值后停止使用。
1.3.2 临床资料收集 收集并记录患者临床资料,包括姓名、性别、年龄、肝功能Child-Pugh分级、是否为病毒性肝炎、静脉曲张严重程度分级、术前内镜下治疗、是否合并门静脉高压性胃病、手术前后门静脉直径、手术前后门静脉流速差、手术前后门静脉压力差、脾容量(经腹部B超检查测量)、腹水量、手术时间、术中出血量、BMI、术后7 d血清C反应蛋白(CRP)、视觉模拟评分(VAS)。
1.3.3 JAK-STAT通路表达检测 分别于术前1 d、术后7 d,抽取两组患者清晨空腹静脉血,采用淋巴细胞分离液分离外周血单个核细胞,采用Trizol试剂提取外周血单个核细胞中总RNA,并用紫外分光光度计检测总RNA纯度和浓度。按照逆转录试剂盒将RNA逆转录为cDNA,将逆转录后的cDNA储存于-20 ℃冰箱内备用。引物由Invitrogen公司合成,引物序列为,JAK2上游引物:5′-TTCTACATGGGGGGATAG-3′,下游引物:5′-TAAGTATGGAAACCCTCTAA-3′;STAT3上游引物:5′-GGTTAGAACCCTACACGAAG-3′,下游引物:5′-CTACAGA GCCCACTATCCG-3′;β-actin上游引物:5′-CGTGGACATCCGCAAA GAC-3′;下游引物:5′-AAGAAAGGGTGTAACGCACT-3′。采用实施荧光定量PCR法进行检测,反应条件为:94 ℃ 3 min;94 ℃ 10 s,55 ℃ 30 s,72 ℃ 45 s,共完成35个循环。以β-actin作为内参基因,采用2-△△Ct法计算目的基因相对表达量。

2 结果
2.1 单因素分析 血栓组41例患者经治疗后,血栓均消失。血栓组患者术前门静脉直径、术后门静脉直径、门静脉流速差、脾容积均显著高于非血栓组(P值均<0.05)(表1)。
2.2 两组手术前后JAK-STAT通路表达 术后两组患者外周血单个核细胞JAK2 mRNA及STAT3 mRNA相对表达量较术前显著升高(P值均<0.05),同时血栓组患者JAK2 mRNA及STAT3 mRNA相对表达量升高程度明显高于非血栓组(P值均<0.05)(表2)。
2.3 多因素Logistic回归分析 对上述比较具有统计学意义的各因素进行多因素logistic回归分析,结果显示,门静脉流速差、术后JAK2 mNRA、术后STAT3 mRNA及术前门静脉直径为影响患者术后门静脉血栓发生的重要因素(P值均<0.05)(表3)。
2.4 ROC曲线分析术后JAK2 mRNA、STAT3 mRNA对门静脉血栓的预测价值 采用ROC曲线分析患者术后JAK2 mRNA、STAT3 mRNA相对表达量对门静脉血栓预测价值,结果显示,ROC曲线下面积分别为0.850、0.787(表4,图1)。
3 讨论
肝硬化门静脉高压主要临床表现为脾肿大以及脾功能亢进,同时伴有腹水、便血、呕血等。目前对于肝硬化门静脉高压患者行脾切除的目的主要包括:改善脾功能亢进而引起的血小板减少,减少门静脉血流、降低门静脉高压,改善食管胃底静脉曲张,减少消化道再次出血倾向[5-6]。目前研究[7]显示,对于肝硬化门静脉高压患者采取脾切除术治疗,其临床效果显著,既能有效降低患者门静脉压力,又能有效纠正机体脾功能亢进状态。
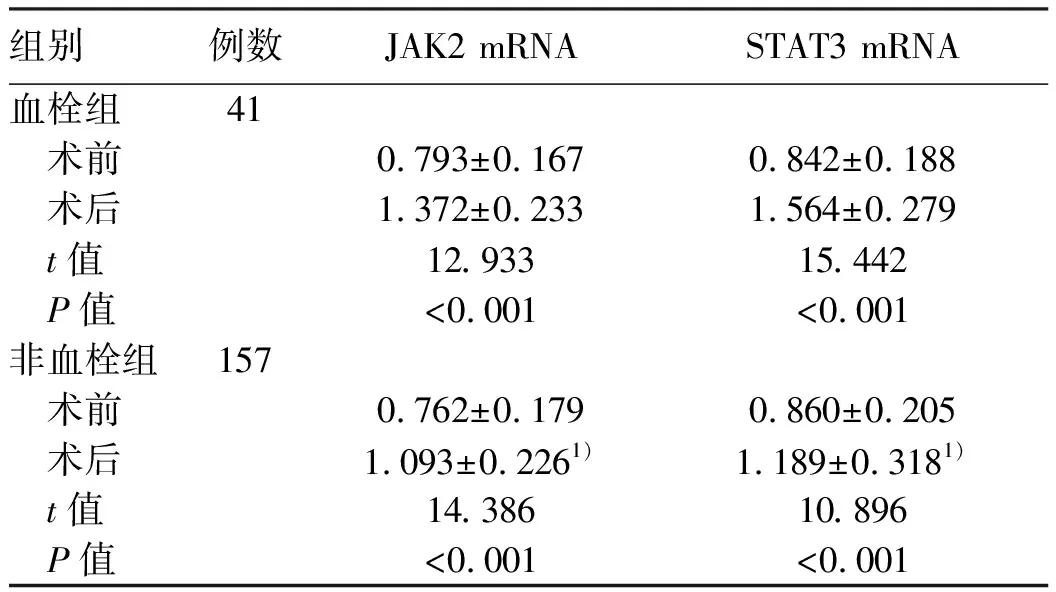
表2 两组患者手术前后JAK-STAT通路表达
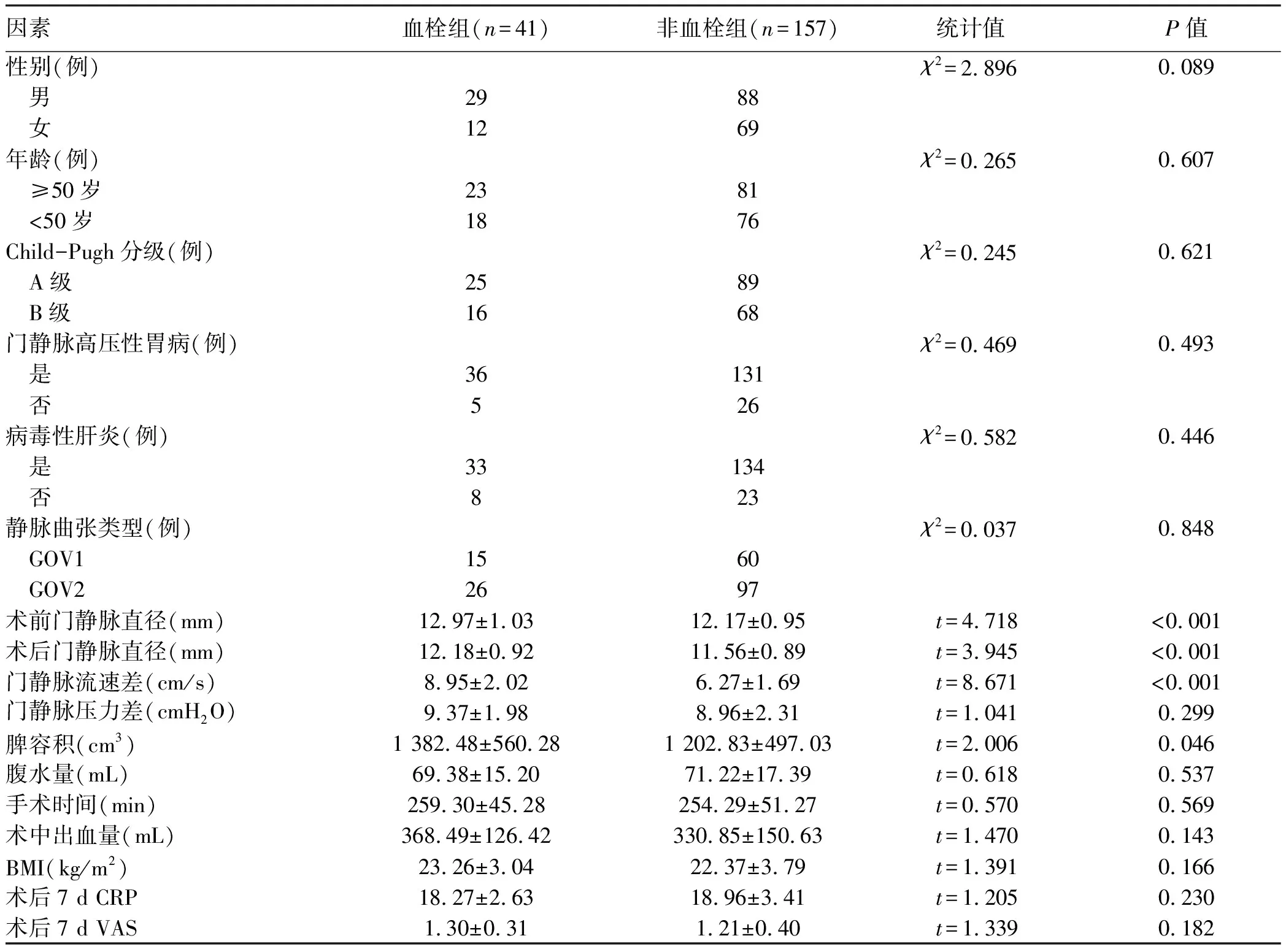
表1 单因素分析

表4 术后JAK2 mRNA、STAT3 mRNA对门静脉血栓预测价值ROC曲线分析
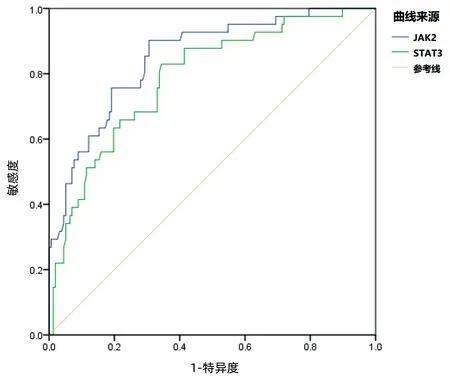
图1 ROC曲线分析术后JAK2 mRNA、STAT3 mRNA对门静脉血栓的预测价值
血小板是血液的有形成分之一,有一定的形态和体积,是由骨髓巨核细胞质裂解而来的无核细胞,血小板可通过释放凝血因子、黏附以及聚集等功能在止血过程中发挥重要作用[8-9]。对于肝硬化患者,由于脾功能亢进、脾脏肿大以及患者血液中存在抗性血小板抗体或抗巨核细胞抗体,而导致机体血小板数量减少,同时加之存在骨髓抑制从而引起血小板功能的减退[10-11]。而脾切除后,患者血液流变学可出现血液黏滞度增加,机体呈现高凝状态,同时血小板可出现反跳性增高,因此患者术后容易出现门静脉血栓等相关并发症,对患者治疗预后造成严重影响[12-13]。
血栓形成作为围术期的常见并发症之一,研究[14-15]认为,血栓形成是一个涉及多基因、多系统的过程,深入分析血栓形成相关基因及其调控途径,对于及时诊断和有效治疗血栓的形成具有重要意义。JAK/STAT信号通路是细胞因子信号转导的重要途径之一,该信号可将细胞膜感受到的信号直接传递至核内,从而激活靶基因的转录[16-17]。动物实验[18]结果显示,JAK/STAT信号通路参与大鼠术后深静脉血栓的形成过程,认为JAK/STAT信号通路末端效应基因的异常表达,可调控血管内皮细胞功能而影响血管内皮细胞的凋亡和周期等,同时JAK/STAT信号通路可能通过氧化应激、炎症通路等作用而促进术后深静脉血栓的形成。关于肝硬化门静脉高压患者术后门静脉血栓形成是否有JAK/STAT信号通路的参与,尚无相关研究报道。
本研究比较了可能影响患者术后血栓形成的各因素,结果显示,除了术前门静脉直径、术后门静脉直径、门静脉流速差、脾容积两组比较具有差异外,研究可见两组患者手术前后JAK/STAT信号通路主要基因JAK2 mRNA及STAT3 mRNA表达也出现了明显变化。初步验证了JAK/STAT信号通路可能参与患者术后门静脉血栓的形成,与笔者推测结果一致。此外,通过多因素Logistic回归分析显示,术后JAK2 mRNA及STAT3 mRNA表达水平进入回归模式,可能是影响患者术后门静脉血栓发生的重要因素;此外,采用ROC曲线分析患者术后JAK2 mRNA、STAT3 mRNA相对表达量对门静脉血栓预测价值,结果显示,ROC曲线下面积分别为0.850、0.787(P<0.05)。提示患者术后JAK/STAT信号通路的激活可能是门静脉血栓形成的重要机制之一,术后JAK/STAT信号通路状态可有效预测门静脉血栓的形成,有望成为患者术后门静脉血栓预防和治疗的潜在生物学途径,但是其具体的作用途径和下游影响基因,还需要进一步研究深入探讨分析。
伦理学声明:本研究方案于2017年12月23日经由贵州医科大学附属医院伦理委员会审批,批号:伦(审)2017-12-89。所纳入患者均签署知情同意书。
利益冲突声明:本研究不存在研究者、伦理委员会成员、受试者监护人以及与公开研究成果有关的利益冲突。
作者贡献声明:王欢负责课题设计,资料分析,撰写论文;申晓旭参与收集数据,修改论文;陈良琪、龚天兰负责拟定写作思路,指导撰写文章并最后定稿。

