2D TSE与3D SPACE序列对直肠癌术前T分期的诊断价值比较
马文帅,高远翔,高耸,郝小磊,冯卫华
青岛大学附属医院放射科,山东 青岛 266555;*通信作者 冯卫华 fengweihua@qdu.edu.cn
2020年全球结直肠癌的新发病例超过190万,死亡病例达93.5万,约占癌症病例和死亡病例的1/10。总体上,结直肠癌的发病率居第3位,死亡率居第2位[1]。运用现代影像学检查方法评价直肠癌患者的个体情况,并制订合理的治疗方法,能够有效降低直肠癌的复发并改善预后。中国结直肠癌诊疗规范(2020年版)推荐将MRI作为直肠癌常规检查项目[2]。对于局部进展期直肠癌患者,须在新辅助治疗前后分别行基线、术前MRI检查,以评价新辅助治疗效果,建议行非抑脂、小视野轴位高分辨T2WI扫描。
目前,美国国立综合癌症网络关于直肠癌的分期包括T、N、M分期,不同的TNM分期,尤其是TN分期对直肠癌治疗方式的选择具有重要的指导意义。直肠癌术前诊断中T2与T3的分期鉴别最重要,也最困难。针对T分期,目前准确度最高的术前检查方法为高分辨磁共振[3-5]。高分辨磁共振具有高软组织分辨率、高信噪比,该技术运用垂直于病变段肠管的小视野高分辨二维快速自旋回波(two-dimensional fast spin echo,2D TSE)序列扫描,利用直肠壁各层及病变区含水量的差异,将病变部位与正常直肠结构区分开。但2D序列由于受到层厚所致的容积效应、层间隔、肠管结构以及病变本身位置和形态的影响,常使临床医师对T分期的判断产生误差。本研究通过比较2D TSE与三维可变翻转角各向同性快速自旋回波(three-dimensional variable rotation angle isotropic fast spin echo,3D SPACE)序列对直肠癌术前T分期的诊断价值,旨在优化直肠癌患者的影像学检查方法,更好地为临床决策提供影像学依据。
1 资料与方法
1.1 研究对象 选取2018年1月—2019年12月青岛大学附属医院收治的直肠癌患者75例,其中男50例,女25例,年龄35~78岁,平均(62.5±11.9)岁。纳入标准:①病理活检诊断为直肠癌;②病变位于直肠段(距肛门≤15 cm);③所有患者均接受手术治疗;④手术前进行MRI检查,且图像经医师评估无伪影、少噪声干扰诊断;⑤手术切除组织病理结果证实为直肠癌。本研究通过本院伦理委员会批准(QYFYWZLL26570),所有患者均签署知情同意书。
1.2 检查方法 采用Siemens Magnetom Skyra 3.0T MRI系统,患者取头先进、仰卧体位,采用18通道体部表面线圈。具体扫描参数见表1:①2D TSE序列组包括人体盆腔正矢状位2D T2 TSE(Sag T2 TSE)、定位线垂直于病变段肠轴的斜横轴位2D T2 TSE(OAx T2TSE)、定位线平行于病变段肠轴的斜冠状位2D T2 TSE(OCor T2 TSE),无后处理;②3D SPACE序列组:盆腔段横轴位3D SPACE T2,利用GE sdc工作站ADW4.7 MPR后处理软件,分别参照对照组的定位方法,重建出Sag SPACE T2、OAx SPACE T2和OCor SPACE T2图像。扫描前患者排空直肠,无需其他准备。

表1 两组序列主要扫描参数
1.3 图像质量评估 主观评价:选取6个解剖结构(直肠黏膜层、直肠肌层、直肠浆膜层或外膜、肠周脂肪、直肠系膜筋膜、肿瘤)采用5分法对2D TSE及3D SPACE序列图像进行结构可见性评分[6]。0分:不可见;1分:图像显示不清晰或有伪影;2分:图像较好;3分:图像好;4分:图像非常好,并不存在伪影。比较2个序列的平均分数。
客观评价:计算信噪比(SNR)和对比噪声比(CNR),使用GE sdc工作站ADW4.7测量组织信号强度,两组序列并排观察,通过直接视觉对比实现感兴趣区放置一致性,4个椭圆形感兴趣区分别放置于典型层面的瘤体、肌肉、脂肪和空气区域(噪声),大小为20 mm2,取其平均值。SNR为组织的平均信号强度/背景噪声的标准差,CNR为脂肪与瘤体的SNR差/背景噪声的标准差[7-8]。
1.4 图像分析 由2位副主任医师采用盲法分别对两组图像进行独立诊断,意见不统一时由第三位主任医师综合各方意见给予最终诊断。诊断标准依据国际抗癌联盟及美国癌症联合会颁布的第8版直肠癌T分期[9],①T1:肿瘤侵犯黏膜下层(未累及固有肌层);②T2:肿瘤侵犯固有肌层;③T3:肿瘤侵透固有肌层并侵犯浆膜下层(浆膜覆盖段)或侵犯直肠系膜(无浆膜覆盖)或内外括约肌间隙,根据肿瘤侵入直肠系膜部分与固有肌层的垂直距离分为:T3a(<1 mm)、T3b(1~5 mm)、T3c(5~15 mm)、T3d(>15 mm);④肿瘤侵犯覆膜脏层或侵犯或粘连于邻近器官,T4a:肿瘤侵犯脏层腹膜(浆膜覆盖段),T4b:肿瘤侵犯邻近器官或结构。
1.5 统计学分析 采用SPSS 19.0软件。符合正态分布的计量资料以±s表示,不同序列数据比较采用t检验;不符合正态分布的计量资料以M(Q1,Q3)表示,不同序列数据比较采用Z检验。计数资料以例数表示;对同一病灶进行2D T2 TSE和3D SPACE T2序列扫描,对其进行T分期诊断,采用Kappa系数评估两种序列术前诊断T分期与病理结果的吻合度,并计算敏感度、特异度和准确度。采用U检验对图像质量评估进行数据分析,P<0.05为差异有统计学意义。
2 结果
2.1 病理结果 75例直肠癌患者中,T1期4例、T2期21例、T3期46例、T4期4例。
2.2 2D T2 TSE结果 2D T2 TSE扫描方案显示:T1期0例,T2期13例(敏感度为61.53%,特异度为38.10%),T3期58例(敏感度为97.82%,特异度为77.59%),T4期4例(敏感度和特异度均为100.00%)。对比术后病理结果,2D T2 TSE序列对术前T分期的诊断一致性差(Kappa=0.49,P=0.000),T分期准确度为76.00%,见表2、图1~3。

表2 2D TSE扫描方案结果与病理结果对照(例)

图1 男,56岁,直肠中位恶性肿瘤。2D TSE T2高分辨成像(A)显示直肠外壁低信号环中断不连续(箭),诊断为T3期;3D SPACE T2成像(B)显示肿瘤局限于肠壁黏膜层和肌层,未突破肠外壁,诊断为T2期;病理组织切片(HE,×100,C)显示肿瘤组织浸润肌层,诊断为T2期
2.3 3D SPACE 结果 3D SPACE T2扫描方案显示:T1期3例(敏感度为100.00%,特异度为75%),T2期22例(敏感度为95.45%,特异度为100%),T3期46例(敏感度和特异度均为100.00%),T4期4例(敏感度和特异度均为100.00%)。对比术后病理结果,3D SPACE T2对术前T分期的诊断一致性高(Kappa=0.95,P=0.000),T分期准确度为98.67%,见表3、图1~3。
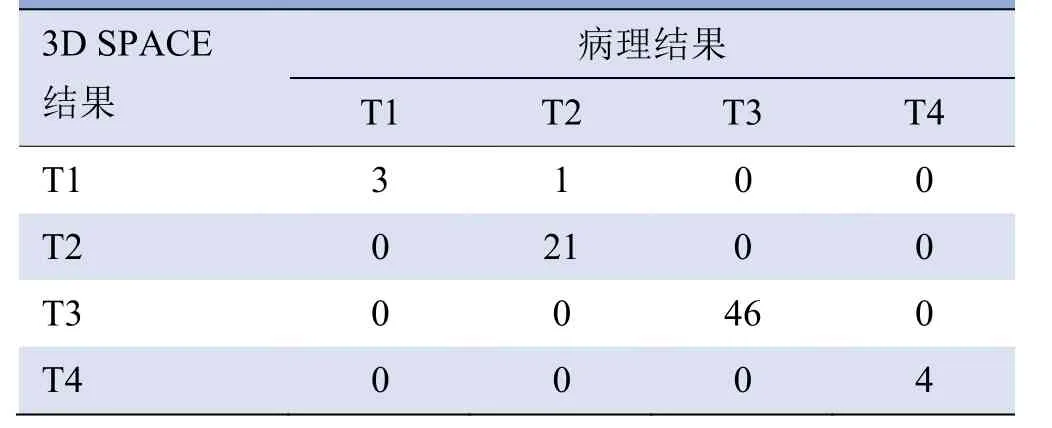
表3 3D SPACE扫描方案结果与病理结果对照(例)

图2 女,62岁,低位直肠癌。2D TSE T2高分辨成像(A)显示癌肿以宽基底贴附于直肠后壁,直肠外壁低信号环完整,诊断为T2期;3D SPACE T2成像(B)显示在直肠截面8点钟方向直肠外壁连续性中断(箭),诊断为T3期;病理组织切片(HE,×100,C)显示肿瘤细胞被肠周脂肪包绕,病理结果为T3期

图3 女,63岁,低-中位直肠癌。2D TSE T2(A)显示直肠外壁低信号环不连续(箭),可疑T3期;3D SPACE T2(B)显示肿瘤局限于直肠黏膜层与肌层,外壁低信号环完整;基于3D SPACE T2进行MPR重建的斜冠状位图像(C)、矢状位图像(D)显示直肠外壁完整,诊断为T1/2期;病理图像(HE,×100,E)显示异型的肿瘤细胞局限于直肠肌层,最终诊断为T2期
2.4 图像质量评估 对于瘤体,3D SPACE序列的SNR优于2D TSE(P<0.05)。对于脂肪及肌肉,两序列的SNR差异无统计学意义(P>0.05),两序列的CNR差异无统计学意义(P>0.05)。两序列显示直肠浆膜层或外膜、肠周脂肪、直肠系膜筋膜及瘤体一样可靠(均P>0.05)。3D SPACE序列对于显示直肠黏膜层及直肠肌层要优越(均P<0.05),见表4、5。

表4 2D TSE和3D SPACE序列的图像质量评分[M(Q1,Q3)]
表5 2D TSE和3D SPACE序列图像的SNR及CNR比较(±s)

表5 2D TSE和3D SPACE序列图像的SNR及CNR比较(±s)
序列SNR CNR瘤体脂肪肌肉2D TSE 83.94±40.34 213.56±95.26 41.86±19.34 19.36±10.11 3D SPACE 27.54±18.72 t值 -2.54 0.80 0.24 -1.54 119.95±39.83 191.23±59.47 40.40±15.58 P值0.016 0.430 0.820 0.140
3 讨论
传统2D成像技术由于受到层厚所致的容积效应、层间隔较大等因素影响,在一定程度上影响了医师对直肠癌T分期的诊断。3D SPACE技术为3D可变翻转角各向同性自旋回波成像技术,克服了传统2D自旋回波序列图像的模糊效应和高SAR值的问题,其3D容积成像技术可以实现亚毫米级别无间隔各向同性扫描成像,空间分辨率较传统2D序列高[6]。随着多层同步成像、并行采集、压缩感知等加速技术的发展,短时高效的3D SPACE扫描已成为现实。此外,其各向同性成像的特点使其可以通过MPR软件进行多平面重建,还能按照器官如直肠的走行进行任意层面重建,不仅有助于节省扫描时间,还可以提高诊断能力。3D SPACE技术目前已广泛应用于神经[10-12]、脑血管[13]、骨关节系统[14-15]等。
Hossein等[7]将3D SPACE技术应用于腰椎扫描,发现对于除椎体和椎间盘外的所有腰椎区域,3D SPACE序列具有更高的SNR、CNR和可见性。Bathala等[6]发现3D SPACE序列提供的前列腺和前列腺周围解剖结构在质量上与传统的2D TSE序列一样可靠。目前未见有确切数据对3D SPACE序列扫描直肠癌的图像进行质量评价以及SNR和CNR测量。本研究采用对同一患者分别进行2D TSE与3D SPACE序列扫描,排除了个体差异造成的干扰。通过对图像质量进行主、客观分析得知,3D SPACE序列扫描瘤体的SNR优于2D TSE序列,直肠周围脂肪及肌肉的SNR与传统2D TSE序列扫描的SNR无显著差异。2D TSE序列和3D SPACE序列的CNR无显著差异。3D SPACE序列对于显示直肠黏膜层及直肠肌层优于2D TSE序列,对直肠浆膜层或外膜、肠周脂肪、直肠系膜筋膜及瘤体的显示与2D TSE序列一样可靠。
随着MRI技术对直肠癌术前T分期研究的深入,肿瘤与直肠及其与周边各层结构的浸润关系得到更好的显示。本研究中共计13例病灶行2D TSE序列扫描诊断为T3期,行3D SPACE序列扫描诊断为T2期,最终经病理证实为T2期,这是由于当肿瘤存在于直肠纡曲处,在图像上极易与正常直肠外壁重叠,表现为肿瘤突破直肠外壁的假象。1例经2D TSE序列扫描诊断为T2期,经3D SPACE序列扫描诊断为T3期,最终经病理诊断为T3期,则是由于直行的直肠外壁重叠至肿瘤区域,图像上表现为直肠外壁完整。本研究中,2D TSE序列对诊断T分期准确度为76.00%,3D SPACE序列为98.67%,较孙轶群等[16]的结果高,考虑是由于本研究参数优化后层厚更薄以及样本量的差异所致。2D TSE序列在直肠癌扫描的层厚一般在3 mm以上,层间距通常设置为层厚的20%~30%,而厚层成像的直接影响就是部分容积效应,同时层间隔的存在会漏检相应的结构信息,这2个因素严重降低了层间分辨率。3D SPACE序列对2D TSE序列最大的优势是大幅增加层间分辨率,实现层面内与层面间的三维高分辨率[17],部分容积效应接近消除。此外,3D SPACE序列扫描还支持任意平面重建,在获取任何倾角的图像时不依赖于操作人员,可用于复杂骨盆解剖的可视化,对于直肠这类走行不规则、个体化差异较大的器官,其诊断效率更高[18-20]。
综上所述,3D SPACE序列对于显示直肠癌病灶具有更高的SNR。对于直肠黏膜层及直肠肌层的显示具有更高的可见性。3D SPACE序列对于直肠癌T分期的诊断效能优于2D TSE序列。因此在临床工作中可以用3D SPACE序列替代2D TSE序列,对于患者的新辅助治疗[2],提高手术切除率和保肛率,延长患者无病生存期有重要意义。
利益冲突 全部作者均声明无利益冲突

