电助淀粉絮凝蛋白质及在制革废水处理中的应用
谭琼,单志华,戴睿,陈慧*,龙忠珍
(1.四川大学轻工科学与工程学院,四川 成都 610065;2.四川大学制革清洁技术国家工程实验室,四川 成都 610065;3.江苏鸿丰资源循环利用研究院,江苏 徐州 221200)
引言
制革、酿造、食品加工的废水成分复杂,氨氮含量高,处理难度大[1-2]。其中,制革废水中氨氮主要源于原料皮中蛋白质、氨基多糖成分的溶出、分解,以及少量来自各工序中未吸收的含氮化工原料分解[3-4]。去除制革废水中蛋白质,不但可以减小臭味,还能有效减少氨氮含量,降低制革废水中COD和浊度,对含蛋白废水的处理具有现实意义[5-6]。
现有文献报道中尚无专一处理制革废水中蛋白质的方法,但对COD及氨氮的处理方法中,有许多方法涉及对蛋白质的处理,如絮凝法[7]、电化学法[8]及生物处理法等[9]。其中常见的有絮凝法和电化学氧化法,絮凝法作为一种经济实用的方法,备受青睐,但由于纯天然有机高分子絮凝剂存在一定的缺陷,如不易被生物降解、稳定性不好以及用量大[10-11]。淀粉广泛存在于植物中,来源丰富[12]、廉价易得、无毒无害,通过改性制备絮凝剂具有良好的应用前景[13-14]。电化学氧化法操作简单、绿色环保、无二次污染,是一种具有良好发展前景的水处理技术,被广泛运用于各个行业[15-16]。将氯化钠作为支持电解质,利用电解过程中产生的氧化性成分,将水中的有机污染物氧化成无毒或低毒的小分子化合物实现废水处理[17-18]。由于废水水质成分太过复杂,单一的电化学氧化法很难将有机物彻底分解,有的甚至使氨基化合物分解出氨氮。通过电化学法氧化淀粉,将淀粉多糖的聚集态高效分散或溶解,增加分子中活性基团羰基和羧基,增强反应活性,去除废水中蛋白质,避免蛋白质分解产生氨氮,是一个值得探索的课题。
本文以工业明胶模拟蛋白质,探究电化学氧化法作用下活性淀粉的凝聚沉积性对废水中蛋白质沉降去除,分析其影响因素,同时对处理条件进行优化。在最优参数条件下,进行制革废水中蛋白质的絮凝测试,对电助淀粉絮凝蛋白质的实际应用提供理论指导。
1 实验
1.1 材料与仪器
硫酸铜、可溶性淀粉、氯化钠、明胶、双缩脲试剂、PBS缓冲液(pH=7.4)、酒石酸钾钠、氢氧化钠、碘化钾、磷酸氢二钠、磷酸二氢钠等,均为分析纯。
LW3J直流稳压稳流电源、电流表(500 mA)、UV-2000紫外光光栅分光光度计、石墨电极、101-2-S恒温干燥箱、pHS-3C型精密pH计、TDL-40B台式离心机等。
1.2 电助淀粉絮凝装置与方法
1.2.1 电助淀粉絮凝装置
本实验采用明胶溶液模拟配置蛋白质废水,氯化钠溶液为电解质,阳极和阴极均为石墨电极板;从明胶溶液质量分数、氯化钠质量分数、淀粉质量分数和电解时间来考察电絮凝作用对蛋白质的去除效果;采用二次通用旋转组合设计实验,并测定溶液中剩余蛋白质含量,含量最低者为最优处理参数。
实验采用电解槽极板间距为50 mm,电流密度为5 mA/cm2,电解液初始pH值为中性,电解液温度为室温,其中阴阳极均采用石墨板电极,通过磁力搅拌器搅拌电解液进行电解反应,电解实验装置如图1。

图1 石墨极板的电解装置Fig.1 The electrolyzer using graphite electrode
1.2.2 电助淀粉絮凝方法
根据二次通用旋转组合设计参数表[19],以明胶质量分数(x1)、淀粉质量分数(x2)、氯化钠质量分数(x3)和电解时间(x4)四个影响因素设计实验方案,拟定总共进行n=31次试验,其中,7次零水平试验次数,由因素个数查知r=2,用量值及编码如表1所示。

表1 四元二次通用旋转组合设计的因素水平编码Tab.1 Factor level coding of quaternion quadratic general rotary combination design
根据上述因素水平编码表,设计得到二次通用旋转组合的实验方案。
1.2.3 絮凝结果表征
该研究采用双缩脲法[20]对有机氮蛋白质进行测定。用体积为0,0.2,0.4,0.6,0.8,1.0 mL的标准蛋白质溶液,以蛋白质含量为横坐标,光吸收值为纵坐标,绘制工作曲线。
得到工作曲线(1)为:

其中:X——蛋白质含量(mg/mL);
Y——为吸光度。
1.3 蛋白质溶液的絮凝实验
参照明胶模拟絮凝优化组合参数对制革废水进行絮凝实验。在2000 r/min转速下,离心10 min,取上层清液稀释适当倍数,将其中一部分放进电解槽中,在最有参数条件下进行电助淀粉絮凝作用。处理完成后,取最后处理废液作为待测试样。用双缩脲法(Biuret法)分别测定制革废水中蛋白质含量和电助淀粉絮凝作用后制革废水蛋白质含量。
1.4 能耗计算
电化学处理废水最重要一点即是能耗问题,为了评估该方法的电能耗,我们采用以下公式(2)计算:

其中:W——能耗,单位kW·h;
U——极板间电压,单位V;
I——电流密度,单位A/m2;
t——电解时间,单位min。
2 结果与讨论
2.1 絮凝参数优化
根据实验得到二次通用旋转组合设计实验结果,如表2所示。

表2 二次通用旋转组合设计实验结果Tab.2 Results of quadratic general rotary unitized designed experiments
应用SPSS统计软件,根据下列二次多项式回归模型方程,对二次通用旋转组合设计的实验数据进行分析。方程:

得到蛋白质去除率(y)回归方程。剔除P<0.05的项目后,回归方程可简化如下:
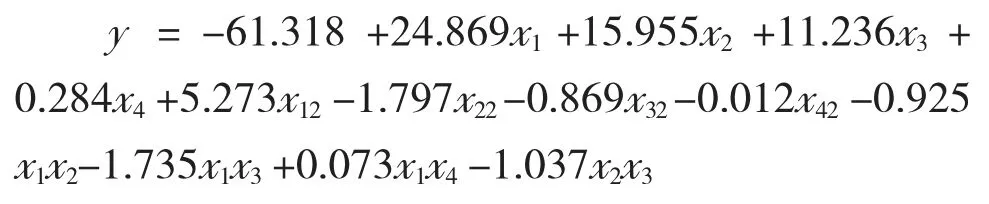
利用该模型获得最优参数为明胶含量2.5%、淀粉含量3%、氯化钠质量分数0.3%、电解时间20 min。在该条件下,用数学模型所预测的蛋白质去除率为66.6%。
2.2 单因素效应分析
根据上述回归方程,选取其中一个因素(x),改变其水平取值,将其余因素均设于零水平,经过计算绘制出单因素x-y的曲线图,分析单个试验因素对蛋白质去除率的影响效应。上述回归方程由四个因素共同拟合得出,当对其中一个因素进行分析时,由于其余因素均为于零水平,所以纵坐标蛋白质去除率呈现负数,但该数值不影响变量对蛋白质去除率的变化趋势。
由图2单因素效应曲线图(a)可知,随着明胶质量分数(x1)增加,蛋白质去除率(y)先缓慢增加,随后显著提高。说明了蛋白质浓度越低,越难以去除。这是由于低浓度蛋白质体系下,蛋白质分子难以与淀粉活化的絮凝场进行相互作用。由图2(b)可知,随着淀粉质量分数(x2)增加,蛋白质去除率(y)不断增加,但当增加到一定程度的时候,蛋白质去除率趋于稳定。该数据说明淀粉分子与蛋白质发生了结合,当淀粉质量分数增加时,增加了淀粉分子与蛋白质结合的强度,但当淀粉质量分数达到一定量后,其体系中蛋白质结合产生饱和,继续增加淀粉质量分数,多余的淀粉已无法与蛋白质结合,因此表现出平衡曲线。
由图2(c)可见,随着氯化钠质量分数(x3)的增加,蛋白质去除率显著增加,其中起作用的是氯离子,氯离子在体系中为活化触媒,在电场作用下,氯离子转化为次氯酸根离子,次氯酸具有较强的氧化性,可以将淀粉进行氧化增加淀粉的活性。因此在一定浓度范围增加氯离子浓度可以增加活化淀粉的活化度,从而提高蛋白质去除率。由图2(d)可知,当电解时间(x4)在5~20 min范围之内时,蛋白质去除率随着时间增加而不断提高。20 min后,随着时间增加,蛋白质去除率不断的降低。这是由于在电解初期,随着电解时间的增加,与蛋白质结合的活化淀粉数量相应增多,使得絮凝蛋白质的效果增强,蛋白质去除率增加。后期由于电解过度使氯离子无法顺利的转化为次氯酸根离子,或淀粉结构被破坏无法继续进行絮凝作用,蛋白质浓度去除率反而降低。

图2 单因素效应曲线图(x1(a)、x2(b)、x3(c)、x4(d))Fig.2 Single factor effect curve(x1(a)、x2(b)、x3(c)、x4(d))
2.3 双因素效应分析
为了进一步分析明胶质量分数(x1)、淀粉质量分数(x2)、氯化钠质量分数(x3)和电解时间(x4)对蛋白质去除率的交互影响,通过改变其中两个试验因素的水平取值,取其余两个试验因素为零水平,将其代入回归方程,用SPSS软件计算后绘制得到两个因素间交互效应曲面图,如图3所示。
图3(a)为淀粉质量分数与明胶质量分数之间的相互作用关系曲线,由图可知,淀粉质量分数与明胶质量分数之间相互影响不大,但当淀粉质量分数与明胶质量分数比例增加时,蛋白质去除率显著增加,相比之下,可以发现淀粉质量比明胶质量分数对蛋白质去除率的影响更大。
图3(b)为明胶质量分数与氯化钠质量分数相互作用关系曲线,由图可以知,在氯化钠质量分数与明胶质量分数比例增加时,蛋白质去除率显著增加。两个因素相比,明胶质量分数对蛋白质去除率的影响更大,这是由于使蛋白质产生絮凝作用的不是氯离子本身,而是电解后由氯离子形成的次氯酸根离子氧化淀粉形成的活化淀粉,活化淀粉与蛋白质结合产生絮凝作用,从而实现蛋白质的去除。
图3(c)为明胶质量分数与电解时间相互作用关系曲线,由图可知,在电解时间一定的情况下,明胶质量分数越高,蛋白质去除率也越高。最初的时候蛋白质去除率随时间增加而不断提高,20 min后,随着时间增加,蛋白质去除率不断降低。这是由于在电解初期,随着活化淀粉数量的增加,淀粉不断的絮凝蛋白质,从而降低蛋白质的含量,然后后期由于电解过度,氯离子无法顺利的转化为次氯酸根离子,蛋白质去除率降低。
图3(d)淀粉质量分数与氯化钠质量分数相互作用关系曲线,由图可知,氯化钠质量分数与淀粉质量分数之间的关系较为复杂,在适当的氯化钠质量分数以及较高的淀粉含量下,蛋白质的去除率较高,这可能是由电化学淀粉活化机理所致,由于氯化钠中氯离子并不是直接使蛋白质絮凝的物质,其中氯离子需要在电解后产生次氯酸根离子后,氧化活化淀粉,使活化淀粉与蛋白质结合絮凝产生降解效果,因此需要在一个合适的氯离子浓度下,产生足够但是不过量的次氯酸根,再进一步与淀粉氧化,形成含有大量活化基团的淀粉,当氯离子浓度较低时,无法产生足够的次氯酸根离子活化淀粉,因此蛋白质的去除率较低,反之在氯离子浓度过高时,生成了过多次氯酸根离子,其可能过度氧化淀粉,破坏了淀粉的絮凝基团从而失去了去除能力。
图3(e)和(f)分别为淀粉质量分数与电解时间和氯化钠浓度与电解时间相互作用关系曲线,由图可知,在不同的淀粉质量分数和氯化钠浓度的情况下,时间对蛋白质的去除率没有影响,电解体系本身的构成影响大于电解的时间影响,说明优化实验条件对于蛋白质的降解非常重要。

图3 双因素交互效应曲面图(x1x2(a)、x1x3(b)、x1x4(c)、x2x3(d)、x2x4(e)、x3x4(f))Fig.3 Two-factor interaction effect surface plot(x1x2(a)、x1x3(b)、x1x4(c)、x2x3(d)、x2x4(e)、x3x4(f))
由上述分析可知,在最佳条件下,明胶质量分数2.5%、淀粉质量分数3%、氯化钠质量分数0.3%、电解时间20 min,电助淀粉絮凝法对蛋白质的去除率为66.6%。本实验电助淀粉絮凝法对低浓度蛋白质的去除,与牛雅倩[21]等人研究的单一絮凝法对高浓度蛋白质的去除相比,去除率相当,均超过60%。说明将电化学氧化法和絮凝法结合处理废水中低浓度蛋白质是切实可行的,不仅能有效降低氨氮值,对蛋白质的去除也具良好的效果。
2.4 蛋白质絮凝结果分析
实验测得制革废水蛋白质含量为0.879 mg/mL,在上述实验条件下,经过电助淀粉絮凝作用后,蛋白质的含量为0.383 mg/mL,蛋白质的去除率为56.4%。与模拟实验相比去除率有所降低,是因为制革废水成分更为复杂,处理难度增加。但电助淀粉絮凝法能够有效降低制革废水中蛋白质含量,说明该方法可以运用于实际制革废水体系中。
根据能耗计算公式,本实验条件下,电解20 min,制革废水中蛋白质含量从0.879 mg/mL降低到0.383 mg/mL,所 用 能 耗 为3.67×10-4kW·h。由图4絮凝时间及能耗与蛋白质去除率的关系图,可以看出该方法的能耗与时间关系成线性增加,制革废水中蛋白质浓度与时间成S型曲线降低。这是由于初始阶段淀粉处于电化学活化过程,基本没有絮凝效果,在电化学活化过程完成之后,活化淀粉与蛋白质结合产生了絮凝作用,废水中蛋白质含量随之迅速降低,从而达到降低废水中蛋白质的目的。因此在实际体系中应根据实际需要的蛋白质去除率设计电化学处理时间,此外由于需要一段初始的淀粉活化时间,可采用改变电解条件,来加速淀粉活化过程,之后再进行普通电解条件的废水处理,该部分研究可在未来的研究中继续探索。
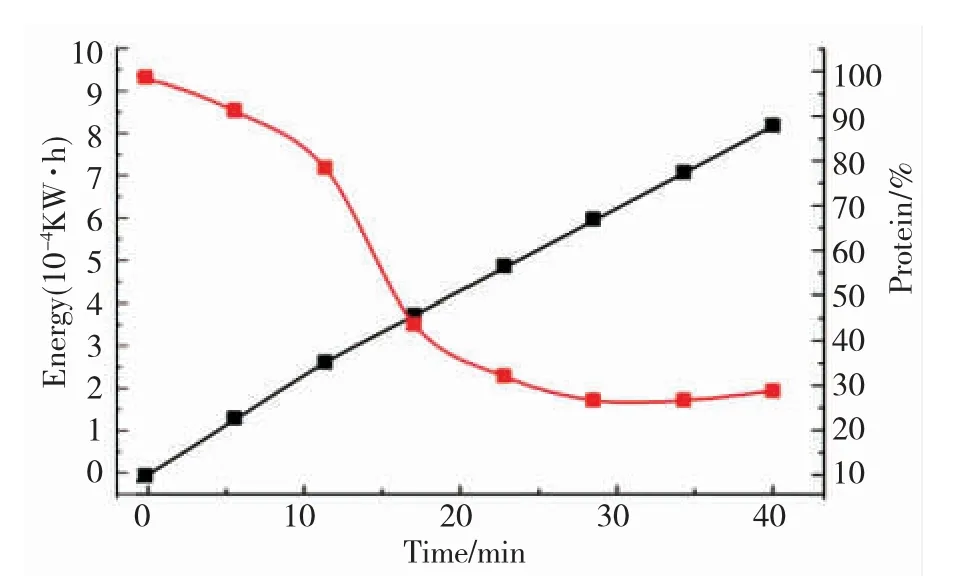
图4 絮凝时间及能耗与蛋白质去除率的关系图Fig.4 Time dependent energy cost of water treatment and protein content in water
3 结论
本文首次探究了电助淀粉絮凝法对制革废水中蛋白质的絮凝作用,通过电化学预处理淀粉得到活性淀粉,让其与废水中蛋白质进行相互作用从而达到絮凝沉淀蛋白质的作用,实现降低废水中蛋白质浓度的目的。获得最优处理参数为明胶质量分数2.5%、淀粉质量分数3%、氯化钠质量分数0.3%、电解时间20 min。在该条件下,用数学模型所预测的蛋白质去除率为66.6%。制革废水中蛋白质的去除率为56.4%,能耗仅为3.67×10-4kW·h。能耗与时间关系成线性增加,制革废水中蛋白质浓度成S型曲线降低。通过本实验研究可知,电化学氧化法和絮凝法的结合能够为制革废水中低浓度蛋白质的去除提供理论指导。为了扩大该方法的应用,还需进一步探究淀粉在预处理过程中的化学变化机理以及对蛋白质的絮凝机理。

