钼锑抗分光光度法测定水中磷酸盐不确定度的评定
陈明月
(安徽中科澄信检测技术有限公司,安徽 合肥 230001)
磷是动植物生长必需的元素,但过量的磷(如果超过0.2 mg/L),会造成水体富营养化等各种问题。《污水综合排放标准》(GB 8978-1996)中磷的三级排放标准为0.3 mg/L,《巢湖流域城镇污水处理厂和工业行业主要水污染物排放限值》(DB 34/2710-2016)中磷的排放限值最大为0.5mg/L。从上面两个排放标准可以看出,磷的排放限值很小,这就要求检测结果尽可能得准确。因此,能准确地检测出水中的含磷量是非常重要的,而不确定度能表明检测结果的可信赖程度,它是测量结果质量的指标。本文以钼锑抗分光光度法测定废水中的磷酸盐[1],并根据《测量不确定度评定与表示》[2]和《测量不确定度评定和表示》[3]标准,并参考相关的文献资料[4-12],对本文实验的测量结果进行不确定度评定。
1 实验方法
1.1 仪器与试剂
UV754N紫外分光光度计及3 mm玻璃比色皿;FA2204B十万分之一电子天平;50 mL比色管、1 000 mL容量瓶(A级)、10.00 mL单标移液管(A级)、250 mL容量瓶(A级)、10.0 mL分度移液管(A级)、5.00 mL单标移液管(A级);磷酸二氢钾(优级纯);钼酸盐溶液;抗坏血酸溶液。
1.2 实验原理
实验原理为《水和废水监测分析方法第四版增补版》(2002)钼锑抗分光光度法。在酸性条件下,正磷酸盐与钼酸铵、酒石酸锑氧钾反应,生成磷钼杂多酸,被还原剂抗坏血酸还原,变成蓝色络合物,通常称为磷钼蓝。
1.3 分析步骤
(1)磷酸盐标准使用液的配制。称取0.219 7 g已干燥的优级纯磷酸二氢钾,将其溶于水后倒入1 L的容量瓶中,加(1+1)硫酸5 mL后用水定容,制成磷酸盐贮备液,用单标移液管吸取10.00 mL贮备液于250 mL容量瓶中,用水稀释至标线。此溶液每mL含2.00 μg磷。
(2)校准曲线的绘制。取7支50 mL具塞比色管,分别取(1)溶液0 mL,0.50 mL,1.00 mL,3.00 mL,5.00 mL,10.0 mL,15.0 mL,用水稀释至50 mL。向比色管中加入1 mL的抗坏血酸(浓度为100 g/L),混匀。30 s后加入2 mL钼酸盐溶液,充分混匀,放置15 min后用30 mm比色皿在波长为700 nm处测定其吸光度。
(3)样品测定。取5 mL经滤膜过滤的水样于50 mL比色管中,用水定容至50 mL。按照与(2)相同步骤进行测定。减去空白后的吸光度可以从校准曲线上查出结果。
1.4 计算公式
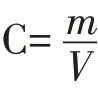
式中:C—磷酸盐含量(mg/L);m—试样测得含磷量(μg);V—试样体积(mL)。
1.5 数学模型的建立
由方法原理和计算公式分析得出合成相对不确定度的模型为:

式中:u(c1)—配制标准贮备液引入的不确定度;u(f)—将标准贮备液稀释至使用液过程中引入的不确定度;u(v5)—取样过程中产生的不确定度;u(m1)—校准曲线拟合引入的不确定度;u(m2)—样品测量重复性引入的不确定度。
2 不确定度的来源分析
由测量方法和不确定模型分析本次测量过程不确定度的来源,见表1。

表1 不确定度的来源
具体分析如下:
(1)配制标准贮备液引入的不确定度。包括称量优级纯磷酸二氢钾引入的不确定度、磷酸二氢钾纯度引入的不确定度、用来定容贮备液的1 000 mL容量瓶引入的不确定度、分子摩尔质量引入的不确定度。
(2)将标注贮备液稀释至使用液过程中引入的不确定度。包括A级10.00 mL的单标移液管引入的不确定度(体积校准引入的不确定度、充满液体至满刻度的变动性引入的不确定度、温度变化引入的不确定度)、50 mL比色管(A级)、250 mL容量瓶(A级)、10.0 mL分度移液管(A级)引入的不确定度。
(3)取样过程中产生的不确定度。A级5.00 mL单标移液管引入的不确定度(体积校准引入的不确定度、充满液体至满刻度的变动性引入的不确定度、温度变化引入的不确定度)。
(4)校准曲线拟合引入的不确定度。
(5)样品测量重复性引入的不确定度。
3 结果与讨论
以下按照配制磷酸盐标准贮备液、标准贮备液稀释至使用液、取样过程、校准曲线拟合、样品重复性来分析不确定度分量,进而计算出合成不确定度和扩展不确定度。
3.1 配制磷酸盐标准贮备液引入的不确定度
磷酸盐贮备液可以购买环境保护部标准样品研究所提供的标准物质[13],可以减少分析步骤。标准贮备液在本文中是用优级纯磷酸二氢钾固体称量配制而成,优势为成本较低,保存时间长且量较多。
3.1.1 称量引入的不确定度
天平校准证书给出的扩展不确定度为0.3 mg(k=2),一次称量的标准不确定度为u(m)=0.3 mg/2=0.15 mg,相对标准不确定度为urel(m)=2×0.15÷219.7=0.000 965。
3.1.2 试剂纯度引入的不确定度
标签给出优级纯磷酸二氢钾的纯度为99.5%,因此,扩展不确定度为0.005,按均匀分布(k=),相对标准不确定度为urel(p)=0.005/=0.002 89。
3.1.3 1 000 mL容量瓶引入的不确定度
1 000 mL容量瓶引入的不确定分量有以下三个部分:
(1)校准证书给出的扩展不确定度为0.2 mL(k=2),则其体积校准引入的标准不确定度为0.2 mL/2=0.1 mL。
(2)1 000 mL(A级)容量瓶充满液体至满刻度的变动性引入的标准不确定度可参考文献[14]得到,为0.35 mL。
(3)温度变化引入的标准不确定度为(1 000×2×2.1×10-4)/=0.242 mL(实验室温度变化为±2℃,k=)。
计算可得,1 000 mL容量瓶引入的相对不确定度为:
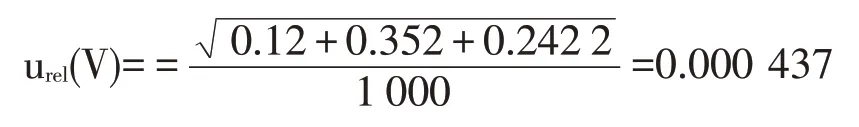
3.1.4 分子摩尔质量引入的不确定度
磷酸二氢钾中各元素相对原子质量的标准不确定度见表2。
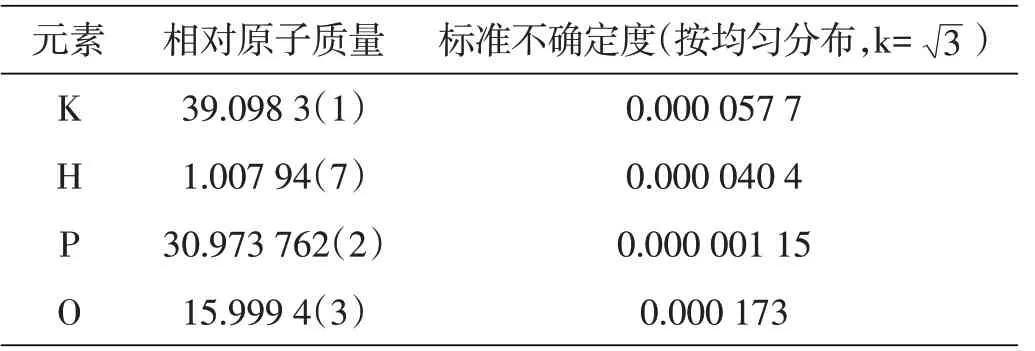
表2 元素相对原子质量的标准不确定度
磷酸二氢钾(KH2PO4)的分子摩尔质量:M=1×k+2×H+1×P+4×O=1×39.098 3+2×1.007 94+1×30.973 762+4×15.999 4=136.085 542 g/mol
磷酸二氢钾(KH2PO4)分子摩尔质量引入的相对不确定度:

综上,配制磷酸盐标准贮备液引入的相对标准不确定度由上述内容可得:
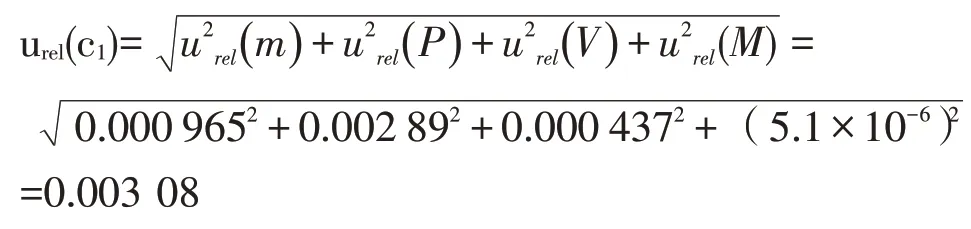
3.2 将标准贮备液稀释至使用液过程中引入的不确定度
3.2.1 10.00 mL的单标移液管体积校准引入的不确定度
校准证书给出的10.00 mL的单标移液管的扩展不确定度为0.010 mL(k=2),标准不确定为u1(V10)=0.010 mL/2=0.005 mL
3.2.2 10.00 mL的单标移液管充满液体至满刻度的变动性引入的不确定度
将移液管充满液体至刻度,通过10次重复测量,结果见表3。
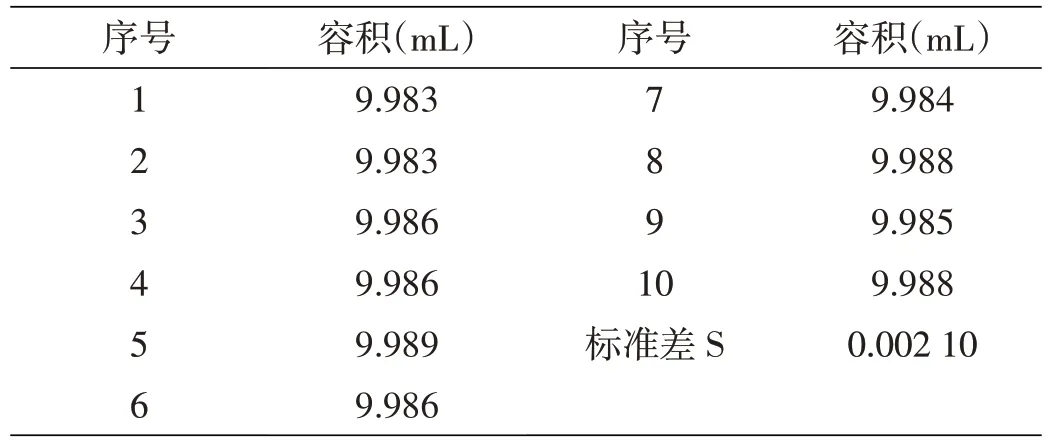
表3 10.00 mL单标移液管充满液体至刻度实验结果
用贝塞尔公式计算:u2(V10)=0.002 10 mL
3.2.3 10.00 mL的单标移液管温度变化引入的不确定度
所以,以上三项合成得出10.00 mL单标移液管引入的相对标准不确定度为
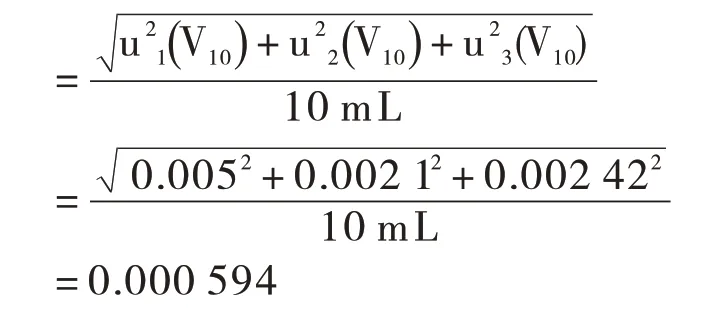
50 mL比色管(A级)、250 mL容量瓶(A级)、10.0 mL分度移液管(A级)引入的不确定度来源和计算同上,具体见表4。

表4 玻璃量器引入的不确定度
3.2.4 标准贮备液稀释至使用液过程中引入的不确定度合成为:

3.3 取样过程中产生的不确定度
取样使用A级5.00 mL单标移液管,不确定度来源和计算同3.2,具体见表5。

表5 5.00 mL单标移液管(A级)引入的不确定度
所以,以上两项合成得出相对标准不确定度urel(V5)为0.000 555。
3.4 校准曲线拟合引入的不确定度
钼锑抗分光光度法测定水中磷酸盐的校准曲线结果见表6。
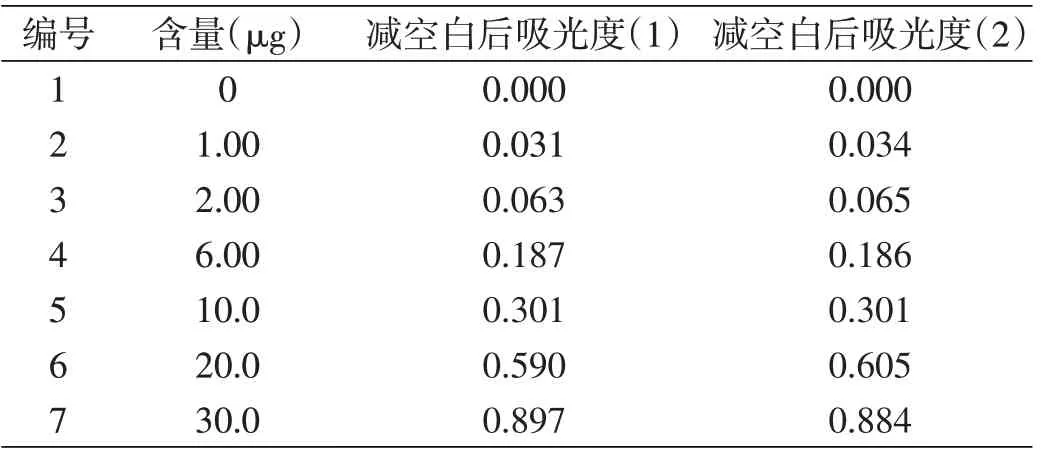
表6 磷酸盐校准曲线测定结果
由表6数据得:y=0.029 6x+0.004,b=0.029 6,a=0.004,r=0.999 9。校准曲线的剩余标准差:
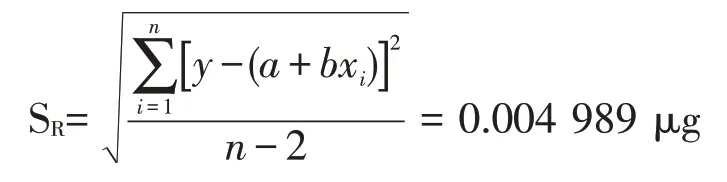
校准曲线的标准不确定度:
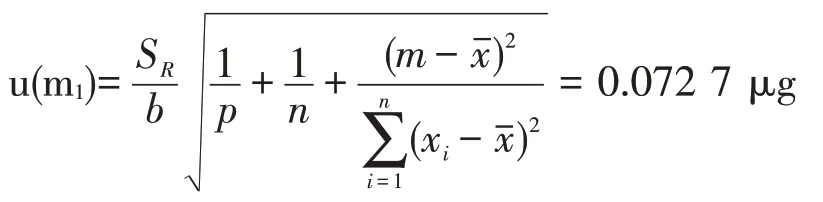
校准曲线拟合引入的相对标准不确定度为:

3.5 样品重复性产生的不确定度
取生活废水水样,平行测量10次,测量结果见表7。
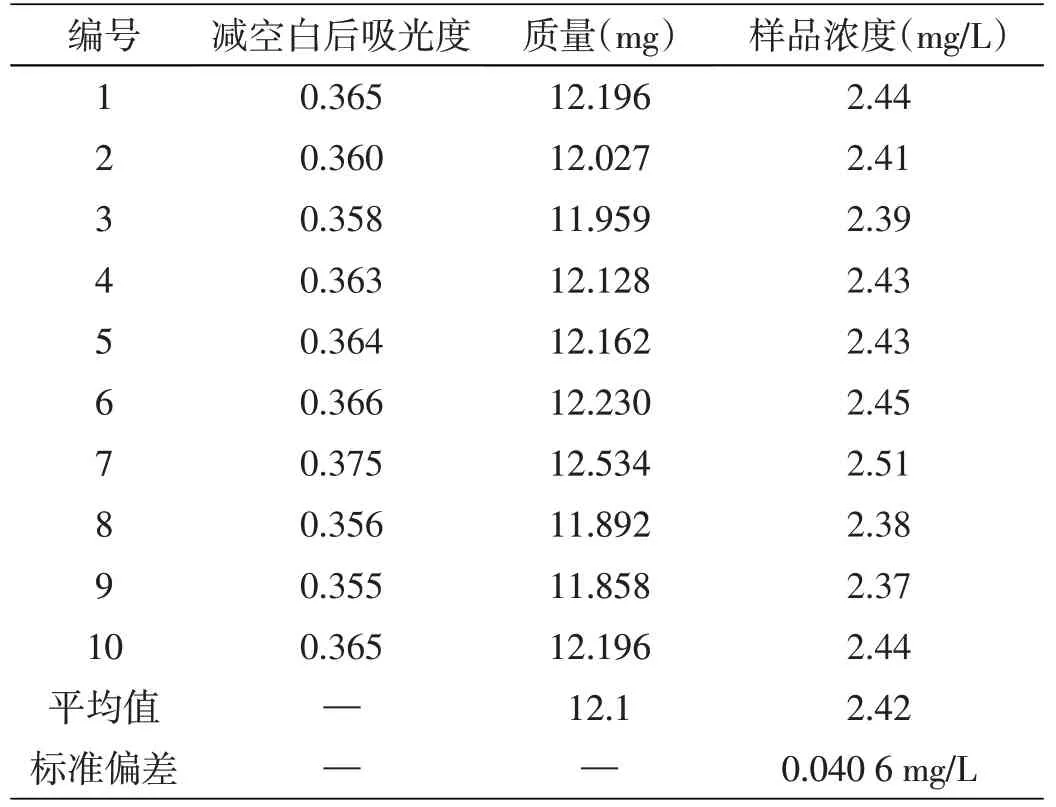
表7 水中磷酸盐含量测定结果
分别使用格鲁布斯(Grubbs)法和Q检验法来剔除异常值[14]。
3.5.1 格鲁布斯(Grubbs)法
将测得结果由小到大排列:
2.37 ,2.38,2.39,2.41,2.43,2.43,2.44,2.44,2.45,2.51
其中2.37或2.51可能是异常值。
查T值表,得T0.05,10=2.18,T<T0.05,10,所以2.37这个数据应当保留。
查T值表,得T0.05,10=2.18,T>T0.05,10,所以2.51这个数据应当舍去。舍去2.51这个值后,磷酸盐含量测定结果见表8。

表8 水中磷酸盐含量测定结果
查T值表,得T0.05,9=2.11,T<T0.05,10,所以2.45这个数据应当保留。
3.5.2 Q检验法
将测得结果由小到大排列:

其中2.37或2.51可能是异常值。
假设2.37是可疑的,则统计量Q为:
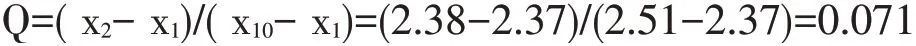
已知n=10,查Q值表,得到Q0.90=0.41,Q<Q0.90,所以2.37应当保留。
假设2.51是可疑的,则统计量Q为:

Q>Q0.90,所以2.51应当舍弃。
假设2.45是可疑的,则统计量Q为:

已知n=9,查Q值表,得到Q0.90=0.44,Q<Q0.90,所以2.45应当保留。
使用Q检验法来判断异常值与用格鲁布斯(Grubbs)法判断所得的结论一致。所以,最大值2.51为异常值,应将其剔除。
样品重复性相对标准不确定度:

3.6 合成不确定度
各不确定度分量见表9。
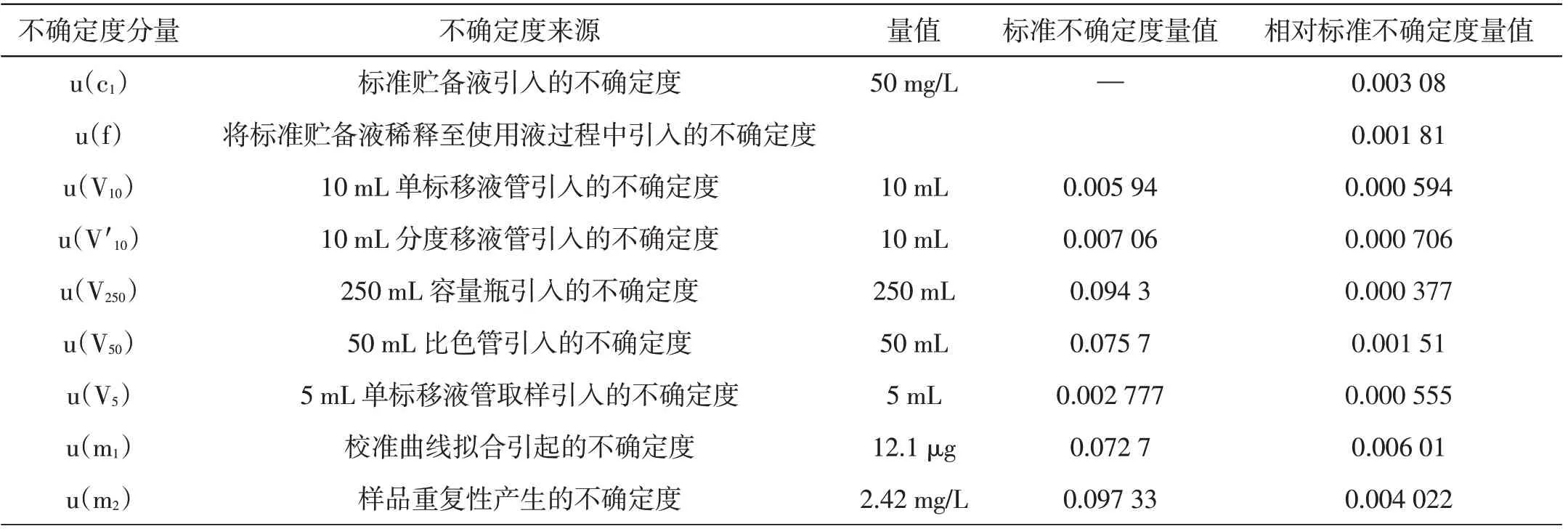
表9 相对标准不确定度分量一览表
合成相对标准不确定度为:
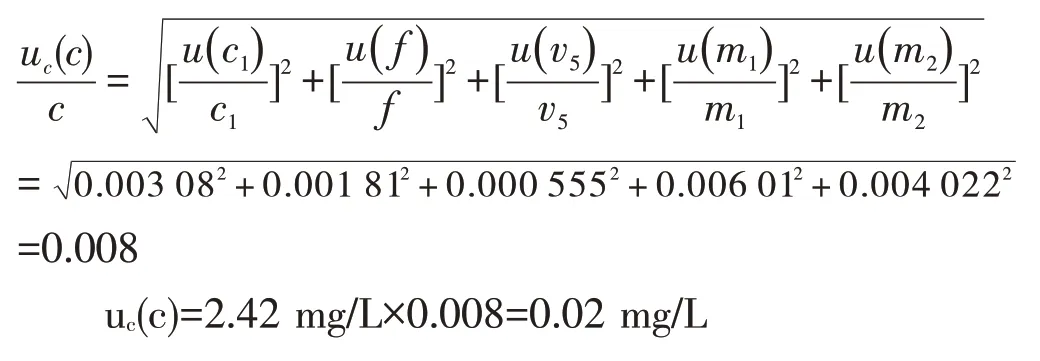
3.7 扩展不确定度
取包含因子k=2,则扩展不确定度:
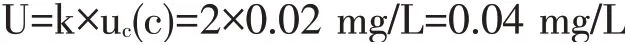
4 结论
钼锑抗分光光度法测定水中磷酸盐,测量结果为2.42 mg/L,扩展不确定度为0.04 mg/L(k=2)。校准曲线拟合引入的不确定度是贡献最大的不确定分量,其次是样品重复性产生的不确定度、标准贮备液引入的不确定度和将标准贮备液稀释至使用液过程中引入的不确定度,贡献最小的分量是取样体积引入的不确定度。因此,在磷酸盐测定的过程中,为了降低测量不确定度,提高检测结果的准确性,在绘制校准曲线时应尽可能增加标准溶液浓度系列的点数;其次,选择使用质量较好且已校准的玻璃器皿、精度较高的天平和纯度达到优级纯以上的试剂;最后,提高分析人员的技术水平,适当增加样品的测量次数。

