二氧化碳和冲洗液加温在行腹腔镜手术妇科癌症患者中的应用效果
李敏, 邓恋, 林辉瑞, 李巧慧
(广东省妇幼保健院 麻醉科手术室,广东 广州,510010)
于妇科癌症患者而言,腹腔镜手术是常见的治疗方式之一,但腹腔镜手术采用的全身麻醉方式、建立的二氧化碳(CO2)气腹,以及女性群体自身的生理状况均是造成术中发生低体温的主要原因[1]。目前,通过被服保暖、限制手术室人员流动等措施预防低体温的发生,但是上述措施受多种因素的影响,在临床运用中的有效率较低[2]。陈红等[3]指出,术中通过实施加温CO2和冲洗液等措施,可减少低体温的发生,使患者血液循环处于较为稳定的状态。本研究将CO2和冲洗液加温措施应用于行腹腔镜手术的妇科癌症患者,以探讨该干预方法的应用效果。
1 对象与方法
1.1 研究对象
以2019年3月至2020年10月广东省妇幼保健院收治的126例妇科癌症患者为研究对象,研究内容已取得本院医学伦理委员会批准。纳入标准:① 符合腹腔镜手术指征;② 美国麻醉医师协会(ASA)分级为Ⅰ~Ⅲ级;③ 手术时间为2~4 h。排除标准:① 伴有其他恶性肿瘤;② 伴有严重凝血功能障碍;③ 临床资料不完善。按随机数字表法将所有患者分为对照组和观察组,各63例。对比2组间输液量、冲洗量、ASA分级等一般资料,差异均无统计学意义(P均>0.05),见表1。

表1 2组患者一般资料对比
1.2 方法
1.2.1 手术方法 2组患者均由同一组手术医师实施手术。在手术开始前,护士将心电监护仪等设备连接好,以监测患者的心率、血压、呼吸和血氧饱和度等生命体征变化;借助体温传感器监测患者的核心体温;协助患者取膀胱截石位。护士协助麻醉医师采用气管插管全身麻醉方式进行麻醉,在麻醉诱导结束后进行常规消毒铺巾。手术医师以患者脐部为穿刺点进行穿刺,穿刺后注入CO2气体形成气腹,并置入镜头开展手术,术中控制气腹压力,避免气腹压力过高对腹膜造成刺激。
1.2.2 护理方法 ① 对照组患者给予常规保温措施,直至手术结束。由巡回护士在术前1 h将手术室温度调节至25 ℃。从病房将患者转运至手术室的途中须为其覆盖手术被进行保暖,避免身体暴露于空气中。在转运期间密切监测患者的体温,对于体温较低或者较高的患者及时为其加减保温物品;在转运至手术室后,巡回护士协助患者摆好体位后,将手术室温度调节至27 ℃,并询问患者的感觉,若患者主诉依然感觉寒冷,则可为其适当增加棉被。在手术开始时,巡回护士通过监测体温及时调节手术室温度,保持恒定温度。术中所用纱布均经37 ℃的0.9%氯化钠溶液浸泡后再使用。手术结束后,在送患者回病房或麻醉复苏室的途径中注意保暖,避免皮肤暴露。② 观察组患者在常规保温措施的基础上予以CO2和冲洗液加温措施,直至手术结束。术中使用自动加温并补气的气腹机,将CO2加温至37 ℃后再建立气腹,术中根据患者的具体情况酌情补气,所补充气体仍加温至37 ℃。术中所使用的各种冲洗液,使用前均借助输血输液加温仪加温至37 ℃后再进行冲洗。
1.3 观察指标
1.3.1 核心体温变化情况 使用体温传感器以麻醉开始、建立气腹、手术开始60 min、90 min及120 min为时间节点记录患者的核心体温。
1.3.2 应激水平 术前及术后1 d抽取患者2 mL静脉血,运用放射免疫法检测血清肾上腺素(AD)及去甲肾上腺素(NE)水平,运用免疫透射散射浊度法检测C反应蛋白(CRP)水平。
1.3.3 凝血功能 术前及术后1 d抽取患者3 mL静脉血,检测血小板计数(PLT)、凝血酶时间(TT)及纤维蛋白原(FIB)水平。
1.3.4 低体温发生率 术后统计2组患者低体温的发生率。
1.4 统计学方法

2 结果
2.1 2组核心体温变化情况对比
观察组在建立气腹,手术开始60 min、90 min及120 min后的核心体温均高于同期对照组(P均<0.05),见表2。
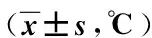
表2 2组核心体温变化情况对比
2.2 2组应激水平对比
术后1 d,2组的AD、NE、CRP水平均高于术前(P均<0.05),但观察组均低于对照组(P均<0.05),见表3。

表3 2组应激水平对比
2.3 2组凝血功能对比
术后1 d,2组的PLT均低于术前,TT均长于术前,FIB水平均高于术前(P均<0.05),且观察组的PLT高于对照组,TT短于对照组,FIB水平低于对照组(P均<0.05),见表4。

表4 2组凝血功能对比
2.4 2组低体温发生率对比
观察组发生1例低体温,发生率为1.59%(1/63);对照组发生8例低体温,发生率为12.70%(8/63)。观察组的低体温发生率较对照组低(χ2=4.307,P=0.038)。
3 讨论
腹腔镜手术是现阶段各种妇科癌症常见的治疗方式之一,但该手术方式需在建立CO2气腹的基础上开展。妇科手术中因女性对体温的敏感性等,低体温发生率可达33%,不仅影响其脏器功能,而且还会增加术后感染等并发症的发生风险[4]。王江华等[5]指出,术中经腹腔镜注入室温下的CO2可增加患者发生低体温的概率。因此,对行腹腔镜手术的妇科癌症患者实施保温措施已成为临床亟待解决的问题之一。现阶段通过控制手术室温度、增加盖被等措施控制患者的体温波动,但术中大量冲洗液的运用仍然可使体温下降,难以降低低体温的发生率[6]。李欣[7]等指出,在腹腔镜手术过程中采用相应仪器加热CO2及冲洗液,不仅可维持患者体温恒定,同时还可降低术后并发症的发生率。
手术是一种有创操作,术中可致机体释放应激因子。AD是当机体受到某些刺激由肾上腺分泌出的一种激素,当其过度释放时会使心脏、肝脏的血管扩张,以及皮肤、黏膜的血管收缩,从而影响术中生命体征的稳定[8]。NE是肾上腺素去掉N-甲基后形成的物质,属于儿茶酚胺,该物质的过度释放也会对患者产生诸多的不良影响[9]。此外,术中CO2气腹的建立及冲洗液的使用可改变红细胞形态,使红细胞发生形态学改变,影响凝血功能,减少血小板、各种凝血因子的总量及降低凝血酶活性,进而会对凝血功能产生一定的影响,延长出血时间。而凝血功能的改变也会增加冲洗液的使用量,反复如此,形成恶性循环[10]。本研究结果显示,观察组在建立气腹,以及手术开始60 min、90 min 和 120 min的核心体温均低于同期对照组,在术后1 d的AD、NE、CRP水平均低于对照组,在术后 1 d 的PLT、TT及FIB水平均优于对照组,低体温的发生率低于对照组,上述比较均有统计学差异(P均<0.05)。这说明CO2和冲洗液加温措施不仅能够维持患者术中的体温恒定,还能改善其应激反应和凝血功能,且术中低体温发生率更低。可能的原因是,经加热后的CO2温度与腹腔温度接近(约为37 ℃),故不会产生明显的热量传递,进而可避免体温出现较大波动。当体温处于恒定状态时,能减少低体温对血红蛋白的影响,保持凝血因子的活性及血小板的总量,进而对凝血功能的影响变小[11]。此外,冲洗液经加温后,温度接近于机体正常体温,故在冲洗过程中不仅可降低冲洗液对体温的影响,还可降低因温差过大而引起应激因子的分泌,减少AD、NE、CRP等应激因子的释放,维持患者生命体征稳定,从而降低低体温的发生率[12]。
综上所述,将CO2和冲洗液加温措施用于行腹腔镜手术的妇科癌症患者,有助于减小其术中体温的变化,改善其应激水平和凝血功能,且术后低体温发生率更低。

