聚N-羟乙基丙烯酰胺-明胶基水凝胶传感器的制备及性能
姜 旻,郝雪芳,叶 磊,罗水源,冀 峰
(1. 泉州师范学院化工与材料学院福建省绿色环保功能鞋材工程研究中心,福建 泉州 362000;2. 内蒙古民族大学纳米创新研究院,内蒙古 通辽 028000;3. 山东大学 药学院,山东 济南 250012)
随着电子器件的飞速发展,可以追踪佩戴者身体运动的传感设备层出不穷[1]。传统传感器主要是由金属材料制备而成,该类传感器具有高灵敏度的优点,已经在高精度设备中使用,但是刚性大和硬度高等特征,使其无法与皮肤紧密贴合,无法适应人体的运动[2]。与传统传感器相比,柔性传感器因具有柔韧性好的优点而在电子皮肤等领域有着广阔的应用前景[3]。水凝胶是含有大量水分并且具有三维结构网络的交联聚合物,具有柔性特征,是柔性传感器构建的理想材料[4]。
化学交联是形成水凝胶的主要策略,但是由于其不可逆的共价作用,故通常存在功能性不足的问题[5]。基于物理交联作用的水凝胶通过其交联作用的可逆性能有效提高水凝胶的黏附特性等性能[6]。通过向水凝胶中掺杂自由离子是赋予其导电特性常用的方法。例如,Ge 等以化学交联的聚丙烯酰胺和基于氢键交联的聚乙烯醇作为水凝胶的基体材料,通过向前驱体溶液中加入氯化钾,制备了具有优异拉伸性能的导电水凝胶[7]。Liu 等以化学交联的聚丙烯酰胺和基于氢键交联的结冷胶作为水凝胶的基体材料,制备了具有优异拉伸性能的导电水凝胶[8]。基于这些水凝胶的传感器能够有效监测人体的肢体运动。
虽然在水凝胶传感器研制方面取得了诸多研究成果,由于其缺乏黏附性能,在使用过程中需要额外的辅助手段来实现传感器与基材间的紧密接触,这会降低检测的准确性。更为重要的是,水凝胶高含水量的本质特征,使其在低温条件下容易冻结,导致其失去柔性特征,限制了其在寒冷环境中的使用。因此,研发一种具有黏附性能和抗冻性能的水凝胶是扩宽水凝胶基传感器应用范围和提高监测精度的关键。
为了解决这些问题,诸多研究人员进行了相关的探索,例如为了提高黏附性能,Wang 等以聚乙烯醇和两性离子作为水凝胶的基体材料,制备了一种具有黏附性能的水凝胶基传感器[9];为了提高其抗冻活性,Yu 等将聚丙烯酰胺和黄原胶基水凝胶浸泡在甘油和水的溶液中,制备了具有抗冻性能的水凝胶基传感器[10]。但是,这类水凝胶基传感器在制备过程中存在浸泡过程复杂和浸泡不均匀等问题,对后续的大规模生产和实际产业化应用带来困难。因此,如何通过简单的方法研发出一种具有黏附性能和抗冻性能的水凝胶基传感器是推动其大规模应用的关键。
本课题组前期基于可逆的氢键交联作用制备了一种具有优异力学性能的PHEAA-GE-Gl-LiCl 水凝胶[11]。研究结果表明,向PHEAA 单网络水凝胶中引入GE 网络,可以大幅度提高水凝胶的力学性能。同时,抗冻试剂甘油通过与水分子之间形成氢键作用,能够赋予水凝胶优异的抗冻性能。考虑到抗冻试剂乙二醇分子中的羟基数目小于甘油分子中的羟基数目,采用乙二醇制备的水凝胶有望具有更低的弹性模量和更高的断裂应变。此外,NaCl 比LiCl具有更加优异的生物相容性。因此,本工作尝试向PHEAA-GE 水凝胶的前驱体溶液中引入氯化钠和乙二醇,制备了PHEAA-GE-EG-NaCl 水凝胶,并详细研究了水凝胶的力学性能、抗冻性能、黏附性能及在人体运动检测中的应用。
1 实验部分
1.1 试剂与仪器
N-羟乙基丙烯酰胺(分析纯)、明胶(胶强度~250 g Bloom)、氯化钠(分析纯)和乙二醇(分析纯):均从上海阿拉丁生物科技股份有限公司购买;实验用水:均为去离子水。
红外光谱仪:IS50 型,美国Nicolet 公司;高低温万能拉力机:3369 型,美国Instron 有限公司。
1.2 样品制备
首先,将N-羟乙基丙烯酰胺(HEAA,质量分数36%)、明胶(GE,质量分数4%)、2-羟基-4’-(2-羟乙氧基)-2-甲基苯丙酮(光引发剂I2959,质量分数1%)、氯化钠(NaCl)、乙二醇(EG)和H2O 的混合物在60 ℃搅拌2 h。然后,将上述溶液注射到模具中,降低体系的温度至室温后,在紫外灯下照射2 h,制得PHEAA-GE-EG-NaCl 水凝胶样品。
1.3 测试与表征
1.3.1 结构表征:采用傅里叶变换红外光谱仪对水凝胶样品的结构进行表征。测试波数范围为1000~4000 cm−1,扫描次数是32 次,分辨率是4 cm−1。
1.3.2 力学性能测试:采用高低温万能试样机测试水凝胶样品在室温和-30 ℃的力学性能,拉伸速度固定为100 mm/min。水凝胶的拉伸应力(σ)定义为负载力与水凝胶的截面积之比。拉伸应变(ε)定义为长度的变化值与原始长度之比。
1.3.3 抗冻性能测试:采用差示扫描量热仪(Discovery DSC25 型,美国TA 公司)测试水凝胶的结晶温度,扫描温度范围从﹣60~20 ℃,降温速度设定为2 ℃/min。采用旋转流变仪(DHR-2 型,美国TA 公司)测试水凝胶的动态低温流变性能,应变固定为1%,频率固定为1 Hz,温度扫描范围为-40~20 ℃,降温速度是2 ℃/min。
1.3.4 黏附性能测试:采用拉伸剪切实验测试水凝胶对基材的黏附强度。首先,用2 个相同的基材把水凝胶加在中间,然后用砝码压10 min,以保证水凝胶与基材紧密贴合。随后用10 mm/min 的速度进行拉伸,用拉伸过程中的最大力除以水凝胶的剪切面积得到水凝胶对基材的黏附强度。
1.3.5 导电性能测试:采用电化学工作站,通过线性扫描伏安法测试水凝胶的导电性能。水凝胶电导率的计算公式如式(1)

式中:σ——水凝胶的离子导电率;l和A——分别是2 个电极之间的距离和水凝胶的横截面积;R——水凝胶的电阻。
1.3.6 传感性能测试:采用电化学工作站和拉力机连用研究水凝胶基传感器在拉伸和释放过程中的电阻变化,进而研究其传感性能。通过电阻-应变曲线的斜率来评估水凝胶基应变传感器的灵敏度,该斜率称为应变因子(GF),其计算公式如式(2)

式中:R0——水凝胶在初始状态下的电阻值;R——水凝胶在产生应变时的实时电阻值;∆l——应变。
1.3.7 水凝胶基传感器在人体运动检测中的应用分析:为了研究水凝胶在人体运动检测中的应用,将水凝胶基应变传感器贴附在志愿者的关节和喉咙等部位,并将水凝胶的两端连接到电化学工作站上。通过记录和分析志愿者关节和喉咙等部位运动过程中的电阻变化数据,实现对人体运动的检测。
2 结果与讨论
2.1 水凝胶的合成与表征
PHEAA-GE-EG-NaCl 水凝胶的制备过程见Fig.1。首先,将HEAA、GE、光引发剂I2959、EG 和NaCl 的混合溶液在60 ℃加热2 h,使凝胶前驱体形成均一的溶液。然后,降低体系的温度至室温,随后通过紫外光引发HEAA 单体光聚合得到PHEAA,此时基于PHEAA 分子之间的氢键作用形成PHEAA网络并与GE 网络相互渗透。至此,成功制备了PHEAA-GE-EG-NaCl 双网络水凝胶。

Fig.1 Schematic of the one-pot synthesis of a fully physically cross-linked PHEAA-GE-EG-NaCl hydrogel
采用红外表征了凝胶分子间的相互作用,如Fig.2 所示,在PHEAA 凝胶的红外谱图中,3266 cm−1处宽的吸收谱带是O—H 和N—H 的伸缩振动,1628 cm−1和1551 cm−1处的吸收峰分别是C=O 的伸缩振动和酰胺中N—H 的弯曲振动。向PHEAA 凝胶前驱体溶液中加入乙二醇后,O—H 和N—H 的伸缩振动、C=O 的伸缩振动和N—H 的弯曲振动分别移动到3270 cm−1,1636 cm−1和1557 cm−1,这说明乙二醇与PHEAA 凝胶中的O—H,N—H 和C=O 基团之间形成了氢键作用。在明胶的红外谱图中,3274 cm−1处宽的吸收谱带是N—H 的伸缩振动,1629 cm−1和1521 cm−1处的吸收峰分别是C=O 的伸缩振动和酰胺中N—H 的弯曲振动。向明胶前驱体溶液中加入乙二醇后,N—H 的伸缩振动,C=O 的伸缩振动和酰胺中N—H 的弯曲振动分别移动到3278 cm−1,1632 cm−1和1544cm−1,这说明乙二醇与明胶中的N—H 和C=O 基团之间形成了氢键作用。与PHEAA 和GE 凝 胶 相 比,在PHEAA-GE 凝 胶 的 红 外谱图中,没有形成新的吸收谱带和吸收峰,这说明PHEAA 和GE 之间没有发生化学反应。同时,O—H和N—H 的伸缩振动、C=O 的伸缩振动和N—H 的弯曲振动分别移动到3281 cm−1,1628 cm−1和1548 cm−1,这说明PHEAA 与GE 之间存在氢键作用。与PHEAA-GE-NaCl 凝胶的红外谱图相比,在PHEAAGE-EG-NaCl 凝胶中,O—H 和N—H 的伸缩振动、C=O的伸缩振动和N—H 的弯曲振动由3272 cm−1,1631 cm−1和1546 cm−1分别移动到3278 cm−1,1633 cm−1和1548 cm−1,这说明乙二醇降低了凝胶中分子间的氢键作用。

Fig.2 FT-IR spectra of different hydrogels
2.2 水凝胶的力学性能
Fig.3(a~c)是PHEAA-GE-EG-NaCl 水凝胶的光学图片。由Fig.3(a)和Fig.3(b)可知,PHEAA-GE-EGNaCl 水凝胶在伸直或扭曲状态下都可以拉伸16倍。由Fig.3(c)可知,PHEAA-GE-EG-NaCl 水凝胶具有优异的耐戳性能。Fig.3(d)是PHEAA-GE 水凝胶、PHEAA-GE-NaCl 水 凝 胶 和PHEAA-GE-EG-NaCl 水凝胶的应力-应变曲线。前期研究结果表明,当PHEAA 的质量分数是36%、GE 的质量分数是4%时,PHEAA-GE 双网络水凝胶具有最佳的力学性能[11]。如Fig.3(d)所示,在该比例下PHEAA-GE 双网络水凝胶的拉伸强度和拉伸应变分别是1.39 MPa 和1158%。由Fig.3(e)可知,向PHEAA-GE 水凝胶前驱体溶液中引入氯化钠和乙二醇制备的PHEAA-GENaCl 水凝胶和PHEAA-GE-EG-NaCl 水凝胶仍然具有优异的拉伸性能,3 种水凝胶的拉伸应变在926%~1567%范围内。Fig.3(f)是不同NaCl 浓度下制备的PHEAA-GE-NaCl 水凝胶的应力-应变曲线,可以看到,当NaCl 的质量分数从0.2%增加到1.6%时,PHEAA-GE-NaCl 水凝胶的应变都在800%附近。Fig.3(g)是不同质量比的乙二醇与水制备的PHEAAGE-EG-NaCl 水凝胶的应力-应变曲线,可以得到,当乙二醇与水的质量比从1:6 增加到1:2 时,PHEAAGE-EG-NaCl 水凝胶的断裂应力从0.95 MPa 降低到0.36 MPa。当乙二醇与水的质量比是1:4 时,PHEAA-GE-EG-NaCl 水凝胶的弹性模量是0.16 MPa。与前期构建的PHEAA-GE-Gl-LiCl 水凝胶相比,PHEAA-GE-EG-NaCl 水凝胶具有更低的弹性模量和断裂应力[11,12]。这表明PHEAA-GE-EG-NaCl 水凝胶中分子间的相互作用低于PHEAA-GE-Gl-LiCl水凝胶。因此,PHEAA-GE-EG-NaCl 水凝胶具有更高的断裂应变。

Fig.3 Photos of PHEAA-GE-EG-NaCl hydrogel at different states of (a) stretching, (b) curly stretching and (c) puncture resistance; (d) tensile stress-strain curves of PHEAA-GE hydrogel (wPHEAA=36%, wGE=4%), PHEAA-GE-NaCl hydrogel(wPHEAA=36%, wGE=4%, wNaCl=1.2%), PHEAA-GE-EG-NaCl hydrogel (wPHEAA=36%, wGE=4%, wNaCl=1.2%, m(EG):m(H2O)=1:4); (e) their corresponding elongations at break; (f) effect of NaCl concentration on the mechanical property of PHEAA-GE-NaCl hydrogel; (g) effect of the mass ratios of EG/water on the mechanical property of PHEAA-GE-EGNaCl hydrogel

Fig. 4 Anti-freezing properies of PHEAA-GE-EG-NaCl hydrogels DSC curves of (a) different solutions and (b)hydrogels; (c) storage modulus and (d) stress-strain curves of hydrogels at -30 ℃
2.3 水凝胶的抗冻性能
水凝胶中含有大量的水分,当外界温度低于水凝胶中水分子的结晶温度时,水凝胶中的水分子将会被冻结,这会影响水凝胶的低温力学性能和导电性能,进而限制其在低温下的使用。Fig.4(a)和Fig.4(b)分别是不同种类的溶液和采用这些溶液制备的水凝胶的DSC 曲线。由Fig.4(a)可知,纯水的结晶温度是-14 ℃,氯化钠水溶液中水的结晶温度是-15 ℃。当向氯化钠水溶液中引入乙二醇后,水分子的结晶温度进一步降低,同时,水分子的结晶温度随着乙二醇含量的增加而降低。这表明抗冻试剂乙二醇能够有效抑制溶液中水分子的结晶。由Fig.4(b)可知,水凝胶中的水分子具有比对应溶液更低的结晶温度,这表明水凝胶的凝胶网络也能够降低水凝胶中水分子的结晶温度。王万杰教授研究团队基于分子间的氢键作用构建了聚N-羟乙基丙烯酰胺-壳聚糖基抗冻水凝胶,在研究过程中发现水凝胶的凝胶网络中的羟基等基团同样能够与水分子之间形成氢键作用,降低水凝胶中水分子的结晶温度[13]。这与笔者的研究结果相一致。Fig.4(c)是水凝胶的流变曲线,由图可知,PHEAA-GE-NaCl 水凝胶的储能模量在-18 ℃左右急剧增加,这说明PHEAA-GE-NaCl 水凝胶中的水分子在该温度下已经结冰了。当向水凝胶体系中引入乙二醇后,PHEAA-GE-EG-NaCl 水凝胶(乙二醇与水的质量比是1:6)的储能模量急剧增加的温度降低至-35 ℃。继续增加乙二醇与水的质量比到1:4 或1:2 时,PHEAA-GE-EG-NaCl 水凝胶的储能模量在-40~20 ℃范围内都保持优异的稳定性。流变与DSC 的研究结果相一致,结果都说明了乙二醇能够抑制低温下冰晶的形成。Fig.4(d)是水凝胶在-30 ℃的应变-应力曲线,由图可知,PHEAA-GE-NaCl 水凝胶的断裂伸长率只有100%,而PHEAA-GE-EG-NaCl 水凝胶的断裂伸长率都大于350%,结果进一步证明了乙二醇的加入使PHEAA-GE-EG-NaCl 水凝胶具有优异的抗冻性能。
2.4 水凝胶的导电性能
通过向水凝胶前驱体溶液中加入NaCl 赋予水凝胶导电性能。如Fig.5(a)所示,当NaCl 的质量分数从0%增加到1.6%时,水凝胶的导电率从0.01 S/m增加到0.53 S/m,这说明NaCl 的添加对水凝胶导电率的提升起着至关重要的作用。Fig.5(b)是乙二醇与水的质量比对PHEAA-GE-EG-NaCl 水凝胶导电性能的影响。可以看出,当乙二醇与水的质量比从0:1增加到1:2 时,PHEAA-GE-EG-NaCl 水凝胶的电导率从0.33 S/m 降低到0.06 S/m。结果表明,随着乙二醇含量的增加,PHEAA-GE-EG-NaCl 水凝胶中离子的运动能力降低。Fig.5(c)是温度对PHEAA-GE-EGNaCl 水凝胶导电率的影响,可以看出,当外界温度从室温降低到-30 ℃时,PHEAA-GE-EG-NaCl 水凝胶的导电率从0.33 S/m降低到0.17 S/m。结果表明,在低温下导电离子的运动能力减弱。考虑到乙二醇与水的质量比对PHEAA-GE-EG-NaCl 水凝胶的力学性能和导电性能的影响,选择乙二醇与水的质量比为1:4 的PHEAA-GE-EG-NaCl水凝胶用于后续实验的研究。

Fig.5 Effect of (a) NaCl concentration, (b) mass ratio of EG/water and (c) temperature on the change of conductivity

Fig. 6 Adhesion properties of PHEAA-GE-EG-NaCl hydrogel
2.5 水凝胶的黏附性能
具有黏附性能的水凝胶基传感器能够更加灵敏地捕捉到运动信号,因此,黏附性能是评价水凝胶基传感器的一项重要指标。水凝胶与基材的黏附力大多归因于水凝胶与基材表面间的物理相互作用,例如:氢键、金属配位和疏水相互作用[14]。因此,含有大量羟基和亚氨基等活性基团的PHEAAGE-EG-NaCl 水凝胶很可能对不同基材都具有黏附能力。Fig.6(a)说明了PHEAA-GE-EG-NaCl 水凝胶对众多固体材料(例如:塑料、橡胶、玻璃、金属、陶瓷、纸、猪皮、聚四氟乙烯、石头和树叶)都具有黏附能力。
随后,通过拉伸剪切实验进一步评价PHEAAGE-EG-NaCl 水凝胶对不同基材的黏附强度。如Fig.6(b)和Fig.6(c)所示,PHEAA-GE-EG-NaCl 水凝胶在纸片、玻璃、铜片和聚四氟乙烯片上的黏附强度分别是42.26 kPa,22.16 kPa,17.06 kPa 和11.89 kPa。研究结果证明了PHEAA-GE-EG-NaCl 水凝胶对这些基材表现出良好的黏附能力。PHEAA-GE-EG-NaCl水凝胶与纸片之间强的黏附强度主要来源于纤维素中的羟基基团与PHEAA-GE-EG-NaCl 水凝胶之间的氢键作用[14]。PHEAA-GE-EG-NaCl 水凝胶与玻璃或金属铜片之间相对较强的黏附强度可能来源于水凝胶与玻璃或者金属铜片之间的氢键和金属配位作用[14]。PHEAA-GE-EG-NaCl 水凝胶与PTFE 之间相对较低的黏附强度是因为,疏水的PTFE 不能与PHEAA-GE-EG-NaCl 水凝胶形成大量的氢键以保证二者之间的黏合[15]。此外,由Fig.6(c)可知,PHEAA-GE 和PHEAA-GE-NaCl 水凝胶对不同基材具有相当的黏附强度,这说明NaCl 对黏附具有较小的影响。而PHEAA-GE-EG-NaCl 水凝胶对不同基材的黏附强度稍高于PHEAA-GE 水凝胶和PHEAAGE-NaCl 水凝胶,这可能是因为乙二醇分子中的羟基基团也能够与基材表面形成氢键作用。
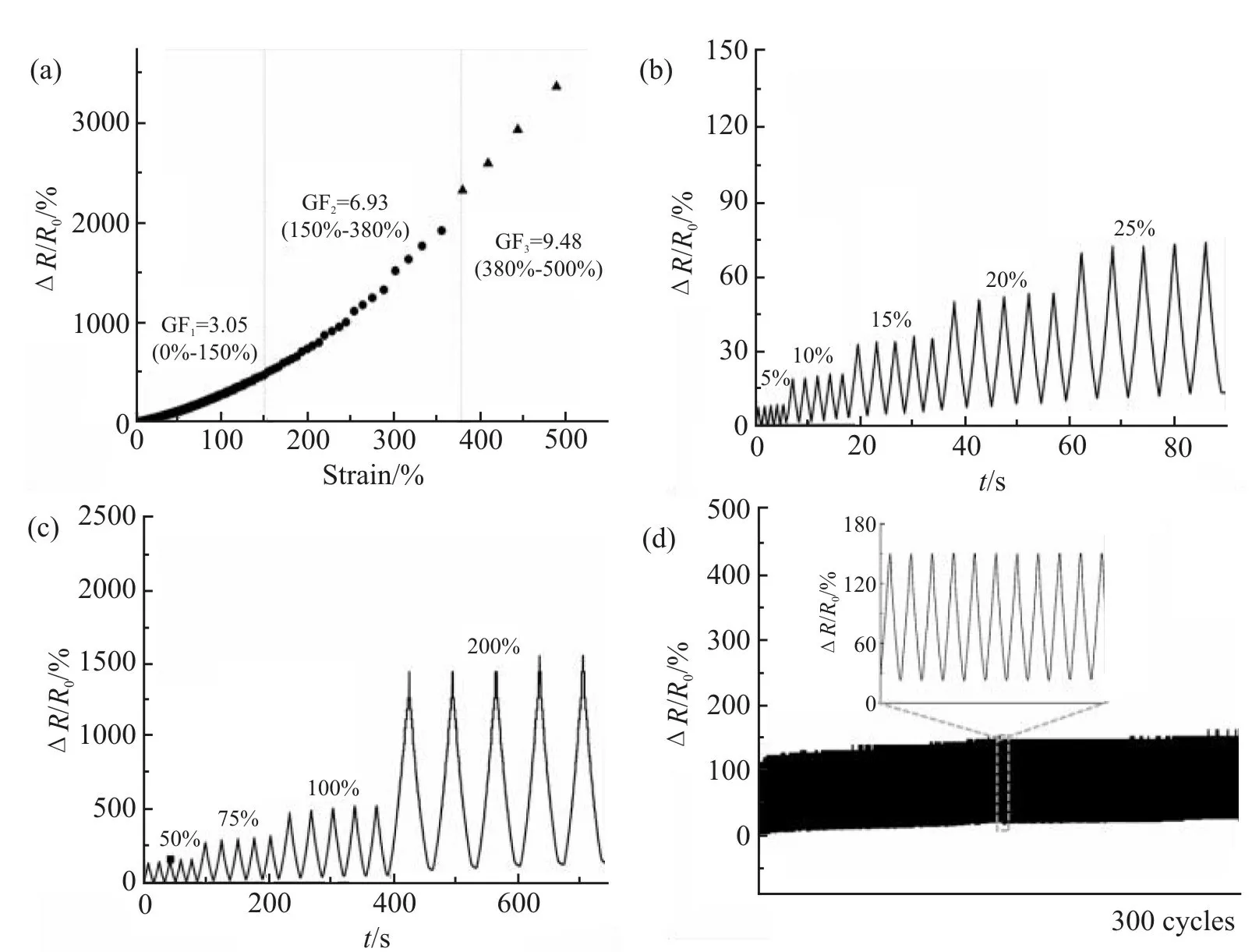
Fig. 7 Strain sensitivity of PHEAA-GE-EG-NaCl hydrogel
2.6 PHEAA-GE-EG-NaCl 水凝胶的传感性能
如Fig.7(a)所示,首先测试了PHEAA-GE-EGNaCl 水凝胶在0-500%拉伸应变范围内的实时电阻变化来表征PHEAA-GE-EG-NaCl 水凝胶对应变的敏感性。研究结果表明,在0 500%拉伸应变范围内,随着应变的增加,PHEAA-GE-EG-NaCl 水凝胶的相对电阻的变化率也不断增加。当应变在0 150%范围内,水凝胶的应变因子GF是3.05,当应变在150% 380%范围内,水凝胶的GF是6.93,当应变在380% 500%范围内,水凝胶的GF是9.48,水凝胶较高的GF值表明PHEAA-GE-EG-NaCl 水凝胶具有较高的应变灵敏度。传感器在使用过程中,除了需要具备应变灵敏度,还需要具有稳定性。Fig.7(b)和Fig.7(c)表明PHEAA-GE-EG-NaCl 水凝胶基传感器在小应变(5% 25%)和大应变(50% 200%)范围内,当应变固定时,PHEAA-GE-EG-NaCl 水凝胶基传感器呈现的电信号是可重复的,这说明PHEAA-GE-EGNaCl 水凝胶基传感器对应变具有优异的稳定性。为了进一步证明PHEAA-GE-EG-NaCl 水凝胶基应变传感器的稳定性,对PHEAA-GE-EG-NaCl 水凝胶基传感器施加了50%的应变,并连续进行300 次循环拉伸实验。如Fig.7(d)所示,结果表明,PHEAA-GEEG-NaCl 水凝胶基传感器在300 次循环拉伸-释放过程中相对电阻的变化表现出了优异的稳定性,这再次证明了PHEAA-GE-EG-NaCl 水凝胶基应变传感器具有优异的稳定性。

Fig. 8 Real-time monitoring of human activities based on wearable PHEAA-GE-EG-NaCl hydrogel sensor

Fig. 9 Real-time monitoring of human activities based on wearable PHEAA-GE-EG-NaCl hydrogel sensor. Relative resistance changes (ΔR/R0) of different imitative human joints motions: (a) finger bending at different angles; (b) wrist joint bending; (c) elbow joint bending; (d) knee joint bending
2.7 PHEAA-GE-EG-NaCl 水凝胶基传感器在人体运动检测中的应用
由于PHEAA-GE-EG-NaCl 水凝胶具有优异的拉伸性能、导电性能和传感性能,因此在人体运动检测中具有巨大的应用前景。为了研究PHEAA-GEEG-NaCl 水凝胶基传感器在人体运动检测中的实际应用,将PHEAA-GE-EG-NaCl 水凝胶组装成电阻式应变传感器检测人体大幅度的关节运动和人体其它部位的细微动作,结果如Fig.8 所示。由Fig.8(a)可以看出,将PHEAA-GE-EG-NaCl 水凝胶基传感器放置在手指上,当手指的弯曲角度由0°依次增加到30°,60°,90°时,ΔR/R0分别从0%增加到37.03%,63.50%,99.04%。当手指弯曲角度固定时,ΔR/R0也固定。当手指再次从90°依次降低到60°,30°和0°时,水凝胶基传感器的相对电阻变化会恢复到原来的水平,这说明PHEAA-GE-EG-NaCl 水凝胶基传感器具有高度敏感的传感性能。由Fig.8(b)~Fig.8(d)可以看出,PHEAA-GE-EG-NaCl 水凝胶基传感器同样能够稳定地检测手腕、大腿和手肘关节的周期性伸展-弯曲运动。Fig.8(e)可以看出,当志愿者反复做出“震惊”表情时,贴在脸部的PHEAA-GE-EG-NaCl水凝胶基传感器能够成功捕捉到脸部的细微动作变化。从Fig.8(f)和Fig.8(g)可以看出,当志愿者反复做出“抬头”和“吞咽”动作时,贴在喉处的水凝胶基传感器能够成功感知到喉部的细微动作变化。Fig.8(h)和Fig.8(i)可以看出,当志愿者重复发出单词“gel”或者“hello”时,水凝胶基传感器能够得到稳定的周期性电信号。同时,不同的单词对应不同的电信号。以上结果表明,PHEAA-GE-EG-NaCl 水凝胶基传感器能够成功实时将人体大幅度的肢体运动和小幅度的应变信号转变为电信号,最终实现对人体运动的检测。
由于PHEAA-GE-EG-NaCl 水凝胶在低温下仍然具有优异的拉伸性能和导电性能,因此,PHEAAGE-EG-NaCl 水凝胶基传感器在低温下仍然可以实现对肢体运动的检测。为了进一步验证,首先,将PHEAA-GE-EG-NaCl 水凝胶基传感器绑在木头人或者木手的指定部位,随后,将其放置在-30 ℃冰箱中,并用手快速扳动木头人或木手的指定部位,同时用电化学工作站记录在此过程中电信号的变化。由Fig.9 可以看出,PHEAA-GE-EG-NaCl 水凝胶基传感器在-30 ℃仍然可以成功检测肢体运动。
3 结论
基于分子间物理相互作用,采用简单高效“一锅法”制备了一种具有优异拉伸性能、抗冻性能和黏附性能的PHEAA-GE-EG-NaCl 水凝胶。基于PHEAA-GE-EG-NaCl 水凝胶的应变传感器在较宽的温度范围内能够稳定地检测人体大幅度的肢体运动和小幅度的生理信号。这项研究工作不仅为PHEAA-GE-EG-NaCl 水凝胶在柔性可穿戴传感器中的应用提供了理论和实验依据,同时为快速制备水凝胶基传感器提供了新思路。

