富马酸替诺福韦二吡呋酯片治疗HBV感染孕妇及阻断母婴传播的效果
黄熙琳
我国 1992年乙型肝炎病毒(hepatitis B virus,HBV)乙肝表面抗原(HBsAg)携带率为9.75%,2016年降至6.10%,其中5岁以下儿童HBsAg携带率低于1%[1]。由于婴儿感染最主要的途径是母婴垂直传播,因此在妊娠期进行HBV母婴传播阻断尤为重要。母婴垂直传播根据感染的时机不同可分为宫内感染、产时感染和产后感染,在婴儿出生时给予主被动免疫可有效预防产时和产后感染,但常规护肝治通过葡萄糖、肌苷等保肝药物治疗,并不能有效防止胎儿宫内感染,导致阻断HBV母婴传播效果不理想[2-3]。富马酸替诺福韦二吡呋酯片(TDF)为无环5’-单磷酸腺苷类似物,其活性成分替诺福韦二磷酸可与5’-三磷酸腺苷类似物竞争,阻断病毒DNA链延长,进而抑制病毒复制,降低机体内病毒含量,提高谷丙转氨酶(ALT)复常率及乙型肝炎病毒-脱氧核糖核酸(HBV-DNA)转阴率,阻断HBV向婴儿传播[4]。基于此,本研究将回顾性分析82例HBV感染孕妇的病历资料,观察TDF治疗效果,报告如下。
1 资料与方法
1.1 一般资料
回顾性分析2020年1-12月深圳市人民医院收治的82例HBV感染孕妇,按治疗方法将入选者分为常规保肝治疗组(常规保肝治疗,40例)、TDF治疗组(TDF治疗,42例)。纳入标准:(1)符合文献[5]HBV感染诊断标准;(2)患者ALT水平升高,病毒载量不低于2×106IU/ml;(3)单胎妊娠;(4)孕周 <24周;(5)临床资料完善;(6)对本研究所用药物不过敏。排除标准:(1)合并严重的糖尿病、高血压等;(2)近期需服用抗免疫类药物;(3)伴有其他病毒感染。常规保肝治疗组:年龄22~30岁,平均(26.27±2.52)岁;孕周15~23周,平均(20.16±1.38)周;HBV DNA 载量(5~8)×106IU/ml,平均(6.11±1.23)×106IU/ml;体重指数(BMI)20~27 kg/m2,平均(23.62±2.11)kg/m2;HBV感染病程9~40个月,平均(26.53±6.34)个月。TDF治疗组:年龄21~29岁,平均(26.29±2.54)岁;孕周16~23周,平均(19.89±1.62)周;HBV DNA 载量(5~8)×106IU/ml,平 均(6.16±1.25)×106IU/ml;BMI 19~27 kg/m2,平均(23.49±2.38)kg/m2;HBV 感染病程10~43个月,平均(25.40±6.22)个月。两组年龄、ALT水平、HBV DNA载量、BMI等一般资料对比差异无统计学意义(P>0.05),具有可比性。本研究所使用的相关患者临床资料均经医学伦理委员会同意后再使用。
1.2 方法
常规保肝治疗组:给予日常饮食、情绪、睡眠管理,或者服用葡萄糖、肌苷等保肝药物治疗。
TDF治疗组:给予口服富马酸替诺福韦二吡呋酯片(齐鲁制药,国药准字H20173185,300 mg/片)治疗,根据检查结果,孕妇于孕24周后清晨服用1次,300 mg/次,服用至分娩后1个月。
新生儿于出生后的24 h内,接种重组乙型肝炎疫苗(深圳康泰,国药准字20110026,10 µg/瓶)20 µg,注射免疫球蛋白(浙江海康,国药准字S20063058,100 IU/瓶)100 IU,进行乙肝免疫阻断治疗。
1.3 观察指标及评价标准
孕妇恢复情况:于不同孕周(30周、35周、分娩前)抽取孕妇空腹静脉血5 ml,用高速离心机以3 000 r/min的速度离心分离得血清,取血清进行检测。采用酶联免疫吸附试验(ELISA)检测血清中ALT水平,采用荧光定量PCR法检测HBV-DNA载量,试剂盒由深圳匹基生物技术开发公司提供。复常标准:ALT水平低于40 U/L以下为恢复正常。转阴:机体HBV-DNA载量降低至500 IU/ml以下[6]。
肝功能指标:于治疗前、分娩后6个月,分别抽取产妇空腹静脉血 5 ml,用高速离心机以 3 000 r/min的速度离心分离得血清,取血清进行进行检测。采用全自动生化分析仪(深圳盛信康,sk6000)测定血清谷丙转氨酶(ALT)、门冬氨酸氨基转移酶(AST)、总胆血红素(TBIL)水平。
婴儿阳性携带率情况:分别于出生时、出生后6个月抽取婴儿空腹静脉血5 ml,用高速离心机以3 000 r/min的速度离心分离得血清,取血清进行进行检测。采用全自动化学发光免疫分析仪(深圳盛信康,sk6000)及配套试剂检测乙型肝炎表面抗原(HBsAg)、乙型肝炎表面抗体(HBsAb)表达状况,试剂盒由上海科华生物工程股份有限公司提供。
不良反应发生情况:观察并记录两组胆汁酸增高、羊水浑浊、胎儿畸形的发生例数。
1.4 统计学处理
所有数据均应用EPidate软件,平行双录入,保证录入数据的准确一致。录入SPSS 22.0软件中分析,计量资料以(±s)表示,采用t检验,计数资料以率(%)表示,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组孕妇恢复情况比较
TDF治疗组孕妇不同孕期ALT复常率、HBVDNA转阴率均高于常规保肝治疗组(P<0.05),见表1。

表1 两组孕妇恢复情况比较[例(%)]
2.2 两组肝功能指标比较
治疗前,两组孕妇ALT、AST、TBIL水平对比差异无统计学意义(P>0.05);分娩后6个月,TDF治疗组ALT、AST、TBIL水平低于常规保肝治疗组(P<0.05),见表 2。
表2 两组肝功能指标比较(±s)

表2 两组肝功能指标比较(±s)
*与本组治疗前比较,P<0.05。
组别 ALT(U/L)AST(U/L)TBIL(µmol/L)治疗前 分娩后6个月 治疗前 分娩后6个月 治疗前 分娩后6个月常规保肝治疗组(n=40) 217.35±34.81 51.81±6.42* 204.18±33.46 49.32±6.38* 35.46±5.44 21.05±3.40 TDF 治疗组(n=42) 218.44±34.86 47.67±5.37* 205.04±34.09 45.24±5.87* 34.79±5.20 16.58±3.16 t值 0.142 3.159 0.115 3.009 0.570 6.159 P值 0.888 0.002 0.909 0.004 0.571 <0.001
2.3 两组婴儿HBsAb、HBsAg阳性率比较
TDF治疗组婴儿出生时、出生后6个月HBsAb阳性率高于常规保肝治疗组,出生后6个月HBsAg阳性率低于常规保肝治疗组(P<0.05),两组出生时HBsAg阳性率对比差异无统计学意义(P>0.05),见表3。
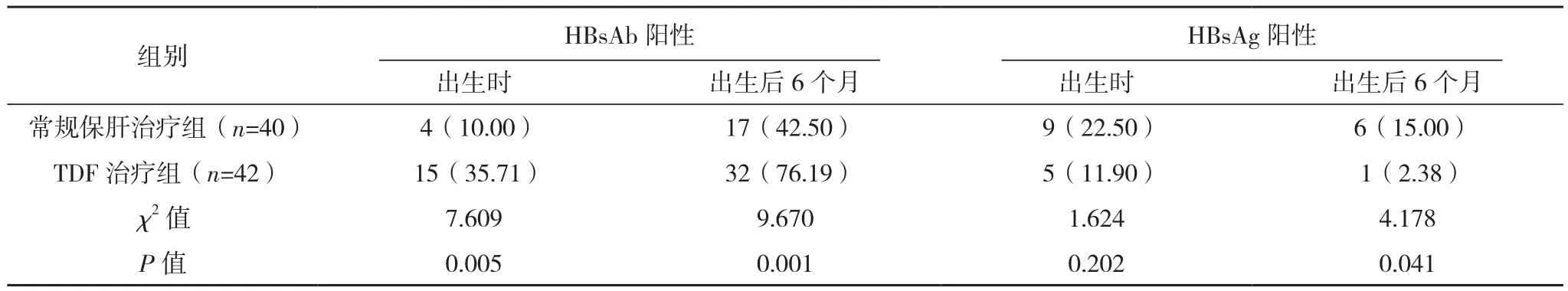
表3 两组婴儿HBsAb、HBsAg阳性率比较[例(%)]
2.4 两组药物不良反应发生情况比较
TDF治疗组药物不良反应发生率低于常规保肝治疗组(4.76%<20.00%),差异有统计学意义(P<0.05),见表 4。

表4 两组药物不良反应发生情况比较[例(%)]
3 讨论
HBV的传播方式主要包括血液、母婴垂直及性传播,其中母婴垂直传播是婴儿患慢性肝炎最主要的途径[7],因此为有效防治婴儿HBV感染,需对HBV感染孕妇进行有效的治疗。临床常规选择对感染孕妇进行护肝治疗,于婴儿出生后,再实行免疫球蛋白注射及乙肝疫苗接种,这种主、被动的联合免疫阻断,可使大部分婴儿避免HBV感染,但少部分孕妇孕期表现为血清高HBV-DNA伴HBeAg阳性所分娩的婴儿,给予阻断后仍会感染HBV[8]。因此,有研究提出,对出现上述高危因素的孕妇进行抗病毒药物治疗,可有效阻断母婴垂直传播,降低婴儿HBeAg阳性率[9]。TDF是抗HBV治疗药物,可阻断病毒DNA转录,降低孕妇血清HBV-DNA载量,减少肝损伤,降低婴儿HBV感染率。
ALT为评估肝脏病毒感染损害的主要指标,当血清中ALT含量明显升高时,表明肝细胞受到损伤。HBV-DNA为机体病毒复制和活跃情况相关指标,其升高反映机体病毒复制较活跃,患者处于传染期,胎儿发生宫内感染风险较高[10]。本研究结果中,TDF治疗组不同孕周恢复情况均高于常规保肝治疗组,ALT、AST、TBIL水平低于常规保肝治疗组(P<0.05),说明服用TDF可通过降低病毒复制的活跃度及传染性,防止肝细胞损伤和胎儿感染。TDF是抗HBV治疗一线药物,可通过阻断病毒DNA转录,抑制病毒复制,从而降低血液中HBV-DNA载量,减少其对孕妇造成持续性肝损伤,恢复血清中ALT、AST 水平[11]。
HBeAg是HBV核心蛋白质,其水平升高提示人体肝细胞受到损伤,并处于较强的传染期。HBsAb是机体病毒感染后产生的保护性抗体,其呈阳性提示机体对乙肝病毒产生抵抗力[12]。本研究结果中,TDF治疗组婴儿出生时、出生后6个月HBsAb阳性率高于常规保肝治疗组,出生后6个月TDF治疗组HBsAg阳性率低于常规保肝治疗组(P<0.05),说明TDF可阻断母婴垂直传播,降低婴儿病毒感染发生率。当孕妇血清中病毒含量过高时,可通过胎盘细胞对胎儿造成宫内感染,TDF抑制病毒DNA复制,减少其机体内病毒数量,进而降低胎儿HBsAg携带率,起到阻断母婴传播的效果,与张永萍[10]研究一致。另有研究显示,应用TDF于孕24周开始治疗HBV感染孕妇对阻断母婴垂直传播的效果较好[13],本研究与之相符。
本研究结果中,TDF治疗组药物不良反应发生率低于常规保肝治疗组(P<0.05),说明TDF治疗HBV感染孕妇能减少不良反应的发生。TDF主要经肾脏排泄,其安全性研究表明,是可用于孕妇治疗的B类药物,不会增加婴儿先天畸形发生率[14];另于春燕[15]的研究中,保肝治疗组不良反应发生率为20.00%,高于替诺福韦组3.33%,表明替诺福韦可降低不良反应的发生,本研究结果与之相似。
综上所述,TDF用于治疗HBV感染孕妇,可有效抑制病毒复制,提高HBV-DNA转阴率,从而改善患者的肝功能,促进ALT复常,同时能阻断HBV母婴垂直传播,且不良反应少,安全性较高。本研究也有一定不足,因HBV感染孕妇机体内还存在炎症反应,而本研究未观察TDF对孕妇体内炎症的影响。另外,本研究为回顾性分析,部分结果易受选择偏倚和回忆偏倚的影响。在未来的研究中,可行前瞻性、大样本研究,以更深入探讨TDF治疗HBV感染孕妇的临床价值。

