介入治疗增加残肝体积二期行吲哚菁绿辅助腹腔镜右半肝切除1例报告
汪大刚 吴昊钧,陈利平 李 唐,廖尔文
成都高新区合作社卫生服务中心 四川大学华西医院胆道外科 华西医院上锦分院普外一科
我中心成功为1例术前评估残肝体积不足的巨大右肝肝癌患者经门静脉栓塞(portal vein embolization,PVE)联合动脉化疗栓塞术(transarterial chemoembolization,TACE)增加残肝体积后,施行吲哚菁绿(indocyanine green,ICG)辅助腹腔镜右半肝切除术,经文献检索,国内外少有报道,现将病例资料总结如下。患者女,34岁,因“上腹隐痛1个月”收入我科。体格检查上腹部轻压痛。CT示:右肝巨大占位性病变,大小约15.2 cm×9.4 cm,右肝动脉供血。查血结果:甲胎蛋白>1 210.00 ng/mL,余未见异常。ICG 15 min清除率8.7%。既往乙肝病史。术前行三维重建,见图1。肿瘤紧邻肝中静脉,保留肝中静脉可能为临界切除,且依照预切线计算残肝体积为467 mL,22.2%。评估残肝体积过小,术后肝衰竭风险大。与患者、家属商议后决定介入后二期手术。先行PVE,使用聚乙烯醇颗粒栓塞剂、弹簧圈选择性栓塞门静脉右支。复查肝功能无异常,于PVE术后3 d行TACE,使用碘化油及表柔比星高选择性注入供应瘤体动脉。PVE术后40 d复查肝功能正常,再次行三维重建示瘤体明显缩小,与肝中静脉距离明显增加,按照智能门静脉分段计算左半肝残肝体积为575 mL,31.5%。于PVE术后45 d行ICG辅助腹腔镜前入路右半肝切除术。手术顺利,术中情况见图2、图3,手术时间260 min,术中出血约400 mL。剖视标本见肿瘤部分液化坏死。术后无≥Clavien-Dindo Ⅱ级并发症发生,术后7 d复查CT,患者恢复良好。术后12 d顺利出院。
讨 论 肝脏切除术是肝癌患者首选的根治性治疗手段。有相当比例的患者诊断时因肿瘤大小、位置及邻近主要血管,根治性手术需要切除大范围的肝脏,残肝体积不足成为患者肝功能衰竭与死亡的主要原因。文献建议,无肝病背景的患者残肝体积需超过30%,而伴有肝病背景的患者则需超过40%[1]。1990年Makuuchi等[2]首次为1例肝门胆管癌患者行PVE增加残肝体积,效果良好。PVE后栓塞侧门静脉血供减少,动脉血供会补偿性增加,可能加速肿瘤生长。因此PVE联合TACE治疗既可有效控制肿瘤生长,又可显著增加残肝体积,且相对安全[3]。本例患者介入治疗后残肝体积增加,瘤体缩小,肿瘤部分坏死,无并发症发生。
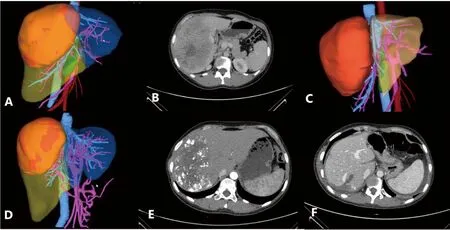
图1 A:PVE前三维重建门静脉智能分段;B:PVE+TACE治疗前CT;C:PVE前三维重建预切线分段,可见肿瘤可能超过右半肝范围,肝中静脉可能无法保留,且残肝体积不足;D:PVE+TACE治疗后三维重建门静脉智能分段;E:PVE+TACE治疗后的CT;F:术后5天CT
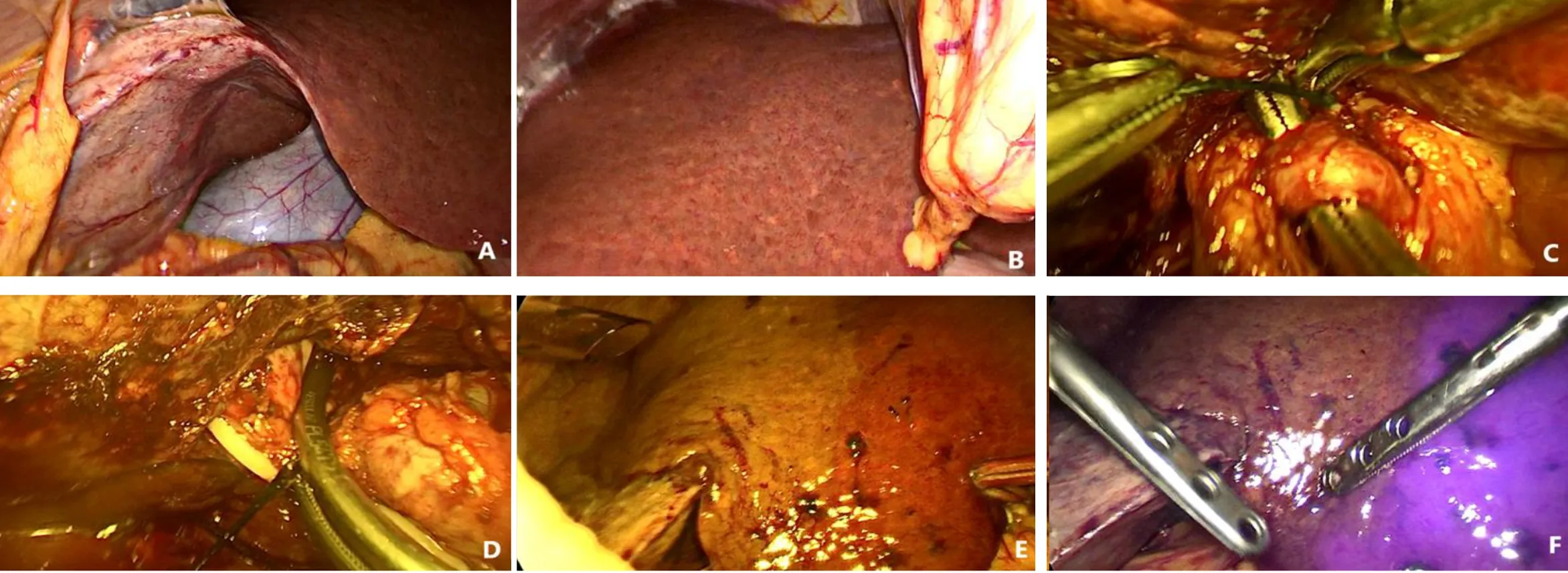
图2 探查阶段(A:PVE后肝组织改变;B:可见瘤体处;C:结扎肝右动脉;D:鞘外法阻断右肝蒂起始部;E:半肝缺血线;F:ICG反染)

图3 A、B:右侧尾叶被ICG染色,予以保留;C:离断右肝蒂;D、E:完全按照ICG染色分界离断肝组织;F:离断前裂静脉;G:离断肝右静脉;H、I:肝断面,未显露肝中静脉等结构标识。五角星为右侧尾叶;圆圈为右肝蒂起始部
随着微创理念的发展进步、腹腔镜技术与器械的改进普及,腹腔镜肝切除术的肿瘤学效果已被证实与开放手术相当[4],趋于成为常规术式。本例患者术前计划采用前入路[5]行腹腔镜右半肝切除术,考虑到肝脏体积改变导致的功能性左右肝分界可能已经失常,选择术中行ICG荧光辅助。结扎右肝动脉、门静脉右支主干后,静脉注射5 mg ICG反染左半肝。在肝脏切除过程中,ICG荧光融合影像技术可帮助术者精准确定切除界面,正逐渐得到广泛应用[6]。对于本例患者,我们希望能在获得足够切缘的情况下尽量保留正常功能的肝脏。依靠术前3D重建智能门静脉分段的半肝切线并未与阻断右肝蒂后术中ICG染色的分界线完全重合,尤其右侧尾叶区域被ICG染色。我中心认为,ICG辅助显示的边界更接近残肝的功能性范围,因此术中完全沿ICG染色边界断肝,未刻意显露肝中静脉,并保留ICG染色的部分右侧尾叶,术后复查CT,见残肝体积进一步增大。断面与肝中静脉间的肝组织也有部分增生,可见其部分功能尚存。而术中ICG将右侧尾叶染色,原因可能是右侧尾叶的脉管来自于左肝系统。
综上所述,PVE联合TACE增加肝癌患者残肝体积是安全、有效的,二期手术采用ICG辅助,可更精准地保留功能性残肝,降低术后并发症发生率。然而其效果仍需要更大数量的研究与随访验证。

