氮掺杂超薄碳纳米片复合铂钌单原子合金催化剂的电化学析氢性能
范建玲,唐 灏,秦凤娟,许文静,谷鸿飞,裴加景,陈文星
(1.桂林师范高等专科学校物理与工程技术系,桂林 541199;2.北京理工大学材料学院,能源与催化中心,北京 100081;3.北京化工大学有机无机复合材料国家重点实验室,软物质科学与工程北京市先进创新中心,北京 100029)
人类文明的可持续发展战略迫使当前能源结构的转变与发展.氢能作为洁净绿色能源备受青睐,其具备来源丰富,燃烧释放热值高等优点[1~3].通过电化学技术制氢是获取氢能的一种有效途径,该方式具备易操作、绿色无污染和能耗低等优点[4~8].目前,贵金属铂基材料仍是电化学析氢反应(Hydrogen evolution reaction,HER)最优的催化剂,然而其地球储量稀少、价格昂贵,严重阻碍了此项技术的规模化发展,是氢能经济迅速发展道路上不可避免的障碍[9~11].因而降低贵金属铂的载量,是发展低成本、高效析氢催化剂的一个重要路线,进而促进电解水制氢效率,对我国能源结构加速演变影响深远.
贵金属Ru作为一种优秀的铂基析氢催化材料潜在替代品引起了广泛的关注,同时其价格也是铂族金属中最便宜的[11~13].但是单纯的金属Ru在酸碱性介质中的产氢活性有待于进一步提高[2,14,15].研究发现,通过合金化、磷化等手段优化金属钌表面的化学性质,可促使其制氢活性大幅度提升,同时又具有良好的催化成本竞争力[13,16].近年来,单原子材料因其最大化的原子利用率和独特的金属中心配位结构,在能源化工、生物医药合成和环境治理等催化领域成为了研究的热点[17~24].Tour等[19]在氮掺杂碳片上负载少量的钴单原子,其在酸性和碱性介质中均表现出良好的析氢性能.通过锚定少量钴单原子物种,优化了氮掺杂的碳片的本征活性,该单原子钴催化剂是首个应用于催化电解水制氢的单原子催化剂.虽然钴单原子成功应用于催化电解水产氢,但其过电势仍然有待降低.将金属铂的尺寸降低至原子层次,不仅可以有效减少铂的用量,降低成本,而且优化了金属铂的电子结构,是一种直接可行的有效措施.Bao等[25]将Pt单原子掺入硫化钼,触发了原本惰性材料的协同效应,展现出优异的电催化产氢性能.与纯的硫化钼相比,单原子Pt替代Mo原子嵌入硫化钼表层,其在10 mA/cm2电流密度下,过电位降低了60 mV,但仍需要进一步降低,并提升催化活性.因此,构建PtRu 单原子合金(Single-atom alloy,SAA)是开发高效电解水制氢催化材料的设想.
本文采用热解法在氮掺杂超薄碳纳米片上,制备出超小钌团簇颗粒复合铂单原子的铂钌单原子合金催化剂(PtRu SAA/NC).研究发现,该铂钌单原子合金催化剂表现出优异的电解水析氢活性和稳定性.相较于氮掺杂碳片和纯Ru团簇,PtRu单原子合金具备优化的电子结构,显示出最优的析氢性能;低载量的Pt单原子促使Ru团簇接近商业化20%Pt/C催化剂的产氢活性.
1 实验部分
1.1 试剂与仪器
氯铂酸(H2PtCl6,纯度>99%)购自国药集团化学试剂有限公司;乙酰丙酮钌(C15H21O6Ru,钌含量>25%)、二氰二胺(C2H4N4,纯度>99%)和1,3,5-均苯三甲酸(C9H6O6,纯度>99%)购自北京伊诺凯公司;无水乙醇(C2H5OH,纯度>99.5%)购自北京化工厂;氮气(N2,纯度>99.999%)购自林德气体公司.
Hitachi H-7700型透射电子显微镜(TEM,操作电压为100 kV)和ARM-200CF型配备双球差校正器的透射电子显微镜(AC-TEM,操作电压为200 kV),日本电子株式会社;Bruker D8-Advance 型粉末X射线衍射仪(PXRD,德国布鲁克公司,CuKα射线,λ=0.15418 nm);Thermo Fisher IRIS Intrepid Ⅱ型电感耦合等离子体原子发射光谱仪(ICP-AES,美国赛默飞世尔公司);HJY LabRAM Aramis型共聚焦显微拉曼光谱仪(Raman,法国H.J.Y公司);CHI760型电化学工作站(上海辰华公司).
1.2 实验过程
1.2.1 PtRu 单原子合金催化剂的制备 将10 mg H2PtCl6,50 mg C15H21O6Ru,1.2 g C2H4N4和0.12 g C9H6O6溶解在5 mL C2H5OH中,然后在80 ℃水浴中搅拌混合至干燥;将干燥后的粉末样品平铺于瓷舟中,并放入管式炉,在N2气氛下以升温速率5 ℃/min升温至800 ℃,热解2 h,即制得PtRu SAA/NC.
1.2.2 Ru 团簇催化剂的制备 将50 mg C15H21O6Ru,1.2 g C2H4N4和0.12 g C9H6O6溶解在5 mL C2H5OH中,然后在80 ℃水浴中搅拌混合至干燥;将干燥后的粉末样品平铺于瓷舟中并放入管式炉,在N2气氛下以升温速率5 ℃/min升温至800 ℃,热解2 h,即制得Ru团簇催化剂(RuNPs/NC).
1.2.3 氮掺杂碳材料的制备 将1.2 g C2H4N4和0.12g C9H6O6研磨混合均匀,然后平铺于瓷舟中并放入管式炉,在N2气氛下以升温速率5 ℃/min升温至800 ℃,热解2 h,即制得氮掺杂碳材料(N-GO).
1.2.4 电催化析氢性能测试 采用标准三电极体系进行测试,将玻碳(GC)电极作为工作电极、石墨碳棒作为对电极、饱和甘汞电极(SCE)作为参比电极[26,27].将4 mg催化剂超声分散在含有5%(质量分数)Nafion 的水/异丙醇(体积比1∶3)混合溶液中,超声2 h使混合液均匀分散.将催化剂混合液滴涂到GC电极上形成一层催化剂薄膜.HER 极化曲线在氢气饱和的0.5 mol/L 硫酸溶液中进行测试,扫描速率为5 mV/s,转盘电极转速为1600 r/min.获得曲线均需要进行内部电阻(iR)矫正,并换算为可逆氢电极(RHE)电势.电化学阻抗(EIS)实验:在10 kHz~1 Hz的交流频率范围内测量溶液电阻(R),其中电压扰动振幅为10 mV.
2 结果与讨论
2.1 PtRu单原子合金材料的表征
通过热解法制备了PtRu单原子合金材料,其中原子级分散的Pt单原子随机分散在Ru团簇表面.首先通过一步整体均匀混合金属前驱体与配体物种,再进行高温热解[图1(A)].图1(B)是PtRu单原子合金材料的TEM照片,可见,超小的PtRu单原子合金物种均匀分散在氮掺杂超薄碳纳米片上,颗粒大小均匀,没有明显的团聚现象.X射线能谱(EDS)面积分布扫描图显示了Pt,Ru,N和C 4种元素在氮掺杂超薄碳纳米片上的分散状态,其中Pt单原子主要分布在Ru团簇表面[图1(C)~(F)].
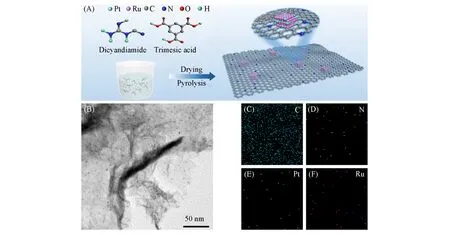
Fig.1 Illustration of the formation of PtRu SAA/NC(A),TEM image(B) and EDS element mapping images(C—F)of PtRu SAA/NC
进一步采用PXRD 和拉曼光谱对合成样品进行表征[图2(A)和(B)].由图2(A)可见,PtRu SAA/NC 在15°~45°范围内有两个加宽的峰,分别归属于石墨碳的(002)和(010)晶面.由PXRD 结果可知,氮掺杂碳载体的结晶度很差,并且PtRu单原子合金材料与纯Ru团簇催化剂的衍射峰结果类似.通过拉曼光谱表征,发现在样品中只检测到1338.6 cm−1(D 带)和1613.9 cm−1(G 带)两个碳的特征峰[图2(B)].D带来源于碳材料本身的缺陷,代表结构的不规则性,而G带来源于碳材料中碳原子sp2杂化的面内伸缩振动.从拉曼光谱表征计算出的D 带/G 带的强度比(ID/IG)为1.09,表明碳基体材料在800 ℃热解发生了高度石墨化,有利于析氢反应过程中电子的移动,促进氢质子的还原,并能进一步提高析氢反应性能.

Fig.2 XRD patterns(A)of the PtRu SAA/NC and Ru NPs/NC and Raman spectra(B)of PtRu SAA/NC
为了验证样品中C 和N 的电子结构和化学价态,进行了软X 射线吸收近边结构(XANES)光谱表征.PtRu 单原子合金材料中C 的K 边谱中有3 个明显的峰,285.6 eV(峰A)、292.5 eV(峰B)和298.3 eV(峰C),分别对应于C1s内核电子跃迁至π*(C=C),π*(C—N)和σ*(C—C)反键轨道[图3(A)].此外,PtRu单原子合金材料中N 的电子态也可通过N的K边软X射线吸收近边谱来检测[图3(B)].在N的K边谱中,有3个峰分别属于吡啶氮(峰A)、吡咯氮(峰B)和石墨氮(峰C).
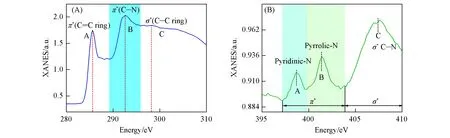
Fig.3 C K⁃edge(A)and N K⁃edge(B)XANES spectra of PtRu SAA/NC
扩展X射线吸收精细结构谱(EXAFS)和XANES技术已被广泛用于表征金属纳米粒子或团簇的性质.为了在原子水平上进一步揭示所制备的PtRu 单原子合金材料的结构,进行了X 射线吸收光谱(XAS)测量.从XANES表征中能够大致了解样品中Pt和Ru物种的平均价态[28][图4(A)和图5(A)].通过比较PtRu SAA/NC与Pt foil,PtO2参考样的Pt L3-edge的XANES光谱,可见,PtRu SAA/NC的吸收边位于Pt foil 和PtO2之间,表明样品中Pt 的化学价态介于两者之间,即Pt 的氧化态介于0~+4 价之间.同理,通过比较PtRu SAA/NC 与Ru foil,RuO2参考样的Ru K-edge的XANES光谱,可知样品中Ru的化学价态低于RuO2,并且与Ru foil 接近,即Ru 的氧化态接近0 价.傅里叶变换(FT)被用于提取EXAFS 光谱的有效数据并对其进行解释[29].在PtRu SAA/NC 的Pt L3-edge 的FT-EXAFS 图像中,没有观察到Pt—Pt 散射峰,排除了团聚Pt 原子的存在.同时,发现存在Pt—O、Pt—Ru 信号[图4(B)].而在PtRu SAA/NC的Ru K-edge的FT-EXAFS中,观察到了Ru—Ru信号[图5(B)].根据这些结果,可以确定Pt物种在Ru团簇表面的原子分散性.
由于k和R空间的强大分辨率,采用Pt L3-edge 和Ru K-edge 小波变换(WT)-EXAFS 探索了PtRu SAA/NC的原子结构.WT-EXAFS也是进一步确认Pt单原子结构的有效方法[30,31].PtRu SAA/NC的小波变换在55 和89 nm−1处出现最强峰,分别与Pt—O 和Pt—Ru 的贡献有关.此外,与Pt foil 小波变换相比,Pt—Pt配位散射相关的峰没有出现[图4(C)],这进一步证实了Pt单原子的存在.与钌箔和RuO2相比,PtRu SAA/NC的WT-EXAFS图中在100 nm−1处出现最强峰,这可以归因于Ru—Ru键[图5(C)].经过R空间拟合,结构模型图也被展现在图5(D)插图中.

Fig.4 Pt L3⁃edge XANES(A)and Pt L3⁃edge FT⁃EXAFS spectra(B)of Pt foil,PtO2,PtRu SAA/NC,WT⁃EXAFS of the Pt foil(C1),PtO2(C2) and PtRu SAA/NC(C3), R space(D) and q space(E)FT⁃EXAFS fitting curves of PtRu SAA/NC
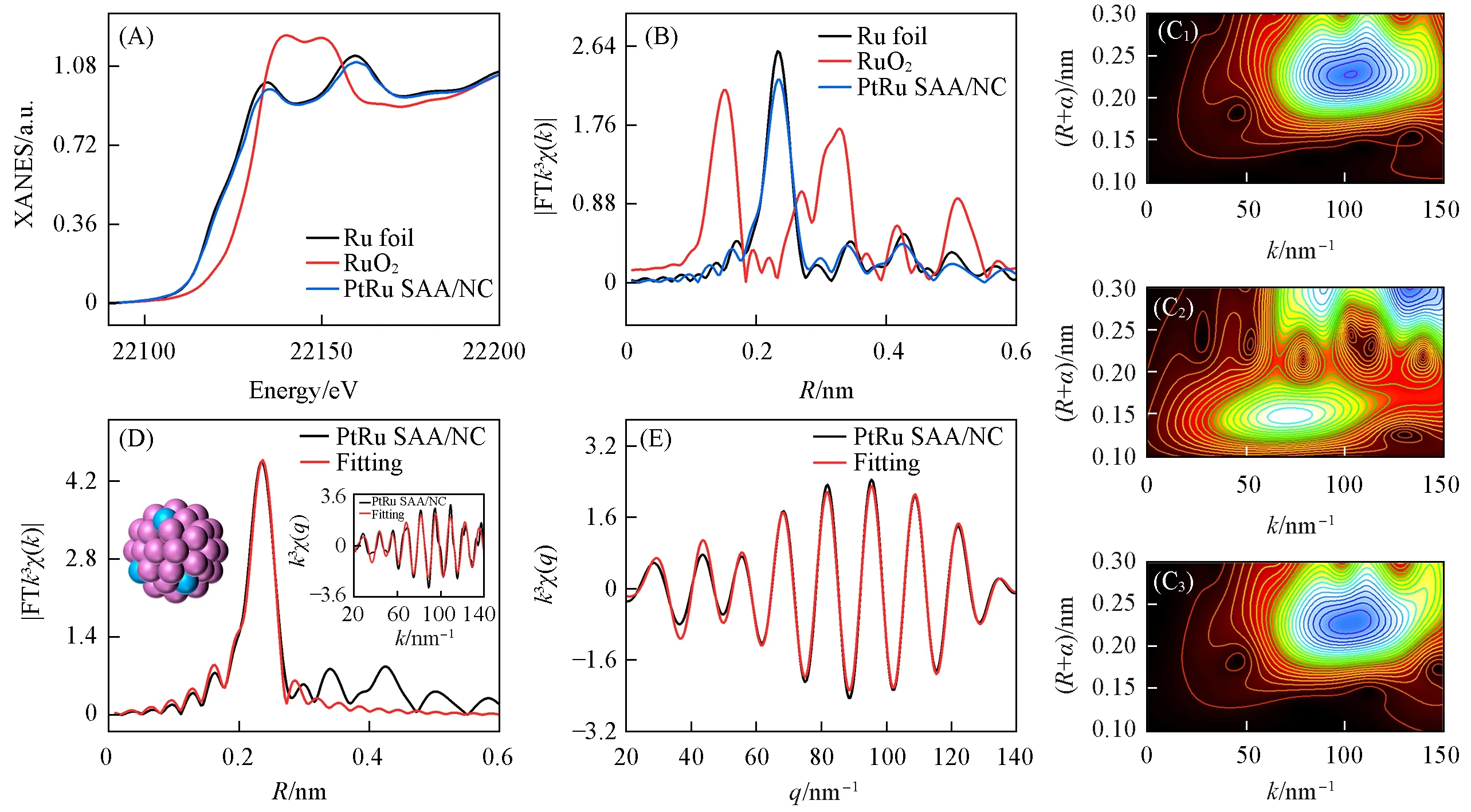
Fig.5 Ru K⁃edge XANES(A)and Ru K⁃edge FT⁃EXAFS spectra(B)of Ru foil,RuO2 and PtRu SAA/NC,WT⁃EXAFS of the Ru foil(C1),RuO2(C2) and PtRu SAA/NC(C3), R space(D)and q space(E)FT⁃EXAFS fitting curves of PtRu SAA/NC
对PtRu SAA/NC 进行了最小二乘法EXAFS 拟合[图4(D)和(E),图5(E)],定量提取了Pt L3-edge和Ru K-edge的结构参数,并给出了拟合结果通过定量拟合得到的结构参数(表1).结果表明,拟合曲线与实验谱吻合较好.根据EXAFS 拟合结果,中心Pt 原子的第一壳层由O 原子和Ru 原子配位,平均键长分别为0.202 和0.273 nm,同时Ru—Ru 键平均键长为0.267 nm.拟合结果也说明了原子级分散的Pt单原子随机分散在Ru团簇表面.
Table 1 Structural parameters extracted from the Pt L3-edge and Ru K-edge EXAFS fitting(=0.85)*
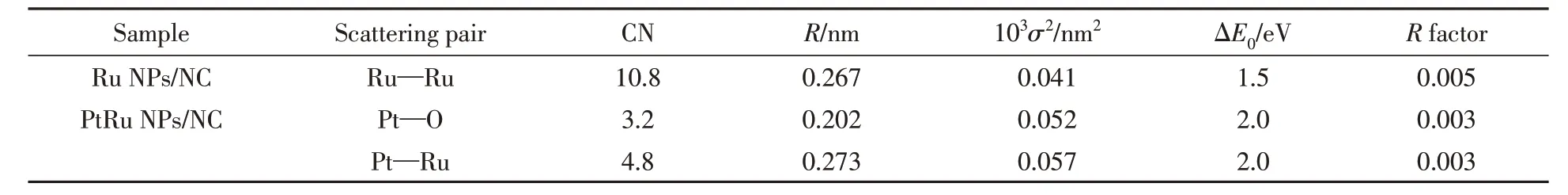
Table 1 Structural parameters extracted from the Pt L3-edge and Ru K-edge EXAFS fitting(=0.85)*
* is the amplitude reduction factor;CN is the coordination number;R is the interatomic distance(the bond length between central atoms and surrounding coordination atoms);σ2 is the Debye-Waller factor(a measure of thermal and static disorder in absorber-scatterer distances);ΔE0 is the edge-energy shift(the difference between the zero kinetic energy value of the sample and the theoretical model);R factor is used to value the goodness of the fitting.
2.2 电解水制氢性能
为了分析引入Ru物种晶格中的少量Pt单原子对Ru电子结构的影响,以电化学析氢为模型反应,评价了PtRu 单原子合金材料、纯Ru 团簇、氮掺杂碳片以及商业Pt/C 催化剂的产氢活性.采用标准三电极体系,在0.5 mol/L 硫酸介质中进行了测试,结果如图6和图7所示.

Fig.6 Polarization curves with a scan rate of 5 mV/s(A)and corresponding Tafel plots(B)
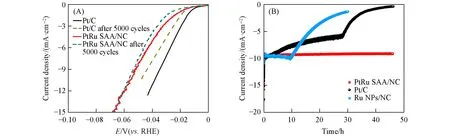
Fig.7 Stability curves(A)and corresponding current density⁃time curves(B)of Pt/C and PtRu SAA/NC before and after 5000 cycles
图6(A)为所有催化剂的线性扫描伏安(LSV)曲线图.可见,纯氮掺杂碳片几乎没有电化学产氢活性.当负载有Ru团簇物种时,电解水产氢活性大幅度提升.相比于Ru团簇,引入Pt单原子形成PtRu单原子合金催化剂的产氢活性再次大幅度提升.Ru NPs/NC,PtRu SAA/NC和商业Pt/C催化剂的起始电势分别为200,8,和5 mV,说明引入Pt 单原子改变了纯Ru 催化的产氢本征活性.Ru NPs/NC,PtRu SAA/NC和商业Pt/C催化剂在10 mA/cm2电流密度下,过电位分别为104,54和37 mV;在相同的电流密度条件下,PtRu单原子合金催化剂比Ru团簇的过电位减小了50 mV,甚至接近商业Pt/C催化剂的反应活性.这是因为Pt单原子的引入,加速了PtRu单原子合金位点与氮掺杂超薄碳纳米片基质间的电荷传导,从而降低了HER过电位,充分体现出Pt单原子的催化优势.图6(B)给出了Ru NPs/NC,PtRu SAA/NC和商业Pt/C催化剂的Tafel曲线,可见,它们的Tafel斜率分别为56,43和39 mV/dec.
表2 列出了PtRu SAA/NC 催化剂与文献报道的其它Ru 基催化剂活性的比较结果,可看到PtRu SAA/NC具有优异的析氢反应活性[14,31~34].表明Pt单原子的引入不仅使Pt物种的原子利用效率最大化,而且协同提高了Ru团簇表面的电荷传递特性,增强了氢离子的迁移和析出速率,使PtRu SAA/NC催化剂的整体产氢活性与商业Pt/C接近.
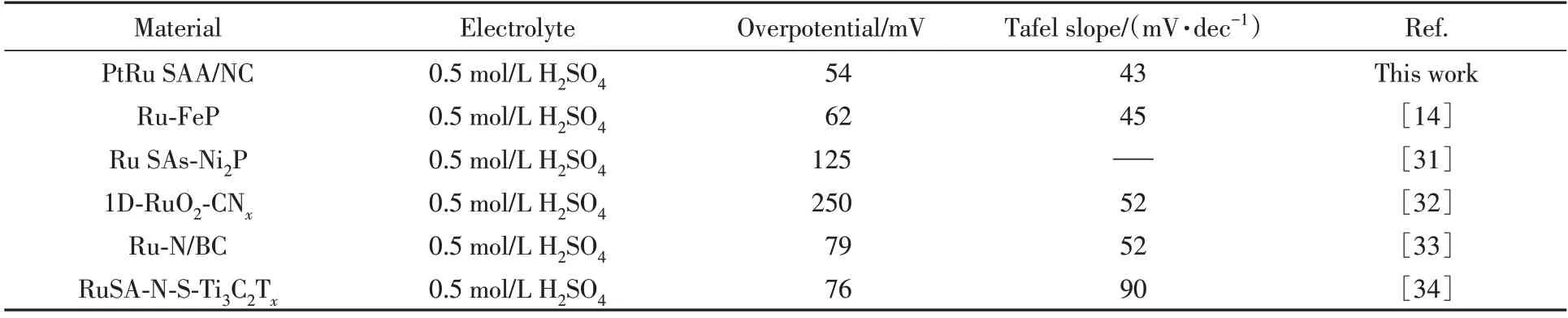
Table 2 Summary of various Ru based catalysts in acidic condition at 10 mA/cm2
为了评估PtRu SAA/NC催化剂长周期的实用性,进一步测试其与商业Pt/C催化剂、纯Ru团簇的稳定性.图7(A)为PtRu SAA/NC 和商业Pt/C 催化剂的初始LSV 曲线和经历5000 次循环后的LSV 曲线.从图中看出,经历5000次循环后,商业Pt/C催化剂的电流密度大幅下降,而PtRu SAA/NC样品仅表现为起始电势的小幅度增加;在大的电流密度下与初始LSV 曲线保持吻合.图7(B)为PtRu SAA/NC、商业Pt/C 催化剂和纯Ru 团簇在固定电势下的电流随时间变化曲线.可见,随着电解时间逐渐增加至30 h,纯Ru团簇的电流密度明显降低乃至失活;电解时间增至50 h后,商业Pt/C催化剂的电流密度也明显降低甚至失活;而PtRu SAA/NC样品的电流密度始终保持稳定,充分说明了PtRu单原子合金在酸性介质中电解水制氢过程的稳定性.这主要归因于Pt单原子的引入,形成了稳定的Pt—Ru键,从而形成PtRu单原子合金,优化了Ru团簇的结构性质,极大地增强了位点的本征活性,体现出其商业发展的应用潜力.
3 结 论
基于一步热解法制备了PtRu 单原子合金催化剂,与Ru NPs/NC 和NC 样品对比,其拥有最优的电解水产氢活性;PtRu SAA/NC 样品在10 mA/cm2电流密度下的过电位仅为54 mV,其Tafel 斜率达到43 mV/dec,并接近商业20%Pt/C催化剂的反应活性;其具备比商业Pt/C催化剂更优异的HER稳定性.Pt单原子的引入改变了Ru团簇物种表面的电荷传递特性,增强了氢离子的迁移和析出速率,还可使Pt原子位点的利用效率最大化,降低了催化成本.这种高效能原子层次的单原子合金催化剂的设计,为清洁能源结构转换开发提供了新的研究方向.

