Morphogo骨髓细胞形态分析系统对正常、感染及多发性骨髓瘤骨髓涂片辅助诊断的效率评价
齐超,钟玉虹,王小粉,付鑫焱,乔赛,金红,杨肃文,张钧(1.浙江大学医学院附属邵逸夫医院检验科,杭州 10000;2.浙江省医学精准检验与监测研究重点实验室,杭州 10000;.凯德诺医疗器械(武汉)有限公司医学事务部,武汉 40000)
细胞形态学(morphology)、免疫学(immunology)、细胞遗传学(cytogenetics)、分子生物学(molecular biology)相结合的MICM 分型方案是目前全世界通用的血液系统疾病诊断与分类标准[1]。其中,骨髓涂片人工显微镜检查作为形态学评估的金标准,是血液系统疾病诊断和预后评估不可缺少的重要环节。然而,人工显微镜检查既耗时又繁琐,并且需要经过专业培训和具有一定经验积累的医生来完成[2]。这种人工显微镜检查项目相比于自动化的检验项目而言,其效率显然不能满足临床对患者诊疗和评估的需求。全玻片成像(WSI)、人工智能(AI)、计算机深度学习算法、聚焦算法等新技术已被应用于骨髓细胞形态分析仪的研发当中,但由于骨髓标本涉及转移性肿瘤细胞在内的多种形态异常细胞,其复杂性和特殊性使得骨髓细胞形态分析仪的普及应用仍面临很大的挑战[3-6]。目前,国际上对于骨髓涂片检查这一项目,仍旧以人工显微镜检查为主要手段。
Morphogo骨髓细胞形态分析系统集成扫描硬件和基于计算机智能学习的软件系统,能自动扫描骨髓涂片,随后生成骨髓涂片的全数字图像,根据内部细胞识别算法对有核细胞进行计数和预分类,随后由形态学医生对仪器预分类结果进行审核,最后出具诊断性报告[6]。本研究采用仪器预分类辅助下人工审核、传统人工显微镜检查这2种方式对正常、感染及多发性骨髓瘤骨髓涂片进行分析与诊断,探讨Morphogo能否辅助提高诊断效率。
1 材料与方法
1.1 标本来源 收集2020年1月至2021年12月在我院行骨髓穿刺患者的骨髓涂片90 例,其中正常、感染、多发性骨髓瘤各30例,采用瑞氏-吉姆萨染色对涂片进行染色。纳入标准:(1)患者临床资料(基本资料、主诉、既往史、现病史、相关辅助检查、临床诊断等)完整;(2)骨髓涂片取材良好,骨髓小粒丰富;(3)骨髓涂片制片良好,涂片头、体、尾分明。排除标准:(1)排除既往血液系统疾病史者(包括良性、恶性血液系统疾病患者及治愈者);(2)感染组需排除骨髓穿刺前进行抗感染治疗者;(3)排除外周血部分稀释及外周血稀释者;(4)排除骨髓穿刺前使用过细胞毒性药物者。收集上述90例患者的临床资料,正常组年龄(52.0±17.7)岁,男性20 例,女性10 例;感染组年龄(56.5±16.7)岁,男性12例,女性18例;多发性骨髓瘤组(67.8±9.3)岁,男性11例,女性19例。
1.2 仪器与试剂 Morphogo-MG-G0R-BA1-027 骨髓细胞形态学分析系统(杭州智微信息科技公司);瑞氏-吉姆萨染液(贝索公司);Nikon ECLIPSE 50i显微镜(日本尼康公司)
1.3 对骨髓有核细胞进行计数、预分类及人工审核 不参与骨髓涂片阅片和审核者对90 例标本进行随机编号(1~90 号),并且记录编号对应的患者信息。标本信息对于仪器操作者和负责阅片、审核者双盲。阅片、审核者具有3年以上细胞形态学分析经验,定期参与实验室内部形态学培训,并且通过ISO15189及实验室内部的细胞形态学考核。
将染色、晾干、编号后的骨髓涂片放入仪器中进行全片扫描,仪器将在高倍镜(40×)下计数全片巨核细胞数量,在油镜(100×)下分类25 个巨核细胞及200 个有核细胞,仪器将对粒细胞系统(粒系)、红细胞系统(红系)、淋巴细胞系统(淋系)、单核细胞系统(单核系)、浆细胞系统(浆系)、巨核细胞系统(巨核系)的细胞进行预分类。对仪器预分类结果中的细胞图像进行审核,对预分类错误的细胞进行纠正。基于上述预分类及纠正后的结果,在显微镜下对骨髓涂片进行复核,给出诊断报告,记录人工审核、复核及诊断过程的总耗时T1。
1.4 人工显微镜检查 由该阅片、审核者对上述骨髓涂片进行人工显微镜检查,在低倍镜下(10×)预览全片并计数全片巨核细胞数量,在高倍镜下评估有核细胞增生程度,在油镜下分类25 个巨核细胞及200个有核细胞,分类部位为体尾交界细胞形态平展良好的区域,最后综合全片情况给出诊断报告,记录全过程的总耗时T2。
1.5 统计学分析 用SPSS 17.0 统计软件进行。由上述编号人员将仪器预分类的原始结果、人工审核后的纠正结果及诊断意见导出,将数据整合到对应的患者信息中,以人工纠正后的结果作为有核细胞分类的“金标准”来评估仪器预分类结果的准确度。以患者临床诊断为“金标准”,分析阅片、审核者在仪器辅助下给出的诊断结果及人工显微镜检查后给出的诊断结果与“金标准”之间的符合率。T1、T2数据用中位数(第25 百分位数,第75 百分位数)表示,用Shapiro-Wilk 进行正态性检验,偏态分布采用Wilcoxon signed-rank 检验来分析差异是否有统计学意义。以P <0.05 为差异有统计学意义。
2 结果
2.1 仪器预分类准确度 见表1。Morphogo 对于正常组和感染组有核细胞预分类结果的总准确度分别为85.7%和84.4%,对于多发性骨髓瘤组有核细胞预分类结果的总准确度为63.0%。

表1 仪器预分类结果准确度(%)
2.2 诊断意见符合率 形态学医生在仪器辅助下的诊断意见、人工显微镜检查后的诊断意见与临床诊断“金标准”之间的符合率均为100%。
2.3 T1与T2比对 见表2。对于正常组、感染组骨髓涂片的分片和诊断,仪器辅助下耗时T1 较人工显微镜镜检耗时T2 短,同组T1、T2 间差异有统计学意义。而多发性骨髓瘤组T1 与T2 之间差异无统计学意义。
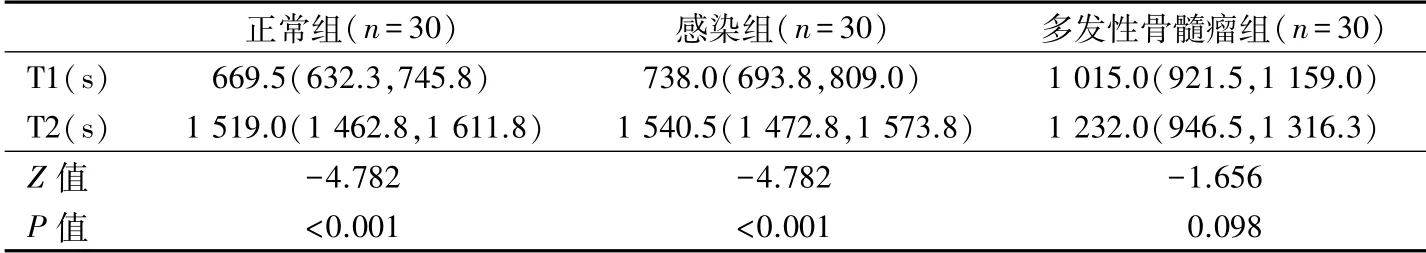
表2 各组T1、T2耗时比较
3 讨论
对于正常和感染患者的骨髓涂片,Morphogo是一种有效的辅助诊断工具。而对于多发性骨髓瘤这类合并明显形态学改变的疾病,建议以仪器预分类结果为示警,及时进行人工显微镜镜检,第一时间为临床医生和患者出具诊断报告。
多发性骨髓瘤患者的浆细胞本质上是异常的单克隆细胞株,其免疫表型及细胞形态均与正常浆细胞存在差异。尤其是恶性程度较高的骨髓瘤细胞,细胞形态存在明显异质性,呈聚集性分布。此外,部分患者会同时存在多种异常浆细胞[7]。目前,细胞识别算法不能完全准确识别这些形态异常的浆细胞和骨髓瘤细胞。其次,由于免疫球蛋白的异常会增加细胞间的黏连性,导致细胞舒展欠佳,进而影响人工显微镜镜检和仪器预分类[8]。这就导致了人工审核预分类结果耗时较久,仪器辅助下的诊断效率较人工显微镜镜检无明显提高。
在后续工作中,需要进一步扩大样本库中合并明显形态学异常的病种类型和数量,以完善和升级骨髓细胞识别算法。同时,由于单核细胞和浆细胞在正常骨髓有核细胞组成中占比较低,也需进一步扩大样本量来降低仪器预分类准确度结果的偏倚。此外,Morphogo清晰的全数字化图片可以永久性保存骨髓涂片的原始数据,解决了目前临床上骨髓涂片标本保存10年所需的空间占用问题。中小医疗机构可以通过仪器采集的细胞全数字化图片实现远程会诊,为分级诊疗提供新途径,具有很好的临床应用前景。

