心肌肌钙蛋白Ⅰ检测方法的性能评价*
刘春燕,邓朝晖,宋颖博,梁学立,葛若卿,张新(新疆生产建设兵团医院&石河子大学医学院第二附属医院检验科,乌鲁木齐 830002)
心肌肌钙蛋白(cardiac troponin,cTn)是心肌损伤的特异性标志物[1]。2020 年欧洲心脏病学会发布的指南中突出了高敏心肌肌钙蛋白(high-sensitive cardiac troponin,hs-cTn)在非ST段抬高型急性冠脉综合征(non-ST-segment elevation acute coronary syndrome,NSTEACS)诊断中的作用,标志着急性心肌梗死(aeute myocardial inraretion,AMI)的诊断标志物进入高灵敏度检测的时代[2]。hs-cTn 是指用高灵敏度的方法测定cTn,普遍认为高灵敏度方法检测cTn的能力要满足健康人群中测量cTn 浓度在低于第99 百分位值时的检出率至少达50%以上,且健康人群参考区间上限第99 百分位值的变异系数(coefficient of variation,CV)≤10%[3]。但目前国内外临床诊疗中应用众多不同厂家的hs-cTn试剂盒,hs-cTn检测方法学尚未实现标准化,检测灵敏度及低值检测稳定性方面良莠不齐,需要引起高度重视[4-5]。因此,各实验室在选择不同厂家的hs-cTn试剂时,应评估检测试剂的分析性能。本研究对雅培公司的高敏心肌肌钙蛋白I(high-sensitive cardiac troponin I,hs-cTnI)进行分析性能评价及表观健康人群生物学变异的评估,且建立了本实验室hs-cTnI第99百分位值参考上限(99thURL)。
1 对象与方法
1.1 研究对象 表观健康人组:纳入体检中心表观健康个体350例,男性194例,中位年龄39.5岁,女性156例,中位年龄43.0 岁。纳入标准:(1)无心血管疾病、肺部疾病、肾病、糖尿病、高血压等,半年内无心脏手术,无急性炎症、剧烈运动;(2)心电图检查无明显异常;(3)年龄≥18 岁。排除标准:(1)患有心脏瓣膜病、房颤、心肌炎、心包炎及病窦综合征等心源性疾病者;(2)拒绝抽血行hs-cTnI检验及资料不全的患者。其中,244 例表观健康个体的血清标本用于本实验室hs-cTnI 的99thURL 建立,22例用于评估hs-cTnI 长期和短期生物学变异,84例用于高浓度血清样本倍比稀释。AMI 组:纳入2020年3月至9月在新疆生产建设兵团医院急诊科或心内科诊断为AMI 的住院患者共60 例,中位年龄63.0岁,男性44例,女性16例,AMI患者的确诊符合2015年ESC的诊断标准[6]。本研究经兵团医院医学伦理委员会批准(批准文号:20200101),研究对象均自愿参加本研究并签署知情同意书。
1.2 标本采集与处理 采血前AMI患者和表观健康个体需空腹8 h,采集坐位肘前静脉血,注入5 mL带分离胶的促凝管,3 000×g 离心10 min 后,分别配制新鲜混合血清。采用ARCHITECT 原装配套hs-cTnI稀释液倍比稀释各项目低浓度新鲜混合血清,用于hs-cTnI分析性能评价。
1.3 主要仪器和试剂 雅培公司ARCHITECT i2000SR全自动免疫分析仪及原装配套hs-cTnI 检测试剂盒(批号:27305UD01)、校准品(批号:26305UD01)及2个水平质控品(批号:28499UD01)。
1.4 空白限(LoB) 用ARCHITECT 原装配套hs-cTnI稀释液作为空白样品,依据EP17-A2 文件[7]要求:每个空白样品每天检测2 批,间隔时间大于2 h,每批重复检测6次,连续检测5 d,获得60个检测结果。依据国际标准化组织(International Organization for Standardization,ISO)推荐在规定水平的Ⅰ类错误下,设定α =5%,采用非参数检验将空白样品的检测结果按从小到大排列,第95 百分位数即为LoB[8]。
1.5 检出限(LoD) 采用表观健康人群新鲜混合血清倍比稀释成8 个低浓度样品,理论浓度分别为:0.1 ng/L、0.4 ng/L、0.7 ng/L、1.0 ng/L、1.3 ng/L、1.6 ng/L、1.9 ng/L 及2.2 ng/L。每个浓度样品每天各检测2 批,每批重复检测2 次(取均值),连续检测5 d,获得80个检测结果。因低浓度样品常呈非正态分布,因此依据ISO 的要求,采用非参数检验,在规定Ⅱ类错误水平β =5%的条件下,确定LoD。则LoD =LoB+DS,β(DS,β是低浓度样品测定值的中位数和第5百分位数的间距)[7-8]。
1.6 定量检出限(LoQ) 依据临床要求和室间质量评价的允许误差[7],设定本实验室hs-cTnI 的总误差目标为15%~20%,在不考虑分析偏差的条件下,总误差=2CV,如果低浓度样品的CV≤1/2总误差,则LoQ=LoD[7-8]。
1.7 功能灵敏度 参照文献[9],将hs-cTnI 高值血清混合样品(H:100.0 ng/L)4 mL 与表观健康人混合血清(L)40 mL,以1H ∶9L 将高值样品稀释至10.0 ng/L,检测3次取均值(M)。将M作为原液,K为原装配套hs-cTnI 稀释液,倍比稀释10 个浓度,浓度范围为1.0 ~10.0 ng/L。以10M ∶0K、9M ∶1K、8M ∶2K、7M ∶3K、6M ∶4K、5M ∶5K、4M ∶6K、3M ∶7K、2M ∶8K及1M ∶9K混合各1.0 mL,最终理论浓度(由高到低)分别为10.0 ng/L、9.0 ng/L、8.0 ng/L、7.0 ng/L、6.0 ng/L、5.0 ng/L、4.0 ng/L、3.0 ng/L、2.0 ng/L 及1.0 ng/L。每天检测上述系列浓度血清,连续检测10 d,计算天间CV 值,以hs-cTnI系列浓度为横坐标、CV为纵坐标作图,计算CV=10%时hs-cTnI 浓度值,设为该方法的功能灵敏度。
1.8 精密度 依据WS/T 492—2016 行业标准[10],用表观健康人群新鲜混合血清倍比稀释hs-cTnI高值样品,配制浓度分别为20.0 ng/L(L)、190.0 ng/L(M)及15 100.0 ng/L(H)。每天测定1个分析批,每批3个浓度水平,每批重复3 次,连续检测5 d。计算批内、批间精密度,与厂商提供的性能参数相比较,判断其符合性。
1.9 线性范围 将hs-cTnI 高值混合血清样品(H:44 924 ng/L)和 低 值 混 合 血 清 样 品(L:19.0 ng/L),以5H ∶0L、4H ∶1L、3H ∶2L、2H ∶3L、1H ∶4L、0.7H ∶4.3L、0.3H ∶4.6L、0.1H ∶4.9L及0H ∶5L混合各1.0 mL,最终理论浓度(由高到低)分别为45 000.0 ng/L、36 000.0 ng/L、27 000.0 ng/L、18 010.0 ng/L、9 000.0 ng/L、6 310.0 ng/L、3 610.0 ng/L、920.0 ng/L 及19.0 ng/L。每个样品重复测量3次,取均值。将实测值与预期值进行比较,以预期浓度值为横轴,实际测得浓度值均值为纵轴作线性回归图,计算回归方程:Y =aX+b 与相关系数(r)。决定系数(R2)≥0.95为符合要求。
1.10 生物学变异 短期生物学变异:采集22例表观健康人1 d内连续5个时间点(每隔2 h 1次)的血液标本,将血清分装后于-80 ℃保存。长期生物学变异:采集22名表观健康人连续6 周、每周同一时间点的血液标本,将血清分装后置于-80 ℃保存。上述每个标本重复检测2 次,取均值,分别计算个体内变异(CVi)、个体间变异(CVg)、总变异(CVt)及天内和天间个体指数。
1.11 表观健康人群hs-cTnI的99thURL建立 收集本院体检中心244例表观健康人的血清样品,依据C28-A3 文件[11],按性别分为男性组和女性组(每组人数≥120 人),确定2 组表观健康人的99thURL。
1.12 统计学分析 采用SPSS 17.0 统计软件进行。正态分布的计量资料以均数±标准差表示,非正态分布的计量资料用中位数表示。非正态分布的计量资料的比较采用秩和检验,男、女性两独立样本间的比较采用Mann-Whitney U 检验。率的比较采用χ2检验。采用回归分析中的线性相关进行相关性分析。以P<0.05为差异有统计学意义。
2 结果
2.1 LoB LoB =[重复检测次数×(95/100)+0.5]=57.5位置上的结果,即第57 和58 个检测值的均数。将60个空白样本检测值按从小到大排序后,第57和58 个检测值分别为0.4 和0.5 ng/L,见表1。故LoB为0.45 ng/L。
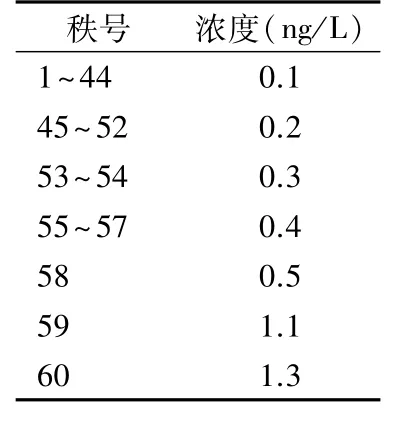
表1 60个空白检测值由小到大排序结果
2.2 LoD LoD=LoB+DS,β,其中DS,β为第40.5百分位数和第4.5 百分位数的间距。hs-cTnI 低浓度样本测定结果见表2。因此,LoD为1.45 ng/L。
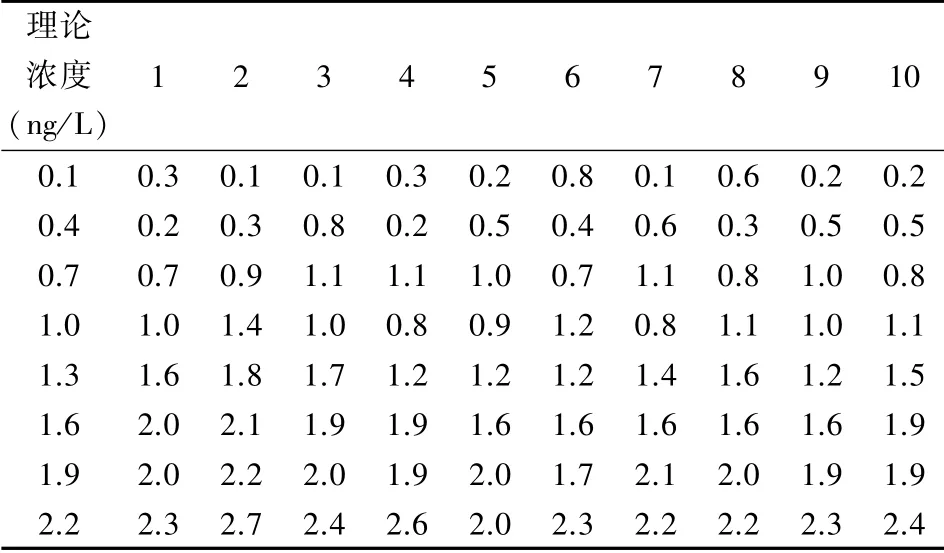
表2 hs-cTnI低浓度样本测定结果
2.3 LoQ 设定hs-cTnI 的总误差目标为15%~20%,在不考虑分析偏差的条件下,允许总误差(TEa)=2CV,即CV =1/2TEa。hs-cTnI 浓度在1.90 ng/L时日间CV值为6.6%(<7.5%),符合质量目标要求。因此,LoQ=1.90 ng/L,见表3。

表3 系列低浓度hs-cTnI的日间CV(%)
2.4 功能灵敏度 依据hs-cTnI 测定CV≤10%的要求,CV=10%时对应的浓度值为1.93 ng/L,因此该方法的功能灵敏度为1.93 ng/L,见图1。

图1 hs-cTnI系列低浓度CV图
2.5 精密度 hs-cTnI批内及批间不精密度结果以变异系数(CV)表示,均<10.0%,符合质量要求,见表4。

表4 hs-cTnI检测不精密度(%)
2.6 线性范围 在19~45 000 ng/L范围内,hs-cTnI线性方程为Y =1.030 2X-42.179,R2=0.997 7,临床可报告范围满足厂商说明书要求,见图2。
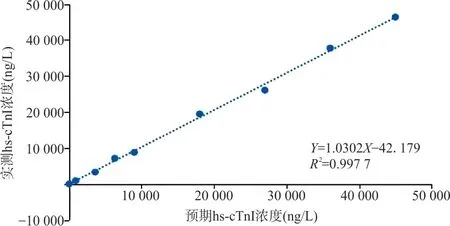
图2 hs-cTnI的线性范围回归曲线
2.7 生物学变异 22名表观健康人的短期生物学变异及长期生物学变异见表5。

表5 hs-cTnI短期和长期生物学变异
2.8 表观健康人群hs-cTnI 的99thURL 建立 hs-cTnI的99thURL 为8.25 ng/L,男性和女性分别为9.52 ng/L和8.28 ng/L,女性组低于男性组(Z =-2.616,P<0.05),见表6。不同性别组hs-cTnI 浓度显著低于厂商说明书参考区间,见图3。

表6 表观健康人群hs-cTnI检测结果及99th URL

图3 不同性别及年龄hs-cTnI浓度分布
3 讨论
cTn 的临床应用从根本上改善了ACS 患者的诊断、预后和治疗,其对AMI 的诊断被国际指南列为Ⅰ级a类推荐[12]。随着cTn 检测灵敏度的不断提高,不同cTn检测试剂盒生产商选用不同的捕获抗体和检测抗体、不同的发光系统及检测体系,因此各品牌检测试剂盒间的检测值存在较大差异,使其在AMI患者早期诊断方面的安全性和有效性受到了挑战和质疑[13-14]。本研究依据美国临床和实验室标准协会(CLSI)EP17-A2 文件及国内行业标准的相关要求,对基于化学发光微粒子免疫检测法的试剂盒从LoB、LoD、LoQ、功能灵敏度、精密度、线性范围等方面对hs-cTnI 检测试剂盒进行了验证,结果显示该试剂盒检测效能均符合临床需求。
本研究LoB 结果为0.45 ng/L,低于厂商说明书(1.0 ng/L),LoD为1.45 ng/L,LoQ为1.90 ng/L,验证了试剂说明书声明的性能。为避免基质效应的干扰,本研究采用新鲜血清倍比稀释hs-cTnI 系列低浓度样品,评估该检测系统的功能灵敏度[9],结果显示CV =10%的最低浓度值为1.93 ng/L,临床医生可放心使用浓度高于1.93 ng/L 的hs-cTnI结果。hs-cTnI精密度结果显示,低、中及高浓度样品的批内和批间CV 均<10%,除低浓度样品批间CV为7.60%以外,其余均满足厂商说明书hs-cTnI第99百分位数的精密度(CV =4.0%)。其中,低浓度样品CV 值偏高,可能是由于本实验采用新鲜混合血清倍比稀释hs-cTnI 系列低浓度样本,样品保存时间及条件均会影响hs-cTnI 检测结果的稳定性[15],也可能与新鲜血清样品反复冻融有关[16]。本研究短期和长期的CVi和CVg均大于宋凌燕等[9]对hs-cTnT生物学变异的试验结果,这可能与使用的分析系统、试验的不精密度及两者检测方法的检测低限数量级不同等原因有关。个体化指数有效地反映了个体检测结果波动的意义,临床对于AMI 疾病的诊断及治疗判断,需要参考个体化指数,合理选择治疗方案,为个体化治疗提供有价值的实验室数据。
本研究建立的hs-cTnI总体人群的99thURL为8.25 ng/L,男性为9.52 ng/L,女性为8.28 ng/L,所得结果与已报道的北京地区使用相同试剂盒、相同标本类型的研究结果大体一致[17],但显著低于厂商说明书(男性34.2 ng/L,女性15.6 ng/L)和国内其他地区[18],这与hs-cTnI 存在年龄、性别及种族差异相关[19-21],也可能与表观健康人群入选标准存在差异相关[22]。而表观健康男性人群的hs-cTnI值高于女性[23],本研究结果亦印证了这点。本研究纳入hs-cTnI的99thURL 研究样本偏小,结果存在一定的局限性,Apple等[24]提议用于建立hs-cTnI的99thURL健康个体数应大幅增加。因而,本实验室将进一步建立多中心、大样本的适用于新疆地区表观健康人群hs-cTnI 的99thURL,为本地区成年人AMI疾病的诊断及治疗提供实验室基础。
总之,本研究对雅培公司i2000SR全自动免疫分析仪检测的hs-cTnI试剂盒进行了分析性能评价及表观健康人群生物学变异的评估,为临床提供准确、可靠的hs-cTnI检测结果,并初步建立本实验室hs-cTnI的99thURL,因样本量偏小,存在一定的局限性,尚需今后进一步探讨。

