探讨乳腺影像报告和数据系统分级在超声诊断乳腺癌的临床应用价值
尹 鹏,倪卫东,赵宜勇,桑灵芝
(北京市门头沟区京煤集团总医院功检科 北京 102300)
乳腺癌是女性发病率最高的恶性肿瘤疾病,随着乳腺癌发病率增高,年轻女性也成为主要患病群体,乳腺癌早期诊断及治疗是提升患者死亡率的关键[1-2]。伴随世界维生组织对乳腺癌研究不断深入,2020年的IARC研究显示,乳腺癌患者数量已经达到226 000人次,肺癌发病人次在为220 000人,乳腺癌患者数量已经超过肺癌,是世界发病率最高的癌症[3]。早期诊断乳腺癌,有利于采取早期治疗方式,提升患者生存质量,降低患者死亡率,对此,早期筛查乳腺癌对患者疾病治疗具有重要意义。在临床诊断中通过影像学技术进行诊断,彩色多普勒超声技术在临床应用范围广,应用率高,该技术操作简单、费用低,优势较为明显。在相关文献调查中[4],乳腺影像报告和数据系统(breast imaging reporting and data system,BI-RADS)分级方法可降低医生诊断疾病的主观性,以客观的角度分析疾病,提升乳腺癌的检出率、诊断准确率。为分析BI-ERADS分级的应用价值,将北京市门头沟区京煤集团总医院2016年11月—2021年11月纳入的352例病例作为观察对象,对结果进行数据讨论,获得以下研究结果。
1 资料与方法
1.1 一般资料
研究时间在选取2016年11月—2021年11月,352例患者均在北京市门头沟区京煤集团总医院确诊为乳腺癌的患者,研究的患者均为女性,最大年龄为16~86岁,最小年龄16岁,平均年龄(53.45±5.32)岁,其中16~20岁者4例,21~30岁者25例,31~40岁者65例,41~50岁者1 021例,51~60岁者88例,61~70岁者50例,71~80岁者15例,81~90岁者4例。手术前应用高频彩色多普勒对研究对象肿物进行重新探查,共探查出359个病灶,使用超声BI-RADS完成分级研究。
纳入标准:①患者均在医院检查为乳腺癌;②患者以CT、MRI检查确诊;③患者均同意本研究。排除标准:将合并其他重大肝肾肿瘤疾病及精神疾病患者排除。
1.2.1 仪器和方法
LOGIQ E9、Philips iU22彩色多普勒超声诊断仪是本次研究中的主要仪器,在配置过程中,选择线阵探头,对探头频率进行调整,参数在为(7.5~13)MHz。乳腺癌患者在接受检查前,医务人员帮助患者调整放松状态,在检查过程中保持仰卧位,双手上举后,充分暴露乳房及腋窝,也要把握上举幅度,避免乳腺大范围牵拉,保持肿物处于病变位置。医务人员对患者的乳房形态进行评估,观察乳头颜色及形态,分析患者乳头是否发生异常变化。在二维超声诊断中,乳头是诊断的中心点,以放射扫描方式对整个乳腺形态进行评价,评估乳腺状态时,应当注意扫描病灶数量及内部回声、边界、周围组织、血管分布等基本情况,为诊断疾病提供依据[5]。
1.2.2 图像分析
医务人员诊断乳腺癌时,需结合患者基本情况,保证检查全面性,从而获得清晰的影像。检查工作完成后, 影像科医生对扫描的图像进行辨识,解读患者信息,参与阅片的医生具有5年以上乳腺癌检查经验。在某项评价中,医生存在阅片分歧,请专家进行评价,从而确定影像信息情况。
1.3 BI-RADS分级诊断标准
0级:超声检查后,影像正常,结合患者体征进一步评估。1级:影像无明显异常,经一年随访未见病变[6]。2级:影像呈现出良性,通过影像将恶性病变排除,患者诊断的疾病一般是乳腺单纯囊肿、乳腺结节,患者在确诊后使用药物治疗,半年后进入医院复诊。3级:呈现良性病变,发生恶性肿瘤的概率在2%以内,病变影像为椭圆形,具有清晰的边界,横纵比在1以内(见图1),在诊断后的90~180 d患者再次进入医院复查。4级:检查中发现明显异常,通过穿刺活检明确实际病变,发生恶性病变的概率较高,在3%~94%区间(见图2)。5级:影像学检查中,95%以上可能是恶性肿瘤,应当积极接受治疗(见图3)。6级:病理已证实为恶性病变。
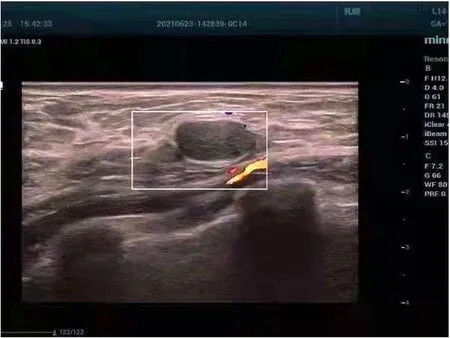
图1 BI-RADS 3级
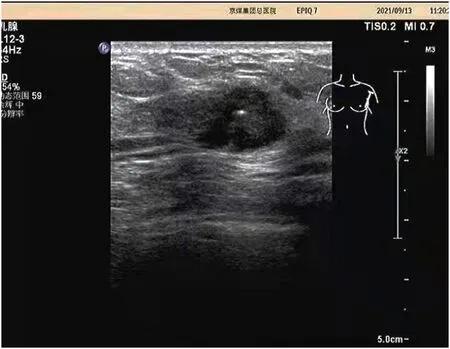
图2 BI-RADS 4级
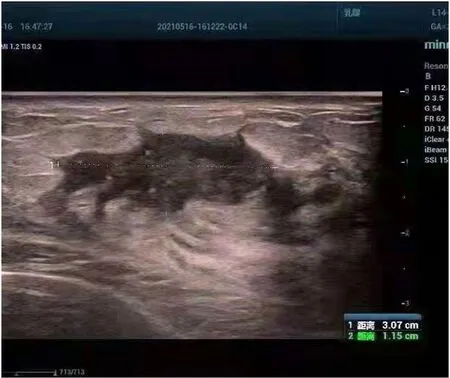
图3 BI-RADS 5级
1.4 统计学方法
采用SPSS 21.0统计软件进行数据处理。计数资料以频数(n)、百分比(%)表示,行χ2检验;计量资料标以(± s)表示,采用t检验。P<0.05表示差异有统计学意义。
2 结果
2.1 BI-RADS分级诊断标准及超声表现
BI-RADS分级中,352个例患者有359个病灶,病灶呈现出钙化、回声、血流RI值评估。在结果中显示,BI-RADS分级3~5分级中的形态、回声、钙化、边界、血流RI等指标差异均有统计学意义(P<0.05,表1),病灶形态、走行等对比中(P>0.05)。见表1。
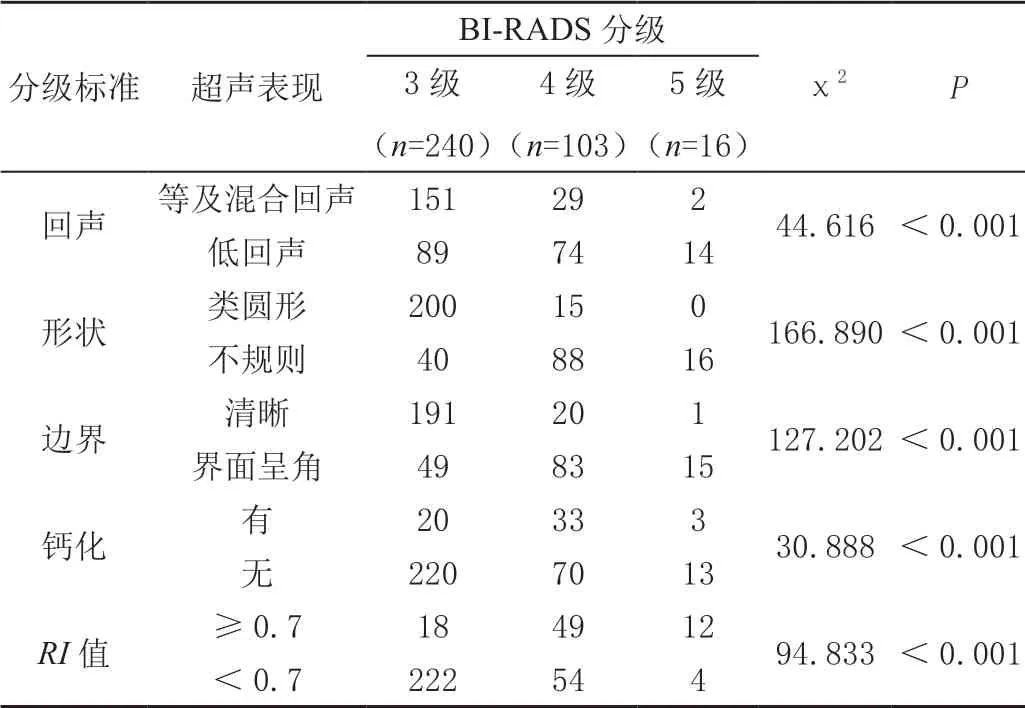
表1 按BI-RADS 3~5分级诊断标准的超声表现 单位:个
2.2 乳腺病灶的BI-RADS 3~5分级和病理结果的比较
在病理检查中,良性病灶239个,恶性病变恶性120个(见表2)。其中,良性肿瘤中乳腺纤维腺瘤及增生性病变分别为109个、61个,乳腺腺病37个,炎性病变15个,乳腺腺病伴纤维腺瘤8个,错构瘤2个,余7个病灶为导管乳头状瘤。
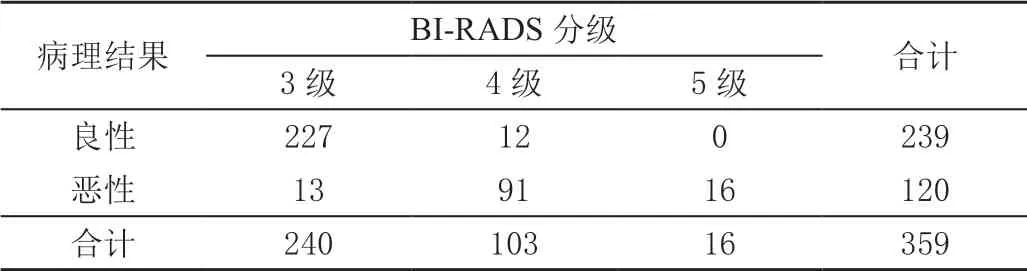
表2 乳腺病灶的BI-RADS 3~5分级和病理结果的比较 单位:个
在乳腺恶性肿瘤分类中,浸润型导管癌、浸润型导管癌伴导管内癌分别比为88个、9个,浸润性小叶癌6个,浸润型导管癌伴导管原位癌5个,黏粘液癌5个,霍奇金淋巴瘤3个,浸润性导管癌伴腺癌3例,恶性腺肌上皮瘤1个,在乳腺癌患者的病灶分析中,通过病理学分析,BI-RADS 3级病灶数量240个,良性227个(94.58%%),恶性13个(5.42%);在病理学检查中,BI-RADS 4级103个病灶,其中良性病灶12个,占比(11.65%),恶性病灶91个,占比(88.35%)。在病理学研究中,BI-RADS 5级病灶16个,其中,良性病灶为0,恶性病灶为16个(占比为16.00%)。BI-RADS分级标准诊断乳腺癌阳性率为在92.59%(107/119),灵敏度为92.73%%(107/120),特异度为94.9%%(227/239),对图4进行分析,BI-RADS 3级病灶中,良性病灶占比94.58%,BI-RADS 5级恶性病灶占比100.00%。
3 讨论
作为女性常见的恶性肿瘤疾病,乳腺癌是乳腺上皮组织发病率较高的的恶性肿瘤病变,女性在40~60岁发病率高,疾病发生原因复杂,早期无明显症状,伴随患者病情不断发展,发生全身性病变或者局部病变,自总体上看,乳腺癌预后效果不佳,病情严重患者5年生存期占比小,该疾病死亡率较高[7]。在乳腺癌诊断中,通过超声诊断有利于诊断疾病,为疾病治疗提供帮助[8]。使用超声诊断乳腺癌良恶性质过程中,医生发挥着巨大的作用,医生的主观评价往往对诊断结果产生影响。对此,在临床诊断乳腺癌过程中,医生应当具有高超的技术,选择合理化的乳腺癌诊断方案,避免患者疾病治疗延误[9],美国放射学会报道中[10],二十世纪初对乳腺影像报告和数据系统(breast imaging reporting and data system,BIRADS)分级诊断有明确的规定,对超声诊断乳腺癌BIRADS分级有全面的描述,这对医生诊断乳腺癌疾病提供帮助,为判断病变良恶性质奠定坚实的基础(见图4)。超声BI-RADS分级主要是对乳腺癌疾病进行检查,降低患者穿刺活检率,避免患者身体受到创伤,也能为早期诊断乳腺癌提供帮助,为疾病治疗奠定坚实的基础,使患者生存率提升[11-12]。彩色多普勒超声仪器在诊断乳腺癌良恶性质过程中灵敏度较高,在过往的研究资料中,BI-RADS分级结果与病理检查结果具有相似性,该结果充分体现出BI-RADS分级诊断的价值[13]。
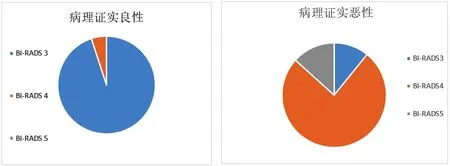
图4 乳腺病灶的BI-RADS 3~5分级和病理结果的比较
此次研究对352例乳腺肿瘤患者给予彩色多普勒超声诊断,结果显示BI-RADS 3~5分级病灶及病理数据对照分析,证实乳腺肿物BI-RADS分级是可以根据高频彩色多普勒超声图像进行指导,避免诊断过程中的主观意识判断,增加客观依据,根据BI-RADS分级诊断标准进行,有助于提高乳腺肿瘤良恶的诊断率[14]。在352例患者(359个病灶)中,病理学活检结果显示:240个BI-RADS 3级的病灶中,良性227个(94.58%%),恶性13个(5.42%);103个BI-RADS 4级的病灶中,良性12个(11.65%%),恶性91个(88.35%%);16个BI-RADS 5级的病灶中,良性0个(0.00%),恶性16个(100.00%)。BI-RADS分级诊断乳腺癌的灵敏度和特异度分别为89.2%、88.35%,说明在高频彩色多普勒超声检查诊断中,通过BI-RADS分级标准有利于提升医生阅片的客观性,保证诊断结果的准确性及统一化,该分级标准对鉴别乳腺癌良恶性质具有重要意义,为临床诊断乳腺癌提供依据[15]。自图4中进行分析,BI-RADS 4~5级发生恶性病变的概率高,临床应当关注BI-RADS 4~5级患者,必要情况下通过穿刺活检进行分析,掌握患者病变类型,早期完成手术治疗。
综上所述,在超声检查乳腺癌病变过程中,使用BIRADS分级标准进行标准化评价,有利于早期发现乳腺癌,降低误诊及漏诊率,为提升手术提供帮助。超声医生根据BI-RADS分级标准内容制定评估分界线,避免受到主观情绪影响,提升病变诊断的准确性,对此,BIRADS分级标准在超声诊断乳腺癌过程中具有临床应用价值。

