生物医用镁合金表面改性涂层研究进展
张源,郑瑞宁,刘芸,田亚强,魏英立,国海瑞,陈连生
(1.华北理工大学 现代冶金技术教育部重点实验室,河北 唐山 063210;2.北京科技大学 新金属材料国家重点实验室,北京 100083)
以不锈钢、钛合金、镍钛形状记忆合金和钴基合金为代表的传统生物惰性医用材料在人体生理环境中会长期稳定存在,需再次手术取出,增加了手术难度和康复费用[1]。因而,新型的医用金属材料渐渐走进人们的视野,其中镁合金作为“可降解生物医用金属材料”表现出巨大的应用潜力和发展前景。镁合金自身优异的生物安全性、良好的载荷传递性及自发的可降解性为其在骨移植/血管支撑等医用领域的应用提供了坚实的基础[2]。然而,镁合金较差的耐蚀性限制了其在生物医用领域的广泛应用。尤其是在富Cl-的腐蚀介质和真实的人体服役环境中,镁合金的高降解速率会导致成分流失加速、力学衰减显著等问题,进而延缓组织愈合以及使植入件提前失效[3-5]。因此,如何有效提高镁合金耐蚀性能,是当下亟需解决的核心问题。
当前,合金化、热处理、塑性加工和表面改性是4 种常见的改善镁合金降解性能的手段,前3 种改善手段由于不能充分地限制合金内部产生的电偶腐蚀,使得表面改性处理更具优势。表面改性就是人为地在镁合金材料表面制备一层或多层与基体化学成分、组织结构及性能均有差异的表面层。在本课题组先前的研究成果中发现[6-14]:相比于常规热处理、塑性加工及微合金化的途径,表面改性手段在合金表面建立的物理屏障在使镁合金保持良好自身属性的同时,还可有效抑制合金内部电偶腐蚀的激烈程度来调控其腐蚀速率及满足其他特殊的功能性需求。如通过改变改性膜层成分、结构可赋予合金良好的抗菌性能,促进成骨能力,改善合金表面的细胞黏附性、扩散性和增殖性[15-16]。目前,化学转化、微弧氧化等几种常见的表面改性手段在保证涂层满足合金表面多覆盖度、高膜层厚度、强附着力等要求的同时,实现了镁合金降解性能以及生物相容性的双提升[17-19]。
本文主要从改性涂层的形成机制及其降解机理出发,综述了近年来镁合金表面改性涂层的研究动态;简要介绍了几种表面改性工艺的原理,并对比其优缺点;系统阐述了涂层对镁合金降解过程的影响规律,以及部分元素或粒子对涂层微观结构及性能的作用机理。最后,对生物医用镁合金表面改性涂层的发展方向进行了展望。
1 表面改性分类
1.1 化学转化法
化学转化是指采用化学或电化学的方法在合金表面形成活性较低的碳酸盐、磷酸盐、氟化物等,从而起到保护基体的作用。当前,研究较多的化学转化膜有碳酸膜、磷化膜和氟化膜等,其中磷化膜和氟化膜可有效调控合金的腐蚀速率。而碳酸膜虽然在腐蚀初期可以对基体起到保护作用,但由于其会逐渐溶解在腐蚀溶液中,进而导致涂层脱落,对合金的长期保护效果不佳。Prabhu 等[20]通过化学转化法在Mg-4Zn合金表面制备了MgCO3·3H2O 涂层,涂层的厚度和致密度随处理时间的延长而增加,均匀无裂纹的涂层对合金起到良好的保护作用。但是,涂层会逐渐溶解在SBF 中,产生的裂纹使腐蚀溶液渗透到基体中,引发电偶腐蚀效应,进而导致基体周围间隙的pH 值升高,腐蚀产物(如氢氧化镁和磷酸钙)在合金表面形成半保护层。随着腐蚀溶液进一步渗透到材料与涂层之间的界面中,最终导致涂层脱落,合金腐蚀速率升高。
磷转化涂层是指通过化学转化方法在镁合金表面生成含磷化物的涂层,常见的有磷酸盐和镧基磷酸盐等。Zaludin 等[21]对不同处理方式的磷酸钙涂层(磷化和碱性)在模拟体液中的腐蚀行为进行了分析。研究结果显示:磷化和碱性涂层分别由脱水磷酸二钙和羟基磷灰石组成,与未涂覆的样品相比,磷化和碱性涂层的极化电阻分别提高了约40 倍和2 倍。由此可见,磷化处理涂层可显著提高合金的耐蚀性能,而碱性处理由于会导致合金表面涂层变薄和孔隙率变大,对耐蚀性能的影响不明显。Mao 等[22]对比了有无磷酸盐涂层的铸态Mg-Nd-Zn-Zr 合金在模拟体液中的耐蚀性能。研究结果显示:磷酸盐涂层的附着使镁合金电化学腐蚀速率由0.337 mm/a 降至0.253 mm/a。这是由于镁合金在溶解过程中会产生稳定的Mg(OH)2,Mg(OH)2不溶于水溶液,但在含氯环境中会逐渐溶解。而磷酸盐涂层主要由Mg3(PO4)2构成,具有致密的层状结构,可防止Mg(OH)2层与腐蚀溶液接触,从而提高合金的耐蚀性能。Maurya 等[23]通过化学转化法在LAT971 和LATZ9531 合金上制备了磷酸盐(PCC)涂层,从表面轮廓图(图1)可看出:LAT971和LATZ9531 的表面粗糙度分别为0.14 μm 和0.12 μm,而PCC 涂层的LAT971 和LATZ9531 表面粗糙度分别为88.7 μm 和84.6 μm。XRD 分析发现涂层主要由CaHPO4·2H2O、Ca3(PO4)2和Mg3(PO4)2组成。腐蚀试验结果显示:在3.5% NaCl 水溶液中,涂覆PCC 涂层的LAT971 和LATZ9531 合金的腐蚀电流密度分别为6.74×10-7mA/cm2和5.39×10-7mA/cm2,远低于未涂层的LAT971(0.82 mA/cm2)和LATZ9531(0.34 mA/cm2),腐蚀防护效率为99%。Jayaraj 等[24]通过化学转化法在AZ31 镁合金表面制备了镧基磷酸盐涂层(硝酸盐浴溶剂分别采用水和乙醇),并研究了其微观组织及耐蚀性能。研究结果显示:以水为溶剂制备的涂层中以La(OH)3为主,而以乙醇为溶剂制备的涂层中La完全转化为LaPO4,有利于形成均匀且裂纹小的涂层。但由于磷酸镁的不完全溶解,最终形成的涂层由两层不同的膜层组成:底层的磷酸镁以及上层的少量磷酸镁和LaPO4的混合物。以乙醇为溶剂制备的涂层表现出较好的耐蚀性能,而以水为溶剂制备的涂层中La(OH)3含量较高,易在干燥过程中产生裂纹,导致其耐蚀性能较差。磷转化涂层在一定程度上可改善镁合金的降解性能,且涂层释放的磷离子可促进细胞增殖、分化和血管再生,但过量的磷会使体内的钙流失,导致骨质疏松。
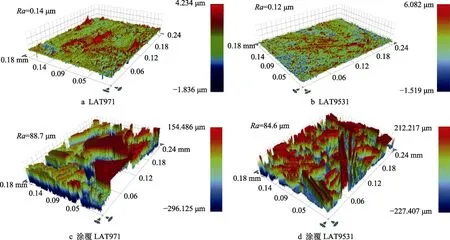
图1 未涂覆(a,b)和涂覆(c,d)的LAT971 和LAT9531 合金的光学表面轮廓[23]Fig.1 Surface profiling of uncoated (a, b) and PCC coated (c, d) LAT971 and LAT9531 alloys, respectively[23]
氟处理是指通过氢氟酸溶液处理,在合金表面生成氟化镁保护层,从而延缓腐蚀速率。同时,氟也是人体必需的微量元素,在软组织和硬组织中均有存在,有助于改善人体的内分泌功能和骨骼组织稳定性。Panemangalore 等[25]探究了氟化物涂层的Mg-Zn-Er合金在PBS 溶液中的动态降解行为。研究结果显示:合金表层的 M g(O H)2在酸性介质中不稳定,MgO/Mg(OH)2于HF 中浸泡后,在合金表面形成MgF2层,可有效降低合金的腐蚀速率。这是由于氟化物涂层通过建立腐蚀屏障,有效地防止Cl-渗入,进而保护合金基体。Yu 等[26]通过氟转化法在AZ31支架上制备了MgF2涂层,并进一步探究了其耐蚀性能。研究结果显示:AZ31 支架中Mg2+释放较快,MgF2涂层AZ31 支架中Mg2+释放较慢,且随着培养时间的延长Mg2+的释放量降低,促进了细胞的附着、增殖及成骨分化。这是由于MgF2涂层减弱了α-Mg与金属间化合物之间的微电偶腐蚀效应,从而提供了一个有利于细胞黏附和增殖的界面。Barajas 等[27]研究了HF 溶液处理时间对镁合金耐蚀性能的影响。研究结果显示:随着处理时间的延长,涂层的厚度呈抛物线形增加,腐蚀电流密度显著降低。随着处理时间的延长,涂层的性能开始变差。这表明羟基氟化镁转化层的形成可阻止化学物质在金属/涂层、涂层/腐蚀介质界面上扩散,进而增强了AZ31 合金的耐蚀性。但过长的处理时间会导致表面涂层产生裂纹,促进腐蚀产物的生长,从而导致氟化物涂层的脱落。综上,氟转化膜可有效调控镁合金的腐蚀速率,且结合能力良好,组织结构致密的氟转化层在作为预处理层时可和后续涂层结合得更紧密。但是氟处理中使用的氢氟酸具有一定的危险性,需谨慎使用。
1.2 阳极氧化与微弧氧化技术
阳极氧化是指在特定工艺和外加电流下使阳极合金表面生成一层稳定的氧化物薄膜,从而提高合金的耐蚀性。Geng 等[28]对比了不同Mg-Gd 合金阳极氧化后的耐蚀性。研究结果显示:经阳极氧化处理后,Mg-1Zn-1Gd(ZG11)、Mg-1Gd(G1)和AZ31 合金的耐蚀性均有显著提高。AZ31 样品具有更好的初始耐蚀性,这是由于其阳极氧化膜中含有一定量的Al2O3。此外,阳极氧化处理的Mg-Gd 合金,特别是ZG11 合金的局部腐蚀或点蚀得到了有效延缓,具有较好的长期降解性能。为进一步研究阳极氧化镁合金的降解性能,lshihara 等[29]分别在空气和3%氯化钠溶液中对不同表面处理的镁合金试样进行了腐蚀疲劳试验。研究结果显示:在实验室空气中,阳极氧化和涂漆处理对合金疲劳寿命的影响均较小。在氯化钠溶液中,未加工试样的疲劳寿命明显缩短,未涂漆的阳极氧化膜试样和未加工试样的疲劳寿命无明显差异。因此,单独的阳极氧化处理并不能有效地提高合金的腐蚀疲劳寿命。阳极氧化膜的厚度和涂层与阳极氧化膜界面的粗糙度是决定合金腐蚀疲劳性能的关键因素。
微弧氧化是在电解液中使合金表面发生原位反应生成陶瓷氧化物。微弧氧化技术具有工艺简单、处理效率高、膜层整体综合性能指标好等优点。Ly 等[30]探究了等通道角挤压(ECAPP)预处理对Mg-Zn-Ca合金微弧氧化涂层组织和耐蚀性能的影响。研究结果显示:ECAP/MAO 涂层比铸态/MAO 涂层更致密,孔径更小。在此基础上,复合处理可降低合金的腐蚀速率,延长涂层保护时间。这是由于ECAP 预处理改变了基体的微观组织结构,致密的ECAP/MAO 涂层可有效抑制腐蚀溶液渗透到合金的基体/涂层界面。Ly 等[31]研究了不同电流模式(单极、双极和混合电流模式)下MAO 涂层镁合金的微观结构以及对降解行为的影响规律。研究结果显示:相比于单极、双极模式下,混合电流模式下的MAO 涂层镁合金的平均微孔尺寸最小。不同电流模式下的MAO 涂层均可提高合金的耐蚀性能,其中在混合模式下的MAO 镁合金具有最佳的表面完整性及致密性。为进一步探究微弧氧化镁合金的降解机理,Cui 等[32]研究了微弧氧化Mg-Ca 合金的腐蚀影响因素。研究结果显示:MAO涂层Mg-Ca 合金的腐蚀速率主要与基体的耐蚀性、涂层的孔隙率以及涂层与基体间的电偶效应有关,涂层厚度对涂层耐蚀性的影响不显著。从降解机理图(图2)中可看出,MAO 涂层中的通孔和微裂纹是导致镁钙合金基体电化学腐蚀的主要因素。随着通孔数量的增多,电偶腐蚀效应愈发严重,致使降解速率升高。
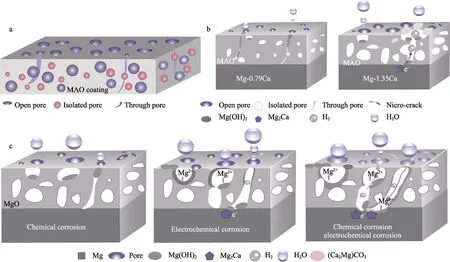
图2 镁合金MAO 涂层中的气孔示意图(a),孔径对腐蚀影响的示意图(b),Mg-Ca 合金表面MAO 涂层的化学降解和电化学腐蚀机理示意图(c)[32]Fig.2 Schematic illustration of the various pores in the MAO coatings on Mg alloys (a), schematic illustrations of the influence of pore diameter on corrosion (b), schematic illustrations of the chemical degradation and electrochemical corrosion mechanisms of the MAO coatings on Mg-Ca alloys (c)[32]
在MAO 涂层中添加适当的元素或粒子(如Cu、Li 等)可通过控制孔隙数量、致密度来改善合金的耐蚀性能。甚至部分元素在不影响合金生物相容性的同时还可赋予合金良好的抗菌性能、促进成骨能力等。Chen 等[33]研究了含Cu 离子的MAO 涂层Mg-2Zn-1Gd-0.5Zr 合金的耐蚀性能及生物相容性。研究结果显示:含Cu 的MAO 涂层镁合金的耐蚀性高于无Cu的MAO 涂层镁合金。2 种样品的生物相容性相差不大,但含Cu 的MAO 涂层镁合金具有良好的抗菌性。这是由于Cu 元素以化合物的形式进入到MAO 涂层中,避免了Mg 基体与Cu 之间的电偶腐蚀。Cu 离子水解还可使涂层表面微孔中沉积更多的Ca-P,使合金表面腐蚀产物更均匀致密,从而抑制腐蚀过程。同时Cu2+可通过破坏细菌的蛋白质来抑制细菌增殖。Lin 等[34]通过微弧氧化技术在纯Mg 上制备了含和不含Li 的涂层,并对比了其耐蚀性和生物相容性。研究结果显示:在MAO 涂层中加入Li 可使涂层中的孔隙数量减少,从而提高镁合金的耐蚀性能。MAO涂层可提高镁合金的生物相容性,而Li-MAO 涂层镁合金可进一步促进细胞的增殖分化以及相关成骨基因的表达。Zheng 等[35]研究了含CeO2粒子的Ca-P 基微弧氧化膜的纯镁的腐蚀性能。研究结果显示:CeO2粒子的加入使多孔MAO 涂层转变为自封闭的MAO涂层,合金的耐蚀性得到显著提高。试验后,含CeO2粒子的MAO 涂层的封闭区域仍然存在。因此,含CeO2粒子的MAO 涂层可以为镁合金提供长期稳定的保护。微弧氧化(MAO)的优点在于加工迅速方便,并能获得均匀、高附着力和高热稳定性的涂层,在生理条件下可以有效降低镁合金的降解速率。但微弧氧化过程会导致膜层中存在大量的微孔和裂纹,涂层的长期耐蚀性较差。由此可见单一的涂层不能完全满足镁合金性能的需求,而复合涂层具有均匀、无缺陷等优点,具有巨大的发展潜力。
1.3 离子注入
离子注入是在真空、低温的情况下,将获得较大动能的离子溅射到合金表面以使表面成分、结构改性的一种技术。离子注入可以在不改变合金尺寸和克服金属间热动力溶解度的情况下,在合金表面形成结合牢靠的改性层。Dong 等[36]研究了Mn 离子注入纯镁后的腐蚀行为。研究结果显示:Mn 离子以金属和氧化态的形式注入到纯Mg 表面,降低了表面粗糙度。在浸泡初期,由于金属锰与镁之间存在电位差会发生严重的电偶腐蚀效应。但是金属锰易于转化为锰氧化物,随着浸泡时间的延长,电偶腐蚀得到了缓解。此外,在纯Mg 表面均匀分布的微点蚀促进了表面含Ca、P 元素的保护层的形成,从而降低了腐蚀速率。Ba 等[37]研究了Sn 离子注入Mg-Gd-Zn-Zr 合金的耐蚀性能。研究结果显示:注入锡离子的合金表面涂层由SnO2和MgO 组成,涂层致密,裂纹数量少。相比之下,未处理的合金表现为局部腐蚀,形成的涂层表面松散。Wei 等[38]研究了不同NH2+注入量的AZ31 镁合金的耐蚀性能。从合金表面形貌(图3)可看出:未经处理的样品表面比较粗糙,颗粒较多,当注入一定的NH2+后,表面变得更致密、颗粒更细。随着注入剂量的增加,凹坑的数量大幅度减少,耐蚀性能显著提升。

图3 AFM 下试样的表面形貌[38]Fig.3 Surface morphology of the samples observed by AFM: a) untreated; b) implanted sample with dose of 1×1016 ions/cm2; c) implanted sample with dose of 5×1016 ions/cm2;d) implanted sample with dose of 1×1017 ions/cm2[38]
近年来,部分研究[39-41]发现某些注入离子在调控合金腐蚀速率的同时还可改善合金生物相容性,这些离子具有较低的细胞毒性,可提高合金生物相容性,有效促进细胞增殖分化。Wei 等[40]通过离子注入法将羧基离子注入到ZK60 镁合金表面,并研究了其耐蚀性和体外细胞毒性。研究结果显示:随着羧基离子注入剂量的增加,镁合金腐蚀电流密度逐渐减小,耐蚀性能显著提高。尽管离子注入镁合金在不同浓度的提取液下的细胞存活率不同,但均明显高于同条件下未处理样品,无明显细胞毒性。这是由于羧基离子注入促进了基材表面形成相对光滑、功能良好的含羧基、碳酸盐、金属氧化物/氢氧化物的表面层,可防止腐蚀溶液渗透到基材表面。同时羧基比金属离子毒性小,有利于细胞的黏附和增殖分化。Liu 等[41]对比了有无Zn 离子注入的Mg-1Ca 合金的生物相容性。通过观察MC3T3-E1 细胞的形态和存活率发现:含Zn离子的镁合金表面存在大量延伸的丝状伪足细胞,细胞存活率高于不含Zn 离子的镁合金。这是由于无Zn离子注入的镁合金与细胞共培养后,其表面出现了许多严重腐蚀造成的裂纹,裂纹的存在使得细胞难以在样品表面黏附。但是Zn 离子的注入使合金腐蚀表面变得均匀致密,无明显裂纹,从而为细胞的黏附、增殖提供了良好的环境。综上所述,离子注入虽然能有效改善医用镁合金的耐蚀性和生物相容性,但注入深度有限。金属元素的注入还可能引起合金基体的电偶腐蚀,无法对合金提供长期保护。在此基础上,离子注入法的综合成本较高,不适合广泛的应用。
1.4 等离子喷涂
等离子喷涂是指将喷涂材料加热到熔融或半熔融状态后,高速喷射到经预处理的合金表面形成牢固的表面层。这种技术具有涂层质量高、工艺稳定、加工合金尺寸不受限制等优点。Lstrate 等[42]在Mg-Ca和Mg-Ca-Zr 上制备了2 种陶瓷涂层材料(ZrO2-Y2O3和ZrO2-CaO),并对比了其耐蚀性能。研究结果显示:合金从晶界处开始降解,在表面形成可溶盐,化学侵蚀在合金整个表面均匀发生。相较于ZrO2-CaO 涂层镁合金,ZrO2-Y2O3涂层镁合金表现出更好的耐蚀性。这是由于ZrO2-CaO 涂层镁合金表面存在气孔和微裂纹,会导致沉积层与基材界面发生电偶腐蚀效应。其中ZrO2-Y2O3涂层镁合金表面更均匀致密,气孔和微裂纹数量较少。Bansal 等[43]研究了不同ZnO 浓度的HA 涂层AZ31 合金的耐蚀性能。研究结果显示:纯HA 涂层的耐蚀性能优于裸 AZ31 合金,但低于HA/ZnO 增强涂层。随着ZnO 含量的增加,涂层厚度更加均匀,耐蚀性逐渐增强。由此可见,在纯HA 粉末中加入氧化锌增强剂可增强镁合金的耐蚀性能。总体来看,等离子喷涂技术方法较为新颖丰富,有望成为未来发展方向,尤其是在医用镁合金沉积涂层方面,具有极大的潜力。
1.5 化学沉积和电沉积
化学沉积是在无电流作用下,合金于可溶性盐溶液中发生化学反应并使反应产物沉淀到合金表面的方法。Wang 等[44]研究了有无SrHPO4涂层的JDBM合金在大鼠股骨中的腐蚀行为。研究结果显示:裸JDBM 合金直接暴露于髓腔内液体中会加快腐蚀速率,产生的过量氢气在髓腔内聚集,进而导致裸JDBM 合金过早丧失机械强度,在愈合过程中过早地将更多应力转移到骨折部分,以致种植体失效。而SrHPO4涂层的JDBM 合金可保护基体完整性,降低种植体的失效率,进而诱导新骨的生成。Hiromoto等[45]研究了HAp 涂层对纯Mg、MgCa、WE43、EW31和RE4 合金体内降解行为的影响。合金腐蚀示意图如图4 所示,除RE4 合金外,Mg/Mg 合金表面均形成均匀的HAp 层,进一步抑制了腐蚀产生和发展。其中在含稀土元素的合金中,Y 含量较高的WE43 合金的腐蚀产物溶解度较低,腐蚀产物的稳定性得到提高,从而提高了合金的腐蚀防护性能。化学沉积处理后合金的耐蚀性能较好,但溶液中的第二相易导致沉积不均匀,导致涂层的结合力降低。
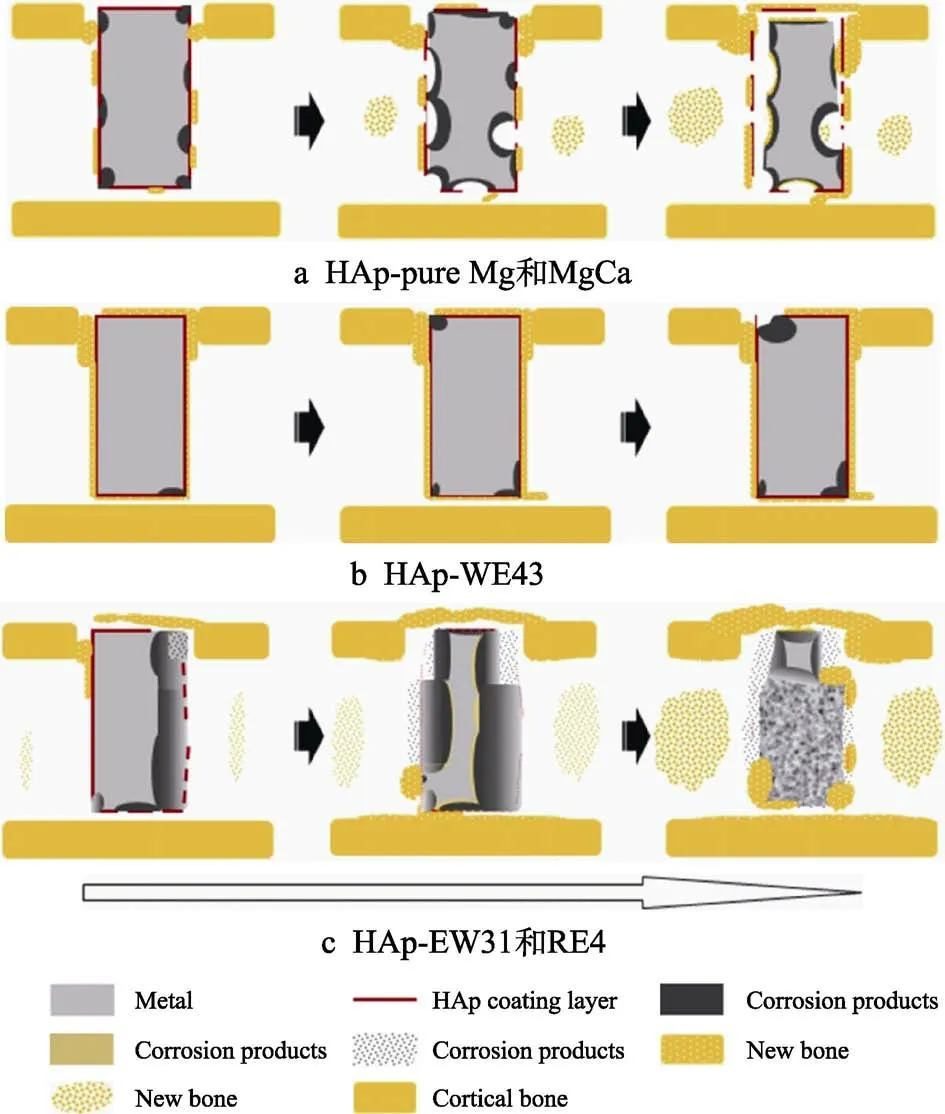
图4 不同合金的腐蚀行为示意图[45]Fig.4 Schematic illustration of corrosion behavior of HAp-pure Mg and MgCa (a), HAp-WE43 (b) and HAp-EW31 and RE4 alloys (c)[45]
电沉积是在外加电流作用下,通过电解液中离子迁移发生的氧化还原反应在合金表面形成镀层,可显著提高合金硬化及降解能力。Prakash 等[46]通过电沉积法在Mg-5Zn-0.3Ca 合金表面制备了Si-HA 涂层,并测试了其降解速率。研究结果显示:Mg-Zn-Mn 合金的降解速率由0.82 mm/a 降低到0.07 mm/a。这是由于涂层由CaMg、Mg-Zn、Mn-CaO、Mn-P 和Ca-Mn-O等金属间氧化物相组成,致密的金属间相作为稳定的阻挡层,延缓了合金表面降解。Liu 等[47]采用电解沉积技术在 WE43 镁合金表面制备了 Al2O3-ZrO2陶瓷涂层。XRD 和EDS 结果显示,O、Al、Zr 等元素均匀分布在合金表面,表明涂层已均匀沉积到合金表面;电化学试验结果显示:合金的腐蚀电位由-1.681 V 升至-1.354 V,降解速率由13.027 mm/a 降至0.239 mm/a。Shi 等[48]研究了含锶的羟基磷灰石涂层Mg-4Zn 合金的耐蚀性能。研究结果显示:掺Sr的HA 包覆样品的Mg 离子释放量较小,耐蚀性能得到改善,且随Sr 含量的增加,耐蚀性能提高。这是由于Sr 掺杂样品中密集排列的晶体可在Mg-4Zn 基体与腐蚀溶液之间起到阻挡层的作用。总体来说,电化学沉积操作简单,可以在不同形状的样品表面制备涂层,但这种方式制备的涂层与基体结合力较低,不能承受过高的应力。
1.6 复合涂层
复合涂层相较于单一涂层能长期使合金维持低降解速率,且能同时满足镁合金的多种功能性需求,是未来镁合金表面改性的主要发展趋势。复合涂层的外涂层由于直接和体内环境接触要求其生物学性能较好,而内涂层为防止与基体脱落要求其具有良好的结合能力。Dou 等[49]研究了 MAO/CS 复合涂层Mg-Zn-Ca 合金在生理环境下的腐蚀速率。研究结果显示:MAO/CS 涂层合金在生理环境下保持较低的降解速率,溶液 pH 值保持在中等水平。Bordbar-Khiabani 等[50]在AZ91 镁合金表面制备了MgO/ZnO复合镀层,并研究了其耐蚀性能,涂层形成机制如图5 所示。研究结果显示:纳米ZnO(ZnONPs)的加入降低了涂层的厚度、表面粗糙度和孔隙率。同时ZnO NPs 在涂层结构中的存在增加了涂层的致密度和渗透路径的难度,进而提高了涂层的耐蚀性能。Daroonparvar 等[51]对比了Al2O3-13%TiO2和Al2O3-13%TiO2/TiO22 种纳米复合陶瓷涂层镁合金的耐蚀性能。研究结果显示:与其他样品相比,Al2O3-13%TiO2/TiO2涂层能够有效缓解镁合金在氯化物溶液中的阳极溶解。上述现象的原因为:Al2O3-13%TiO2涂层中存在较多的针孔、连通孔隙和裂纹等微缺陷。这些微缺陷为腐蚀溶液渗入到涂层内部提供了途径/扩散通道,而Al2O3-13%TiO2/TiO2涂层较为致密,可有效防止腐蚀因子的渗透/扩散。Bakhsheshi-Rad 等[52]在Mg-Ca 表面制备了NiCrAlY/nano-YSZ/PCL 复合涂层。研究结果显示:3 层等离子体/聚合物涂层合金的腐蚀电流密度明显低于单层和双层等离子体涂层合金。这是由于PCL 聚合物涂层对纳米YSZ 等离子体层起到密封作用,从而提高了镁钙合金的耐蚀性能。Zhou 等[53]研究了复合涂层对WE43 合金腐蚀性能的影响。研究结果显示:复合涂层的合金腐蚀速率比裸合金以及单一涂层合金的都低。上述现象产生的原因为:磷酸镁预处理层提高了磷酸钙涂层的完整性、均匀性和致密性,使其具有较高的抗基体脱层能力,进而抑制了腐蚀溶液的渗透。同时,复合涂层阻碍了WE43 合金腐蚀产生的阳离子迁移到临近区域,维持了局部电荷平衡,减缓了电化学腐蚀过程。由此可见,相比于单一涂层,复合涂层可更有效地改善涂层表面缺陷,进而抑制腐蚀过程,为合金提供更全面的保护。
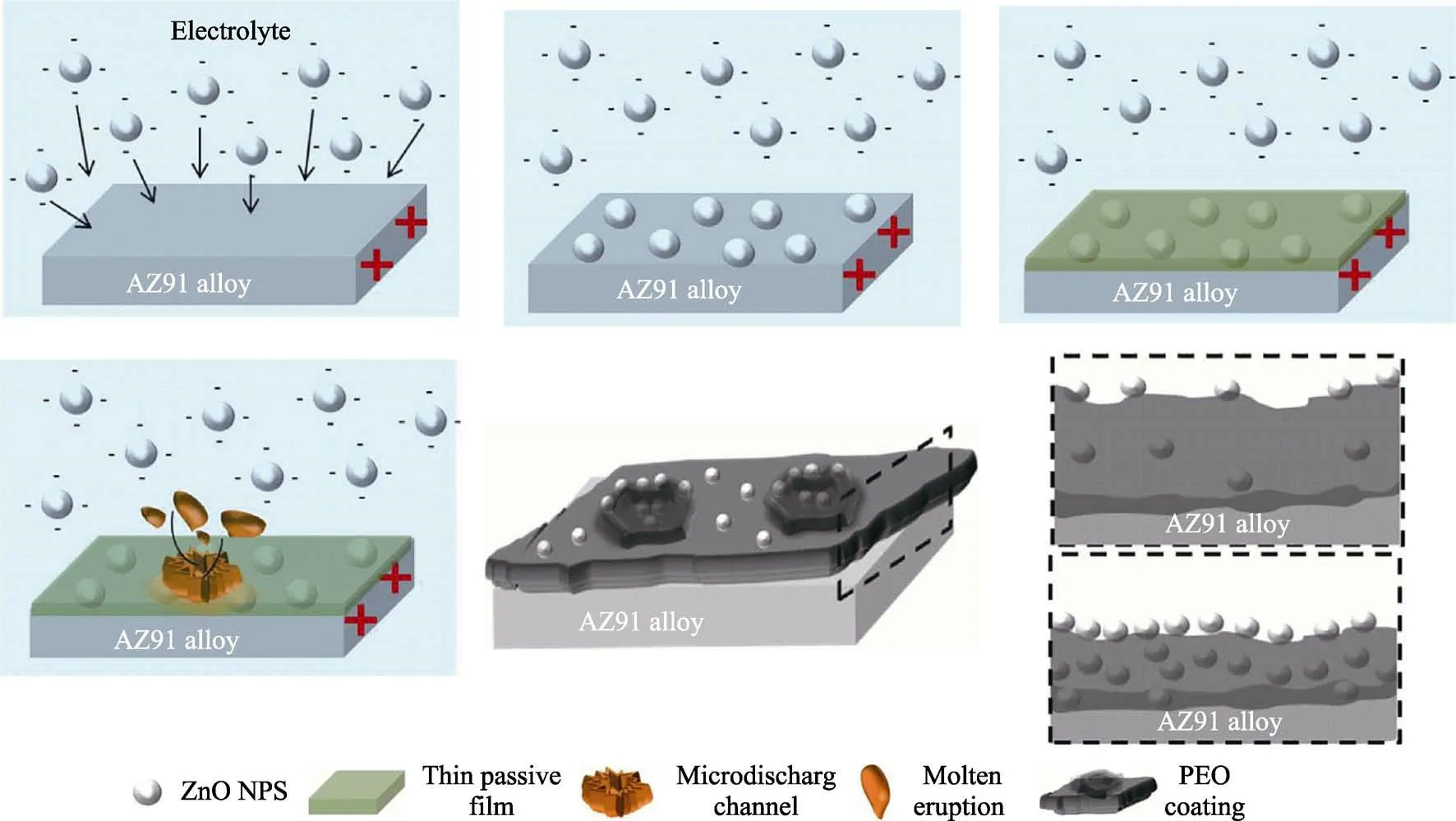
图5 涂层生长机制示意图[50]Fig.5 Diagram of coating growth mechanism[50]
2 总结与展望
近年来,镁合金作为“新型的医用金属材料”渐渐走进人们的视野,但较高的降解速率是制约其进一步发展的主要原因。表面改性可通过在合金表面建立腐蚀屏障来提高合金的耐蚀性能,对促进可降解生物医用镁合金在临床上的广泛应用具有积极的意义。尽管目前多种医用镁合金表面改性技术已趋于成熟,但还是存在诸多缺点。在目前的研究成果上,镁合金表面改性研究可以考虑以下几个方面:
1)确保医用涂层镁合金的生物安全性,避免因氢气的过量聚集而影响周围组织的正常生长。同时在保证绿色环保的前提下,要积极降低镁合金表面处理技术的成本,提升现有表面处理工艺的技术水平。
2)人体不同植入部位对镁合金的表面性能要求不同。例如:镁合金用作小型薄壁件血管支架材料时,希望镁合金表面具有促内皮化、抗血栓的能力;而作为大型骨修复材料时,则希望镁合金表面具有促骨细胞分化、抗菌性能。因此,要针对性地研究特定改性涂层及制备技术,以满足特定的医学需求。
3)相比于在体外生理环境下的腐蚀,镁合金在体内往往处于比较复杂的受力状态。单一的涂层往往很难满足长时间服役的需要,多级复合涂层是未来主要的发展趋势。但复合涂层间的结合情况和降解机制尚无系统性的研究,需要大量的体内体外试验去进一步补充和验证。

