miR-495对食管癌细胞株Eca109在不同放射剂量和顺铂浓度作用的影响及机制研究
刘 伟,周 杨,边 超,东 丽
(内蒙古自治区人民医院a.放射治疗科;b.肿瘤内科, 呼和浩特 010010)
食管癌是中国第六大常见癌症,也是导致肿瘤相关死亡的第四大原因,2018年统计数据显示,全球有超过57 万例新诊断食管癌病例和51 万左右食管癌死亡病例[1]。尽管食管癌的诊断技术和治疗取得了进步,但是食管癌患者的总体生存率仍然很差[2]。食管癌患者对化疗和放疗敏感度降低是患者病情进展导致预后不良的重要原因[3],而食管癌化疗和放疗抵抗的分子机制尚未完全明确,因此迫切需要进行探讨,以寻找新的治疗手段改善患者疗效。研究报道微小核糖核酸(microRNA, miRNA)密切参与肿瘤的恶性进展,包括增殖、侵袭和转移以及肿瘤的化疗和放疗抵抗[4]。MiR-495 是肿瘤抑制因子,在子宫内膜癌和口腔鳞状细胞癌等恶性肿瘤中抑制肿瘤的发生发展[5-6],在非小细胞肺癌和胃癌中与肿瘤耐药相关[7],并且研究报道miR-495 抑制食管癌的增殖[8],但是miR-495 与食管癌化疗和放疗敏感度的关系未见有报道。基于顺铂的化疗方案是治疗食管癌的一线药物,也常常引起患者耐药[9],因此本文对miR-495 在食管癌细胞顺铂和放射敏感度中的作用及机制进行了探讨,以期发现miR-495增加食管癌细胞对顺铂和放射治疗敏感度的作用及机制,以及作为逆转食管癌化疗和放疗抵抗候选靶点的证据。
1 材料与方法
1.1 研究对象 食管癌细胞系Eca109,购于中国上海科学院, 快速复苏后重悬至含有10g/dl 胎牛血清的细胞培养液中培养,放置在37℃,5ml/dl CO2的全湿度培养箱中。隔天更换新鲜培养液,细胞长至95%左右时,一比三进行细胞传代。
1.2 仪器与试剂 基础培养液、胎牛血清和胰蛋白酶(美国Hyclone 公司);miR-495 mimic(中国上海吉凯生物技术有限公司);Trizol 试剂(日本TaKaRa 公司);OneStep RT-PCR Kit 试剂盒、RIPA和荧光素酶报道基因试剂盒(北京索莱宝试剂公司);miR-495 和GAPDH 引物(上海捷瑞生物工程有限公司);Annexin V-FITC/PI 凋亡检测试剂盒(上海碧云天生物技术有限公司);CCK8 试剂(美国GlpBio 公司);BCA 检测蛋白浓度试剂盒(美国Thermo 公司);Bcl-2,Bax 和caspase 3 抗体(美国proteintech 公司);ECL 化学发光试剂盒(美国millipore 公司)。
1.3 方法
1.3.1 Eca109-RAD 及Eca109-DDP 的构建:取对数生长期的Eca109 细胞1×105个接种至6 孔板中,进行分次递增放射,1,2,4 和8Gy 剂量各辐射3次,总量为45 Gy。辐射后敏感性细胞死去,存活的放射抵抗细胞形成细胞克隆,获得的放射抵抗细胞(Eca109-RAD)可在4 Gy 放射剂量下生长。Eca109-RAD 扩大培养用于后续实验研究。
取对数生长期的Eca109 细胞1×105个接种至6 孔板中,以0.1,0.2,0.4 和0.8ng/ml 顺铂分次处理诱导,顺铂敏感的细胞死去,具有耐药性的细胞形成细胞克隆,获得顺铂耐药的细胞(Eca109-DDP)可在0.4ng/ml 浓度下生长。将Eca109-DDP 扩大培养用于后续实验研究。
1.3.2 细胞转染:取对数生长期的Eca109-RAD 细胞或Eca109-DDP 细胞1×105个接种至6 孔板中,分为NC 组和miR-495 mimic 组,12h 后采用脂质体2000 进行各组细胞的转染,10h 后更换新鲜完全培养液,转染48h 进行后续实验研究。
1.3.3 qRT-PCR 细胞:经Trizol 试剂裂解后加入氯仿,低温高速离心后获取上层上清液,加入异丙醇和无水乙醇试剂获取细胞中总RNA,根据OneStep RT-PCR Ki 试剂盒说明书配制反应体系,25×One Step 1μl,RTase mix 5×One Step RT Mix Buffer 5μl,Primer (1)2.5μl,Primer (2)2.5μl,RNA 0.5μg和双蒸水补足25μl。以反转录 50℃ 20min,变性95℃ 3min(变性95℃ 15 s,退火延伸60℃ 30 s,延伸72℃ 30 s)40 个循环进行qRT-PCR 扩增反应,miR-495 引物F:5’-TCCGATTCTTCACGTGGTAC-3’,R:5’-GTGCAGGGTCCGAGGT-3’;U6引物F:5’-CTCGCTTCGGCAGCACATATACT-3’,R:5’-ACGCTTCACGAATTTGCGTGTC-3’。按照2-ΔΔCt公式计算,以U6 为内参计算miR-495 相对表达量。
1.3.4 CCK8 检测放射敏感度:转染的NC 组和miR-495 mimic 组Eca109-RAD 细胞或Eca109-DDP细胞以每孔3 000 个细胞接种至96 孔板中,每组包含6 个复孔,接种12h 后分别采用不同放射剂量(0,1,2,4,8,16,32 和64 Gy)照射Eca109-RAD细胞各组细胞、不同浓度的顺铂(0,0.05,0.1,0.2,0.4,0.8,1.6 和3.2μg/ml)处理Eca109-DDP 细胞,放置于37℃,5ml/dl CO2的全湿度培养箱中48h,加入10μl 的CCK8 试剂,孵育1h,采用酶标仪检测各个孔的490nm 吸光度值(A)。细胞存活率=(处理组平均A值/不处理组平均A值)×100%。
1.3.5 平板克隆实验检测克隆形成率:各组细胞经胰酶消化后以500 个细胞接种至6 孔板中,每组包含3 个重复孔,NC 组和miR-495 mimic 组Eca109-RAD 细胞以4Gy 的放射剂量进行辐射,NC 组和miR-495 mimic 组Eca109-DDP 细胞以0.4ng/ml 放射剂量进行辐射。各组细胞放置于37℃,5ml/dl CO2的全湿度培养箱中培养10 天左右,细胞克隆团形成。终止培养,PBS 洗两次,甲醇溶液固定10min,吉姆萨染液染色10min,晾干后计数细胞克隆团数目,细胞克隆形成率=(miR-495 mimic 组平均克隆团数目/NC 组平均克隆团数目)×100%。
1.3.6 流式细胞仪检测细胞凋亡:各组细胞经胰酶消化后以500 个细胞接种至6 孔板中,每组包含3个重复孔,NC 组和miR-495 mimic 组Eca109-RAD细胞以4Gy 的放射剂量进行辐射,NC 组和miR-495 mimic 组Eca109-DDP 细胞以0.4ng/ml 放射剂量进行辐射。各组细胞放置于37℃,5ml/dl CO2的全湿度培养箱中培养48h。终止培养,经胰酶消化后按照Annexin V-FITC/PI 染色试剂盒依次加入染色缓冲液500μl,Annexin V-FITC 5μl 和PI 5μl混匀后常温放置10min 后,采用流式细胞仪检测细胞凋亡率。
1.3.7 Western blotting:增强型电化学发光法。细胞经RIPA 裂解后,14 000r/min 离心30min,获得上清细胞总蛋白。采用BCA 试剂盒检测细胞总蛋白浓度,沸水中煮5min 蛋白变性,上样进行凝胶电泳(SDS-PAGE)分离蛋白(80V,2h),电湿转(350mA,2h)将蛋白转移至PVDF 膜上。8%封闭液室温封闭1h,一抗4℃孵育过夜,二抗室温孵育2 h,增强型化学发光试剂盒(enhanced chemiluminescence, ECL)加至PVDF 膜上,显影液和定影液曝光。
1.4 统计学分析 采用软件SPSS19.0 进行统计学分析。数据以均数±标准差(±s)表示,采用独立样本t检验比较两组间的统计学差异。P<0.05为差异具有统计学意义。
2 结果
2.1 qRT-PCR 检测Eca109-RAD 和Eca109-DDP 细胞中miR-495 的表达 qRT-PCR 检测显示miR-495在Eca109,Eca109-RAD 细胞和Eca109-DDP 细胞中的表达分别为0.99±0.01,0.48±0.03 和0.52±0.05,与Eca109 细胞相比,Eca109-RAD 细胞和Eca109-DDP 细胞中miR-495 的表达显著降低,差异均有统计学意义(t=27.930, 15.970, 均P=0.000)。
2.2 qRT-PCR 检测miR-495 mimic 转染效果 qRTPCR 检测miR-495 mimic 转染食管癌细胞Eca109-RAD 和Eca109-DDP 的过表达效果,结果显示miR-495 在NC 组Eca109-RAD 细胞、miR-495 mimic 组Eca109-RAD 细胞、NC 组Eca109-DDP 细胞、miR-495 mimic 组Eca109-DDP 细胞中miR-495 的相对表达量分别为1.00±0.03,4.82±0.48,1.00±0.01,5.68±0.54。在Eca109-RAD 和Eca109-DDP 细胞中与NC 组相比,miR-495 mimic 组中miR-495 相对表达量均增加,差异有统计学意义(t=13.760,15.100,均P=0.000)。表明miR-495 mimic 成功转染至Eca109-RAD 和Eca109-DDP 细胞中,可以进行后续实验。
2.3 miR-495 对食管癌细胞放射和顺铂敏感度的影响 见表1。NC 组和miR-495 mimic 组Eca109-RAD 细胞经不同放射剂量照射48h,CCK8 结果显示在相同放射剂量作用下,miR-495 mimic 组Eca109-RAD 细胞存活率显著低于NC 组,表明miR-495 mimic增加Eca109-RAD细胞放射敏感度。NC 组和miR-495 mimic 组Eca109-DDP 细胞经不同浓度的顺铂处理48h,CCK8 结果显示在相同浓度顺铂作用下,miR-495 mimic 组Eca109-DDP 细胞存活率显著低于NC 组,表明miR-495 mimic 增加Eca109-DDP 细胞顺铂敏感度。
2.4 miR-495 对食管癌细胞克隆形成能力的影响miR-495 mimic 转染Eca109-RAD 和Eca109-DDP后,平板克隆实验结果显示,NC 组细胞克隆形成数目分别为93.33±4.51 个,89.00±4.03 个,miR-495 mimic 组细胞克隆形成数目分别为46.33±5.69个,34.67±2.52 个,与NC 组相比,miR-495 mimic组Eca109-RAD 和Eca109-DDP 细胞平板克隆形成能力均显著降低,差异均有统计学意义(t=11.210,19.800,均P=0.000)。
表1 miR-495 对食管癌细胞放射和顺铂敏感度的影响(±s)
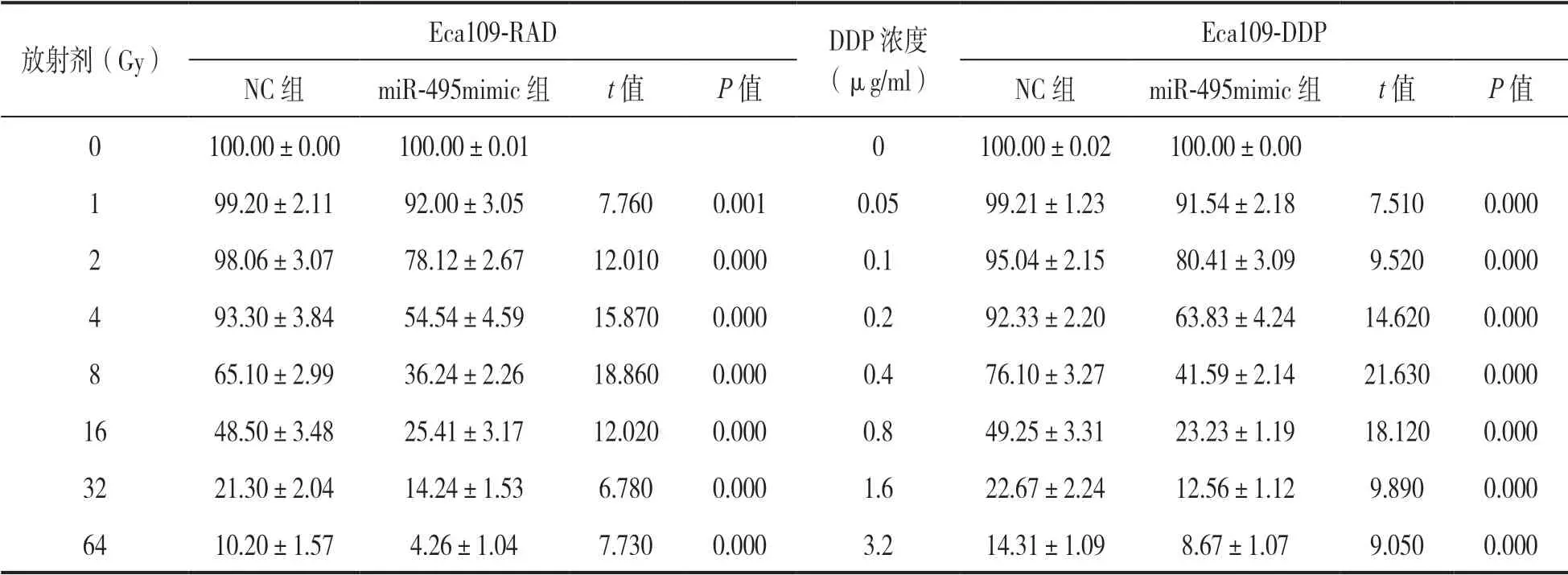
表1 miR-495 对食管癌细胞放射和顺铂敏感度的影响(±s)
放射剂(Gy)Eca109-RADDDP 浓度(μg/ml)Eca109-DDP NC 组miR-495mimic 组t 值P 值NC 组miR-495mimic 组t 值P 值0100.00±0.00100.00±0.010100.00±0.02100.00±0.00 199.20±2.1192.00±3.057.7600.0010.0599.21±1.2391.54±2.187.5100.000 298.06±3.0778.12±2.6712.0100.0000.195.04±2.1580.41±3.099.5200.000 493.30±3.8454.54±4.5915.8700.0000.292.33±2.2063.83±4.2414.6200.000 865.10±2.9936.24±2.2618.8600.0000.476.10±3.2741.59±2.1421.6300.000 1648.50±3.4825.41±3.1712.0200.0000.849.25±3.3123.23±1.1918.1200.000 3221.30±2.0414.24±1.536.7800.0001.622.67±2.2412.56±1.129.8900.000 6410.20±1.574.26±1.047.7300.0003.214.31±1.098.67±1.079.0500.000
miR-495 mimic 转染Eca109-RAD 和Eca109-DDP 后,流式细胞仪检测结果显示NC 组细胞凋亡率分别为(8.39±0.82)%,(8.67±1.15)%,miR-495 mimic 组 细 胞 凋 亡 率 分 别 为(25.66±2.41)%,(21.05±5.37)%,与NC 组相比,miR-495 mimic 组Eca109-RAD 和Eca109-DDP 细胞的细胞凋亡率均显著增加,差异均有统计学意义(t=11.750, 10.030,P=0.000,0.001)。
2.5 miR-495 对食管癌细胞凋亡相关蛋白表达的影响 见表2。Western blotting 结果显示Eca109-RAD 细胞经辐射、Eca109-DDP 细胞经顺铂处理后,与NC 组相比,miR-495 mimic 组Eca109-RAD 和Eca109-DDP 细胞中Bcl-2 蛋白表达均降低,Bax 和caspase 3 蛋白的表达均增加(P<0.05) 。
表2 Western blotting 检测miR-495 对食管癌细胞凋亡相关蛋白表达的影响(±s)
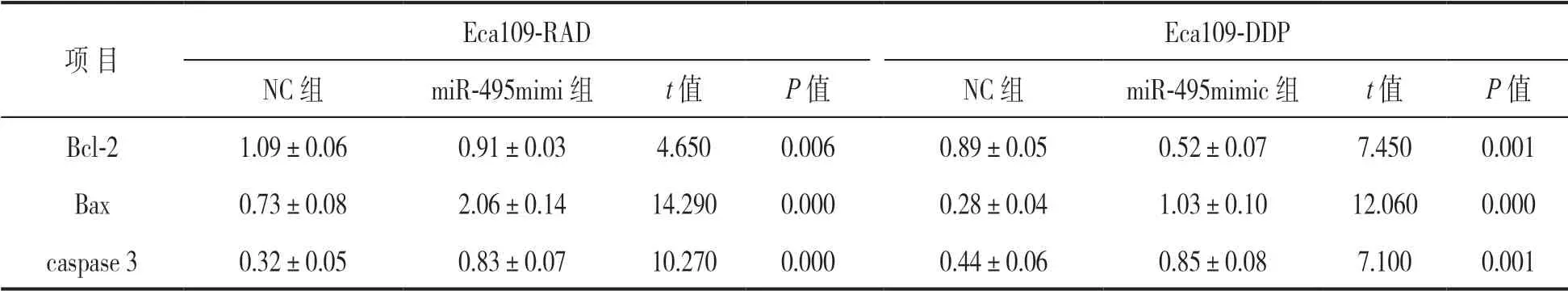
表2 Western blotting 检测miR-495 对食管癌细胞凋亡相关蛋白表达的影响(±s)
项 目Eca109-RADEca109-DDP NC 组miR-495mimi 组t 值P 值NC 组miR-495mimic 组t 值P 值Bcl-21.09±0.060.91±0.034.6500.0060.89±0.050.52±0.077.4500.001 Bax0.73±0.082.06±0.1414.2900.0000.28±0.041.03±0.1012.0600.000 caspase 30.32±0.050.83±0.0710.2700.0000.44±0.060.85±0.087.1000.001
3 讨论
食管癌是导致世界范围内高死亡率和预后差的最常见恶性消化系统肿瘤之一,严重威胁患者的生命健康和降低患者的生存质量[1]。根据组织病理学食管癌分为两种亚型:食管鳞状细胞癌和食管腺癌,其中食管鳞状细胞癌是最主要和最普遍的组织学亚型,在中国食管癌病例中食管鳞状细胞癌占90%以上[10]。早期食管癌的治疗主要是手术切除,但是由于患者早期缺乏特异的临床症状,食管癌患者往往被诊断为晚期,晚期患者由于出现转移和周围组织器官浸润,无法进行手术切除,因此化学治疗和放射治疗是晚期患者的主要治疗手段,但是大部分患者出现化疗和放疗抵抗,导致患者5年生存率较低,不足30%[2]。因此研究食管癌化疗和放疗敏感度相关的分子机制,对探索治疗靶点,改善食管癌患者预后具有重要意义。
miRNA 属于长度为19 ~24 个核苷酸的小非编码RNA,不具备编码蛋白质的功能,可以通过与靶mRNA 的互补结合而在转录后调控靶基因,在细胞分化、生长、发育和运动等几乎所有的生理过程中发挥重要调控作用[11]。研究报道miRNA 表达异常导致疾病的发生,其中人类恶性肿瘤发生发展中具有关键作用[4],是目前的研究热点。人类14q32.31 基因簇位于基因组的印迹区域,包含许多编码miRNA 的基因,参与促进正常组织的发育并调节肿瘤细胞的增殖、凋亡、转移和化学敏感性[12]。miR-495 是14q32.31 miRNA 簇的成员,是正常胰腺发育的重要因子,其与miRNA let-7b 一起诱导分化,通过抑制肝细胞核因子6 来防止胰腺腺泡细胞的化生,同时 miR-495 与14q32.31 簇中的其他miRNA 一样,密切参与肿瘤的进展[13]。miR-495在口腔鳞状细胞癌组织和细胞系中表达下调,并显著抑制口腔鳞状细胞癌细胞的增殖、迁移、侵袭和上皮-间质转化(EMT)相关蛋白[6]。同时miR-495 在食管癌中也有研究报道,MAO 等[8]报道在食管癌组织中miR-495 的表达降低,并与淋巴结转移、侵袭、TNM 分期增加和患者预后不良相关,miR-495 的过表达抑制细胞增殖、迁移和侵袭能力,诱导细胞周期阻滞,表明miR-495 在食管癌中是具有重要功能的分子。在非小细胞肺癌中miR495-UBE2C-ABCG2/ERCC1 轴通过下调抗药基因和减少顺铂抗性逆转顺铂的抗性,以及miR-495 低表达与胃癌多药耐药性相关[7],表明miR-495 与肿瘤的耐药相关,但是miR-495 在食管癌耐药方面的相关报道未知,miR-495 是否与食管癌包括肿瘤化疗和放疗的治疗抵抗相关,引起我们的关注。
本文首先诱导建立了放疗抵抗食管癌细胞Eca109-RAD 及顺铂耐药食管癌细胞Eca109-DDP,qRT-PCR 检测发现miR-495 在Eca109-RAD 及Eca 109-DDP 细胞中表达降低,提示miR-495 与食管癌放疗抵抗和化疗耐药相关。以及miR-495 mimic 转染Eca109-RAD 细胞后发现miR-495 增加食管癌细胞对放疗敏感度,以及经4 Gy 剂量照射NC 组和miR-495 mimic 组Eca109-RAD 细胞后,miR-495 mimic 组细胞增殖和平板克隆形成能力降低,细胞凋亡增多,表明miR-495 与食管癌放疗敏感性相关。CHEN 等[8]研究发现miR-495 通过抑制耐药相关基因ABCG2 和ERCC1 逆转非小细胞肺癌细胞顺铂的耐药。顺铂是广泛应用于各种恶性肿瘤的化学药物,具有广谱性,在食管癌患者的化疗治疗中处于一线药物地位,但食管癌细胞对其常常产生抵抗性,导致患者治疗效果不佳[9],因此本文研究了miR-495 在食管癌细胞顺铂耐药方面的作用。首先miR-495 mimic 转染Eca109 细胞后发现miR-495 增加食管癌细胞对顺铂作用的敏感度,经0.4 ng/ml 浓度处理NC 组和miR-495 mimic 组Eca109-DDP 细胞后,miR-495 mimic 组细胞增殖和平板克隆形成能力降低,细胞凋亡增多,表明miR-495 与食管癌化疗耐药相关。同时结果表明miR-495 增加食管癌细胞对放射和顺铂敏感性可能是通过调控细胞凋亡发挥作用,而细胞凋亡的发生是在细胞凋亡蛋白的调控作用下发生的,因此本文采用Western blotting 检测了相关凋亡蛋白的变化,其中Bcl-2 基因是经典的抗凋亡基因,和促凋亡基因Bax 均属于Bcl-2 家族,Bcl-2蛋白的活性可被Bax调控,两者在肿瘤的放疗、化疗和靶向治疗等治疗作用中发挥重要的调控作用[14],在已有的报道中两者与食管癌的化疗和放疗敏感性中均具有重要作用[15]。在凋亡信号刺激的作用下,Bax 蛋白表达升高,导致线粒体膜的通透性增加,促使凋亡蛋白caspase 3 的激活,caspase 3蛋白的激活是凋亡发生不可逆转的重要标志[16]。本文发现在Eca109-RAD 细胞和Eca109-DDP 细胞中过表达miR-495,并在放射线和DDP 的作用下,细胞中抗凋亡蛋白Bcl-2 表达降低,促凋亡蛋白Bax和caspase 3 的表达增加,表明miR-495 通过调控凋亡相关蛋白促进细胞凋亡在食管癌放疗和化疗中发挥增敏作用。
综上所述,miR-495 促进食管癌细胞化疗和放疗的敏感性,其作用机制可能通过调控凋亡蛋白促进细胞凋亡发挥作用,miR-495 可能是逆转食管癌化疗和放疗抵抗性,以及治疗食管癌的潜在分子靶点。

