电化学氧化脱氢交叉偶联构建C―N键
——电化学技术在有机化学实验教学中的设计与探索
赵梦龙,苑岱雷,叶梓,房芳,于月娜
南方科技大学化学系,广东 深圳 518055
有机化学学科发展迅速,新概念、新方法不断更新,实验设备和技术也迅速更迭换代,一些传统方法已不再是合成目标产物最优策略。有机化学实验课程作为化学专业教学体系的重要环节,应紧随学科研究前沿,不断深入革新,将科研新成果、新技术融合贯穿到实验教学,引导学生的国际性学术视野,激发学生的创新意识,培养专业拔尖创新型人才[1]。
有机电化学合成是一种非常高效的氧化还原方法,反应以电子作为氧化还原试剂,有机分子或催化媒介的外层电子层在“电极/溶剂”表面得到或失去电子,然后转化生成新化合物(图1)。反应通常在常温、常压下进行,避免了有毒或危险的氧化剂和还原剂的使用,过程缓慢可控,选择性高[2],官能团耐受性强,原子经济性高,环境污染小,是公认的绿色合成策略[3]。有机电化学合成策略由于其独特优势,近年来广泛应用于有机化学领域,并取得了一系列突破性成果[4–6]。
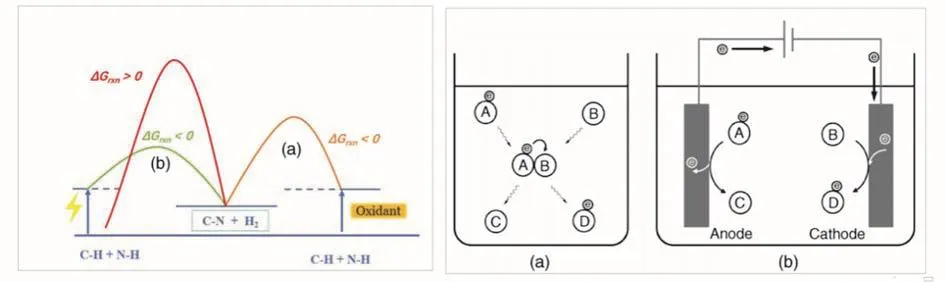
图1 (a) 化学氧化反应;(b) 电化学氧化反应
C―N键作为一类重要的化学键广泛存在于天然产物、药物等生物活性分子中[7],C―H/N―H氧化脱氢交叉偶联反应是构建C―N键最直接、经济的方法之一。由于有机电化学合成绿色、选择性高的特点,与传统方法相比,其在构建C―N键方面呈现出显著的优势,逐渐成为有机合成的热点研究领域之一[8–11]。因此,基于最前沿的科研成果[12–14],将其转化为教学实验,设计了一个电化学阳极氧化芳胺对位高选择性胺化的开放性综合实验。
首先以吩噻嗪和N,N-二甲基苯胺为模板底物,对电流、电量和电解质三个影响因素进行考察;确定最优条件后,再对芳胺的适用性进行考察,最后通过循环伏安法对反应规律进行探索。实验以石墨电极为阳极,铂电极为阴极,反应在室温空气条件下进行,操作简便,绿色友好。此方案融合了电化学合成技术、反应条件筛选、核磁内标法定量、产物结构表征、循环伏安法探索反应规律五部分内容,实验综合性、系统性高,可以锻炼与培养学生的专业综合能力。
1 实验目的
(1) 学习电化学氧化脱氢交叉偶联构建C―N键的反应原理;
(2) 初步学习电化学合成技术的基本概念、原理与仪器操作;
(3) 掌握核磁内标法定量分析在有机反应条件筛选中的应用;
(4) 学习循环伏安法在电化学反应机理探索中的应用。
2 实验原理
2.1 电化学氧化脱氢交叉偶联反应
富电子芳胺与吩噻嗪在电化学氧化条件下,可以发生C―H/N―H交叉偶联反应,生成三芳基胺衍生物。影响电化学反应的因素除一般的化学反应动力学涉及的压力、温度、时间、溶液组成、催化剂等,还有电极电位、电流、电量、电极材料、电解池、电路连接等因素。综合考虑,此方案仅对电流、电量和电解质进行考察,以石墨棒为阳极,铂片为阴极,MeCN/MeOH为溶剂,在单室电解池中以恒电流模式电解,反应能以中等以上的收率获得对位选择性的C(sp2)-H/N-H偶联产物。此合成方法可在空气氛围中进行,具有很好的对位选择性和官能团耐受性。
基于文献报道[12–14],反应可能的机理如图2所示:首先,吩噻嗪在阳极上氧化生成a;同时,芳胺也在阳极氧化并脱去质子生成b;随后,自由基阳离子a与N-自由基b交叉偶联,偶联高选择性地发生在芳胺对位,形成中间体c;最后,脱质子化得产物3a。在反应过程中,氢离子在阴极被还原释放出H2。
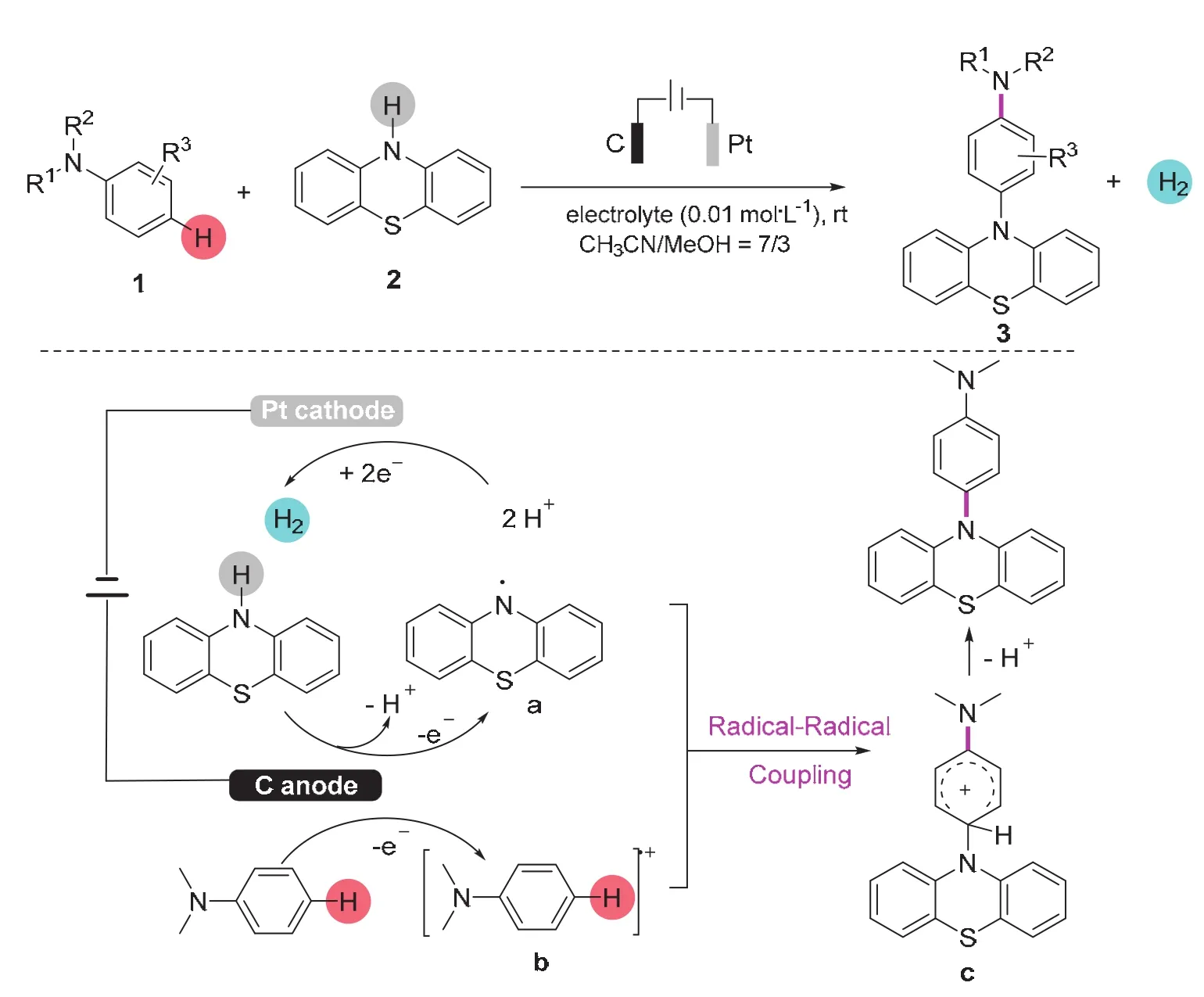
图2 电化学氧化交叉偶联构建C―N键
2.2 电化学合成体系
电化学合成体系一般由电化学工作站、阳极、阴极、反应物、反应介质和电解质等组成。电化学反应是成对出现的,即同时发生阴极还原和阳极氧化,但在通常的有机电合成过程中,一般只利用某一电极(阴极或阳极)上的反应来合成所需化合物,而溶剂在对电极发生“牺牲”反应放出氢气或氧气[15]。
(1) 电解池:是实现电化学反应的装置,实验室常用单室电解池和“H”型分隔电解池[4](图3)。
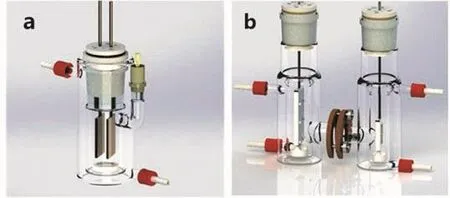
图3 电解池
(2) 电解方式:分为恒电压和恒电流两种;恒电流反应,便于计算总电荷消耗,但当底物反应完后,电压升高,会有副反应发生。恒电压反应,不容易发生副反应,但体系电阻过大将导致电流降低,反应速率低。反应时可以调节电解质类型与浓度、溶剂等来控制电流或电压,实验常采用恒电流方式。
(3) 电极材料:电极材料需导电性好、稳定耐用、易于加工,机械强度好;电极材料决定电极电势,它不仅影响反应收率与纯度,甚至决定反应是否发生以及产物类型。常用Pt、C (石墨、玻碳、掺硼金刚石)、PbO等作阳极材料,Pt、C、Hg、Pb、Al、Ag等作阴极材料。
(4) 电解质:是指具有足够溶解度和氧化还原稳定性的离子盐,电解质离子可以减缓工作电极产生的活性中间体向对电极的迁移,从而减少其损失。电解质离子通常体积大、配位弱,对亲电或亲核试剂呈惰性,常用的有LiClO4、nBu4NBF4、Et4NOTs、nBu4NOAc等。
(5) 溶剂:有机电化学合成中使用的溶剂必须具有足够的介电常数和溶解能力,以便电子可以自由地移动。溶剂必须具有足够的氧化还原稳定性,不干扰预期反应,可使用电位范围应涵盖具体的实验参数。常用的有乙腈、二甲基甲酰胺、二甲亚砜、甲醇、二氯甲烷等。
2.3 循环伏安法
循环伏安法(Cyclic Voltammetry,CV)是一种常用的电化学反应机理研究方法。CV法通过控制电极电势以不同的速率,如图4(a)所示,随时间以三角波形一次或多次反复扫描;电势变化使电极上能交替发生不同的还原和氧化反应,并记录电流-电势曲线,所得曲线如图4(b)所示。根据曲线形状可以判断电极反应的可逆程度,中间体、相界吸附或新相形成的可能性,以及偶联化学反应的性质等。Epa和Epc分别对应氧化和还原的电压峰值,可分别看作为反应所需的电压值。反应所需电流值也可通过图谱中的电流峰值和电极表面积等参数进行换算[16]。
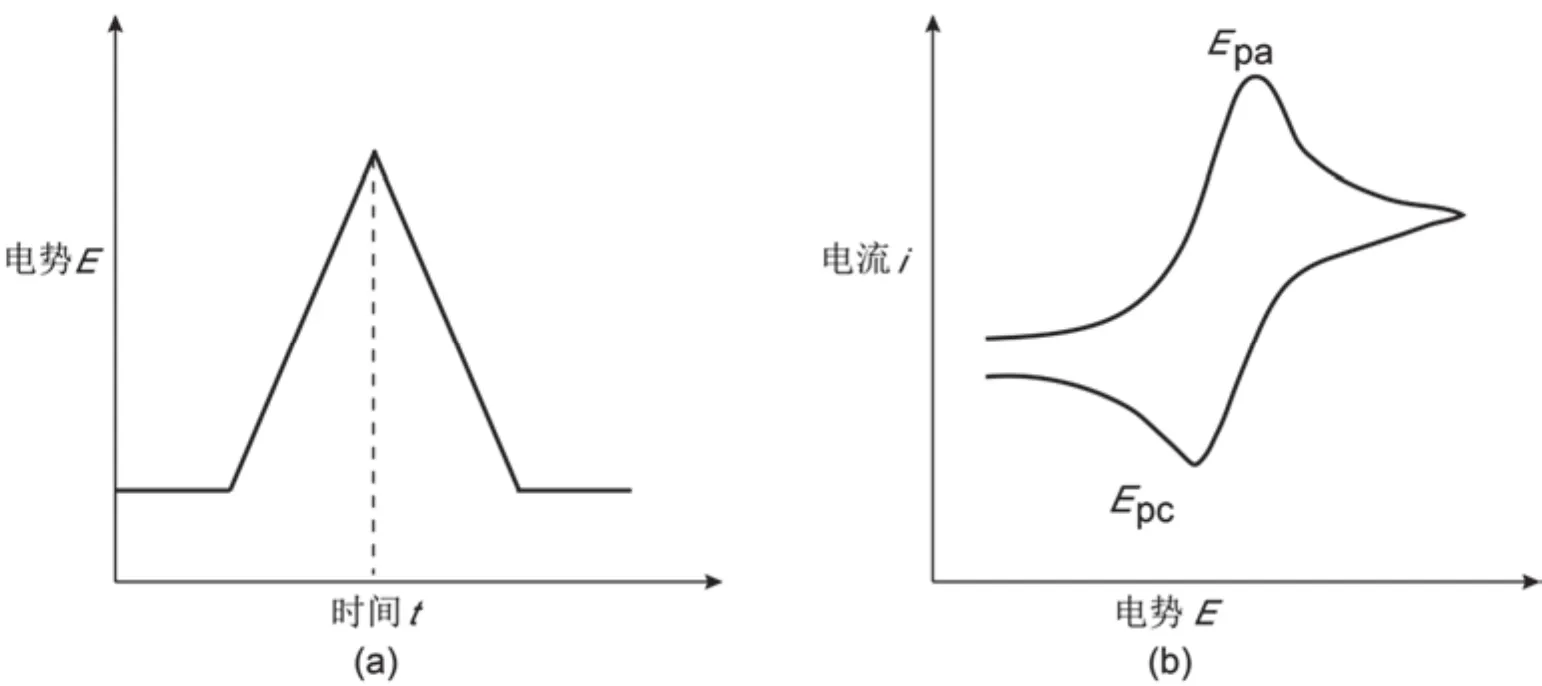
图4 (a) CV法电位扫描;(b) CV法电流-电势曲线
2.4 核磁内标法定量分析
核磁共振氢谱中,共振峰面积与被测组分的含量成正比。内标法定量分析时,一般可对该化合物中某一指定基团上质子引起的峰面积与内标物某一指定基团上质子引起的峰面积进行比较,即可求出其绝对含量。内标物需溶解性好,最好产生单一共振峰,参比共振峰与样品峰的位置至少间隔30 Hz,且不与样品中任何组分反应。将样品与内标物精密称量,配制成一定浓度的溶液,进行1HNMR检测,根据样品和内标指定基团上质子产生的共振峰积分值,可按下式求出样品的含量(WS),式中下标S表示样品,STD表示内标物,A为峰面积,n为特征峰质子当量,M为分子量,W为重量。
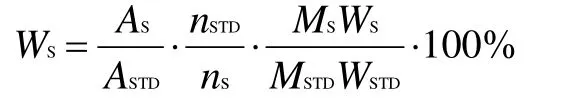
3 试剂
吩噻嗪、N,N-二甲基苯胺、3-甲基-N,N-二甲基苯、3-溴-N,N-二甲基苯胺、N,N-二甲基-1-萘胺、N-苯基-1-萘胺、1-苯基吡咯烷、4-乙酰氨基苯酚、4-二甲氨基苯酚、nBu4NPF6、nBu4ClO4、nBu4NBF4、nBu4NOTf、1,4-二硝基苯(以上均为分析纯,采购自毕得生物医药、安耐吉、百灵威、TCI、Adams等试剂公司);甲醇、乙腈、乙酸乙酯、石油醚、二氯甲烷、无水硫酸钠(以上均为分析纯,采购自上海凌峰);3 mol·L-1KCl溶液、200–300目硅胶、海砂、20 mL样品管等。
4 仪器与耗材
400 MHz核磁仪(德国布鲁克,AVANCE III HD 400)、电化学工作站(华谊,HY3005MT)、石墨电极(阳极,φ6 mm)、铂电极(阴极,10 mm × 10 mm × 0.1 mm)、电化学合成仪(德国IKA,ElectraSyn2.0)、玻碳电极、铂电极、Ag/AgCl参比电极、分析天平、电磁搅拌器、旋转蒸发仪、真空系统、三口烧瓶、圆底烧瓶、分液漏斗、锥形瓶、磁子、移液枪、注射器、微量注射器、翻口塞、针头等。
5 实验步骤
5.1 电化学反应影响因素考察
按照表1中的条件开设实验,共8组实验。
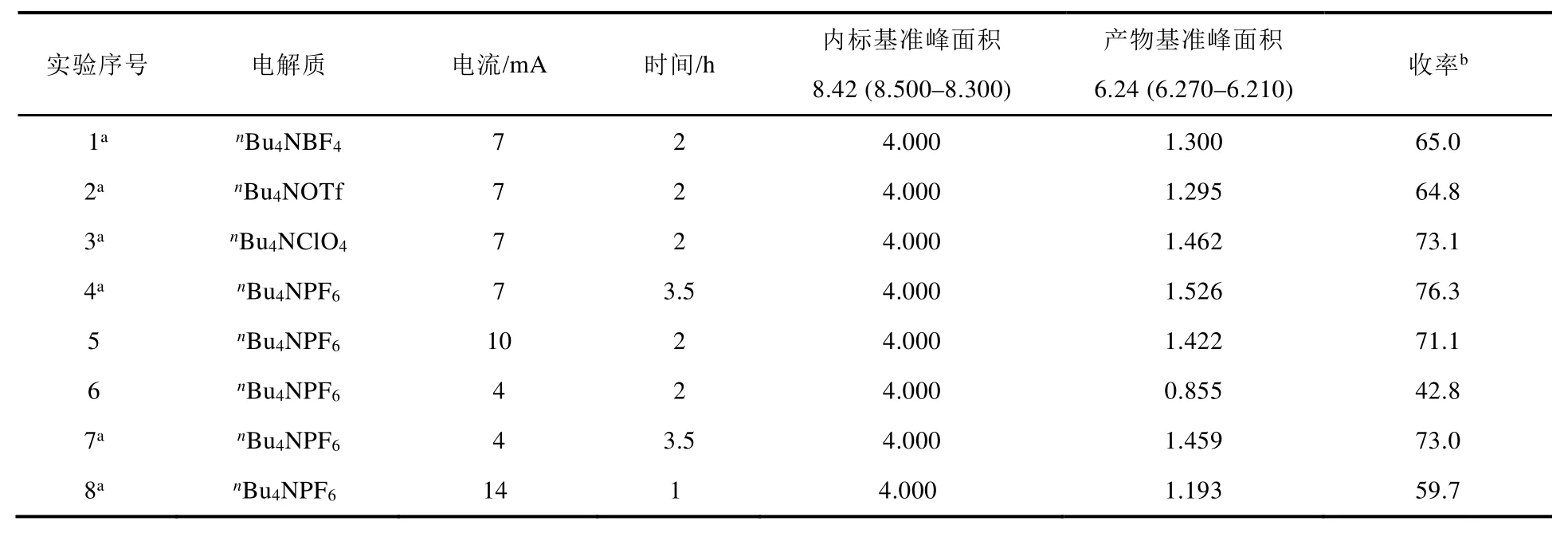
表1 反应影响因素考察
25 mL三口烧瓶中依次加入磁子、吩噻嗪(39.9 mg,0.2 mmol)和电解质(0.1 mmol),随后加入7 mL乙腈和3 mL甲醇(移液枪量取),最后用微量注射器量取N,N-二甲基苯胺(38 µL, 0.3 mmol)加入到三口烧瓶中。
将三口烧瓶固定在电磁搅拌器上,装入石墨电极(阳极,φ6 mm,约18 mm浸入溶液),铂电极(阴极,10 mm × 10 mm × 0.1 mm),通过导线与电化学工作站(图5)。按照表1中的条件设置电流,点击“output”,以恒定电流在室温下反应,溶液颜色逐渐由无色变为浅蓝色,随着反应进行,颜色逐渐加深。薄层色谱监测反应进程(展开剂极性V(石油醚) :V(乙酸乙酯) = 10 : 1),到达表1中时长后,关闭电源,反应结束,此时反应液呈棕黄色。

图5 电化学合成仪
将反应液转移至100 mL圆底烧瓶中,二氯甲烷洗涤反应烧瓶,旋转蒸发仪旋干溶剂。所得固体用乙酸乙酯溶解,然后转移至分液漏斗中,水洗、无水硫酸钠干燥,减压抽滤,收集滤液。向滤液中加入内标物1,4-二硝基苯(33.6 mg,0.2 mmol),充分溶解,然后取1 mL滤液于25 mL圆底烧瓶中,旋转蒸发仪旋干溶剂,油泵真空干燥,除去残留溶剂。向圆底烧瓶中加入0.5 mL左右的氘代氯仿,转移至核磁管内,进行核磁氢谱测试,通过核磁内标法分析特征峰面积之比,以此计算出不同条件下的收率,分析各因素对反应的影响,确定最优的反应条件。
核磁定量测试参数[17]:1H-NMR,400 MHz,测定温度为25 °C,脉冲宽度(P1) 8.58 µs,扫描次数(NS) 32,空扫次数(DS) 2,弛豫延迟时间(D1) 20 s;内标基准峰:8.42 (8.500–8.300),s峰,质子当量4H;样品基准峰:6.24 (6.270–6.210),dd峰,质子当量2H (图6)。
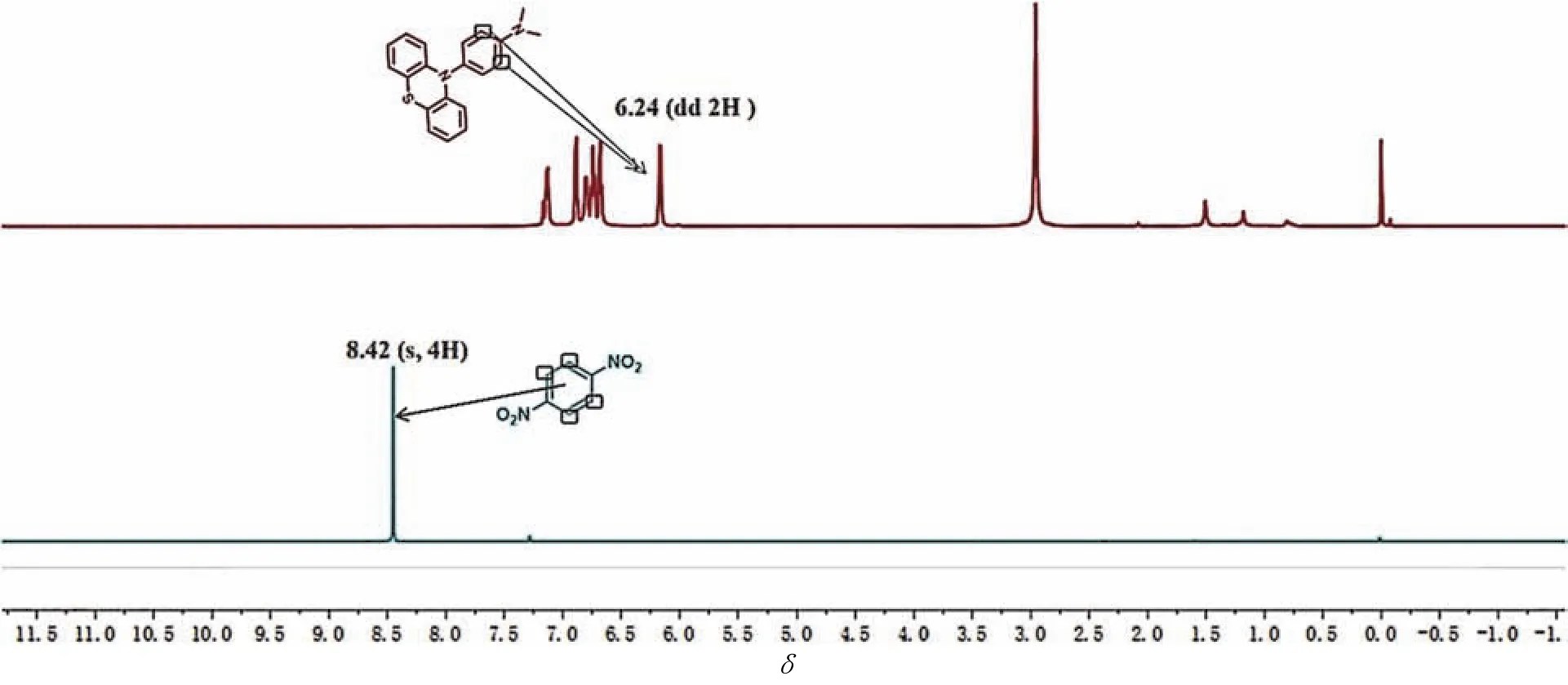
图6 核磁内标法定量分析
5.2 芳胺适用性考察
在最优条件下,对不同类型芳胺的适用性进行考察(图7),反应操作步骤同条件筛选,后处理操作步骤如下:

图7 底物适用性考察
将反应液转移至100 mL圆底烧瓶中,二氯甲烷洗涤反应瓶,加入约1 g硅胶,摇匀,旋转蒸发仪旋干溶剂。干法上样,硅胶柱层析分离纯化,洗脱剂极性为V(石油醚) :V(乙酸乙酯) = 200 : 1,使用TLC监测柱层析进程(展开剂极性V(石油醚) :V(乙酸乙酯) = 10 : 1)。
收集含有产物的洗脱剂于500 mL茄型瓶中,使用旋转蒸发仪旋干溶剂,然后转移至已称重的25 mL圆底烧瓶中,旋干溶剂,使用油泵进行真空干燥,除去残留溶剂,称重,计算收率。
将少量产品溶解于0.5 mL左右的氘代氯仿中,转移至核磁管内,进行核磁氢谱测试,测试结束后回收样品;然后进行高分辨质谱分析(送样),分析核磁氢谱和质谱数据,表征产物结构。
5.3 循环伏安法测试
样品的配制:20 mL样品管中依次加入7 mL乙腈、3 mL甲醇、2.0 mmol电解质,0.1 mmol吩噻嗪或芳胺,共配制9个样品。
向Ag/AgCl参比电极的玻璃管中填充3 mol·L-1KCl溶液,使液面达到玻璃管的中间位置。然后依次连接参比电极、玻碳电极(W)和铂电极(C)至瓶盖上。电极安装完之后,乙醇洗涤电极,将瓶盖与反应管组装在一起,待测样品用注射器经瓶盖上的阀门加入反应管中(图8)。
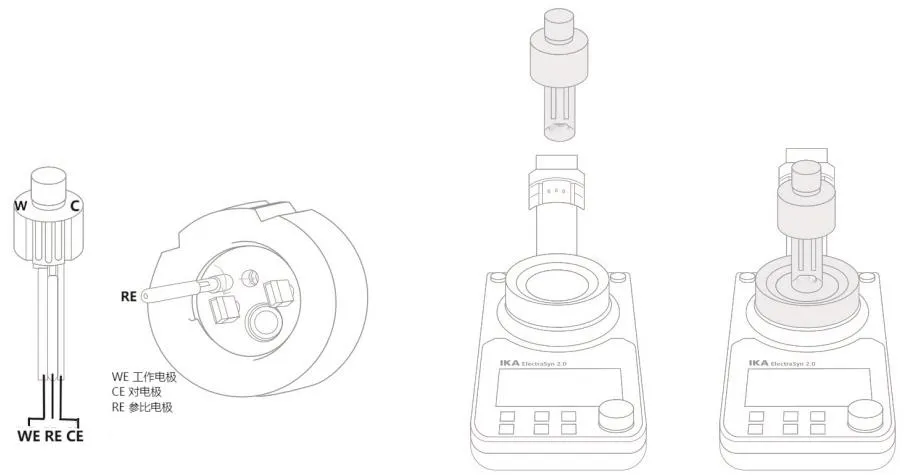
图8 循环伏安分析仪
将反应管套件安装到电化学工作站上,通过阀门向体系内缓慢通入惰性气体,鼓泡脱气3 min,关闭阀门,静置待用。
设置测试参数(段数3,起始电压0 V,最高电压2 V,最低电压-0.1 V,终止电压0 V,扫描速度0.2 V·s-1),点击“start”,开始测量,得到吩噻嗪和不同取代芳胺的CV图。
6 结果与讨论
实验第一部分,对影响电化学反应的三个因素:电解质、电流和电量进行考察,反应收率通过核磁内标法确定,结果如表1所示。首先考察了四丁基四氟硼酸铵、四丁基四氟硼酸铵、四丁基高氯酸铵、四丁基六氟磷酸铵四种电解质(实验1–4),其中四丁基六氟磷酸铵效果最佳,反应核磁收率达76.3% (实验4)。确定了电解质后,又对电量进行考察,当反应时间相同,实验5中电流升至10 mA,反应收率稍有降低(71.1%),实验6降低电流至4 mA,2 h后停止反应,仅得到43%收率;这两组数据说明电流较小时,反应时间短,电量不足影响收率;但电流较大时,电量充足,但是由于电势增大,副反应增多,收率不升反而稍微降低。接下来在电量相同的条件下,考察电流的影响,实验7电流降低4 mA,反应3.5 h收率基本保持,而实验8电流升至14 mA时,收率降至59.7%,这两组数据同样说明电流过高,副反应增多。综合考虑,我们确定反应4的条件为最优条件。确定了最优反应条件后,在实验第二部分考察了8种不同取代芳胺的适用性(图7)。产物结构经核磁氢谱和质谱表征、验证。芳胺对位无取代时,可以高选择性得到芳胺对位胺化产物(3a–e,3f)。芳胺间位取代基电子效应对收率影响显著,当间位是给电子甲基时,收率可达98% (3b);当间位引入吸电子溴时,反应仅以16%的收率得到产物3c。具有环状结构的N-吡咯烷基苯胺(1e)也表现出良好的反应活性,以92%的收率得到目标产物3e。当使用对位氨基取代的酚类底物时(1f–g),可以高选择性生成邻位N―H/C―H键偶联产物,这类底物可能是按照氮自由基对芳香环加成的机理进行反应[18],缺电子的1f反应活性低,收率仅有61%。具有较大共轭体系的N-苯基-1-萘胺(1d)和N,N-二甲基-1-萘胺(1h)反应活性都非常高,收率分别为86%和89%。实验第三部分是循环伏安法测试,测试两类底物的氧化还原电位。如图9所示,所测吩噻嗪和芳胺的氧化电位均低于1.5 V,而反应时的电压均在4.0 V以上,远高于两种底物的氧化电位,因此推测吩噻嗪及芳香胺在实验条件下均在阳极被氧化,失去电子,分别形成碳自由基阳离子和氮自由基,然后发生自由基交叉偶联(图2)。从图9(b)我们可以得出1b,1a,1c的氧化电位依次升高,因此生成自由基的难度增大,从而导致反应活性的差异,这与第二部分的实验结果一致。具有环状结构的N-吡咯烷基苯胺(1e)氧化电位与N,N-二甲基苯胺(1a)相比略低,因此它的反应性高。图9(c)中1a,1d,1h的氧化电位趋势与他们反应收率也基本一致。1d由于氮上引入吸电子苯基,因此氧化电位较高,但是实验结果中,仍然表现出很好的反应性(86% yield)。我们推测是由于与氨基相连苯环上C―H键数量较少,且底物位阻较大,减少了副反应的发生,利于目标产物的生成。

图9 循环伏安曲线
基于芳胺底物适用性的考察结果和循环伏安法的测试结果,可以大致推断,在吩噻嗪2与不同的芳香胺3进行电化学促进下的交叉偶联时,与氨基相连芳环的电子密度越高,越容易被氧化形成自由基,越容易发生交叉偶联反应,表现出较高的反应活性,能够获得更好的反应收率。
7 结语
本实验方案的三个部分内容层层递进,综合性、系统性强。学生首先需要成功实施第一部分实验,分析讨论实验结果,确定最优条件,才可以进行第二部分实验。通过第二部分实验,可以得出不同芳香胺的反应性差异,并分析讨论引起差异性的原因;第三部分循环伏安法测定两类底物的氧化还原电位,不仅可以验证反应机理,还可以解释说明第二部分实验结果。
实验可分组进行,每组2–3个同学。此实验方案可分模块进行,如表2所示,时长在10–22学时之间,可以满足不同层次实验教学需要。

表2 教学建议
在实验教学中引入绿色电化学合成技术,使得课程内容新颖、丰富,反应在室温空气中即可进行,收率理想,操作简便,非常适合教学使用。
通过循环伏安法测试,引导学生对反应机理进行研究和探讨,加深对电化学氧化脱氢交叉偶联构建C―N键机理的理解,同时还可以学习使用电化学工作站。核磁内标定量分析反应收率,不仅可以帮助学生巩固核磁共振仪的工作原理、操作技术和谱图解析能力,还可以提高实验效率,把学生从繁琐枯燥的纯化操作中解放出来,提高了有机实验的友好性。
我们将前沿科研成果转化为教学实验,实验以学生为主导,结果开放,不仅能够培养学生分析、解决实际复杂问题的能力;同时可以调动学生的学习兴趣、拓展科研视野、激发科研热情;更能在科研成果中增强学生的专业认同感、培养学生的创新意识和社会担当,科教融合是实现创新人才培养的一个重要环节。

